第五章 相 图 5
- 格式:doc
- 大小:6.57 MB
- 文档页数:6


第五章相贯线两立体表面相交,交线称为相贯线。
准确地画出相贯线的投影能更完整地表达立体。
实际中两立体相交可分为三种情况:平面立体与平面立体相交;平面立体与曲面立体相交;两曲立体相交,如图5-0-1所示。
相贯线有如下性质:1.相贯线一般是封闭的空间折线或曲线。
其形状随两相交立体表面的性质和相对位置的变化而不同。
2.相贯线是两立体表面的共有线,是两立体表面公共点的集合。
求相贯线,也就是求两相交立体表面的公共点。
第三节两曲面立体相交两曲面立体相交,相贯线为封闭的空间曲线,特殊情况为平面曲线。
下面介绍常用的两种方法。
一、表面取点法两回转体相交,如果其中有一个是轴线垂直于投影面的圆柱,则相贯线在该投影面上的投影,就积聚在圆柱面的有积聚性的投影上。
于是可以在这个相贯线有积聚性的投影上取一些点,按已知曲面立体表面上的点的一个投影,求其它投影的方法,即表面取点法,作出相贯线的投影。
例1:如图5-3-1所示,求作两正交圆柱的相贯线。
解:相贯线系两圆柱表面公共点的集合,应在铅垂轴线的小圆柱面上,其水平投影重合在水平投影中的小圆周上;同理相贯线的侧面投影也应重合在侧面投影的大圆周上。
故只有它的正面投影需要画出,可以用已知曲面上点的一个投影求另外投影的方法。
作图步骤如下:(1)先求特殊点,即求相贯线上的最前、最后、最左、最右、最上、最下等点。
在水平投影的小圆周上直接确定出相贯线上最左、最右点的投影1、3和最前、最后点的投影2、4;对应在侧面投影中为1″、3″和2″、4″,也是最高、最低点的侧面投影;按投影关系可得出它们的正面投影1′、3′和2′、4′。
因为两曲面立体前后对称相贯,故最前、最后两点的正面投影重合。
(2)求作若干一般位置点。
依连线光滑准确的需要,作出相贯线上若干个中间点的投影。
如在水平投影上取5、6点,其侧面投影为5″、6″,再求出其正面投影5′和6′。
(3)依次光滑连接1′、5′、2′(4′)、6′、3′各点,即得相贯线的正面投影。




第五章 相平衡一、本章基本要求1.掌握相、组分数和自由度的意义;2.了解相律的推导过程及其在相图中的应用;3.了解克劳修斯-克拉珀龙方程式的推导,掌握其在单组分两相平衡系统中的应用;4.掌握各种相图中点、线及面的意义;5.根据相图能够画出步冷曲线,或由一系列步冷曲线绘制相图;6.掌握杠杆规则在相图中的应用;7.结合二组分气液平衡相图,了解蒸馏与精馏的原理;8.对三组分系统,了解水盐系统的应用,相图在萃取过程中的应用及分配定律的应用;二、 基本公式和内容提要一基本公式相律的普遍形式:f K n =-Φ+ 克拉珀龙方程:mm d ln d V T H T p ∆∆= 克劳修斯-克拉珀龙方程的各种形式:微分式: 2m vap d ln d RT H T p ∆= vap m H ∆与温度无关或温度变化范围较小vap m H ∆可视为常数, 定积分:vap m 211211ln ()H p p R T T ∆=- 不定积分式:vap mln H p C RT ∆=-+ 特鲁顿规则:K)J/(mol 88b mvap ⋅≈∆T H杠杆规则:以系统点为支点,与之对应的两个相点为作用点,有如下关系:1122()()n x x n x x -=-其中n 1 、n 2 分别表示平衡两相的摩尔数,x 、x 1、x 2分别表示系统的组成及其对应的平衡两相的组成;二内容提要1.单组分系统 单组分系统相律的一般表达式为:f =1-Φ+2=3-Φ图5-1 水的相图可见单组分系统最多只能有三相平衡共存,并且最多有两个独立变量,一般可选择温度和压力;水的相图为单组分系统中的最简单相图之一;图5-1中三条曲线将平面划分成固、液及气相三个区;单相区内f =2;AB 、AD 和AE 分别表示气液、气固和固液两相平衡线;两相共存时f =1;虚线AC 表示应该结冰而未结冰的过冷水与水蒸气平衡共存;A 点为三相点,这时f =0,水以气、液、固三相共存;水的三相点与水的冰点不同,冰点与压力有关;单组分系统两相平衡共存时T 与p 的定量关系式可由克拉珀龙方程式描述;对于有气相参与的纯物质气液两相或气固两相平衡,可用克劳修斯-克拉珀龙方程描述;特鲁顿规则是近似计算气化热或沸点的经验式;2.二组分双液系统 对于二组分系统, f =2-Φ+2=4-Φ;Φ=1时f =3,即系统最多有三个独立变量,这三个变量通常选择温度、压力和组成;若保持三者中的一个变量恒定,可得到p ~x 图、T ~x 图和p ~T 图;在这三类相图中,系统最多有3个相同时共存;1二组分完全互溶系统的气液平衡:这类系统的相图如图5-2;图中实线为液相线,虚线为气相线,气相线与液相线之间为气液二相共存区;靠近气相线一侧为气相区,靠近液相线一侧为液相区;其中Ⅰ为理想液态混合物系统;Ⅱ、Ⅲ分别为一般正、负偏差系统;Ⅳ、Ⅴ分别是最大正、负偏差系统;Ⅰ~Ⅲ类系统中易挥发组分在气相中的组成大于其在液相中的组成,一般精馏可同时得到两个纯组分;Ⅳ、Ⅴ类相图中极值点处的气相组成与液相组成相同,该系统进行一般精馏时可得到一个纯组分和恒沸混合物;二组分系统的两相平衡状态对应一个区域,用杠杆规则可以计算两相平衡共存区平衡二相的相对数量;图5-2 完全互溶系统的气液2部分互溶的二组分系统:因两种液体结构上有显著的差别,会出现一种液体在另一种液体中只有有限的溶解度,超过一定范围便要分成两个液层,即“部分互溶”,相图见图5-3;C点对应的温度称为“临界溶解温度”;温度超过C点,正丁醇与水两组分能以任何比例互溶;还存在另外两类溶解度图,分别见图5-4和图5-5,前者具有下临界溶解温度,后者同时具有上、下临界溶解温度;图5-3 水-正丁醇的溶解图图5-4 水-三乙基胺的溶解度图图5-5 水-烟碱的溶解度图图5-6 邻硝基氯苯、对硝基氯苯二元系统的冷却曲线a 和熔点组成图b3完全不互溶的双液系统:如果两种液体结构相差很大,彼此间的溶解度可以忽略不计,这样的系统可以看作完全不互溶的双液系统;在这类系统中任意液体在某一温度下的蒸气压与该液体同温度下单独存在时的蒸气压相同,与两种液体存在的量无关;总蒸气压**A B p p p =+,因此完全不互溶液体混合物的沸点低于任意纯组分的沸点,这是水蒸气蒸馏的基础;3.二组分固液系统1简单低共熔系统:常用热分析法或溶解度法绘制这类相图;利用“冷却曲线”绘制的邻硝基氯苯A 与对硝基氯苯B 的固液相图见图5-6;aE 和bE 线分别表示邻硝基氯苯与对硝基氯苯固体与熔化物平衡时液相组成与温度的关系曲线,也称为熔点降低曲线;E 点为最低共熔点,对应该温度的水平直线为三相平衡线两端点除外,共存的三相为固体邻硝基氯苯和对硝基氯苯及E 点对应的溶液,aE 、bE 及三相线将图形分成4个部分,各区域的相态分别注在图上;低共熔系统相图与药学密切相关,如利用冷却结晶过程分离提纯化合物;利用熔点变化检查药物或中间体纯度;指导药物配伍及防冻制剂的制备;改良与修饰剂型;与气-液相图联用,对混合物进行分离和提纯;2生成化合物系统:若A 与B 形成的化合物在固相和液相均是稳定的,并且熔化时固相和液相的组成相同,称为生成稳定化合物系统;若A 与B 间形成n 个稳定的化合物,则其固液相图相当于n +1个简单低共熔系统相图的拼合,若A 与B 间形成的化合物C,在加热到熔点之前,就分解成熔化物和另一种固体,熔化物与固态化合物C 的组成不同,称为生成不稳定化合物系统;其相图与前者有所不同;4.三组分系统 当温度和压力同时固定时,在平面上用等边三角形可表示三组分凝聚系统中各平衡系统的状态;其中三个顶点分别表示三个纯物质,三条边分别表示2个端点对应物质构成的二组分系统,三角形内任意一点表示三组分系统,二组分及三组分系统的组成可利用相图得到;三液体间可以是一对、二对甚至是三对部分互溶的,这类系统的相图在液-液萃取过程中有重要作用;除三液系统外,还有水盐系统,其相图对于粗盐提纯、分离具有指导作用;三、 概念题和例题一 概念题1.在一个抽空的容器中,放入过量的NH4Is并发生下列反应:NH4Is NH3g+HIg2HIg H2g+I2g系统的相数Φ= ;组分数K= ;自由度f= ;2.在一个抽空的容器中,放入过量的NH4HCO3s发生下列反应并达平衡:NH4HCO3s NH3g+H2Og+CO2g系统的相数Φ= ;组分数K= ;自由度f= ;3.在一个抽空容器中,放入足量的H2Ol,CCl4l及I2g;H2Ol和CCll完全不互4l中,容器上部的气相中同时含有I2g、H2Og及溶,I2g可同时溶于H2Ol和CCl4CCl4g;该平衡系统的相数Φ= ;组分数K= ;自由度f= ;4.含KNO3和NaCl的水溶液与纯水达渗透平衡,系统的相数Φ= ;组分数K= ;自由度f= ;5.在下列不同情况下,反应:2NH3 g N2 g +3H2 g 达平衡时,系统的自由度各为多少1反应在抽空的容器中进行;2反应在有N2的容器中进行;3反应于一定的温度下,在抽空的容器中进行;6.A和B两种液态物质微观角度讲要满足哪些条件才能形成理想液态混合物7.水的三相点与正常冰点有何不同8.液体的饱和蒸气压越高,沸点就越低;而由克劳修斯-克拉珀龙方程知,温度越高,液体的饱和蒸气压愈大;两者是否矛盾为什么9.对于具有最大正、负偏差的液-气平衡系统,易挥发组分在气相中的组成大于其在液相中的组成的说法是否正确为什么10.在一定压力下,若A、B二组分系统的温度-组成图中出现最高恒沸点,则其蒸气压对拉乌尔定律产生正偏差吗11.导出杠杆规则的基本依据是什么它能解决什么问题如果相图中横坐标为质量分数,物质的数量应取什么单位若横坐标为摩尔分数,物质的数量又应取什么单位二概念题答案1.2,1,12.2,1,13.3,3,24.3, 2, 45.1f=3-1-1-1+2 =2;2f=3-1-1+2=3;3 f=3-1-1-1+1=16.A和B两种液体分子的大小和结构十分接近,使得A-A分子之间、B-B 分子之间及A-B分子之间作用力近似相等时,可构成理想溶液;7.三相点是严格的单组分系统,水呈气、液、固三相共存时对应的温度为,压力为;而冰点是在水中溶有空气和外压为时测得的温度数据;首先,由于水中溶有空气,形成了稀溶液,冰点较三相点下降了;其次,三相点时系统的蒸气压低于冰点时的外压,由于压力的不同冰点又下降了,故冰点时的温度为;8.两者并不矛盾;因为沸点是指液体的饱和蒸气压等于外压时对应的温度;在相同温度下,不同液体的饱和蒸气压一般不同,饱和蒸气压高的液体,使其饱和蒸气压等于外压时,所需的温度较低,故沸点较低;克劳修斯-克拉珀龙方程是用于计算同一液体在不同温度下的饱和蒸气压的,温度越高,液体越易蒸发,故饱和蒸气压越大;9.不正确;因为具有最大正、负偏差系统的相图中有极值点,在极值点处液相组成与气相组成相同,用一般精馏不能将恒沸混合物分离;对于具有最大正、负偏差系统,题中的叙述应修正为适于理想或非理想液态混合物系统的柯诺瓦洛夫规则,即:在二组分溶液中,如果加入某一组分使溶液的总蒸气压增加即在一定压力下使溶液的沸点下降,则这个组分在气相中的组成将大于它在液相中的组成;10.产生负偏差;因为温度-组成图上有最高极值点,压力-组成图上必有最低极值点,故题中所给系统对拉乌尔定律产生最大负偏差;11.导出杠杆规则的基本依据是质量守恒定律,该规则具有普遍意义;可用于计算任意平衡两相的相对数量;相图中横坐标以质量分数表示时,物质的数量以质量为单位;横坐标以摩尔分数表示时,物质的数量以摩尔为单位;三例题例1 水的蒸汽压方程为:4885ln p A T=-, 式中A 为常数,p 的单位为Pa;将10g 水引入体积为10L 的真空容器中,问在323K 达到平衡后,容器中还剩多少水解:将T =,p =101325Pa 代入所给方程中,则:4885ln101325373.2A =- 得A = 于是蒸汽压方程为:Tp 488524.61ln -= 将T =323K 代入上式,得:p =因为 V l +V g =10L, V l V g , 故 V g ≈10L设蒸汽为理想气体,mol 0493.0gg ==RT pV n ,W g =0.888g故还剩水为:10-=9.112g例2 已知298K 时气相异构反应:正戊烷异戊烷的p K =,液态正戊烷和异戊烷的蒸气压kPa 与温度的关系式分别可用下列二式表示: 正戊烷:2002453145.9ln +-=T p 异戊烷:2252453002.9ln +-=T p 假定两者形成的溶液为理想液态混合物,计算298K 时液相异构反应的x K ;解:K p =**x p p K p p =异异正正图5-7 邻硝基氯苯A 与对 硝基氯苯B 的T -x 图 **x p p K K p =正异由已知条件知298K 时,2002453145.9ln +-=T p , *67.99kPa p =正 同理可求得*91.40kPa p =异,则:**67.9913.249.8591.40x p p K K p ==⨯=正异 例3 邻硝基氯苯A 与对硝基氯苯B 的温度-组成图如图5-7:1指出图中点、线、区的意义;2某厂对硝基氯苯车间的结晶器每次处理氯苯硝化料液×103kg,料液的组成为B W =66%,A W =33%间W =1%,可忽略不计,温度约为327K, 若将此料液冷却到290K 此时溶液中含B 35%,如R 点所示,问:1 每次所得对硝基氯苯的产量为多少kg2 平衡产率如何3 冷母液的组成如何冷母液中尚含对硝基氯苯及邻硝基氯苯各多少kg3画出图中f 、g 、h 三物系的步冷曲线;解:1Ⅰ区为邻硝基氯苯与对硝基氯苯二异构体所组成的溶液,为单相区;Ⅱ区为邻硝基氯苯固相与溶液两相平衡共存区;Ⅲ区为对硝基氯苯固相与溶液两相平衡共存区;Ⅳ区为对硝基氯苯固相与邻硝基氯苯固相两相共存区;ac 线为邻硝基氯苯凝固点降低曲线;bc 线为对硝基氯苯凝固点降低曲线;过c 点的水平线与温度坐标的两个交点除外为三相线,线上任意一点都表示邻硝基氯苯固相、对硝基氯苯固态及对应c 点组成溶液的三相平衡共存;a 点为纯邻硝基氯苯的凝固点,b 点为纯对硝基氯苯的凝固点,c 点为低共熔点,该点对应的温度称为低共熔温度;2将W A =33%,W B =66%,温度为323K m 点的系统冷却到190K,此时有大量对硝基氯苯固态析出,冷母液的组成为R 点所示,含对硝基氯苯W B =35%;此时析出的对硝基氯苯固体与溶液的质量比,可由杠杆规则确定,即:66.000.135.066.0B --=溶液m m 又:3B 7.810kg m m +=⨯溶液图5-8 f 、g 、h 三物系的冷却曲1联立以上两式解得:m B =×103kg 272.3%66.0108.71072.333=⨯⨯⨯=平衡产率 3冷母液的组成为含对硝基氯苯W B =35%,含对硝基氯苯的量为:333(7.810 3.7210)35% 1.42810 kg ⨯-⨯⨯=⨯冷母液中含邻硝基氯苯的量为3333(7.810 3.7210) 1.42810 2.62510 kg ⨯-⨯-⨯=⨯3三系统的冷却曲线见图5-8;例 4 下,苯和甲苯的沸点分别为和,摩尔蒸发热分别为30696J/mol 和31967J/mol 设摩尔蒸发热与温度无关;已知苯和甲苯可构成理想液态混合物,问:若使该溶液在,条件下沸腾,其组成应如何解:)11(ln 21m 12T T R H p p -∆= 苯:)2.37314.3531(314.830696101325ln 2-=p 2p = kPa, 甲苯:)2.37318.3831(314.831967101325ln 2-=p 2p = kPa**+p p x p x =苯苯甲苯甲苯176.30+76.10=101.325x x 苯甲苯=1x x +苯甲苯可得 苯x = , 甲苯x =例5 在温度T 时,纯Al 和纯Bl 的饱和蒸气压分别为40kPa 和120kPa;已知A 、B 两组分可形成理想液态混合物;1在温度T 下,将y B =的A 、B 混合气体于气缸中进行恒温缓慢压缩;求第一滴微小液滴不改变气相组成出现时系统的总压力及小液滴的组成x B 各为若干2若A 、B 液态混合物恰好在温度T 、100kPa 下沸腾,此混合物的组成x B 及沸腾时蒸气的组成y B 各为若干解:1设与y B =的气相成平衡的液相组成为x B 时,总压为p ,则有:*B B B **A B B Bp (1)p x y x p x =-+,代入已知数据得: x B =**A B A B B B (1)p p p p x p x =+=-+=40×1-+120×=2由题意知:100 =*A p 1-x B +*B p x B将*A40kPa p =,*B 120kPa p =代入上式得 x B =对应的气相组成: *B B B 0.900100p x y == 例6 在下,将9.0kg 的水A 与30.0kg 的醋酸B 形成的液态混合物加热到378K,达到气液两相平衡时,气相组成y B =,液相中x B =;求气液两相的质量各为多少千克解:由M A =18×10-3 kg/mol,MB=60×10-3 kg/mol 得:mol 500A A A ==M m n ,mol 500BB B ==M m n mol 1000B A =+=n n n 总 系统的总组成:B 0,B 0.500n n n ==总在T =378K 、p =达到气液平衡时,根据杠杆规则,可列出下列关系: g0.5440.5000.34650.5000.417n n -==-总 n g =总n =×1000=n l =总n -n g =1000-=气、液相的平均摩尔质量分别为:M g =Σy i M i =×18+×60×10-3=×10-2 kg/mol图5-9 水-异丁醇沸点-组成示意图 丁醇-水沸点-组成示意图M l =Σx i M i =×18+×60×10-3=×10-2 kg/mol气相的质量:m g =n g M g =××10-3=12.3kg液相的质量:m l = n l M l =××10-2=26.7kg例7 异丁醇-水是液相部分互溶系统,已知其共沸数据如下:共沸点为,共沸组成含异丁醇的质量分数是:气相%,液相中异丁醇层为%,水层为%;今有异丁醇-水液态混合物0.5kg,其中含异丁醇%,将此混合物在压力下加热;1作沸点-组成示意图;2温度接近时,此平衡系统中存在哪些相 各相重多少千克3当温度由刚有上升趋势时,平衡系统中存在哪些相 各相重多少千克解:1根据共沸数据画出相图如图5-9;2温度接近时,平衡系统中存在两个共轭液层,即异丁醇层和水层,设水层重为x kg,则异丁醇层重为-x kg;由上图可知: x 30-=-x 85-30解得: x = 0.36kg异丁醇层重为:-=0.14kg3刚有上升趋势时,系统中亦存在两相,即气相和水层相;设水层重y kg,则气相重为-y kg于是有:y 30-=-y 70-30y = 0.326kg,气相重为:- = 0.174kg四、习题解答1.指出下列平衡系统的组分数、自由度各为多少1NH 4Cls 部分分解为NH 3g 和HClg ;2若在上述系统中额外加入少量的NH 3g ;3NH 4HSs 和任意量的NH 3g 及H 2Sg 平衡;4Cs,COg,CO 2g,O 2g 在100℃时达平衡;解:1K =3-1-1=1, f =1-2+2=12K =3-1-0=2, f =2-2+2=23K =3-1-0=2, f =2-2+2=24K =4-2-0=2, f =2-2+1=12.在水、苯和苯甲酸的系统中,若指定了下列事项,试问系统中最多可能有几个相,并各举一例;1指定温度;2指定温度和水中苯甲酸的浓度;3指定温度、压力和水中苯甲酸的浓度;解:1f=3-Φ+1=4-Φ,f=0时,Φ=4,即最多可有4相共存,如气相、苯甲酸固体、苯甲酸的饱和水溶液及其饱和苯溶液;2f=2-Φ+1=3-Φ,f=0时,Φ=3,故最多可有三相共存,如苯甲酸的饱和水溶液相、苯甲酸的饱和苯溶液相和气相;3f=2-Φ+0=2-Φ,即系统最多可有两相共存,如苯甲酸苯溶液及苯甲酸水溶液;3.求下述系统的自由度数,如f≠0,则指出变量是什么;1在标准压力p下,水与水蒸气平衡;2水与水蒸气平衡;3在标准压力p下,I2在水中和CCl4分配已达到平衡,无I2s存在;4NH3g、H2g、N2g已达化学平衡;5在标准压力p下,NaOH水溶液与H3PO4水溶液混合后;6在标准压力p下,H2SO4水溶液与H2SO4·2H2O固已达平衡;解:1 f=1-2+1=0,即无变量系统2 f=1-2+2=1,即T或p3 f=3-2+1=2,即T和x4 f=2-1+2=3,即T、p和x5 f=3-1+1=3,即T、x1和x26 f=2-2+1=1,即T4.硫的相图如图5-10;图5-10 硫的相图1写出图中各线和点代表哪些相的平衡;2叙述系统的状态由X在恒压下加热至Y所发生的变化;解:1AB:正交与气相;BC:单斜与气相,CD:气相与液相;CE:单斜与液相;BE:过热正交硫的蒸气压曲线;BG:正交与气相;CG:液态与气态;GE:正交与液态;EF:过热正交硫的熔化曲线;B:正交、单斜与气相;C:单斜、液相与气相;E:正交、气相与液相;G:液相、单斜与正交2如图:X→a为正交硫的恒压升温过程,a点为正交硫与单斜硫两相平衡共存,a→b为单斜硫的恒压升温过程,b点为单斜硫与液态两相平衡共存,b→Y为液态硫的恒压升温过程;5.氯仿的正常沸点为外压为,试求氯仿的摩尔气化热及时的饱和蒸气压; 解:由特鲁顿规则知:Δvap H m = 88T b = 88×+ = kJ/mol将已知数据代入克-克方程:)11(ln 21m 12T T R H p p -∆= )15.313165.3341(314.829450325.101ln 2-=p 解得:kPa 0.492=p6.今把一批装有注射液的安瓿瓶放入高压消毒锅内加热消毒,若用的水蒸气进行加热,问锅内的温度有多少度已知Δvap H m = kJ/mol 解:vap m 211211ln ()H p p R T T ∆=- )115.3731(314.840670325.10199.151lnT-= T =385K7.某有机物的正常沸点为外压为,从文献上查得:压力减为 kPa 时,它的沸点为,问在时的沸点为多少 假定~范围内温度对气化热的影响可以忽略; 解:vap m 211211ln ()H p p R T T ∆=- vap m 0.26711ln ()101.3258.314503.15363.15H ∆=- Δvap H m = kJ/mol)115.5031(314.864442325.10133.1ln T-= T =393K8.氢醌的蒸气压实验数据如下: 压力/kPa求:1氢醌的升华热、蒸发热、熔化热设它们均不随温度变化; 2气、液、固三相共存时的温度与压力;3在500K 沸腾时的外压;解:1)11(ln 21m 12T T R H p p -∆= sub m 1.333411ln ()0.13338.314405.55436.65H ∆=-Δsub H m = kJ/molvap m 13.33411ln ()5.33278.314465.15489.65H ∆=- Δvap H m = kJ/molΔfus H m =Δsub H m -Δvap H m = kJ/mol2设三相平衡共存时的温度为T ,压力为p ,则有:sub m 11ln()0.13338.314405.55H p T ∆=- vap m 11ln ()5.33278.314465.15H p T∆=- 二式联立得:T =, p =3沸腾时蒸气压等于外压,即有:)500115.4651(314.8708333327.5ln -=p p =9.为了降低空气的湿度,让压力为的潮湿空气通过一冷却至的管道,试用下列数据,估计在管道出口处空气中水蒸气的分压;水在和时的蒸汽压分别为和,时冰的熔化热为kg 假设所涉及的热效应都不随温度而变;当此空气的温度回升到时压力仍为,问这时的空气相对湿度为若干解:)11(ln 21m 12T T R H p p -∆= vap m 1.22811ln ()0.61068.314273.15283.15H ∆=- vap m 44.93 kJ/mol H ∆=m fus m vap m sub H H H ∆+∆=∆=+××-3= kJ/mol设时冰的饱和蒸汽压为p ,时水的饱和蒸汽压为1p ,则有:)15.248115.2731(314.8509306106.0ln -=p kPa 064.0=p)15.293115.2731(314.8449306106.0ln 1-=pkPa 35.21=p 相对湿度为:%72.2%10035.2064.0=⨯ 10.两个挥发性液体A 和B 构成一理想溶液,在某温度时溶液的蒸气压为,在气相中A 的摩尔分数为,液相中为,求此温度下纯A 和纯B 的蒸气压; 解:由题意知: **AA B A (1)p x p x p +-= *A A A y p x p= 将54.1kPa p =,65.0A =x ,A 0.45y =代入以上二式,得:*A37.45 kPa p =,*B 85.01 kPa p = 11.由甲苯和苯组成的某一溶液含30%质量分数的甲苯,在时纯甲苯和纯苯的蒸气压分别为和,设该溶液为理想溶液,问时溶液的总蒸气压和分压各为多少解:30920.26730709278x ==+甲苯 4.870.267 1.300 kPa p =⨯=甲苯15.76(10.267)11.55 kPa p =⨯-=苯p =12.在下,HNO 3、H 2O 系统的组成为:t/K 373 383 393 395 393 388 383 373 x HNO 3液 y HNO 1画出此系统的沸点组成图;2将3mol HNO 3和2mol H 2O 的混合气冷却到387K,互相平衡的两相组 成为何 相对量为多少3将3mol HNO 3和2mol H 2O 的混合物蒸馏,待溶液沸点升高了4K 时,整个馏出物的组成为若干4将3mol HNO 3和2mol H 2O 的混合物进行精馏,能得到什么纯物质解:1系统的沸点-组成图如图5-11:图5-11 HNO 3-H 2O 系统的沸点-组成图 图5-12 水-异丁醇系统的沸点-组成图 2由图可得:系统点组成、气相组成及液相组成分别为、及,则有:n g -=n l -gl 60540.199260n n -==- 34纯HNO 313.水和异丁醇的气液平衡相图如图5-12;1指出各个相区存在的相态及自由度;2组成为w 1的稀溶液精馏后,在塔顶和塔釜分别得到什么3能根据此相图设计合理的工业分馏过程,完全分离水和异丁醇吗 如果能,请写出大致的分离流程;解:1各区域的相态及自由度分别如下:a 区:气相g,f =2;b 区:液相l 1与气相g 两相共存,f =1;c 区:液相l 2与气相g 两相共存,f =1;d 区:液相l 1与液相l 2两相共存,f =1;e 区:液相l 1,f =2; f 区:液相l 2,f =2;2组成为w 1的稀溶液精馏后,在塔顶和塔釜分别得到恒沸混合物和水;3先将此混合液精馏,在塔釜中得到纯水后,将塔顶得到的恒沸物冷却使其进入液-液两相区,利用分液漏斗将两个液相分离得到水层及异丁醇层,再分别进行精馏,于是在塔釜分别得到纯水及异丁醇;如此进行下去,则可完全分离水和异丁醇;14.已知液体A 与液体B 可形成理想溶液,液体A 的正常沸点为,其摩尔气化热为35 kJ/mol;由2mol A 和8mol B 形成的溶液在标准压力#p 下的沸点为;将x B =的溶液置于带活塞的气缸中,开始时活塞紧紧压在液面上,在下逐渐减小活塞上的压力;求:1出现第一个气泡时系统的总压和气泡的组成;2当溶液几乎全部气化,最后仅有一小滴液体时液相的组成和系统的总压; 解:1设时A 和B 的饱和蒸气压分别为*A p 和*B p ,则有:*A 3500011ln ()101.3258.314338.15318.15p =- *A46.41 kPa p = 由**A A B B 101.325p x p x +=,得*B115.05 kPa p =出现第一个气泡时,液相的组成近似为原溶液的组成,即x B =, x A =,则:A A 46.410.40.211846.410.4115.050.6p y p ⨯===⨯+⨯ 0.78820.21181B =-=y**A A B B 87.61 kPa p p x p x =+=2当溶液几乎全部气化,最后仅有一小滴液体时,气相的组成与原溶液的组成相同,即:y A =,y B = 则有:*A A*B B A Bp x y p p x y p= 解得:x A =,x B =*B 46.410.623072.28kPa 0.4p ⨯== 15.水和乙酸乙酯是部分互溶的,设在,两相互呈平衡,其中一相含有%酯,而令一相含水%都是质量分数;设Raoult 定律适用于各相的溶剂,在此温度时纯乙酸乙酯的蒸气压为,纯水的蒸汽压是;试计算:1酯的分压;2水蒸气分压;3总蒸气压; 解:酯相:0.161883.79100183.79183.79=-+=水x x 酯=1-=p 酯=×水相:0.0146186.75100886.75886.75=-+=酯x x 水=1-=p 水=× =p =p 酯+p 水=16.若在合成某有机化合物之后进行水蒸气压蒸馏,混合物的沸腾温度为;实验时的大气压为,的水饱和蒸汽压为;馏出物经分离、称重,知水的质量分数为%;试估计此化合物的分子量;解:222*H OH O H O *B B B 0.450.55W p M W p M ==图5-13 某二元凝聚系统相图 图5-14 各点对应系统的步冷曲222*H OH O B B *B H Op M W M p W = 2**B H O 99.2084.5314.67 kPa p p p =-=-=B 84.53180.55127 g/mol 14.670.45M ⨯⨯==⨯ 17.某二元凝聚系统的相图如图5-13;1试绘出分别从a 、b 、c 、d 、e 各点开始冷却的步冷曲线;2说明混合物d 和e 在冷却过程中的相变化;解:1a 、b 、c 、d 、e 各点对应系统的步冷曲线分别见图5-14;2d →d 1为液态混合物的恒压降温过程,d 1点开始析出固态B,d 1→d 2为固态B 与溶液二相共存,d 2点为固态B 、固态E 和溶液三相共存,d 2→d 3为固态E 与溶液二相共存,d 3以后为固态A 与固态E 二相共存;e →e 1为液态混合物的恒压降温过程,e 1点开始析出固态B,e 1 →e 2为固态B 与溶液二相共存,e 2点为固态B 、固态E 和溶液三相共存,e 2点以后为固态E 的恒压降温过程;18.下表列出邻-二硝基苯和对-二硝基苯的混合物在不同组成时的熔点数%,w/w K %,w/w K100 4090 3080 2070 1060 0501绘制x T -图,并求最低共熔点混合物的组成;2如果系统的原始组成分别为含对-二硝基苯75%和45%,问用结晶法能从上述混合物中回收得到纯对-二硝基苯的最大百分数为若干解: 1T -x 图如图5-15;图5-15 邻-二硝基苯和对-二硝基苯系统的T-x 图图5-15 邻-二硝基苯和对-二硝基苯系统的T-x 图由上图可知最低共熔混合物的组成为含对位化合物%;2设含对位化合物75%和45%的系统,冷却结晶可得到纯对位化合物的最大百分数分别为x 、y ,则:%7.675.221005.2275=--=x %0.295.221005.2245=--=y 19.图5-16是FeO n -Al 2O 3相图;请指出各相区相态;图5-16 FeO n -Al 2O 3相图解:1区:液相区;2区:浮士体+液相;3区:尖晶石+液相;4区:浮士体;5区:浮士体+尖晶石;6区:尖晶石+液相;7区:刚玉+ 液相;8区:尖晶石;9区:刚玉;10区:尖晶石+刚玉;图5-17 KNO 3-NaNO 3-H 2O 的相图 图5-18 水-乙醚-甲醇三组分系统相图 20.图5-17是三组分系统KNO 3-NaNO 3-H 2O 的相图,实线是298K 时的相图,虚线是373K 下的相图;一机械混合物含70%的KNO 3及30%的NaNO 3,请根据相图拟定分离步骤;解:设含70%KNO 3、30%NaNO 3的系统点在BC 线上的D 点;在298K 时向该系统中加水使其沿DA 线向A 点移动,直至进入KNO 3固体与KNO 3、NaNO 3水溶液二相共存区,此时NaNO 3全部溶解,剩余的固体是KNO 3,但其中可能混有不溶性杂质,这时加热至373K,在该温度时,系统点位于液相区,在高温下过滤除去杂质,再将滤液冷却至298K,即有KNO 3的晶体析出;21.KNO 3-NaNO 3-H 2O 系统在278K时有一三相点,在这一点无水KNO 3和无水NaNO 3同时与一饱和溶液达平衡;已知此饱和溶液含KNO 3为%质量分数,含NaNO 3为%质量分数;如果有一70g KNO 3和30g NaNO 3的混合物,欲用重结晶方法回收KNO 3,试计算在278K 时最多能回收KNO 3多少克解:最多可回收KNO 3为:30700.090463.4g 0.4101-⨯= 22.某温度时在水、乙醚和甲醇的各种三元混合物中二液层的组成如下:甲醇%质量分数 0 10 20 30水%质量分数 液层1 93 82 70 45 液层2 1 6 15 40根据以上数据绘制三组分系统相图,并指出图中各区相态;解:由已知数据绘制的三组分系统的相图及各区相态见图5-18;。
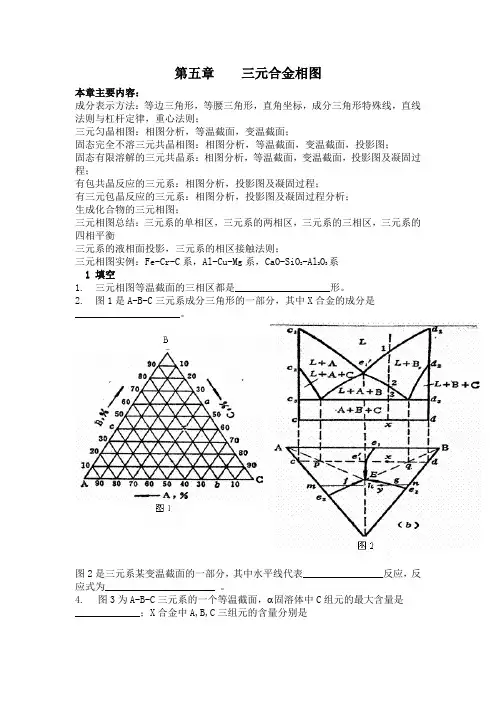
第五章三元合金相图本章主要内容:成分表示方法:等边三角形,等腰三角形,直角坐标,成分三角形特殊线,直线法则与杠杆定律,重心法则;三元匀晶相图:相图分析,等温截面,变温截面;固态完全不溶三元共晶相图:相图分析,等温截面,变温截面,投影图;固态有限溶解的三元共晶系:相图分析,等温截面,变温截面,投影图及凝固过程;有包共晶反应的三元系:相图分析,投影图及凝固过程;有三元包晶反应的三元系:相图分析,投影图及凝固过程分析;生成化合物的三元相图;三元相图总结:三元系的单相区,三元系的两相区,三元系的三相区,三元系的四相平衡三元系的液相面投影,三元系的相区接触法则;三元相图实例:Fe-Cr-C系,Al-Cu-Mg系,CaO-SiO2-Al2O3系1 填空1. 三元相图等温截面的三相区都是___________________形。
2. 图1是A-B-C三元系成分三角形的一部分,其中X合金的成分是_____________________。
图2是三元系某变温截面的一部分,其中水平线代表________________反应,反应式为______________________ 。
4.图3为A-B-C三元系的一个等温截面, 固溶体中C组元的最大含量是_____________;X合金中A,B,C三组元的含量分别是_____________________________;在X合金的相组成物中,α相的百分含量是______,δ相的百分含量是____________。
图4图315图4是Cu-Zn-Al三元相图2%Al的一个变温截面,合金凝固时,L+α+β三相区将发生____________反应。
图中X合金的化学成分是______________________。
6图5是某三元系变温截面的一部分,合金凝固时,L+M+C将发生_________________反应。
7 三元相图的成分用__________________________表示。


5.7 三元相图的应用举例5.7.1. CaO-Al2O3-SiO2系统三元相图具体的硅酸盐系统三元相图往往图形比较复杂。
我们首先以CaO-Al2O3-SiO2系统为例说明判读一张实际相图的步骤(见图5-42)。
本系统15个无变量点标于图中。
(1) 首先看系统中生成了多少化合物,找出各化合物的初晶区,根据化合物组成点与其初晶区的位置关系,判断化合物的性质。
本系统共有10个二元化合物,其中四个是一致熔化合物:CS、C2S、C12A7、A3S2,六个不一致熔化合物:C3S2、C3S、C3A、CA、CA2、CA6。
两个三元化合物都是一致熔的:CAS2(钙长石)及C2AS(铝方柱石)。
这些化合物的熔点或分解温度都标在相图上各自的组成点附近。
(2) 如果界线上未标明等温线,也未标明界线的温降方向,则需要运用连线规则,首先判明各界线的温度下降方向,再用切线规则判明界线性质。
然后,在界线上打上相应的单箭头或双箭头。
图5-42 CaO-Al2O3-SiO2系统三元相图(3) 运用重心规则判断各无变量点的性质。
如果在判断界线的性质时,已经画出了与各界线相对应的连线,则与无变量点相对应的副三角形已经自然形成了;如果先画出与各无变量点相对应的副三角形,则与各界线相对应的连线也会自然形成。
需要注意的是,不能随意在二个组成点之间连连线或在三个组成点间连副三角形。
如A3S2与CA组成点之间不能连连线,因为相图上这二个化合物的初晶区并无共同的界线,液相与这二个晶相并无平衡共存关系;在A3S2、CA、Al2O3的组成点间也不能连副三角形,因为相图上不存在这三个初晶区相交的无变量点,它们并无共同析晶的关系。
三元相图上的无变量点必定都处于三个初晶区,三条界线的交点,而不可能出现其它的形式,否则是违反相律的。
在一般情况下,有多少个无变量点,就可以将系统划分成多少个相应的副三角形(有时副三角形可能少于无变量点的数目)。
本系统共有15个无变量点,所以整个相图可以划分成15个副三角形。
在副三角形化以后,根据配料点所处的位置,运用三角形规则,就可以很容易地预先判断任一配料的结晶产物和结晶终点。
(4) 仔细观察相图上是否指示系统中存在晶型转变、液相分层或形成固溶体等现象。
本相图在富硅部分液相有分液区(2L),它是从CaO-SiO2二元的分液区发展而来的。
此外,在SiO2初晶区还有一条1470℃的方石英与鳞石英之间的晶型转变线。
CaO-Al2O3-SiO2系统与许多硅酸盐产品有关,其富钙部分相图与硅酸盐水泥生产关系尤为密切。
在这一部分相图上(图5-43),共有三个无变量点h、k、F,h、k是单转熔点,F 是低共熔点。
与这三个无变量点相对应的副三角形是CaO-C3A-C3S、C3S-C3A-C2S、C2S-C3A-C12A7。
用切线规则判断,CaO与C3S初晶区的界线在Z点从转熔界线变为共熔界线,而C3S与C2S初晶区的界线则在Y点从共熔性质变为转熔性质。
在Yk段,冷却时,L+C2S→C3S,即C2S被回吸,生成C3S。
但到达k点,L k+C3S→C2S+C3A,即C3S被回吸,生成C2S。
这个有趣的现象说明,系统从三相图进人四相图,是一种质的飞跃,而不是量的渐变,不能简单地从三相图关系类推四相图关系。
图5-43 CaO-Al2O3-SiO2系统的富钙部分相图我们以硅酸盐水泥熟料的典型配料,图上的点3为例,分析一下结晶路程。
将配料3加热到高温完全熔融(约2000℃),然后平衡冷却析晶,从熔体中首先析出C2S,液相组成沿C2S—3连线的延长线变化到C2S-C3S界线,开始从液相中同时析出C2S与C3S。
液相点随温度下降沿界线变化到Y点时,共析晶过程结束,转熔过程开始,C2S被回吸,析出C3S。
当系统冷却到k点温度(1455℃),液相点沿Yk界线到达k点,系统进入相图的无变量状态,L k液相与C3S晶体不断反应生成C2S与C3A。
由于配料点处于三角形C3S-C3A-C2S内,最后L k首先耗尽,结晶过程在k点结束。
获得的结晶产物是C3S、C3A、C2S。
下面我们就硅酸盐水泥生产中的配料、烧成及冷却,结合相图加以讨论,以提高利用相图分析实际问题的能力。
(1) 硅酸盐水泥的配料硅酸盐水泥熟料中含有C3S、C3A、C2S、C4AF四种矿物,相应的组成氧化物为CaO、SiO2、Al2O3、Fe2O3。
因为Fe2O3含量较低(2%~5%),可以合并入Al2O3一并考虑,C4AF则相应计入C3A,这样可以用CaO-Al2O3-SiO2三元来表示硅酸盐水泥的配料组成。
根据三角形规则,配料点落在何副三角形中,最后析晶产物便是这个副三角形三个角顶所表示的三种晶相。
图中1点配料处于三角形CaO-C3A-C3S中,平衡析晶产物中将有游离CaO。
2点配料处于三角形C2S-C3A-C12A7内,平衡析晶产物中将有C12A7,而没有C3S,前者的水硬活性很差,而后者是水泥中最重要的水硬矿物。
因此,这二种配料都不符合硅酸盐水泥熟料矿物组成的要求。
硅酸盐水泥生产中熟料的实际组成是含62%~67%CaO,20%~24% SiO2,6.5%~13%( Al2O3+Fe2O3),即在三角形C3S-C3A-C2S内的小圆圈内波动。
从相图的观点看,这个配料是合理的,因为最后析晶产物都是水硬性能良好的胶凝矿物。
以C3S-C3A-C2S 作为一个浓度三角形,根据配料点在此三角形中的位置,可以读出平衡析晶时水泥熟料中各矿物的含量。
(2) 烧成工艺上不可能将配料加热到2000℃左右完全熔融,然后平衡冷却析晶。
实际上是采用部分熔融的烧结法生产熟料。
因此,熟料矿物的形成并非完全来自液相析晶,固态组分之间的固相反应起着更为重要的作用。
为了加速组分间的固相反应,液相开始出现的温度及液相量至关重要。
如果是非常缓慢的平衡加热,则加热熔融过程应是缓慢冷却平衡析晶的逆过程,且在同一温度下,应具有完全相同的平衡状态。
以配料3为例,其结晶终点是k点,则平衡加热时应在k点出现与C3S、C3A、C2S平衡的L k液相,但C3S很难通过纯固相反应生成(如果很容易,水泥就不需要在1450℃的高温下烧成了),在1200℃以下组分间通过固相反应生成的是反应速度较快的C12A7、C3A、C2S。
因此,液相开始出现的温度并不是k点的1445℃,而是与这三个晶相图的F点温度1335℃(事实上,由于工艺配料中含有Na2O、K2O、MgO 等其它氧化物,液相开始出现的温度还要低,约1250℃)。
F点是一个低共熔点,加热时C2S+C12A7+C3A→L F,即C12A7、C3A、C2S低共熔形成F点液相。
当C12A7熔完后,液相组成将沿Fk界线变化,升温过程中,C3A与C2S继续熔入液相,液相量随温度升高不断增加。
系统中一旦形成液相,生成C3S的固相反应:C2S+CaO→C3S的反应速度即大大增加。
从某种意义上说,水泥烧成的核心问题是如何创造良好的动力学条件促成熟料中的主要矿物C3S 的大量生成。
C12A7是在非平衡加热过程中在系统中出现的一个非平衡相,但它的出现降低了液相开始形成的温度,对促进热力学平衡相C3S的大量生成是有帮助的。
(3) 冷却水泥配料达到烧成温度时所获得的液相量约20%~30%。
在随后的降温过程中,为了防止C3S分解及β-C2S发生晶型转化,工艺上采取快速冷却措施,而不是缓慢冷却,因而冷却过程也是不平衡的。
这种不平衡的冷却过程可以用下面二种模式来加以讨论。
①急冷:此时冷却速度超过熔体的临界冷却速度,液相完全失去析晶能力,全部转变为低温下的玻璃体。
②液相独立析晶:如果冷却速度不是快到使液相完全失去析晶能力,但也不是慢到足以使它能够和系统中其它晶相保持原有的相图关系,则此时液相犹如一个原始配料的高温熔体那样独自析晶,重新建立一个新的平衡体系,不受系统中已存在的其它晶相的制约。
这种现象特别容易发生在转熔点上的液相。
譬如在k点,L k+C3S→C2S+C3A,生成的C2S和C3A 往往包裹在C3S的表面,阻止了L k与C3S的进一步反应,此时液相将作为一个原始熔体开始独立析晶,沿kF界线析出C2S和C3A,到F点后又有C12A7析出。
因为k点在三角形C2S-C3A-C12A7内,独立析晶的析晶终点必在与其相应的无变量点F。
因此,在发生液相独立析晶时,尽管原始配料点处在三角形C3S-C3A-C2S内,其最终获得的产物中可能有四个晶相,除了C3S、C3A、C2S外,还可能有C12A7,这是由过程的非平衡性质造成的。
由于冷却时在k点发生L k+C3S→C2S+C3A的转熔过程,C3S要消耗,如在k点发生液相独立析晶或急冷成玻璃体,可以阻止这一转熔过程。
因此,对某些硅酸盐水泥配料,快速冷却反而可以增加熟料中C3S的含量。
必须指出,所谓急冷成玻璃体或发生液相独立析晶,这不过是非平衡冷却过程的二种理想化了的模式,实际过程很可能比这二种理想化模式更复杂,或者二者兼而有之。
5.7.2.K2O-Al2O3-SiO2系统三元相图本系统有五个二元化合物及四个三元化合物。
在这四个三元化合物的组成中,K2O含量与Al2O3含量的比值是相等的,因而它们排列在一条SiO2与二元化合物K2O·Al2O3的连线上(图5-44)。
三元化合物钾长石KAS6(图中的W点)是一个不一致熔化合物,其分解温度较低,在1150℃即分解为KAS4和富硅液相(液相量约为50%),因而是一种熔剂性矿物。
白榴石KAS4(图中的X点)是一致熔化合物,熔点1686℃。
钾霞石KAS2(图中的Y点)也是一个一致熔化合物,熔点1800℃。
化合物KAS(图中的Z点)的性质迄今未明,其初晶区的范围尚未能予以确定。
由于K2O高温下易于挥发等实验上的困难,本系统的相图不是完整的,仅给出了K2O含量在50%以下部分的相图。
图中的M点和E点是二个不同的无变量点。
M点处于莫来石、鳞石英和钾长石三个初晶区的交点,是一个三元无变量点,按照重心规则,它是一个低共熔点(985℃)。
M点左侧的E点是鳞石英和钾长石初晶区界线与相应的连线SiO2-W的交点,是该界线上的温度最高点,也是鳞石英与钾长石的低共熔点(990℃)。
图5-44 K2O-Al2O3-SiO2系统三元相图本系统与日用陶瓷及普通电瓷生产密切相关。
日用陶瓷及普通电瓷一般用粘土(高岭土)、长石和石英配料。
高岭土的主要矿物组成是高岭石Al2O3·2SiO2·2H2O,煅烧脱水后的化学组成为Al2O3·2SiO2,称为烧高岭。
图5-45上的D点即为烧高岭的组成点,D点不是相图上固有的一个二元化合物组成点,而是一个附加的辅加点,用以表示配料中的一种原料的组成。
根据重心原理,用高岭土、长石、石英三种原料配制的陶瓷坯料组成点必处于辅助三角形QWD(常被称为配料三角形)内,而在相图上则是处于副三角形QWm(常称为产物三角形)内。