盐酸法舒地尔注射液稳定性研究试验
- 格式:pdf
- 大小:438.62 KB
- 文档页数:1



盐酸法舒地尔注射液治疗糖尿病周围神经病变疗效观察摘要目的:从电生理学角度探讨盐酸法舒地尔注射液的组织保护机制。
方法:采用肌电图仪检测38名糖尿病在周围神经病变患者应用盐酸法舒地尔治疗前后腓总神经、胫神经传导速度变化。
结果:治疗前后临床疗效比较有显著性差异(P<0.01),腓总神经、胫神经传导速度比较差异有显著性(P<0.05)。
结论:盐酸法舒地尔治疗糖尿病周围神经病变疗效确切,并从电生理学角度再次证实盐酸法舒地尔注射液的组织保护作用。
关键词盐酸法舒地尔糖尿病周围神经病变神经传导速度本研究应用肌电图检测患者治疗前、后神经传导速度的改变,观察盐酸法舒地尔注射液对38名糖尿病周围神经病变患者的疗效,旨在为糖尿病周围神经病变患者提供新的药物治疗手段,并从电生理角度初步探讨盐酸法舒地尔注射液的组织保护机理。
资料与方法2008年8月~2010年8月收治糖尿病患者38例。
诊断标准按照世界卫生组织(WHO)1999年公布的糖尿病诊断标准;糖尿病周围神经病变采用国内常用标准,糖尿病有下列表现之一者可以诊断为糖尿病周围神经病变:①肢体感觉减退、运动神经病变表现为麻木、疼痛、蚁行感、发凉,肌无力等;②深浅感觉明显减退,跟、膝腱反射明显减退或消失;③肌电图示神经(腓总、胫)传导障碍,运动神经传导速度<45m/秒,感觉神经传导速度<40m/秒;④排除慢性酒精中毒、骨质增生、金属中毒、药源性多发性周围神经炎引起的周围神经损害。
病例。
方法:所有病例均予严格控制饮食及口服降糖药物或用胰岛素治疗,将血糖控制在正常范围之内。
在此基础上,均给予盐酸法舒地尔注射液30mg,加入0.9%氯化钠250ml静脉点滴;1次/日,2周为1个疗程,随后观察临床症状体征的变化,采用上海产NTS-2000肌电图仪测定腓总神经、胫神经传导速度。
治疗期间未用其他治疗神经病变、抗血小板、抗凝、纤溶及非甾体类药物等。
统计学处理:治疗前后所得数值采用均数±标准差(X±S)表示,结果采用t检验,以P<0.05为差异有显著性意义。

盐酸法舒地尔注射液工艺验证概述盐酸法舒地尔注射液是一种新型抗心律失常药物,该药物通过改变心肌细胞膜的离子通道激活状态,以增加心脏对抗心律失常的耐受性。
本文将介绍盐酸法舒地尔注射液的工艺验证,包括工艺过程设计、工艺可行性分析和工艺验证实验过程。
工艺设计盐酸法舒地尔注射液的工艺设计是指针对该药物的性质和特点,设计出符合药品质量标准和临床使用要求的工艺流程和方法。
一般来说,药品的工艺设计需要从以下几个方面考虑:原料准备盐酸法舒地尔注射液的原料主要有舒地尔和盐酸。
这些原料需要严格按照药品质量标准进行采购,并进行充分的质量检验和检测。
在原料准备环节中,需要注意保持原料的品质和纯度,并对原料进行适量的调配。
工艺参数确定在工艺参数的确定环节中,需要选择合适的溶剂、剂量、温度、pH值等关键工艺参数,通过充分的试验和实践确定最佳的工艺参数组合。
此外,需要在确定工艺参数时考虑到药品的可溶性、稳定性、吸收性等因素。
工艺流程设计工艺流程设计是指将上述准备工作汇总,确定由原料准备、混合、过滤、灭菌、灌装等环节组成的工艺流程,并在流程中合理设置关键控制点。
在流程设计中,需要注意流程的合理性、可操作性和质量控制要点的设置。
工艺可行性分析在工艺设计完成后,需要进行工艺可行性分析。
该分析主要包括可操作性分析、安全性评估和经济性分析。
在可操作性分析中,需要评估工艺流程是否简单、易于控制,以及是否符合操作人员的工作习惯;在安全性评估中,需要评估工艺流程是否安全,是否存在风险,以及制定适当的安全措施;在经济性分析中,则需要评估工艺流程的成本,以及是否具有经济价值。
工艺验证实验过程在完成以上工作后,需要进行工艺验证实验。
验证实验包括初步性验证、正式验证和最终验证三个阶段。
初步性验证是指对工艺流程的初步实验验证,主要是为了检测所设计的工艺流程是否可行和有效。
正式验证是在初步性验证验证成功后,对工艺流程进行进一步的验证。
最终验证则是为了确定工艺流程的最终可行性和稳定性。


Vol.5 No.1Feb. 2019生物化工Biological Chemical Engineering第 5 卷 第 1 期2019 年 2 月盐酸法舒地尔注射液的处方与工艺优化研究魏小亮1,2,3,张玉莉3,李学彩4,李文强3(1.陕西国际商贸学院,陕西咸阳 712000;2.陕西省中药绿色制造技术协同创新中心,陕西咸阳 712000; 3.陕西步长制药有限公司,陕西咸阳 712000;4.通化谷红制药有限公司,吉林通化 134000)摘 要:目的:对盐酸法舒地尔注射液的处方及工艺进行优化,筛选出最佳的处方与工艺。
方法:通过考察盐酸法舒地尔注射液的pH、渗透压、性状、含量及有关物质,得到最优的处方与工艺。
结果:本品最优处方为氯化钠用量0.8%,最优pH值为5.0~6.5,最优灭菌工艺为121 ℃灭菌15 min。
本品放置在室温12个月,各项检测指标均在合格的范围内。
结论:本品处方设计合理,工艺可行,质量稳定。
关键词:盐酸法舒地尔注射液;处方与工艺;稳定性中图分类号:R943 文献标志码:AStudy on Formulation and Process Optimization of Fasudil Hydrochloride InjectionWei Xiao-liang1,2,3, Zhang Yu-li3, Li Xue-cai4, Li Wen-qiang3(1.Shaanxi Institute of International Commerce and Trade, Shaanxi Xianyang 712000; 2.Shaanxi Center for Cooperative Innovation of Green Manufacturing Technology of Traditional Chinese Medicine, Shaanxi Xianyang 712000; 3.Shaanxi Buchang Pharmaceutical Co., Ltd., Shaanxi Xianyang 712000; 4. Tonghua Guhong Pharmaceutical Co., Ltd., Jilin Tonghua 134000)Abstract: Objective: To optimize the formulation and process of fasudil hydrochloride injection and select the best formulation and process. Methods: Investigated the pH, osmotic pressure, properties, content and related substances of fasudil hydrochloride injection, the optimal prescription and process were obtained. Results: The optimal prescription was 0.8% sodium chloride, pH 5.0~6.5, and the optimal sterilization process was 121 ℃ for 15 minutes. This product is placed at room temperature for 12 months, and all the detection indicators are within the qualified range. Conclusion: The formulation is reasonable, the process is feasible and the quality is stable.Key words : Fasudil hydrochloride injection; Formulation and technology; Stability盐酸法舒地尔注射液为无色澄明液体,是新一代拮抗钙离子的血管扩张剂,为异喹啉磺胺类衍生 物[1],可舒张血管平滑肌、扩张血管,临床试验证实,该药可用于治疗急性缺血性中风、脑血管病和心绞痛后遗症[2]。


盐酸法舒地尔注射液细菌内毒素检查方法学研究摘要】目的:建立盐酸法舒地尔注射液细菌内毒素检查的方法学研究。
方法:参照2010 年版《中国药典(二部)》细菌内毒素检查法进行试验。
结果:样品经稀释后对内毒素检查无干扰,将细菌内毒素限值定为0.5EU/ml,可以选择灵敏度0.25Eu/ml 的鲎试剂进行内毒素检查。
结论:样品在最大稀释倍数内对内毒素检查无干扰。
【关键词】盐酸法舒地尔注射液;细菌内毒素检查法干扰试验盐酸法舒地尔是一种蛋白激酶抑制剂即细胞内钙离子拮抗剂。
改善及预防蛛网膜下腔出血术后的脑血管痉挛及随之引起的脑缺血症状。
国际医学专家在病理研究中发现,抑制患者组织内的Rho 激酶异常活跃是治疗心脑血管疾病的关键,成为国际上的研究热点,盐酸法舒地尔注射液是国际上唯一一个已经上市的Rho 激酶抑制剂,由日本旭化成制药株式会社研制成功,1995 年6 月在日本上市,商品名为“依立卢”,规格2ml:30mg。
盐酸法舒地尔注射液在我国研究起步于1997 年,天津市药物研究院和天津红日药业公司合作研究,并获得国家科技部科技型企业创新基金支持,于2004 年获得了国家二类新药证书,商品名“川威”。
目前国内标准[1]采用家兔法进行热原检查,由于细菌内毒素检查法具有灵敏、快速、操作简便、结果准确等优点。
因此我们参考《中国药典(二部)》细菌内毒素检查法[2],对盐酸法舒地尔注射液进行细菌内毒素检查的可行性进行研究,报道如下。
1.实验材料及仪器鲎试剂:湛江安度斯生物有限公司生产,批号:1010112(灵敏度0.25EU/ml,规格0.1ml)、批号:1008202(灵敏度0.125EU/ml,规格0.1ml)。
细菌内毒素检查用水:湛江安度斯生物有限公司生产,批号1005240,规格5ml。
细菌内毒素工作标准品:批号201070,效价120EU/支,中国药品生物制品检定所生产。
旋涡混合器:XW-80A 型,厂家:上海医大仪器厂。

0引言盐酸法舒地尔是异喹啉磺胺衍生物,能抑制细胞内游离钙离子的活动,还能抑制蛋白激酶A、G、C 和肌球蛋白轻链激酶,即抑制平滑肌收缩最终阶段的肌球蛋白轻链磷酸化,使血管平滑肌舒张,扩张血管。
用于蛛网膜下腔出血后脑血管痉挛引起的缺血性脑血管疾病症状的改善。
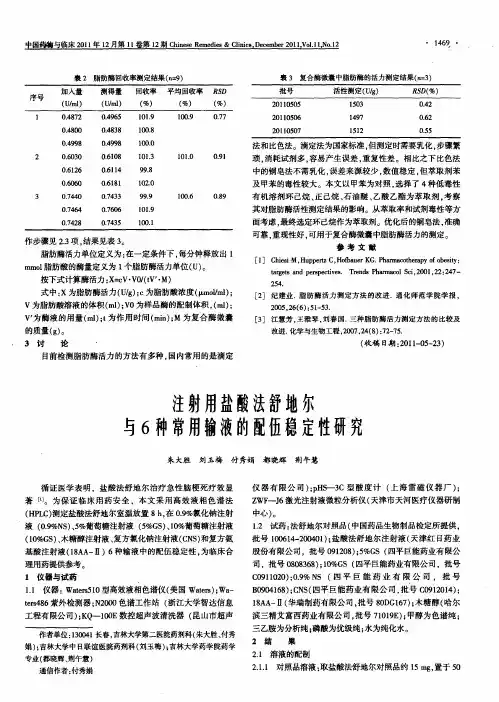
为了观察盐酸法舒地尔注射液制剂的用药安全,按照国家SFDA颁发的《化学药物刺激性、过敏性和溶血性研究技术指导原则》,进行了实验兔血管刺激性、肌肉刺激性、溶血性盐酸法舒地尔注射液局部用药安全评价试验研究ExperimentforLocalDrugSecurityEvaluationofFasudilHydrochlorideInjection张俊明丁琦王丽华李良郑国安徐丽瑛Zhang Junming Ding Qi Wang Lihua Li Liang Zheng Guoan Xu Liying(江西省药物研究所,江西南昌330029)(Jiangxi Institute of Mater Medica,Jiangxi Nanchang330029)摘要:目的:研究盐酸法舒地尔注射液局部用药的安全性。
方法:按照国家SFDA颁发的《化学药物刺激性、过敏性和溶血性研究技术指导原则》进行了局部血管刺激性、肌肉刺激性、溶血性和全身主动过敏性试验。
结果:①盐酸法舒地尔注射液耳缘静脉点滴给药浓度为0.3mg/ml,给药容积为2.0ml/kg,对试验兔血管无刺激性;②盐酸法舒地尔注射液肌肉注射给药浓度为15mg/ml,给药容积为0.5ml/只时,对试验兔肌肉无刺激性;③盐酸法舒地尔注射液药物浓度为0.3mg/ml,在体外试验条件下无溶血反应及红细胞凝聚反应;④盐酸法舒地尔注射液致敏剂量为1.5和4.5mg/kg,激发剂量为3.0和9.0g/kg时,对豚鼠无主动全身过敏性反应,与阴性对照组比较,差异无显著性意义(p>0.05)。
结论:盐酸法舒地尔注射液试验条件下无血管和肌肉刺激性、无溶血性及过敏性反应。

盐酸法舒地尔治疗不稳定性心绞痛60例临床观察目的探讨盐酸法舒地尔治疗不稳定性心绞痛的临床效果。
方法选择笔者所在医院2009年2月~2011年2月不稳定型心绞痛患者120例,将上述患者随机分为观察组和对照组。
两组患者入院后均行心电监护,患者出现不适随时描记心电图。
均给予硝酸酯类药物、抗血小板类药物、抗凝药物、他汀类调脂药等常规治疗,心绞痛发作时舌下含化硝酸甘油。
对照组采用以上常规治疗。
观察组在对照组治疗基础上给予法舒地尔注射液静脉滴注。
两组患者均治疗14 d。
结果观察组总有效率为95.0%,对照组总有效率为76.7%,两组总有效率比较,差异有统计学意义(P<0.05)。
结论盐酸法舒地尔能够显著改善不稳定性心绞痛临床症状和体征,提高临床治疗效果,值得借鉴。
标签:不稳定型心绞痛;法舒地尔不稳定性心绞痛是介于稳定性心绞痛和急性心肌梗死之间的一种临床状态,容易发作为急性心肌梗死,甚至猝死。
所以需要临床及时控制病情,防止发生急性心肌梗死。
盐酸法舒地尔能够抑制平滑肌收缩的最终阶段肌球蛋白轻链的磷酸化从而扩张血管。
本研究观察盐酸法舒地尔治疗不稳定性心绞痛的临床效果,现报道如下。
1资料与方法1.1一般资料选择笔者所在医院2009年2月~2011年2月不稳定型心绞痛患者120例,同时排除严重心律失常、肝肾功能障碍、不愿意参加本试验的患者。
将上述患者随机分为观察组和对照组。
观察组60例,其中男34例,女26例,平均年龄(55.3±4.9)岁,心绞痛类:初发劳累型心绞痛患者33例;恶化型心绞痛患者20例;自发型心绞痛患者7例。
合并慢性疾病:高血压21例;糖尿病6例;高脂血症8例。
对照组60例,其中男35例,女25例,平均年龄(54.7±5.8)岁,心绞痛类:初发劳累型心绞痛患者34例;恶化型心绞痛患者21例;自发型心绞痛患者5例。
合并慢性疾病:高血压20例;糖尿病6例;高脂血症9例。
两组患者性别、年龄、心绞痛分类、合并疾病等一般资料比较,差异无统计学意义(P >0.05),具有可比性。
法舒地尔治疗2型糖尿病并稳定型心绞痛的临床观察摘要】目的评价法舒地尔注射液对2型糖尿病并稳定型心绞痛患者的临床疗效。
方法 86例2型糖尿病并稳定型心绞痛患者,随机分为常规治疗组(45例)和法舒地尔组(41例)。
常规治疗相应用阿司匹林/氯化格雷、β阻滞剂、ACEL,他汀类药物等冠心病二级预防措施,法舒地尔组有常规治疗基础上回用法舒地尔注射液60mg加入生理盐水250ml静脉滴注,每日2次,共治疗14天,随访期间病史及行运动平板检查。
结果 86例患者全部完成随访,没有患者出现药物不良反应需要停药。
A组胸痛发作每周次数减少4.2士0.5次,而B组减少2.1士0.8次,两组相比有统计学差异(P<0.05)。
并且在硝酸甘油消耗量、运动平板持续时间增加、运动至ST段下移1mm的时间延长、运动至ST段压低的最大幅度减少等方面法舒地尔均较常规治疗组效果显著(P<0.05)。
结论法舒地尔可以改善2型糖尿病并稳定型心绞痛患者生活质量,提高运动耐量县安全性好。
【关键词】法舒地尔稳定性型心绞痛 2型糖尿病运动平板试验法舒地尔1 材料与方法1.1病例选择2000年1月至2010年3月间共入选86例稳定型心绞痛合并2型糖尿病患者,随机可分为常规口服药物治疗组(A组,45例)和治疗组(B 组,41例),B组在常规冠心病二级预防口服药物的基础上加法舒地尔注射液(商品名:川威60mg加入生理盐水250ml静脉滴注每日2次,连用14天。
在入组4周内门诊随访,询问病史及行活动平板检查。
其中男46例,女40例,入选年龄平均57士9.8岁(46-72岁),根据患者病情特点服用冠心病二级预防常规抗心绞痛药物如他汀类、阿司匹林或氯吡格雷、β受体阻滞剂或钙离子拮抗剂以及硝酸酯类等。
排除单纯药物控制不理想仍有心绞痛发作以及血糖控制不理想的患者,合并有其他肝肾功能异常的患者以及6个月内接受过冠状动脉内支架置入术的患者。
两组患者基础资料相比无统计学差异(P<0.05),详见表1项目 A组(45例) B组(41例) X2(t) P性别男 25 21 2.01 0.07女 20 20 4.31 0.11年龄 58.7士3.5 57.3士5.8 3.45(t)>0.05FBG(mmol/L) 8.3士1.3 8.6士2.2 4.91 0.17GhbAlc(%) 7.8士1.9 8.3士2.1 3.76 0.21高危因素高血压 10 11 4.33 0.07吸烟 6 7 2.75 0.24外周血管病变 3 4 1.67 0.43家族史 5 4 2.97 0.28两组两两分别相比较均无统计学意义,P>0.05。
盐酸法舒地尔注射液与果糖注射液配伍的稳定性考察
徐梅;韩强
【期刊名称】《中国医院用药评价与分析》
【年(卷),期】2012(012)009
【摘要】目的:考察盐酸法舒地尔注射液在室温[(25±2)℃]下与果糖注射液配伍的稳定性.方法:模拟临床用药浓度将盐酸法舒地尔注射液加入果糖注射液中,混合均匀后,在室温[(25±2)℃]下观察并测定6h内配伍液的外观和pH值变化,采用高效液相色谱法测定法舒地尔的含量,并考察是有无新物质生成.结果:在室温[(25±2)℃]条件下,0~6h配伍液的外观、pH值、盐酸法舒地尔的含量均无明显变化.结论:盐酸法舒地尔注射液与果糖注射液配伍,在室温[(25±2)℃]下6h内配伍液稳定.
【总页数】3页(P814-816)
【作者】徐梅;韩强
【作者单位】徐州医学院附属医院药剂科,江苏徐州221002;徐州医学院附属医院药剂科,江苏徐州221002
【正文语种】中文
【中图分类】R969.2
【相关文献】
1.果糖注射液与5种中药注射剂配伍稳定性考察 [J], 汪怡
2.硫辛酸注射液与木糖醇和果糖注射液的配伍稳定性考察 [J], 甘惠贞;林淑瑜;潘丹婷;杨昌云
3.注射用万古霉素和去甲万古霉素与5%果糖注射液的配伍稳定性考察 [J], 李好;熊建华
4.丰海能果糖注射液与14种中药注射液配伍的稳定性考察 [J], 余黎;朱荃
5.左乙拉西坦注射液在果糖注射液等5种输液中的配伍稳定性考察 [J], 马晓黎;宋艳霞;李直
因版权原因,仅展示原文概要,查看原文内容请购买。
盐酸法舒地尔注射液影响因素试验及其光降解产物的液相色谱-质谱分析湛常娟;冯汉林;严启新;刘小柔;叶勤【期刊名称】《安徽中医学院学报》【年(卷),期】2013(032)002【摘要】Objective To investigate the influencing factors for the quality of Fasudil Hydrochloride Injection and identify its photodegradation product. Methods Fasudil Hydrochloride Injection was put at high temperature and under illumination. The photodegradation product of Fasudil Hydrochloride Injection was identified by liquid chro-matography-mass spectrometry. Results Fasudil Hydrochloride Injection was stable at high temperature, but produced isoquinoline-5-sulfonic acid as an impurity under illumination. Conclusion Fasudil Hydrochloride Injection is stable at high temperature, but it is unstable under illumination, with isoquinoline-5-sulfonic acid as a photodegradation product. Fasudil Hydrochloride Injection should be kept in the dark.%目的考察盐酸法舒地尔注射液的影响因素并鉴定其光降解产物.方法对盐酸法舒地尔注射液进行高温、光照处理,并用液相色谱-质谱联用技术鉴定其光降解产物.结果盐酸法舒地尔注射液高温条件下稳定,光照条件下产生一光降解杂质异喹啉-5-磺酸.结论盐酸法舒地尔注射液在高温条件下稳定,在光照条件下不稳定,应避光保存,光降解杂质为异喹啉-5-磺酸.【总页数】4页(P83-86)【作者】湛常娟;冯汉林;严启新;刘小柔;叶勤【作者单位】广东省深圳海王药业有限公司,广东,深圳,517058【正文语种】中文【中图分类】R92【相关文献】1.液相色谱-质谱/质谱联用技术分析固相合成奈米非肽及其副产物 [J], 金苗;朱颐申;张琪;屠春燕2.中药复方“清开灵”注射液中胆酸类物质的液相色谱/质谱/质谱分析 [J], 刘国文;刘密新;吴筑平;杨成对;罗国安3.超高效液相色谱-串联四极杆飞行时间质谱和超高效液相色谱-串联三重四极杆质谱用于血浆中苦杏仁苷及其代谢产物野黑樱苷的定性和定量分析 [J], 高萌;王跃生;魏惠珍;欧阳辉;何明珍;曾恋情;申峰云;郭强;饶毅4.超高效液相色谱-高分辨质谱联用技术分析地芬尼多代谢产物 [J], 王灵;侯建平5.柱前衍生-液相色谱-串联质谱法测定环境水体中草甘膦及其代谢产物的影响因素研究 [J], 董建芳;董会军;李义;赵峰;马天翼;刘雪瑜因版权原因,仅展示原文概要,查看原文内容请购买。