盐酸法舒地尔说明书
- 格式:doc
- 大小:24.00 KB
- 文档页数:2
盐酸法舒地尔注射液说明书盐酸法舒地尔注射液,适应症为改善和预防蛛网膜下腔出血术后的脑血管痉挛及引起的脑缺血症状。
警示语本品只可静脉点滴使用,不可采用其它途径给药。
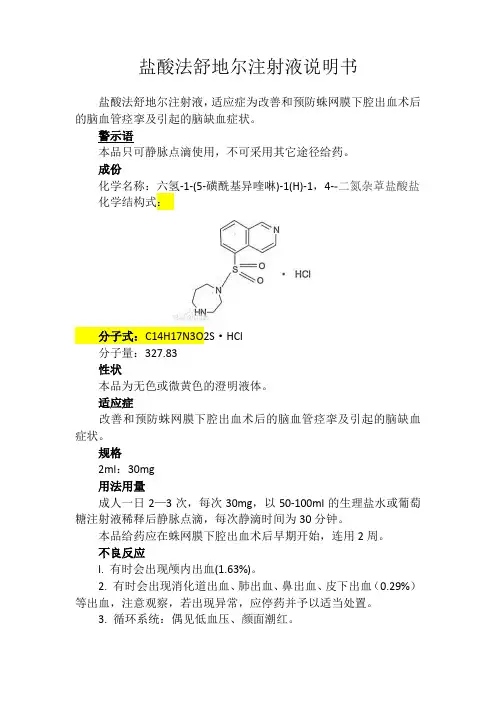
成份化学名称:六氢-1-(5-磺酰基异喹啉)-1(H)-1,4--二氮杂䓬盐酸盐化学结构式:分子式:C14H17N3O2S·HCl分子量:327.83性状本品为无色或微黄色的澄明液体。
适应症改善和预防蛛网膜下腔出血术后的脑血管痉挛及引起的脑缺血症状。
规格2ml:30mg用法用量成人一日2—3次,每次30mg,以50-100ml的生理盐水或葡萄糖注射液稀释后静脉点滴,每次静滴时间为30分钟。
本品给药应在蛛网膜下腔出血术后早期开始,连用2周。
不良反应l. 有时会出现颅内出血(1.63%)。
2. 有时会出现消化道出血、肺出血、鼻出血、皮下出血(0.29%)等出血,注意观察,若出现异常,应停药并予以适当处置。
3. 循环系统:偶见低血压、颜面潮红。
4. 血液系统:偶见贫血、白细胞减少、血小板减少。
5. 有时会出现肝功能异常。
AST(GOT)、ALT(GPT)、ALP、LDH 升高等。
6. 泌尿系统:偶见肾功能异常(BUN、肌酐升高等)、多尿。
7. 消化系统:腹胀、恶心、呕吐等较少见。
8. 过敏症:偶见皮疹等过敏症状。
9. 其他:发热(偶见)、头痛、意识水平低、呼吸抑制(少见)。
禁忌下述患者禁用本品:1.出血患者:颅内出血。
2. 可能发生颅内出血的患者:术中对出血的动脉瘤未能进行充分止血处置的患者。
3. 低血压患者。
注意事项1. 本品只可静脉点滴使用,不可采用其它途径给药(下述患者应慎重用药);(1)术前合并糖尿病的患者、术中在主干动脉有动脉硬化的患者,使用本剂时,应充分观察临床症状及计算机断层摄影,若发现颅内出血,应速停药并予以适当处置;(2)肾功能障碍的患者(例如,1次10 mg);(3)肝功能障碍的患者(有可能延迟代谢,使血药浓度升高而增强作用);(4)严重意识障碍的患者(使用经验少,尚未确立有效性);(5)70岁以上的高龄患者(对预后功能的改善可能无效,尚未确立有效性);(6)蛛网膜下腔出血合并重症脑血管障碍(烟雾病、巨大脑动脉瘤等)的患者(无使用经验,尚未确立有效性及安全性)。


盐酸法舒地尔对糖尿病性肾病的保护作用研究聂荣杰;张波【期刊名称】《中国生化药物杂志》【年(卷),期】2014(000)005【摘要】目的探讨盐酸法舒地尔对糖尿病肾病的保护作用机制.方法动物实验分为空白对照组,糖尿病肾病模型组,盐酸法舒地尔实验组.给大鼠注射60 mg/kg链脲佐菌素(streptozocin,STZ)建立糖尿病肾病模型,盐酸法舒地尔实验组持续注射12周盐酸法舒地尔.检测3组大鼠尿蛋白量、尿素氮(blood urea nitrogen,BUN)、血肌酐(serum creatine,Scr)的含量.分子细胞实验分为4组:空白对照组(5.5 mmol/L的葡萄糖),高张组(5.5 mmol/L葡萄糖+54.5 mmol/L甘露醇),高糖模型组(60 mmol/L的葡萄糖),盐酸法舒地尔实验组(60 mmo/L的葡萄糖+20 μmol/L 的盐酸法舒地尔).高糖培养HK-2细胞并观察其Rho A活性,采用免疫荧光技术和Western blot分别检测各处理组HK-2细胞中上皮钙黏素与α-SMA的表达.结果盐酸法舒地尔实验组大鼠24 h尿蛋白量、血BUN及Scr明显低于糖尿病肾病模型组,差异有统计学意义(P<0.01);60 mmol/L的葡萄糖能提高HK-2细胞中Rho A活性,4h最高,与0h相比差异有统计学意义(P<0.01).盐酸法舒地尔实验组中上皮钙黏素表达量明显高于高糖模型组,差异有统计学意义(P<0.01).盐酸法舒地尔实验组中α-SMA表达量明显低于高糖模型组,差异有统计学意义(P<0.01).结论动物实验与分子水平实验结果表明盐酸法舒地尔对糖尿病肾病具有保护作用,其可能通过抑制肾纤维化而实现保护作用.【总页数】4页(P66-68,71)【作者】聂荣杰;张波【作者单位】海口市人民医院内分泌科,海南海口570100;南京医科大学医学科学部,江苏南京210029【正文语种】中文【中图分类】R246.3【相关文献】1.盐酸法舒地尔对心肌缺血/再灌注损伤的心肌保护作用 [J], 侯凤霞;鲁硕(综述);郑晓群(审校)2.盐酸法舒地尔对急性前壁心肌梗死病人心肌的保护作用 [J], 曲军;王真;王术浩3.盐酸法舒地尔对体外培养星形胶质细胞氧糖剥夺损伤的保护作用 [J], 孙莉;赵燕;陈诚;郭莲军;陈玉华4.盐酸法舒地尔对维持性血液透析患者血管内皮功能的保护作用 [J], 张成果5.盐酸法舒地尔对脂多糖致大鼠大脑皮质神经元损伤的保护作用及机制研究 [J], 何昕;张博爱;贾延劼;王继先因版权原因,仅展示原文概要,查看原文内容请购买。




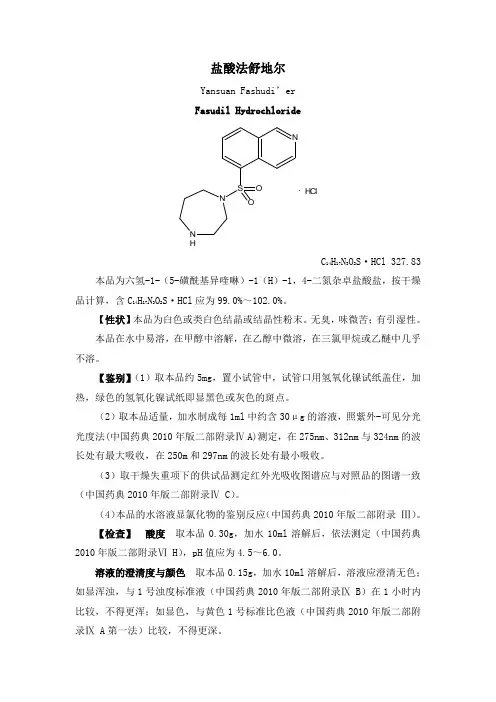
盐酸法舒地尔Yansuan Fashudi’er Fasudil HydrochlorideNS NO ONH.HClC 14H17N3O2S·HCl327.83本品为六氢-1-(5-磺酰基异喹啉)-1(H)-1,4-二氮杂卓盐酸盐,按干燥品计算,含C14H17N3O2S·HCl应为99.0%~102.0%。
【性状】本品为白色或类白色结晶或结晶性粉末。
无臭,味微苦;有引湿性。
本品在水中易溶,在甲醇中溶解,在乙醇中微溶,在三氯甲烷或乙醚中几乎不溶。
【鉴别】(1)取本品约5mg,置小试管中,试管口用氢氧化镍试纸盖住,加热,绿色的氢氧化镍试纸即显黑色或灰色的斑点。
(2)取本品适量,加水制成每1ml中约含30μg的溶液,照紫外-可见分光光度法(中国药典2010年版二部附录ⅣA)测定,在275nm、312nm与324nm的波长处有最大吸收,在250m和297nm的波长处有最小吸收。
(3)取干燥失重项下的供试品测定红外光吸收图谱应与对照品的图谱一致(中国药典2010年版二部附录Ⅳ C)。
(4)本品的水溶液显氯化物的鉴别反应(中国药典2010年版二部附录Ⅲ)。
【检查】酸度取本品0.30g,加水10ml溶解后,依法测定(中国药典2010年版二部附录Ⅵ H),pH值应为4.5~6.0。
溶液的澄清度与颜色取本品0.15g,加水10ml溶解后,溶液应澄清无色;如显浑浊,与1号浊度标准液(中国药典2010年版二部附录Ⅸ B)在1小时内比较,不得更浑;如显色,与黄色1号标准比色液(中国药典2010年版二部附录Ⅸ A第一法)比较,不得更深。
有关物质取本品适量,加流动相制成每1ml中约含0.2mg的溶液,作为供试品溶液,精密量取1ml,置100ml量瓶中,加流动相稀释至刻度,摇匀,作为对照溶液;照含量测定项下的色谱条件,取对照溶液20μl注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高为满量程的10%~20%;再精密量取供试品溶液与对照溶液各20μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4倍。

盐酸法舒地尔治疗78例缺血性脑卒中疗效观察【摘要】目的:分析临床在治疗缺血性脑卒中患者时给予盐酸法舒地尔治疗后的临床效果。
方法:将笔者所在医院收治的155例缺血性脑卒中患者随机分为观察组和对照组,对照组77例患者实施常规治疗,观察组78例患者在对照组基础上加盐酸法舒地尔治疗,比较两组患者治疗后的临床效果。
结果:观察组临床治疗有效率及神经功能缺损评分与对照组比较,差异有统计学意义(p0.05),具有可比性。
1.2 方法对照组实施常规治疗,其中包括:给予患者实施2次/d的甘露醇静脉滴注,剂量为20%甘露醇125 ml,治疗周期为2周;同时给予继之极化液(包括10%葡萄糖溶液500 ml、10%氯化钾溶液15 ml、胰岛素8 u)每日一次静脉滴注,治疗周期为1周。
观察组对照组基础上加盐酸法舒地尔治疗。
盐酸法舒地尔的治疗方法为在100 ml 0.9%氯化钾溶液中加入30 mg盐酸法舒地尔注射液后,为患者实施3次/d的静脉滴注,治疗周期为3周。
1.3 疗效评定标准参照国内相关评定标准,按照患者神经功能缺损评分减少程度对此次治疗后患者的临床效果进行了如下分级:将患者缺损评分减少程度在91%以上的称为治愈;将患者缺损评分减少程度在46%~90%的称为显效;将患者缺损评分减少程度在18%~45%的称为有效;将患者缺损评分减少程度低于17%的称为无效。
临床治疗总有效=治愈+显效+有效。
1.4 统计学方法3 讨论临床上将患者的局部脑组织因血液循环发生障碍而导致的局部脑组织缺氧、缺血坏死现象,继而引起患者发生相应神经功能缺损的症状称为缺血性脑卒中。
近几年对于该病的研究显示rho激酶系统对于该种疾病的发生起着至关重要的作用[2]。
研究显示rho激酶在缺血性疾病中的发生机制主要包含:在动脉粥样硬化、血管痉挛、狭窄等疾病的发生时rho激酶具有重要作;rho激酶会直接影响患者体内神经网络的形成及对神经轴突再生及生长产生抑制作用;对患者体内细胞的凋亡具有促进作用[3]。


分类:化学药品
类别:3.1
【药品名称】
通用名:盐酸法舒地尔注射液
曾用名:
商品名:
英文名:Fasudil Hydrochloride Injection
汉语拼音:Yansuan Fashudier Zhusheye
剂型:注射剂
【成分】
化学名称:六氢—1—(5—磺酰基异喹啉)—1(H)—1,4—二氮杂卓盐酸盐。
化学结构式:
分子式:C14H17N3O2S?HCl
分子量:327.83
【性状】本品为白色、类白色或微黄色的结晶性粉末。
无臭,味微苦。
有引湿性。
本品在水中极易溶,在甲醇中溶解,在乙醇中略溶,在氯仿中极微溶,在乙醚中几乎不溶。
【药理毒理】盐酸法舒地尔是一种蛋白激酶抑制剂即细胞内钙离子拮抗剂。
血管平滑肌的收缩是由于平滑肌细胞内Ca2+浓度显著增高激活了关键酶的缘故。
当CA2+ 达到一定浓度时,与CA2+结合蛋白钙调素结合,激活肌球蛋白轻链磷酸化酶,将肌球蛋白轻链磷酸化,引起肌肉收缩。
蛛网膜下腔出血时,血管中释放出的各种血管收缩物质参与血管痉挛,最终通过肌球蛋白轻链磷酸化造成血管收缩。
盐酸法舒地尔通过阻断血管收缩过程的最终阶段,肌球蛋白轻链磷酸化,来扩张血管,抑制血管痉挛。
急性毒性:小鼠、大鼠口服给药的LD50分别为:小鼠雄性为273.9 mg/kg;雌性为277.3 mg/kg;大鼠雄性为335 mg/kg;雌性为348 mg/kg。
小鼠静脉给药的LD50 为69.5mg/kg。
亚急性毒性:以大鼠、猴静脉内给药1个月,无毒性剂量为:大鼠12.5mg/kg,猴3.125mg/kg。
慢性毒性:以大鼠、猴静脉内给药6个月,无毒性剂量为:大鼠9mg/kg,猴3.125mg/kg。
致突变性实验:细菌回复突变实验及啮齿类动物微核试验均为阴性。
哺乳类细胞染色体试验证明在体内无致突变性。
生殖毒性试验:妊娠前及妊娠初期的大鼠及大鼠胎仔器官形成期生殖和发育的毒性研究,剂量分别为1.56,6.25,25和1.6,8.0,40mg/kg。
结果证明:25mg/kg剂量组引起妊娠前及妊娠初期的黄体数和着床数降低;40mg/kg剂量组能轻度抑制次生代仔的体重增加,但无致畸作用,对其它生殖能力和次生代仔的各项观察指标均无影响。
【药代动力学】吸收:将放射标记的本品快速静脉给予大鼠及猴时,血液中放射性浓度自给药后迅速降低。
而静脉内持续给药时,血中浓度,自给药结束后减少,消失半衰期大鼠约l.4小时,而且AUC随着给药量增加而增大,与血浆浓度呈线性关系。
分布:给药后迅速向组织转移,药物在肝、肾、脾和肠中含量较高。
也可见向脑中转移。
代谢:本品给药后,80%为未变化的原形药物和主要代谢产物一异喹啉骨架l位的氢氧化物及其结合体。
代谢产物总数在大鼠中产生6种,在猴中产生5种。
排泄:大鼠尿、粪和胆汁分别排出原形药为41.1%,6.4%,38.4%。
血浆蛋白结合率:本品血浆蛋白的结合率在体外约80%,在体内约34%一62%。
动物实验表明,本品可通过胎盘,并向乳汁转移。
在健康人体实验,以本品0.2mg/kg 及0.4mg/kg,静脉内持续给药时,给药结束后的消失半衰期约为15分钟。
AUC及最高血药浓度,伴随给药量增大而增加。
给蛛网膜下腔出血的术后病人静脉内点滴30mg/次,其血浆中药物浓度的演变与健康人未见大的差别。
【适应症】蛛网膜下腔出血后脑血管痉挛等引起的缺血性脑血管疾病症状的改善。
【用法用量】成人一日2—3次,每次30mg,以适量的电解质液稀释后静脉点滴,每次需30
分钟。
本品给药应在蛛网膜下腔出血术后早期开始,连用2周。
【不良反应】l.由于本品使血管扩张,可引起低血压,颜面潮红、反射性心动过速及出血。
2.应用本品有时发生GOT、GPT升高,有时出现皮疹、排尿困难或多尿、嗳气、呕吐,并可出现头痛、发热、意识水平下降和呼吸抑制等不良反应。
【禁忌】1.正在出血的患者,尤其颅内出血的患者和低血压患者禁用本品。
2.本品只可静脉点滴使用,不可脊髓腔内注入本品。
【注意事项】1.本品使用时,应密切注意临床症状及CT改变,若发现颅内出血,应立即停药并进行适当处理。
2.本品可引起低血压,应注意血压变化及给药剂量和速度。
3.下列情况使用木品应慎重:严重意识障碍患者,蛛网膜下腔出血合并重症脑血管损害,如脑底异常血管网或巨大脑动脉瘤等患者。
【孕妇及哺乳期妇女用药】妊娠或可能妊娠妇女及哺乳期妇女应避免使用。
【儿童用药】无使用经验。
【老年患者用药】
【药物相互作用】1.Aleviatin注射液、Bitashimin(Vc)注射液,静注用Puremarin、Arepiati(苯妥英钠)与本品配伍时,立即变色或变浑浊,严禁使用。
2.与本品配伍后需迅速使用的药品有:静注用头孢替安、Buroakuto、Fulumarin。
因为以上药物与本品配伍时,经常出现变色或透过率低下,因此,配伍后应迅速使用。
【药物过量】应用本品以2周为限,不可长期给药。
【规格】2ml:30mg
【贮藏】避光保存。
【包装】药用玻璃安瓿,每盒3支、6支、10支。
【有效期】暂定18个月
【批准文号】国药准字H20040356
【生产企业】
企业名称:天津红日药业股份有限公司
地址:天津新技术产业园区武清开发区泉发路。