速率平衡图像专题
- 格式:ppt
- 大小:1.02 MB
- 文档页数:21
![第三十八讲、速率平衡图象专题 [讲义]](https://img.taocdn.com/s1/m/5d8e792ced630b1c59eeb562.png)
第三十八讲、速率平衡图象专题一.常见图象题类型1.v-t图此类图象定性揭示了v(正)、v(逆)随时间(含条件改变对速率的影响)而变化的规律,体现了平衡的“动、等、定、变”的基本特征,以及平衡移动的方向等。
2.c-t图此类图象能说明各平衡体系组分(或某一成分)在反应过程中的变化情况。
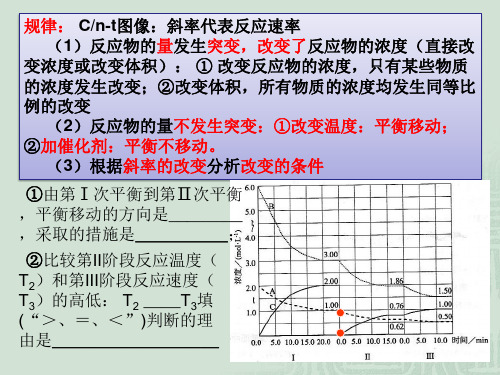
如aA+bB cAB反应情况如下图所示,此类图象要注意各物质曲线的折点(达平衡)时刻相同,各物质浓度变化的内在联系及其比例符合化学方程式中的系数关系。
3.全程v-t图如Zn与足量盐酸的反应,反应速率随时间的变化出现如下情况如图所示,试解释变化的原因。
4.含量-t-温度(压强)图常见形式有如下图所示,(C%指产物百分数,B%指某反应物百分数)(在其他条件不变时,改变任一条件如:使用催化剂或温度升高或压强增大,都能缩短到达平衡的时间),这种图象的折点表示达到平衡的时间,反映了速率的大小,可以T/P的高低/大小),水平线高低对应平衡移动方向。
5.恒压(温)线该类图的纵坐标为物质的平衡浓度(c)或反应物的转化率(α),横坐标为温度(T)或压强(P),常见类型如图所示。
6.v-T(P)图这类图有两种情况:一是不隐含时间因的速率~时间图,二是隐含时间变化的速率~时间图。
如2SO2(g)+O22SO3(g)+Q。
7.其他 下图曲线是其他条件不变时,某反应物的最大转化率(α)与温度(T )的关系曲线,图中标出的1、2、3、4四个点,其含义分别是什么?二.例题例1.在容积不变的密闭容器中,一定条件下进行如下反应:2NO (g )+2CO (g )N 2(g )+2CO 2(g )+746.4 kJ右图曲线a 表示该反应过程中,NO 的转化率与反应时间的关系。
若改变起始条件,使反应过程按照曲线b 进行,可采取的措施是A 加催化剂B 向密闭容器中加入氩气C 降低温度D 增大反应物中NO 的浓度例2.今有反应X (g )+Y (g)2Z (g )(正反应放热),右图表示该反应在t 1时达到平衡,在t 2时因改变某个条件而发生变化的曲线。




化学反应速率、化学平衡图像一、ν-t 图像或c-t 图像1. ν-t 图像:分清正逆反应,分清各因素(浓度、温度、压强、催化剂)对反应速率和平衡移动的影响。
【练习1】对于反应2SO 2(g)+O 2(g) 2SO 3(g) △H <0, 填写改变的条件及平衡移动的方向。
t 1时, , 平衡向 移动。
t 2时, , 平衡向 移动。
t 3时, , 平衡向 移动。
t 4时, ,平衡向 移动。
小结:改变 条件,图像一点保持连续;改变 ,两点突变,_____________使正逆反应速率同等程度的增大而平衡不移动。
【练习2】对达到平衡状态的可逆反应X+Y Z+W ,在其他条件不变的情况下,增大压强,反应速率变化如下图左所示,则图像中关于X 、Y 、Z 、W 四种物质的聚集状态为( )A .Z 、W 均为气体,X 、Y 中有一种是气体B .Z 、W 中有一种是气体,X 、Y 皆非气体C .X 、Y 、Z 、W 皆非气体D .X 、Y 均为气体,Z 、W 中有一种为气体【练习3】在密闭容器,一定条件下进行反应,mA(g)+nB(g)pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,变化过程均如上图右所示,则对该反应叙述正确的是( ) A .正反应是吸热反应 B .逆反应是吸热反应 C .m+n>p+q D .m+n<p+q 【练习4】应N 2(g)+3H 2(g)2NH 3(g) △H<0 在某一时间段中反应速率与反应过程的曲线关系如图,则图中氨的百分含量最低的时间段是( ) ,氨的百分含量最高的时间段是( ) A.t 0-t 1B.t 2-t 3C.t 3-t 4D. t 5-t 62. c-t 图像:分清反应物和生成物,浓度减小的为反应物,浓度增大的为生成物,分清消耗浓度和增加浓度,反应物的消耗浓度和生成物的增加浓度之比,等于化学方程式中各物质的化学计量数之比。
【练习5】今有X (g )+Y(g) 2Z(g) △H<0。
化学反应速率、化学平衡图像一、ν-t图像或c-t图像1. ν-t图像:分清正逆反应,分清各因素(浓度、温度、压强、催化剂)对反应速率和平衡移动的影响。
【练习1】对于反应2SO 2(g)+O2(g) 2SO3(g) △H<0,填写改变的条件及平衡移动的方向。
t1时,,平衡向移动。
t2时,,平衡向移动。
t3时,,平衡向移动。
t4时,,平衡向移动。
小结:改变条件,图像一点保持连续;改变,两点突变,_____________使正逆反应速率同等程度的增大而平衡不移动。
【练习2】对达到平衡状态的可逆反应X+Y Z+W,在其他条件不变的情况下,增大压强,反应速率变化如右图所示,则图像中关于X、Y、Z、W四种物质的聚集状态为( )A.Z、W均为气体,X、Y中有一种是气体B.Z、W中有一种是气体,X、Y皆非气体C.X、Y、Z、W皆非气体D.X、Y均为气体,Z、W中有一种为气体【练习3】在密闭容器,一定条件下进行反应,mA(g)+nB(g) pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,变化过程均如右图所示,则对该反应叙述正确的是( )A.正反应是吸热反应B.逆反应是吸热反应C.m+n>p+q D.m+n<p+q【练习4】应N2(g)+3H2(g) 2NH3(g) △H<0 在某一时间段中反应速率与反应过程的曲线关系如图,则图中氨的百分含量最低的时间段是( ) ,氨的百分含量最高的时间段是( )A.t0-t1B.t2-t3C.t3-t4D. t5-t62. c-t图像:分清反应物和生成物,浓度减小的为反应物,浓度增大的为生成物,分清消耗浓度和增加浓度,反应物的消耗浓度和生成物的增加浓度之比,等于化学方程式中各物质的化学计量数之比。
【练习5】今有X(g)+Y(g) 2Z(g) △H<0。
从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,引起t2→t3曲线变化的原因是( )A.增大X或Y的浓度B.增大压强C.增大Z的浓度D.升高温度【练习6】右图表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间。
专题15 化学反应的速率和平衡图像题的分析化学反应速率和化学平衡图像题是化学试题中的一类特殊题型,其特点为图像是题目的主要组成部分,把所要考查的化学知识寓于图中曲线上,具有简明、直观、形象的特点。
化学反应速率和化学平衡图像题分析方法如下。
1.看图像(1)看面,弄清楚横、纵坐标所表示的含义;(2)看线,弄清楚线的走向和变化趋势;(3)看点,弄清楚曲线上点的含义,特别是曲线上的折点、交点、最高点、最低点等;(4)看辅助线,作横轴或纵轴的垂直线(如等温线、等压线、平衡线等);(5)看量的变化,弄清楚是物质的量的变化、浓度的变化,还是转化率的变化。
2.想规律如各物质的转化量之比与化学计量数之比的关系,各物质的化学反应速率之比与化学计量数之比的关系,外界条件的改变对化学反应速率的影响规律以及反应达到平衡时,外界条件的改变对正、逆反应速率的影响规律等。
3.作判断利用有关规律,结合图像,通过对比分析,作出正确判断。
例1.(2022·河南·高一期中)在恒温恒容条件下,发生反应2A(g)+xB(g)2C(g),反应体系中某物质的浓度c随时间的变化如图中曲线甲、乙所示,已知x为整数。
下列说法正确的是A.x=3B .曲线乙表示的是物质A 在反应进程中的浓度变化C .10~30min 内v(C)=0.05mol·L -1·min -1D .c 点对应物质的浓度与d 点对应物质的浓度相等【答案】A【解析】A .由分析可知x=3,A 正确;B .由分析可知曲线乙表示的是物质C 在反应进程中的浓度变化,B 错误;C .10~30min 内,-1-1(B)=(2-1)mol L =1mol L c ⋅⋅∆,-1-11mo/L v(B)==0.05mol L 20min ⋅,v(B):v(c)=3:2,则-122v(c)=v(B)=0.05mol L 33⨯⋅,C 错误;D .由图可知c 对应物质的浓度为1.6 mol·L -1,d 点对应物质的浓度为0.6 mol·L -1,D 错误;故选A 。
2021-2022学年高一化学期末复习重点专题突破专题08 化学反应速率及平衡图像问题的分析方法探究一、化学平衡建立过程中反应速率变化图像根据图像可进行如下分析:二、化学平衡建立过程中物质的量变化图像根据图像可进行如下分析:1.分清反应物和生成物,物质的量减小的是反应物,物质的量增加的是生成物,生成物多数是以原点为起点。
2.根据相同时间内反应物和生成物的物质的量变化,可计算各物质的化学反应速率,再根据化学反应速率之比等于各自的化学计量数之比,可推出反应的化学方程式。
3.找出反应达到平衡的时间点,进而通过图中数据,可计算得到反应达到一定时间下,反应物的物质的量、生成物的物质的量以及反应物的转化率等。
三、有关化学反应速率和化学平衡的计算解答有关化学反应速率和化学平衡的计算题时,一般需要写出化学方程式,列出起始量、变化量及平衡量,再根据题设其他条件和定律列方程求解。
如:m A(g)+n B(g)p C(g)+q D(g)起始/mol a b0 0转化/mol mx nx px qx平衡/mol a−mx b−nx px qx(1)关于反应物转化率的计算A的转化率=AA的转化量的起始量×100%(计算式中A的量可以指反应物的物质的量、质量、浓度、体积等)(2)关于某气体组分的体积分数的计算气体A的体积分数=A体系中的物质的量体系中气体总的物质的量×100%四、解答化学反应速率及化学平衡图像题的方法技巧化学反应速率及化学平衡的图像,能直观描述反应进行的快慢、反应进行的程度等问题。
图像题是化学中常见的一种题目,做这类题既要读文字内容,又要读图。
解答化学反应速率图像题三步曲:“一看”、“二想”、“三判断”;“一看”——看图像①看坐标轴:弄清纵、横坐标表示的含义;②看线:弄清线的走向、趋势;③看点:弄清曲线上点的含义,特别是一些特殊点,如曲线的折点、交点、最高点与最低点等;④看量的变化:弄清是物质的量的变化、浓度的变化还是转化率的变化等。