速率平衡图像
- 格式:doc
- 大小:547.50 KB
- 文档页数:2




化学反应速率和化学平衡图像图像分析要领2SO2(g)+O2(g)2SO3(g) t随后逐渐增加,说明改变的条件是增加反应物的浓度。
CH4(g)+H2O(g)CO(g)+3H2(g)ΔH>0tmA(g)+nB(g)qC(g)+pD(g) “定一议二”。
m+n>q+p时2NO(g) + 2CO(g)N2(g)+2CO2(g) 先拐先平,先平者高。
T投料比图2SO2(g)+O2(g)2SO3(g) △H<01.b应对应物质的化学计量数之n2.T3.平衡向右移动,分数先增大后减小定位题组1.对于可逆反应:2SO 2(g)+O 2(g)2SO 3(g)△H<0,下列研究目的和示意图相符的是2.工业上可利用CH 4(g)+H 2O(g)CO(g)+3H 2(g)反应生产合成氨原料气H 2。
已知温度、压强和水碳比[)()(42CH n O H n ]对甲烷蒸汽转化反应的影响如下图:图1(水碳比为3) 图2(水碳比为3) 图3(800℃)(1)降低反应的水碳比平衡常数K__________(选填“增大”、“减小”或“不变”);升高温度,平衡向____________方向移动(选正反应或逆反应)。
(2)图2中,两条曲线所示温度的关系是:t 1_____t 2(选填>、=或<);图1中,在800℃、2MPa 比1MPa 时的甲烷含量_______(选填高、低或不变),3.甲醇被称为21世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH 4和H 2O 为原料来制备甲醇。
(1)将1.0 mol CH 4和2.0 mol H 2O(g)通入反应室(容积为100 L),在一定条件下发生反应:CH 4(g)+H 2O(g) CO(g)+3H 2(g)……Ⅰ,CH 4的转化率与温度、压强的关系如图。
①已知100 ℃时达到平衡所需的时间为5 min 。
则用H 2表示的平均反应速率为________。

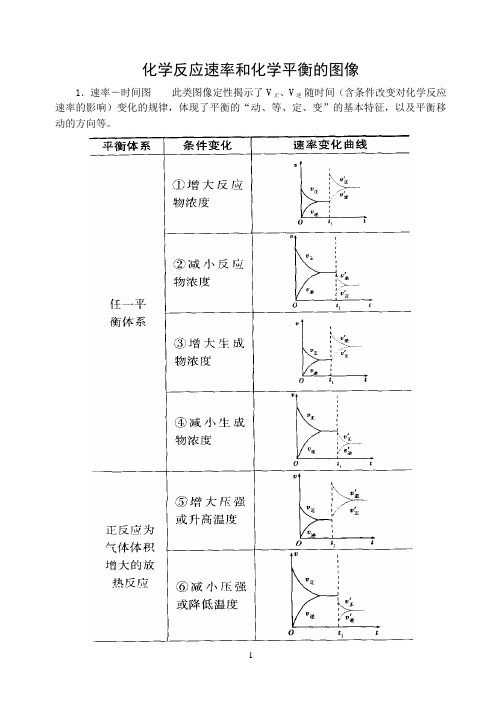
化学反应速率和化学平衡的图像
1.速率-时间图此类图像定性揭示了V正、V逆随时间(含条件改变对化学反应速率的影响)变化的规律,体现了平衡的“动、等、定、变”的基本特征,以及平衡移动的方向等。
2.含量―时间―温度(压强)图常见的形式有下图所示的几种(C%指某产物百分含量,B%指某反应物百分含量),这些图像的折点表示达到平衡的时间,曲线的斜率反映了反应速率的大小,可以确定T(p)的高低(大小),水平线高低反映平衡移动的方向。
3.恒压(温)线该类图像的纵坐标为物质的平衡浓度(c)或反应物的转化率( ),横坐标为温度(T)或压强(p),常见类型如下图:
小结
1.图像分析应注意“三看”
(1)看两轴:认清两坐标轴所表示的含义。
(2)看起点:从图像纵轴上的起点,一般可判断谁为反应物,谁为生成物以及平衡前反应进行的方向。
(3)看拐点:一般图像在拐点后平行于横轴则表示反应达平衡,如横轴为时间,由拐点可判断反应速率。
2.图像分析中,对于温度、浓度、压强三个因素,一般采用“定一议二”的方式进行分析。
化学反应速率、化学平衡图像
一、ν-t 图像或c-t 图像
1. ν-t 图像:分清正逆反应,分清各因素(浓度、温度、压强、催化剂)对反应速率和平衡移动的影响。
【练习1】对于反应2SO 2(g)+O 2
(g) 2SO 3(g) △H <0, 填写改变的条件及平衡移动的方向。
t 1时, , 平衡向 移动。
t 2时, , 平衡向 移动。
t 3时, , 平衡向 移动。
t 4时, ,
平衡向 移动。
小结:改变 条件,图像一点保持连续;改变 ,两点突变,_____________使正逆反应速率同等程度的增大而平衡不移动。
【练习2】对达到平衡状态的可逆反应X+Y Z+W ,在其他条件不变的情况下,增大压强,反应
速率变化如下图左所示,则图像中关于X 、Y 、Z 、W 四种物质的聚集状态为( )
A .Z 、W 均为气体,X 、Y 中有一种是气体
B .Z 、W 中有一种是气体,X 、Y 皆非气体
C .X 、Y 、Z 、W 皆非气体
D .X 、Y 均为气体,Z 、W 中有一种为气体
【练习3】在密闭容器,一定条件下进行反应,
mA(g)+nB(g)
pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,变化过程均如上图右
所示,则对该反应叙述正确的是( ) A .正反应是吸热反应 B .逆反应是吸热反应 C .m+n>p+q D .m+n<p+q 【练习4】应N 2(g)+3H 2
(g)
2NH 3(g) △H<0 在某一时间段
中反应速率与反应过程的曲线关系如图,则图中氨的百分含量最低的时间段是( ) ,氨的百分含量最高的时间段是( ) A.t 0-t 1
B.t 2-t 3
C.t 3-t 4
D. t 5-t 6
2. c-t 图像:分清反应物和生成物,浓度减小的为反应物,浓度增大的为生成物,分清消耗浓度和增
加浓度,反应物的消耗浓度和生成物的增加浓度之比,等于化学方程式中各物质的化学
计量数之比。
【练习5】今有X (g )
+Y(g) 2Z(g) △H<0。
从反应
开始经过t 1后达到平衡状态,t 2 时由于条件改变,平衡受到破坏,在t 3时又达到平衡,引起t 2→t 3曲线变化的原因是( ) A .增大X 或Y 的浓度 B .增大压强
C .增大Z 的浓度
D .升高温度 【练习6】右图表示800℃时A 、B 、C 三种气体物质的浓度随时间的变
化情况,t 1是到达平衡状态的时间。
试回答: (1)该反应的反应物是______; (2)反应物的转化率是______;
(3)该反应的化学方程式为___________________________。
二、平衡图像
1.出现拐点的图像:分析依据“先拐先平”。
在转化率-时间图像或物质的百分含量-时间图像中,
先出现拐点的曲线先达到平衡(代表温度高或压强大或使用合适的催化剂)。
【练习7】已知某可逆反应在密闭容器中进行:
A(g)+2B(g) 3C(g)+D(s) △H <0,图中曲线b 代表一定条件下该反应的过程,若使曲线b 变为曲线a ,可采取的措施是( )
A .增大A 的浓度
B .缩小容器的容积
C .加入催化剂
D .升高温度 【练习8】现有可逆反应A (g)+2B
(g) nC (g) △H <0,在相同温度、不同压强时,A 的转化
率跟反应时间(t )的关系如右图,其中结论正确的是( ) A .p 1>p 2,n >3 B .p 1<p 2,n >3 C .p 1<p 2,n <3
D .p
>p 2,n=3
【练习9】对于可逆反应△H <0,下列图像正确的是
( )
【练习10】可逆反应:aA(g)+ bB(g)cC(g)+ dD(g)
根据图回答:
①压强 P 1比P 2 (填大或小) ; ②(a +b )比(c +d ) (填大或小); ③温度t 1℃比t 2℃
(填高或低)
;
④正反应
热(填吸或放)。
【练习11】在密闭容器中进行下列反应:
M(g)
+ N(g) ,此反应符合右图,下列叙述正确
的是( ) A .正反应吸热 ,L 是气体 B .正反应吸热, L 是固体
C .正反应放热 ,L 是气体
D .正反应放热 ,L 是固体或液体
【练习12】等质量的两份锌粉a 和b ,分别加入过量的稀硫酸中,a 中同时加入少量CuSO 4溶液,
下列各图中表示其产生氢气的总体积(V)与时间的关系正确的是( )
2.受两个变量(P 、T )影响的图像:分析依据“定一议二”。
转化率或百分含量等因素受到压强、温
度两个变量的影响,先确定一个变量,分析另外两个量的关系。
如确定温度分析转化率受压强的影响。
【练习13】可逆反应2A+B 2C(g) △H<0,随温度变化气体平均相
对分子质量如图所示,则下列叙述正确的是( )
A .A 和
B 可能都是固体 B .A 和B 一定都是气体
C .若B 为固体,则A 一定是气体
D .A 和B 可能都是气体 【练习14】反应L(s)+
aG(g)
bR(g)达到平衡时,温度和压强对该反
应的影响如图所示。
图中,压强p 1>p 2, x 轴表示温度,y 轴表示平衡混合气中G 的体积分数。
据此可判断( )
A.上述反应是放热反应
B.上述反应是吸热反应 C. a >b D. a <b 【练习15】某可逆反应
L(s) + G(g) 3R(g) ΔH>0,右图表示外界条
件温度压强的变化对上述反应的影响。
试判断图中Y 轴可以表示( )
A .平衡混合气中R 的质量分数
B .达到平衡时G 的转化率
C .平衡混合气中G 的质量分数
D .达到平衡时L 的转化率
【练习16】反应mA(s) +
nB(g)
eC(g) + fD(g)反应过程中,当其它
条件不变时,C 的百分含量(C%)和压强(P )的关系如图,下列叙述正确的是( )
A .达到平衡后,加入催化剂,则C%增大
B .达到平衡后,若升温,平衡左移
C .化学方程式中n>e +f
D .达到平衡后,增加A 的量有利于平衡右移 【练习17】如图所示,可逆反应:
2A(g)+B(g) 2C(g) △H<0的图像正确的是( )
【练习18】对于可逆反应,A 2(g)+3B 2
(g)
2AB 3(g)△H<0,下列图像不正确的是( )
【练习19】在其它条件一定时,图中曲线表示反应
2NO(g)+ O 2
(g) 2NO 2(g) △H >0达平衡时NO 的转化率与温度
的关系,图上标有A 、B 、C 、D 、E 点,其中表示未达平衡状态且V 正
>V 逆的点是( ) A .A 或E B .B 点
C .C 点
D .D 点
【练习20】反应A 2+B
22AB 在不同条件下,产物AB 百分含量随时
间变化关系如图所示,a 为500℃,b 为300℃时情况,c 为300℃
时从时间t 3开始向容器中加压的情况,则下列叙述正确的是( )
A.A 2、B 2、AB 均为气体,正反应放热
B.AB 为气体,A 2、B 2中最少有一种为非气体,正反应放热
C.AB 为气体,A 2、B 2中最少有一种为非气体,正反应吸热
D.AB 为固体,A 2、B 2中最少有一种为非气体,正反应吸热 【练习21】两种气态单质按下列反应
X 2(g) + Y 2
(g) 2XY(g),X 2与Y 2按一定比例混合,在不同温度下经一
定时间反应,混合物中X 2的体积分数变化如图所示,试确定该反应是吸热反应还是放热反应。