中 国《骨质疏松性骨折诊疗指南》 2017版 解读
- 格式:pptx
- 大小:2.44 MB
- 文档页数:29




骨质疏松症椎体压缩性骨折诊疗指南骨质疏松症是指:骨量减少、骨组织显微结构破坏、骨脆性增加、骨强度下降、骨折风险性增加为特征的全身性、代谢性骨骼系统疾病;当骨质疏松症导致骨密度和骨质量下降,骨强度减低时,轻微外力即可发生的骨折,该骨折累计脊柱时,称为骨折疏松椎体压缩性骨折(OVF),脊柱是骨质疏松症骨折的常发部位。
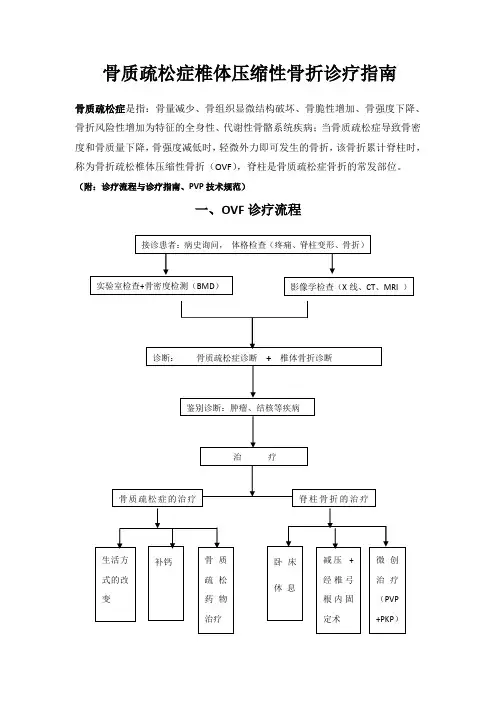
(附:诊疗流程与诊疗指南、PVP技术规范)一、OVF诊疗流程二.OVF诊治指南(一)临床特点疼痛、脊柱变形和发生脆性骨折是骨质疏松症最典型的临床表现。
但许多骨质疏松症患者早期常无明显的自觉症状,往往在骨折发生后经X线或骨密度检查时才发现已有骨质疏松改变。
1、疼痛:患者可有腰背酸痛或周身酸痛,负荷增加时疼痛加重或活动受限,严重时翻身、起坐及行走有困难。
2、脊柱变形:骨质疏松严重者可有身高缩短和驼背。
椎体压缩性骨折会导致胸廓畸形,腹部受压,影响心肺功能等。
3、骨折:轻度外伤或日常活动后发生骨折为脆性骨折。
发生脆性骨折的常见部位为胸、腰椎。
发生过一次脆性骨折后,再次发生骨折的风险明显增加。
(二)实验室检查1. 根据鉴别诊断需要可选择检测血、尿常规,肝、肾功能,血糖、钙、磷、碱性磷酸酶、性激素、25(OH)D和甲状旁腺激素等。
2. 根据病情、药物选择、疗效观察和鉴别诊断需要,有条件的单位可分别选择下列骨代谢和骨转换的指标(包括骨形成和骨吸收指标)。
这类指标有助于骨转换的分型、骨丢失速率及老年妇女骨折的风险性评估、病情进展和干预措施的选择和评估。
临床常用检测指标:血清钙、磷、25-羟维生素D和1,25-双羟维生素D。
骨形成指标:血清碱性磷酸酶(ALP),骨钙素(OC)、骨源性碱性磷酸酶(BALP),l 型前胶原C端肽(PICP)、N端肽(PINP);骨吸收指标:空腹2小时的尿钙/肌酐比值,或血浆抗酒石酸酸性磷酸酶(TPACP)及l型胶原C端肽(S-CTX),尿吡啶啉(Pyr)和脱氧吡啶啉(d-Pyr),尿I型胶原C端肽(U-CTX)和N端肽(U-NTX)等。

骨质疏松性骨折诊疗指南(2022年版)给出的骨质疏松性椎体骨折治疗策略既往,《中华骨科杂志》于2008年和2017年,先后发布了两版《骨质疏松性骨折诊疗指南》。
而骨质疏松性骨折诊疗指南(2022年版) 由中华医学会骨科学分会制订,在2017年版的基础上对骨质疏松性椎体骨折的治疗策略进行更新,部分内容摘抄如下:一、骨质疏松性椎体骨折治疗策略骨质疏松性椎体骨折应根据骨折的程度、症状、全身情况及患者需求等选择保守治疗、微创或开放手术治疗(推荐强度:专家建议)。
骨质疏松性椎体压缩性骨折(OVCF)常用的微创治疗是椎体强化手术,包括椎体成形术(PVP)和椎体后凸成形术(PKP)。
目前对微创手术与非手术治疗OVCF的疗效是否存在差异尚无定论。
美国临床内分泌医师协会和美国内分泌学会2020版指南建议:考虑到对整体疼痛获益的不确定性和邻近椎体潜在增加的骨折风险,不推荐将PVP和PKP等微创手术作为OVCF的一线治疗。
2014年美国介入放射等学会推荐:保守治疗是OVCF传统的一线治疗方式,若PVP应用于骨质疏松相关的椎体骨折,则需用于保守治疗失败或不耐受保守治疗的患者。
英国国家健康与临床最优化研究所2003年指南认为:OVCF患者正规保守治疗至少4周后,采用PVP治疗是一种安全、有效的手段。
美国骨科医师学会2011年指南认为:不建议无神经损伤的急性椎体压缩骨折行PVP(强推荐);PKP对无神经损伤的急性椎体压缩骨折是一种选择(弱推荐)。
而中国医师协会骨科学分会脊柱创伤专业委员会2019年指南认为,对急性症状性OVCF可行PVP(强推荐)或PKP(弱推荐)。
综合分析,本指南强调根据骨质疏松性椎体骨折的程度、症状、全身情况以及患者诉求(如要求更快恢复正常生活状态等)选择合适的干预手段,使患者得到最佳预后。
保守治疗适用于影像学检查显示为轻中度椎体压缩骨折,症状和体征较轻,24h镇痛治疗后能恢复活动;或不能耐受手术者。
保守治疗包括卧床、支具及药物、早期活动、康复锻炼等方法,但需要定期进行复查评估,了解椎体压缩是否进行性加重。


《中国定量CT(QCT) 骨质疏松症诊断指南》要点随着我国社会人口的老龄化,骨质疏松症成为严重威胁老年人群身体健康的慢性疾病之一,并造成沉重的医疗负担。
中华医学会骨质疏松与骨矿盐疾病分会于2017年发布了原发性骨质疏松症诊疗指南》( 2017版),中国老年学和老年医学学会骨质疏松分会(OSCG)在此基础上于2018年发布了《中国老年骨质疏松症诊疗指南》( 2018)。
这些指南明确了骨密度测量在骨质疏松症诊疗与预防中的作用,即骨密度测量是诊断骨质疏松症的主要依据之一。
其中双能X 线骨密度测量(DXA)是认知度和认可度最高的骨密度测量方法,但我国现有骨密度测量仪的数量远不能满足临床需求。
定量CT(QCT)是在临床CT扫描数据的基础上,经过QCT体模校准和专业软件分析,对人体骨骼进行骨密度测量的方法。
QCT采用的是CT三维容积数据进行分析,测量的是真正的体积骨密度(vBMD)。
鉴于QCT的技术优势和CT技术的快速发展,近年来,QCT在各国的骨质疏松研究和临床应用领域越来越受到重视。
CT扫描机在全国各级医疗机构已比较普及,仅需简单配备一套QCT体模和分析软件即可开展QCT骨密度测量检查,因此,QCT 骨密度测量技术适合我国国情,具有良好的应用前景。
基于上述国际和国内QCT临床应用共识,结合国内近年来在QCT临床应用研究的最新研究成果及本次中国QCT大数据项目的结果(即将于本刊2019年第10期刊发),充分考虑中国的医疗实际情况,专家组制定了该QCT骨密度测量临床应用指南,为临床医务工作者在QCT临床应用方面提供科学、具体的指导,促进骨质疏松症的规范诊疗。
1 推荐意见1及其说明1.1 推荐意见1腰椎QCT骨质疏松诊断症标准:取2个腰椎松质骨骨密度平均值(常用第1和第2腰椎),采用腰椎QCT骨密度绝对值进行诊断,骨密度绝对值>120mg/cm3 为骨密度正常,骨密度绝对值于80~120mg/cm3 范围内为低骨量,骨密度绝对值<80mg/cm3 为骨质疏松。

《骨质疏松性骨折诊疗指南》(全文)骨质疏松症是一种以骨量降低、骨微结构破坏、骨脆性增加、易发生骨折为特征的全身性骨病(世界卫生组织,WHO,1994年)。
美国国立卫生研究院提出,骨质疏松症是以骨强度下降、骨折风险性增加为特征的骨骼系统疾病,骨强度包括骨密度和骨质量。
骨质疏松症可分为原发性骨质疏松症和继发性骨质疏松症。
骨质疏松性骨折(脆性骨折)指患骨质疏松症后,因骨密度和骨质量下降导致骨强度减低,受到轻微暴力甚至在日常活动中即可发生的骨折,属病理性骨折,是骨质疏松症最严重的后果。
常见的骨折部位是脊柱、髋部、桡骨远端和肱骨近端。
骨质疏松性骨折的特点及治疗的难点:①骨质疏松症患者罹患骨折并卧床后,将发生快速骨丢失,会加重骨质疏松症;②骨折部位骨量低,骨质量差,多为粉碎性骨折,复位困难,不易达到满意效果;③内固定治疗稳定性差,内固定物及植入物易松动、脱出,植骨易吸收;④骨折愈合过程缓慢,恢复时间长,易发生骨折延迟愈合甚至不愈合;⑤其他部位发生再骨折的风险明显增大;⑥多见于老年人,常伴发其他器官或系统的疾病,全身状况差,治疗时易发生并发症,增加治疗的复杂性与风险性;⑦致残率、致死率较高,严重威胁老年人的身心健康、生活质量和寿命;因此,骨质疏松性骨折的治疗有别于一般的创伤性骨折,既要重视骨折本身的治疗,也要积极治疗骨质疏松症。
骨质疏松性骨折女性多见,60岁以上人群多发。
多为轻微外伤(指平地或身体重心高度跌倒所引起的损伤)或没有明显外伤史,甚至在日常活动中也可发生。
临床特征有:骨折的一般表现;骨折的特有表现;X线检查可确定骨折的部位、类型、移位方向和程度,对骨折诊断和治疗具有重要价值。
X 线片除有骨折的特殊表现外,还有骨质疏松的表现,如骨密度降低、骨小梁稀疏、骨皮质变薄、骨髓腔扩大等。
CT能够准确显示骨折粉碎的程度,并能显示椎管内压迫情况,三维成像技术能清晰显示关节内或关节周围骨折,MRI对于发现隐匿性骨折以及鉴别新鲜和陈旧性骨折具有重要意义。


《中国老年骨质疏松症诊疗指南(2023)》重点内容骨质疏松症是一种以骨量减低、骨组织微结构损坏,导致骨脆性增加、易发生骨折为特征的全身性骨病。
《中国老年骨质疏松症诊疗指南(2023)》是对2018版指南的更新,旨在更好地规范和指导我国老年骨质疏松症的临床诊治工作。
临床问题1骨转换标志物(BTM) 在老年骨质疏松症诊疗中的应用价值及其选择推荐意见1:(1)BTM 能反映骨转换状态(高转换或低转换),具有灵敏度、特异度高的特点,可用于评定老年骨质疏松症的骨转换状态,鉴别是否为继发性骨质疏松症,预测骨折风险,评价抗骨质疏松药物疗效及用药依从性。
推荐I 型胶原N 端前肽(PINP) 和血清I 型胶原C 末端交联肽(CTX) 作为首选的骨形成和骨吸收标志物。
BTM 检测较骨密度检测能更早地反映药物疗效,可在用药后3个月开始检测,每隔3~6个月检测1次。
(1B)(2)应预先检测BTM 的基线水平,作为对照。
复测时应采用相同测量方法,并与最小有意义变化值(LSC) 比较,以便除外系统误差,正确判断BTM 改变的临床意义。
(2C)临床问题2定量计算机断层扫描(QCT) 如何用于老年骨质疏松症的诊断?推荐意见2:(1)QCT 在老年人群中的诊断标准为:通常取2个腰椎椎体松质骨骨密度平均值,腰椎QCT 骨密度绝对值>120 mg/cm3 为骨密度正常,80~120 mg/cm3为低骨量,<80 mg/cm3 为骨质疏松。
(2B)(2)建议QCT与临床影像检查的胸、腹部或髋部等CT扫描同时进行,单独扫描时应尽可能采用低剂量CT 扫描技术。
(2C)临床问题3老年骨质疏松症患者如何补充钙剂推荐意见3:(1)老年骨质疏松症患者普遍存在钙与维生素D 不足或缺乏。
联合补充钙与维生素D 可以增加腰椎和股骨颈的骨密度,小幅降低髋部骨折风险。
老年骨质疏松每日摄入元素钙的总量为1000~1200 mg, 可耐受最高量为2000 mg, 除饮食补充外,每日尚需补充元素钙500~600 mg, 钙剂选择需要考虑元素钙含量、安全性、有效性和依从性。
2023年华医网继续教育专业课《骨质疏松症的全程管理》习题答案一、骨质疏松症治疗的疗效监测与评估1、临床实践中可以将骨折判断为治疗失败的是()A、腰部在抗骨质疏松治疗期间出现两次及以上脆性骨折B、手部在抗骨质疏松治疗期间出现两次及以上脆性骨折C、膝关节骨折在抗骨质疏松治疗期间出现两次及以上脆性骨折D、足骨在抗骨质疏松治疗期间出现两次及以上脆性骨折E、指(趾)骨在抗骨质疏松治疗期间出现两次及以上脆性骨折2、临床实践中通过骨密度改变,判断标准的是()A、骨密度降低B、骨密度升高C、腰椎骨密度下降≥5%D、股骨颈骨密度下降≥4%E、腰椎骨密度下降≥8%3、对于国际临床骨密度测量学会推荐BMD的精确度及LSC 的可接受范围描述正确的是()A、全髋1.8%(LSC=6.0%)B、腰椎1.9%(LSC=6.9%)C、股骨颈2.5%(LSC=7.8%)D、腰椎1.9%(LSC=5.3%)E、全髋1.8%(LSC=7.0%)4、骨密度检测部位的首选的是()A、头部B、股骨颈C、腰椎正位(L1-4)D、全髋部E、腰部5、判断治疗有效的标准是使用抗骨吸收药物的患者骨吸收指标的降低()A、>30%B、>50%D、>20%E、>10%二、继发性骨质疏松的现状和机制1、糖皮质激素(GC)广泛用于各种慢性疾病,Meta分析显示,30岁人群使用GC比例是()A、5%B、3%C、6%D、10%E、7%2、美国国立卫生研究院2001年发表《骨质疏松的预防、诊断及治疗》指南,男性骨质疏松患者与继发性因素相关的人数所占比例()A、30%-60%B、20%-30%C、10%-20%E、10%-25%3、以下药物相对作用强度最高的是()A、氯屈膦酸B、唑来膦酸C、阿伦膦酸D、利塞膦酸E、伊班膦酸4、以下常见风湿性疾病患者骨质疏松发生率所占比例最高的是()A、强直性脊柱炎B、系统性红斑狼疮C、系统性硬化D、类风湿性关节炎E、肝硬化5、糖皮质激素(GC)广泛用于各种慢性疾病,Meta分析显示,50岁人群使用GC比例是()A、4.6%B、4.7%C、4.5%D、3.8%E、3.7%三、警惕甲状腺疾病继发性骨质疏松症1、甲状腺激素参与骨质疏松症发病机制,说法有误的是()A、过量TH直接作用使成骨细胞与破骨细胞,使其活性下降B、TH通过直接或间接途径影响破骨/成骨细胞活性,影响骨吸收C、TH间接作用于成骨细胞(IGFs、FGFs、Wnt途径)、破骨细胞(OPG/RANKL、M-CSF途径)参与调控其增殖分化的过程,即通过各种细胞因子或生长因子影响骨吸收D、破骨细胞活性增加占主导作用E、IL-6还可与其他细胞因子共同作用促进骨吸收2、国内外报道甲亢并发骨质疏松症约()A、10%~50%B、30%~50%C、40%~50%D、20%~60%E、20%~50%3、研究结果显示, 340例甲亢患者中骨质疏松症发生率为()A、32.1%B、13.1%C、27.1%D、23.1%E、18.6%4、属于甲减性骨质疏松症特点的是()A、骨转换增加B、骨矿化下降10%C、低代谢,骨转换减慢D、骨重建的周期缩短50%,为113天E、骨形成期缩短2/35、甲减性骨质疏松症骨重建周期延长为()A、113天B、226天C、500天D、700天E、891天四、2017版《原发性骨质疏松症诊疗指南》解读1、下列抗骨质疏松症药物中具有肿瘤风险,连续使用不超过三个月的是()A、锶盐B、降钙素类C、维生素K类D、甲状旁腺素类似物E、活性维生素D及其类似物2、对于FRAX存在的问题与局限描述错误的是()A、目前FRAX?预测结果可能低估了中国人群的骨折风险B、仅适用于绝经后妇女C、不同国家、性别、不同年龄段应有不同的干预阈值D、不适于已接受有效抗骨质疏松药物治疗的人群E、FRAX?纳入的危险因素不全3、建议行胸腰椎X线侧位影像及其骨折判定的是()A、女性65至69岁和男性70至79岁,椎体、全髋或股骨颈骨密度T-值≥-1.5B、50岁以下男性较年轻时最高身高缩短≤4cmC、女性70岁以上和男性80岁以上,椎体、全髋或股骨颈骨密度T-值≤-1.0D、绝经后女性1年内身高进行性缩短≤2cmE、50岁以下男性近期或正在使用长程(<3个月)糖皮质激素治疗4、亚洲人骨质疏松自我筛查工具(OSTA)的计算公式是()A、OSTA 指数=[体质量(kg)-年龄(岁)]×0.3B、OSTA 指数=[体质量(kg)-年龄(岁)]×0.5C、OSTA 指数=[体质量(kg)-年龄(岁)]×0.2D、OSTA 指数=[体质量(kg)-年龄(岁)]×0.4E、OSTA 指数=[体质量(kg)-年龄(岁)]×0.15、我国50岁以上人群骨质疏松症患病率女性为20.7%,男性为()A、14.4%B、12.4%C、13.4%D、15.4%E、11.4%五、关于补充钙和维生素D的讨论1、在2017原发性骨质疏松症诊治指南中,50岁及以上人群每日钙推荐摄入量为()A、800mgB、600~800mgC、1000~1200mgD、1200~1400mgE、500~800mg2、全球骨质疏松症患者已超过()A、1亿B、11亿C、12亿D、2亿E、3亿3、维持钙稳态的生理意义有()A、维持体内酸碱平衡B、骨矿化重要组成C、调控人体血脂D、参与神经肌肉的应激过程E、以上都是4、髋部骨折1年之内,约20%患者可因各种并发症死亡, 患者因此致残使生活质量明显”下降的比率为()A、30%B、40%C、50%D、 10%E、20%5、钙约占成人体重的()A、0.5%B、1~2%C、2~3%D、3~4%E、4~5%。