有机化学 第十章
- 格式:doc
- 大小:628.00 KB
- 文档页数:4

第十章 醛酮含有羰基的化合物:O H O CH3CCH3 O C CH3醛和酮:CH 3C羧酸 羧酸:CH3CO OHCOOH COOH COOHOH CH3CHCOOHO羧酸衍生物:CH3COCl (CH3CO) ( )2OCOOC 2H 5NHOβ-二羰基化合物:CH3CCH2COOC 2H5CH2COOC2H5 COOC2H5210 醛和酮教学大纲(醛和酮)醛和酮的结构与物理性质 醛和酮的结构与物理性质; 醛和酮的化学性质:1.与氢氰酸加成; 2.与亚硫酸氢钠加成; 3.与醇亲核加成; 4.与氨的衍生物反应; 5.与Grignard试剂加成; 试剂加成 6.醇醛缩合反应; 7 卤化和卤仿反应; 7. 卤化和卤仿反应 还 原 反 应 —— 催 化 加 氢 、 金 属 氢 化 物 还 原 、 Clemmenson 还 原 、 WolffKishner黄鸣龙还原、Cannizzaro反应;氧化反应)。
羰基 carbonylOR C H R O C R'醛(aldehyde)O R C O R C R' Ar H Ar O C O C R H酮(Ketone K t )Oβ αC H(R)CC脂肪族醛、酮芳香族醛、酮α,β-不饱和醛、酮4命名:O CH3CCH2CH2CHOO O CH3CCHCCH3 CH2CH=CH24-氧代戊醛3-烯丙基-2,4-戊二酮OO CHO环己酮CHO2'-氧代环己基甲醛CHO OH O CHO苯甲醛2-羟基苯甲醛 (水杨醛)呋喃甲醛 (糠醛)5z醛和酮的结构2spCσOδ C+δO键角接近 120 °1 C=O双键是由一个σ键和一个π键组成的。
2 羰基碳原子为 sp2杂化轨道与氧原子的 p 轨道和其它两个原子 形成三个 形成 个σ键 键,一个 个 p轨 轨道与氧原子的 与氧 子 p轨 轨道侧面交盖成 侧面交 成π键 键, 氧原子上另有两对孤对电子处于氧的s轨道和p轨道中。







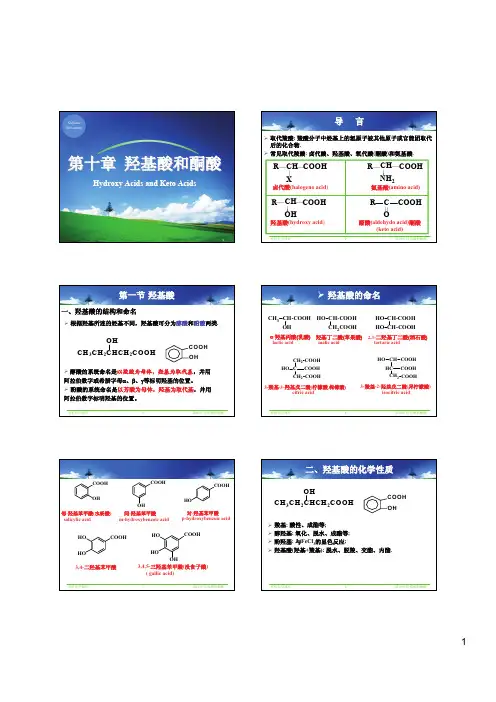


第十章醛酮的结构与性质引言醛酮分之中都会含有羰基( ),羰基中碳原子是sp2杂化的,三个杂化轨道形成三个δ键,其中一个是和氯形成的δ键。
这三个键在同一平面上,彼此间理论键角为120°,但由于三个键所连基团不同,相互作用有差别,因此键角和理论值略有出入。
碳原子和剩下的一个轨道和氧原子的轨道重叠形成Л键,因此羰基是由一个δ键和一个Л键所组成的碳氧双键,如图:图10.1羰基的结构及其电子云示意图羰基中碳氧双键与烯烃中碳碳双键不同,是极性的双键(由于氯原子的电负性比碳大),成键电子云密度在氧原子处较高,氧原子带部分负电荷(δ-),而碳原子处电子云分布较低,因而带部分正电荷(δ+)。
极性碳氧双键易受到带负电荷或孤对电子的试剂(即亲核试剂)的进攻,发生亲核加成反应,这是羰酮经典的反应之一。
羰基是极性基团具有较强的吸电子诱导反应,因而羰基的α-H具有一定的“酸性”,在碱性条件下离去后形成碳负离子,作为亲核试剂与另一分子的醛(或酮)发生醇醛缩合(或醇酮缩合)反应。
另外醇酮的羰基易发生氧化还原反应。
10.1 亲核加成反应醛酮的亲核加成反应是其经典的反应之一,可用下列通式表示:在反应过程中,首先是试剂的亲核部分(Nu-)向羰基碳进攻,形成负氧离子,再与带正电荷的亲电部分(A+)结合。
影响亲核加成速度主要是电子效应和空间效应。
羰基碳原子的正电性的高低决定反应速度的快慢,吸电子取代基加快反应进程,供电子取代基减慢反应进程。
由于在决定反应速度的步骤中碳原子由于sp2杂化转变为sp3杂化,键角变小,基团的排斥作用增强,因此羰基所连的基团的大小也对反应速度产生影响。
基团越大,空间位阻越大,反应速度越慢。
下列醛酮的亲核加成反应活性由强到弱的顺序为:(1)(2)10.1.1含氧亲核试剂的加成反应1.与水的加成反应水和醇都是含氧的亲核试剂。
在一定的条件下水可与醛酮的羰基加成形成水合物,但是水合物极不稳定,很易失水:(平衡主要偏向反应物方向)只有活性较强的醛的水合物较稳定,如甲醛在水溶液中几乎全部以水合物形式存在,但不能分裂,而三氯乙醛的水合物其吸收光谱图表明不含羰基:水合氯醛2.与醇的加成反应:在干燥的HCl作用下,醛与等摩尔的醇亲核加成生成半缩醛,半缩醛可与另一摩尔的醇发生反应,生成缩醛:半缩醛缩醛缩醛对碱和氧化剂都很稳定,在有机合成中常用此反应来保护醛酮。
第十章 醇和醚
一. 写出下列化合物用高碘酸氧化生成的产物:
3
OH CH 2
OH
1.
2.
3.
4.
二. 写出下列化合物在酸催化下的重排产物:
1. 2.
3. 4.
(C 6H 5)2C C(C 6H 5)2
OH
OH OH OH
(C 6H 5)2C C(CH 3)2
OH OH OH OH C(C 6H 5)2
三. 写出下列反应的产物:
CH 2
OH H 3C
CH 3
Br 2, CHCl 3
1.
2.
3.
4.
5.
CH 3
OH
Br
(CH 3)2C=CH 2, H 2SO 4
OH 3323
O
CHO
OH OCH 3
OH
四. 如何完成下列转变?
1. 2. 3. 4.(CH3)3C O(CH3)3C CH3 Br CH2Br
CH2OH
OH
OH
C6H5
OH
6
H5
五. 推测下列化合物的结构:
1. C9H12O, V max: 3350, 3070, 1600, 1490, 1240, 830cm-1, δH: 0.9(t, 3H), 1.5(m, 2H),
2.4(t, 2H), 5.5(b, 1H), 6.8(q, 4H)ppm。
2. C10H14O, V max: 3350, 1600, 1490, 710, 690cm-1, δH: 1.1(s, 6H), 1.4(s, 1H), 2.7(s, 2H), 7.2(s, 5H)ppm。
3. C10H14O, V max: 3340, 1600, 1490, 1380, 1230, 860cm-1, δH: 1.3(b, 9H),
4.9(b, 1H), 7.0(q, 4H)ppm。
4. C9H11BrO, V max: 3340, 1600, 1500, 1380, 830cm-1, δH: 0.9(t, 3H), 1.6(m, 2H), 2.7(s, 1H),
4.4(t, 1H), 7.2(q, 4H)ppm。
5. C8H18O2, V max: 3350, 1390, 1370cm-1, δH: 1.2(s, 12H), 1.5(s, 4H), 1.9(s, 2H)ppm.
与高碘酸无反应。
6. V max: 3600, 1600, 1500, 1160, 1010, 760, 690cm-1, δH: 2.8(s, 1H),
7.3(s, 15H)ppm, Ms, m/z: 260, 183, 78。
7. V max: 3600, 3030, 1600, 1500, 1180, 1020, 826cm-1, δH: 5.1(s, 1H, 加D2O后消失), 6.8(q, 4H)ppm, Ms, m/z: 176(M+4), 174(M+2), 172(M, B), 93(19.5), 75(1), 65(31)。
8. V max: 3200(b), 1500, 1480, 1200(b), 820cm-1, δH: 6.6(s, 4H, ), 7.5(s, 2H, 加D2O后消失)ppm, Ms, m/z: 110(M, B)。
六. 写出下列反应的反应机理:
OHOH
H
NaBH
4
H
答案
一. 写出下列化合物用高碘酸氧化生成的产物:
O
1.
2.
3.
4.
O O
+HCHO
O
O
二. 写出下列化合物在酸催化下的重排产物:
3.1. 2.
4.
(C 6H 5)2C (C 6H 5)3C C 6H 5
C O
O
3
C O
CH 3
C 6H 5
C 6H 5O
三. 写出下列反应的产物:
CH 2
OH H 3C
CH 3
1.
2.
3.
4. 5.
CH 3
OH
Br OH 3
CHO
OH OCH 3
OH Br
(H 3C)3
O O 2N
四. 如何完成下列转变?
1.2.3.
4.
(CH 3)3C
O
(CH 3)3
C
CH 3
Br
CH 2
Br
CH 2OH
OH
OH
C 6H
5
OH 6H 5CH 3MgI
H
Mg HCHO
HBr
HIO 4
NaBH 4
KMnO 4
稀
五. 推测下列化合物的结构:
1.
2.
3. 4.5.
6.
7.8.CH 3CH 2CH 2
OH
CH 2C(CH 3)2
OH
HO
C(CH 3)3
Br
CHCH 2CH 3OH
OH
HO
(C 6H 5)3C
OH
Br OH HO OH。