实验-食盐中碘的含量测定
- 格式:doc
- 大小:39.50 KB
- 文档页数:4

实验11 食盐中碘含量的测定教学目的与要求:1.学习测定食盐中碘含量的原理和方法;2.了解碘量法测定食盐中碘含量的具体步骤;3.让学生熟练掌握移取,称量,配制一定浓度标准溶液等操作;4.进一步熟练掌握滴定操作;5.学会如何合理的设计实验并培养学生的动手操作能力及创新意识。
教学重点与难点:重点:1.碘量法的原理和方法;2.培养学生的动手操作能力及创新意识。
难点:1.降低碘量法测定误差的条件控制;2.碘量法滴定中反应条件的控制。
教学方法与手段:板书,学生操作,现场指导。
学时分配:3学时。
教学内容:食盐,又称餐桌盐,是对人类生存最重要的物质之一,也是烹饪中最常用的调味料。
盐的主要化学成份氯化钠(化学式NaCl)在食盐中含量为99%,部份地区所出品的食盐加入氯化钾以降低氯化钠的含量以降低高血压发生率。
同时世界大部分地区的食盐都通过添加碘来预防碘缺乏病,添加了碘的食盐叫做碘盐。
2011年3月11日,日本本州岛海域发生地震引发核电站爆炸,我国多地居民出现为防止核辐射而抢购食盐的现象,专家表示,吃食盐能防辐射一说不靠谱,市民请勿信谣言。
问题1:食盐中为什么加碘?碘是人体必需的微量元素之一,有智力元素之称。
世界卫生组织将碘缺乏危害简称IDD,为目前导致人类智力发育落后的最主要原因。
现已证实,人脑发育大部分是在胚胎期和婴幼儿期完成的。
在智力发育全过程中,如果碘摄入不足,就会在生长发育过程中产生一系列障碍,即使轻微缺碘,也会引起智力的轻度落后并持续终生。
而严重的缺碘会对儿童的体格发育造成障碍,即身材矮小,性发育迟缓、智商低下。
并可造成早产、死胎、先天畸形、聋、哑、痴呆等,更为常见的为地方性甲状腺肿(即粗脖子病)和地方性克汀病。
这些损害统称为碘缺乏病。
问题2:食盐中添加的碘以什么形式存在?如何检验?食盐中添加的碘以碘酸钾形式存在。
检验方法:①碘单质的检验:淀粉溶液+食盐。
结果:不变蓝,说明食盐中的碘不是碘单质。
②碘化物的检验:5mLH2O2+少量食盐+几滴硫酸+滴入淀粉溶液;对比实验:5mLH2O2+少量碘化钾+几滴硫酸+滴入淀粉溶液。

食盐中碘含量的光度分析法测定李继胜,朱自强,彭 滨 摘要: 目的 用较简单的方法测定食盐中碘的含量。
方法 试用分光光度法(波长为590nm)测定食盐中碘的含量。
结果 在30m in内测定其吸光度,碘浓度在0.3~1.6L g/ml范围内呈线性,碘标准曲线的相关系数r=0.992; 5次精密度测定标准偏差RSD s=0.425%;加标试验平均回收率=100.4%。
结论 试验表明:分光光度法测定食盐中微量碘酸钾含量的方法简单、快速,有较高的灵敏度和较好的准确性。
关键词: 碘酸钾;分光光度法;食盐 中图分类号:O657.3 文献标识码:ASpectrophotometer Determination Of Micro Amounts of Potassium Iodate in Edible Salt Li Jisheng,Zhu Ziqiang,Peng Bin (Dept.o f Chemistry,Wuyi University,Jiangmen529020,China) Abstract: Obj ective A m ethod for the determinati on of m icro amounts of potassium iodate in iodized salt by spec-trophotom eter was reported in this paper. Result The l inear range of the method was0.3~1.6L g/ml and r=0.992 ,the average recovery was100.4%,the RSDs were0.425%(n=5). Conclusion The method is pr oved to be sim-pl e,rapid and reliable with hi gher sensiti vity and better accuracy,and has been used for determination of potassium io-date in edible salt wi th satisfactory results. Key words: Potassium iodate;Spectrophotometer;Edible sal t 食盐加碘是防治碘缺乏病的根本措施,食盐的含碘量一般采用直接滴定方法检测。

食盐中碘含量的测定组员:梁惠芳,何佩芬,龙业添,任华丰,黄华明一.实验目的1.学习使用色度计传感器。
2.使用色度计测定食盐中的碘含量。
二.实验原理在酸性条件下,溶液中的碘酸根离子定量地被碘化钾溶液还原为碘单质,碘与淀粉反应使溶液变蓝,在一定条件下,颜色随碘浓度的增大而加深。
通过色度计传感器测量标准溶液的吸光度后,在标准曲线上查出食盐中碘的含量5I- + IO3- + 6H+ ===3I2 + 3H2O三.实验仪器1.仪器色度计传感器,数据采集器,移液管,烧杯,100ml容量瓶,吸液球,玻璃棒2.试剂0.001mol/L KIO3标准溶液,2mol/LH2SO4溶液,10%KI溶液,淀粉指示剂(5g/L)四.实验步骤及数据处理1.用移液管准确移取0.001mol/L KIO3标准溶液10.00ml,8.00ml,6.00ml,4.00ml,2.00ml分别于50ml烧杯中,然后依次向烧杯中加入0.00ml,2.00ml,4.00ml,6.00ml,8.00ml蒸馏水。
2.向烧杯中依次加入2滴2mol/LH2SO4,摇匀后加入3ml 10%KI溶液,再加入适量的淀粉指示剂直至溶液变为蓝色不再加深。
3.连接色度计传感器与数据采集器,用蒸馏水进行校正使透光率为100%,再依次取上述的待测标准溶液于比色皿中测量吸光度,按照浓度由低到高测量,重复3次平行测量,绘制标准曲线。
4.称取15.0g食用加碘盐于50ml烧杯中,加适量蒸馏水溶解,然后定容至100ml,再用移液管准确移取10.00ml待测溶液于烧杯中,然后按照测量标准溶液吸光度的方法测量待测溶液,重复3次平行测量,然后利用标准曲线查找待测溶液的浓度,再计算食盐中碘的含量。
实验数据记录与处理文献值:碘酸钾(以I计)18-33mg/kg。
![加碘食盐中碘含量的测定[宝典]](https://uimg.taocdn.com/46799ae3f71fb7360b4c2e3f5727a5e9856a2784.webp)
加碘食盐中碘含量的测定一、实验目的1、学会查阅本实验的相关资料;2、设计出该实验的实验原理;3、拟定完成该实验所需试剂及仪器;4、拟定完成该实验的具体步骤;5、进一步熟悉滴定操作。
二、实验原理由于加碘食盐中碘元素绝大部分是以IO3-存在,少量的是以I-形式存在。
食盐溶于水后,在酸性条件下,加入饱和溴水,I-被氧化为IO3-,再用过量的甲酸钠除去过量的溴。
在酸性条件下,加入碘化钾,I-与IO3-反应析出I2,然后用标准的硫代硫酸钠滴定I2,从而确定碘元素的含量。
发生的反应如下:I-+3Br2+3H2O IO3-+6H++6Br-Br2+2HCOO-+2H22CO32-+4H++2Br-IO3-+ 5I-+6H3I2+3H2O I2+ 2S2O32- 2I-+ S4O62-故有 KIO3~I ~ 3I2~ 6Na2S2O3及I ~KIO3~ 3I2~ 6Na2S2O3三、试剂及仪器酸式滴定管,锥形瓶(250mL),容量瓶(250mL),移液管(25mL),FA/JA1004型电子天平,称量瓶,滴定管夹, 托盘天平, 滤纸 , 药匙 , 铁架台, 小烧杯,量筒(5mL,10mL) ,恒温箱;食用加碘盐,蒸馏水,2mol/L盐酸,10%的KI溶液,0.003mol/L的Na2S2O3溶液,1%的淀粉试液,碘酸钾,甲酸钠(10%),饱和溴水。
四、实验步骤1、配制碘酸钾标准溶液在分析天平上称取0.04~0.06g(于110±2°烘至恒重的)碘酸钾,加30mL 蒸馏水,待完全溶解后冷至室温,然后配成250mL溶液。
2、标定硫代硫酸钠用移液管移取25.00mL标准碘酸钾溶液于250mL锥形瓶中,加50mL蒸馏水,2mL 2mol/L盐酸,摇匀后加3mL10%的KI溶液,摇匀后立即用Na2S2O3标准溶液滴至浅黄色,再加入2mL1%的淀粉溶液,继续滴至蓝色恰好消失为止,记录所用Na2S2O3标准液的体积。

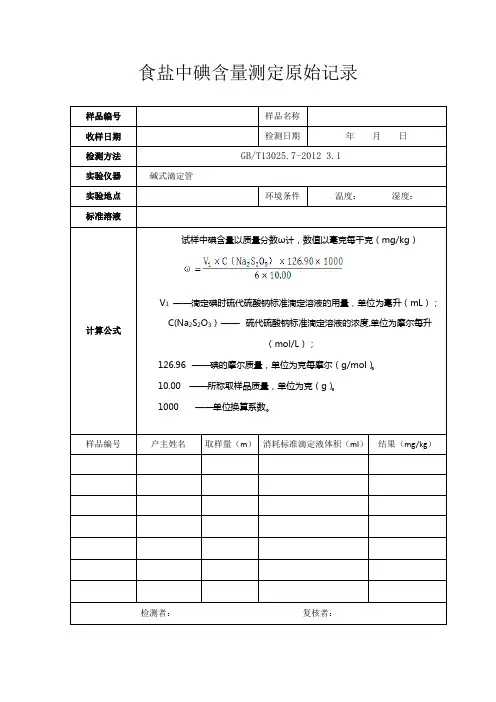
食盐中碘含量测定原始记录
样品编号样品名称
收样日期检测日期年月日检测方法GB/T13025.7-2012 3.1
实验仪器碱式滴定管
实验地点环境条件温度:湿度:标准溶液
计算公式
试样中碘含量以质量分数ω计,数值以毫克每千克(mg/kg)
式中:
V1 ——滴定碘时硫代硫酸钠标准滴定溶液的用量,单位为毫升(mL);C(Na2S2O3)——硫代硫酸钠标准滴定溶液的浓度,单位为摩尔每升
(mol/L);
126.96 ——碘的摩尔质量,单位为克每摩尔(g/mol)。
10.00 ——所称取样品质量,单位为克(g)。
1000 ——单位换算系数。
样品编号户主姓名取样量(m)消耗标准滴定液体积(ml)结果(mg/kg)检测者:复核者:。

·试设计用沉淀滴定法测定加碘食盐中碘含量的实验方案实验目的:设计一种用沉淀滴定法测定加碘食盐中碘含量的实验方案。
实验原理:沉淀滴定法是一种常用的分析方法,通过将待测物与适当试剂反应生成沉淀,然后用标准溶液进行滴定,根据滴定终点的变化确定待测物的含量。
实验步骤及操作:1. 样品制备:a. 取一定质量的加碘食盐样品,称为m1(单位:克)。
b. 将m1溶解在适量的去离子水中,转移至100 mL容量瓶中,并摇匀。
c. 取10 mL溶液转移至50 mL锥形瓶中。
2. 滴定操作:a. 准备0.01 mol/L硫酸钠标准溶液(V1 mL)。
b. 取50 mL锥形瓶中的样品溶液,加入适量甲醇和混合指示剂(如混合铁指示剂),使其呈现明显颜色变化。
c. 用0.01 mol/L硫酸钠标准溶液进行滴定,直至颜色变化消失或从蓝色转变为黄色。
d. 记录滴定所需的标准溶液体积为V2 mL。
3. 数据处理:a. 计算加碘食盐中碘的含量(C,单位:mg/kg):C = (V1 - V2) × 0.0127 × 1000 / m1其中,0.0127为碘的摩尔质量(单位:g/mol)。
实验注意事项:1. 实验操作时需佩戴实验手套和护目镜,避免化学品直接接触皮肤和眼睛。
2. 实验器材应干净无污染,以免影响实验结果。
3. 滴定时要慢慢滴加标准溶液,避免过量滴定造成误差。
4. 所有试剂均应严格按照安全操作规程使用和保存。
实验结果分析:根据上述计算公式可以得到加碘食盐中碘的含量。
通过重复实验并取平均值可以提高结果的准确性。
还可以与其他测定方法进行对比验证所得结果的可靠性。
实验方案评价:本实验方案设计了一种简单、快速、准确测定加碘食盐中碘含量的方法。
该方法采用沉淀滴定法,操作简便,不需要复杂的仪器设备。
通过使用标准溶液进行滴定,可以得到较为准确的测定结果。
同时,该方法也具有一定的经济性和实用性。
总结:本实验方案详细介绍了用沉淀滴定法测定加碘食盐中碘含量的步骤及操作,并给出了计算公式和注意事项。

食盐中碘含量测定问题的探讨杨荣淇碘是合成甲状腺激素的主要成分,适量的碘可供应人体合成生长发育所必需的甲状腺激素,如果缺乏碘,会产生地方性甲状腺肿和地方性克汀病,但碘过量则又可引起甲状腺功能低下和甲状腺肿大。
为了保障人民群众的健康,国家规定食用盐中必须加碘,且严格控制碘加入量,因而对于食用盐中碘含量的测定十分重要。
目前我国国家标准GB/T 13025.7—91《制盐工业通用试验方法碘离子的测定》(简称国标法)•采用的是溴水氧化法,即在酸性溶液中碘离子经溴氧化为碘酸根,再加碘化钾析出碘,而后用硫代硫酸钠标准溶液滴定,测定碘离子含量。
这种方法需消除过量氧化剂,否则将对结果数据产生影响,使试验数据不准确;另外,由于此法使用饱和溴水,对人体的危害和化验室环境的污染较为严重。
为此,本人查阅有关资料,设计了“双氧水氧化—吸光光度法”测定食盐中碘含量的试验方法,通过反复对比试验,认为采用该法能够达到精确度高、操作简便、不需消除过量氧化剂的影响且无污染的效果。
一、试验部分1、原理在酸性条件下,溶液中的碘离子经过过氧化氢(双氧水)氧化为碘,碘与淀粉反应使溶液变蓝,在一定条件下,颜色随碘浓度的增大而加深。
通过分光光度计测量溶液的吸光度后,在标准曲线上查出碘离子的含量。
2I-+H2O2+2H+ → I2+2H2O本试验采用在氯化钠溶液中加入已知浓度的碘化钾溶液来模拟加碘食盐溶液,通过测定出的碘含量与已知值比较,来判断试验的准确性与精确度。
2、试验(1)主要仪器与试剂721分光光度计(上海分析仪器厂)。
本法所有试剂和水未特别注明要求的,均使用分析纯试剂和蒸馏水。
碘化钾标准溶液:100ug/ml,准确称取碘化钾0.1000g溶于水,定容至1l (用时新配)。
碘化钾标准使用液:10ug/ml,准确移取10.00mL碘化钾标准溶液于100ml容量瓶中,用水定容至刻度。
氯化钠溶液:200g/l,称取氯化钠100.0g溶于水,定容至500ml。

食盐中碘含量的测定实验报告食盐中碘含量的测定实验报告引言:食盐是我们日常生活中必不可少的调味品之一,而碘是人体必需的微量元素之一,对于人体的正常生长发育和代谢具有重要的作用。
因此,了解食盐中的碘含量对于人们的健康至关重要。
本实验旨在通过一系列的实验步骤,测定食盐中的碘含量,并对实验结果进行分析和讨论。
实验方法:1. 实验器材准备:分析天平、研钵、研杵、滴定管、锥形瓶、滴定管架等。
2. 食盐样品的制备:将一定量的食盐样品取出,放入研钵中,用研杵研磨成细粉末状。
3. 碘酸钠溶液的制备:称取一定量的碘酸钠固体,溶解于一定体积的去离子水中,搅拌均匀。
4. 滴定实验的进行:取一定量的食盐样品溶解于一定体积的去离子水中,加入淀粉溶液作为指示剂,滴定碘酸钠溶液至溶液呈现蓝色为止,记录滴定所需的碘酸钠溶液体积。
5. 实验数据处理:根据滴定所需的碘酸钠溶液体积和样品的质量,计算出食盐中的碘含量。
实验结果与分析:通过实验测定,我们得到了食盐中的碘含量为X mg/kg。
根据相关标准,食盐中的碘含量应在Y mg/kg范围内。
比较实验结果与标准要求,可以判断该批食盐的碘含量是否符合标准。
在实验过程中,我们使用了滴定法来测定食盐中的碘含量。
滴定法是一种常用的定量分析方法,通过溶液之间的反应来确定物质的含量。
在本实验中,我们使用了碘酸钠溶液作为滴定试剂,它与食盐样品中的碘反应生成碘酸盐,从而确定食盐中的碘含量。
实验中还添加了淀粉溶液作为指示剂。
淀粉溶液在碘溶液中呈现蓝色,而在滴定过程中,当食盐样品中的碘被滴定试剂完全反应消耗后,溶液中的碘浓度降低,淀粉溶液不再呈现蓝色,这时滴定过程结束。
实验中的数据处理非常重要。
通过计算滴定所需的碘酸钠溶液体积和样品的质量,我们可以得到食盐中的碘含量。
在实验中,我们还应注意实验条件的控制,如溶液的浓度、滴定剂的滴定速度等,以保证实验结果的准确性和可靠性。
结论:通过本实验的测定,我们得到了食盐中的碘含量为X mg/kg。

食盐中含碘成分的检验及碘含量的测定一实验研究的目的:市售的碘盐中碘的成分有可能是碘,碘化物或碘酸物等含碘物质,对市场上所售的食盐进行含碘物质的检验,以及测定食盐中的碘含量。
二实验原理:食盐中的碘遇淀粉变成蓝色;食盐中还有可能添加碘化钾,KI与高锰酸钾(氧化剂)反应生成碘,碘遇淀粉呈蓝色;食盐中还有可能添加碘酸钾,KIO3与亚硫酸钠(还原剂)反应生成碘,碘遇淀粉呈蓝色;食盐中加入的碘化钾经溴水氧化后变成碘酸钾,碘酸钾在酸性介质中可以与碘化钾反应析出碘,析出的碘可用硫代硫酸钠滴定。
三实验用品:食盐样品蒸发皿锥形瓶玻璃珠实验试剂:淀粉溶液稀硫酸高锰酸钾溶液亚硫酸钠溶液磷酸溴水碘化钾溶液硫代硫酸钠溶液四实验方案:在超市买一包食盐,进行碘,碘化物和碘酸物的检验。
1 碘的检验:在蒸发皿上加入少量食盐,滴加淀粉溶液,观察是否变成蓝色,色泽越深含碘量越高,如果不变色则说明不含碘。
2 碘化钾的检验:取2g食盐放在蒸发皿上,向盐上滴加稀硫酸与高锰酸钾溶液,再滴加淀粉溶液,观察是否变成蓝色。
3 碘酸钾的检验:取2g食盐放在蒸发皿上,向盐上滴加稀硫酸与亚硫酸钠溶液,再滴加淀粉溶液,观察是否变成蓝色。
4氧化还原法测定碘:精确称取10.000g待检食盐样品与250ml锥形瓶中加水100ml溶解,向其中加入磷酸1ml,摇匀,滴加饱和溴水至溶液呈浅黄色(边滴边摇),需饱和溴水5至6滴(溴水不要过多,以免以后除去难),在室温下放至5分钟。
5分钟后,向锥形瓶中加入3至5个玻璃珠,加热煮沸溶液,以除去过量溴水。
待溴水的浅黄色褪尽后再加热煮沸5分钟以保证溴水除尽。
将锥形瓶冷却,向其中加入5%的碘化钾溶液2ml,摇匀。
立即用硫代硫酸钠标准溶液滴定至浅黄色,加入0.5%淀粉指示剂1ml,继续滴定至蓝色刚刚消失即为滴定终点。
再按计算式计算碘含量。

实验4 食盐中碘含量的测定一、实验目的要求1、要求学生准确、熟练地掌握滴定操作。
2、要求学生准确、熟练地掌握硫代硫酸钠标准溶液的配制。
3、要求学生掌握食盐中碘含量测定的方法和原理。
4、巩固使用不同标准溶液浓度的温度补正值表和把测量体积校正为标准温度体积的方法。
二、实验原理试样中的碘化物在酸性条件下用饱和溴水氧化成碘酸钾,再于酸性条件下氧化碘化钾而游离出碘,以淀粉作指示剂,用硫代硫酸钠标准溶液滴定,计算含量。
三、实验材料及步骤(一)仪器与试剂仪器:分析天平,烘箱,电炉子,移液管,碘量瓶,容量瓶,大肚移液管,量筒,锥形瓶,烧杯,100mL细口瓶,25mL碱式滴定管,玻璃棒,漏斗,滤纸,温度计,洗瓶。
试剂:固体KI(AR)。
H2SO4溶液(1+8)。
Na2S2O3•5H2O(固)。
Na2CO3(固)。
可溶性淀粉。
K2Cr2O7 (A.R.或基准试剂)。
磷酸。
碘化钾溶液(50g/L):临用时配制。
饱和溴水。
淀粉指示液:临用现配。
硫代硫酸钠标准溶液〔c(Na2S2O3)=0.1mol/L〕,临用时准确稀释至50倍,浓度为0.002mol/L。
(二)供检样品:牌食盐。
(三)国家标准:食盐中碘含量测定:《食品卫生检验理化部分总则》GB/T5009.42-2003。
国家标准GB14880-1994中规定加碘盐中碘含量应为20~30mg/kg。
(四)实验步骤1、进入实验室,将实验要用到的有关仪器从仪器橱中取出,把玻璃器皿按洗涤要求洗涤干净备用。
2、0.1mol/L硫代硫酸钠标准溶液的配制及标定:(1)配制①硫代硫酸钠标准滴定溶液c(Na2S2O3)=0.1 mol/L的配制:称取26g 硫代硫酸钠及0.2g 碳酸钠,加入适量新煮沸过的冷水使之溶解,并稀释至1000mL,混匀,避光放置一个月后过滤备用,待标定。
②0.5%淀粉指示液的配制:称取0.5g可溶性淀粉,加5mL水,搅匀后缓缓倒入100mL沸水中(250mL烧杯),煮沸2min,放凉,备用。
食盐中碘含量的测定实验报告班级:应131-1姓名: JOY学号:************一、实验目的1.对人体的作用,熟悉碘盐中碘的添加形式以及含量范围。
2.掌握滴定的基本操作。
3.掌握碘量法测定碘含量的基本原理,方法。
4.掌握硫代硫酸钠的配置与标定,熟悉硫代硫酸钠与基准物重铬酸钾的反应条件。
二、实验原理1. I -的定性检测:通过NaNO 2在酸性环境下氧化I -生成I 2,遇淀粉呈蓝紫色而检验I -的存在。
2. IO 3-的定性:在酸性条件下,IO 3-易被Na ₂S ₂O ₃还原成I 2,遇淀粉呈现蓝紫色。
但Na ₂S ₂O ₃浓度较高时,生成的I 2又和多余的Na ₂S ₂O ₃反应,生成I -使蓝色消失。
Na ₂S ₂O ₃的浓度控制在一定范围可建立此定性反应。
测定范围是每克食盐含30ug 碘酸钾立即显浅蓝色,含50ug 显蓝色。
含碘越多颜色越深。
3.定量测定:在酸性条件下,饱和溴水氧化样品中的I -还原成O 3-,样品中原有及氧化生成的IO 3-于酸性条件下与I -成的I 2,再用Na ₂S ₂O ₃标准溶液滴定所释放的碘,从而间接计算样品中的碘含量。
化学反应式为:I¯ +3Br 2+3H 2 IO 3-+6H ++6Br -IO 3-+ 5I¯+6H 3I 2 +3H 2O I 2 + 2S 2O 32 2I¯+ S 4O 62-故有 KIO 3~I ~ 3I 2 ~ 6Na ₂S ₂O ₃ 及 I ~KIO 3~ 3I 2 ~ 6Na ₂S ₂O ₃4.Na ₂S ₂O ₃的标定:硫代硫酸钠标准溶液通常用Na ₂S ₂O ₃·5H 2O 配制,由于Na ₂S ₂O ₃遇酸即迅速分解产生S ,配制时若水中含CO 2较多,则pH 偏低,容易使配制的Na ₂S ₂O ₃变混浊。
另外水中若有微生物也能够慢慢分解Na ₂S ₂O ₃。
因此,配制Na ₂S ₂O ₃通常用新煮沸放冷的蒸馏水,并先在水中加入少量Na 2CO 3,然后再把Na ₂S ₂O ₃溶于其中。
加碘食盐中的碘元素实验结论
在本次实验中,我们对市售的加碘食盐进行了实验,以确定其
中的碘元素含量。
实验结果显示,加碘食盐中的碘元素含量符合国
家标准要求。
经过仔细的实验操作和数据分析,我们得出以下结论:
1. 加碘食盐中的碘元素含量稳定。
在多次实验中,我们发现不
同批次的加碘食盐中的碘元素含量基本保持在稳定的水平,符合国
家标准规定的范围。
2. 实验结果与标称值相符。
我们对加碘食盐中的碘元素含量进
行了多次测定,结果显示,实验测得的碘含量与包装上标称的数值
基本一致,表明该食盐生产商在生产过程中对碘元素的添加进行了
精确控制。
3. 加碘食盐对碘元素的释放稳定可靠。
我们通过模拟食用加碘
食盐后,对其中的碘元素进行了释放实验,结果显示,加碘食盐中
的碘元素能够在人体消化道中稳定释放,确保了人体对碘元素的充
分吸收。
综上所述,通过本次实验,我们得出结论,市售的加碘食盐中
的碘元素含量稳定,符合国家标准要求,可以作为人们日常生活中的重要碘补充来源。
同时,我们也提醒消费者在购买食盐时,应选择正规渠道购买,并注意查看包装上的产品标识,确保所购买的加碘食盐符合国家标准要求。
食盐中碘含量的测定实验报告一、实验目的1、掌握碘量法测定食盐中碘含量的基本原理和操作方法。
2、学习使用容量分析仪器,如移液管、容量瓶等。
3、培养严谨的科学态度和实验操作技能。
二、实验原理在酸性条件下,碘酸钾(KIO₃)与碘化钾(KI)反应生成碘(I₂),生成的碘用硫代硫酸钠(Na₂S₂O₃)标准溶液滴定,根据硫代硫酸钠的用量计算出碘的含量。
化学反应方程式如下:KIO₃+ 5KI + 3H₂SO₄= 3K₂SO₄+ 3I₂+ 3H₂OI₂+ 2Na₂S₂O₃= 2NaI + Na₂S₄O₆三、实验仪器和试剂1、仪器电子天平容量瓶(250 mL)移液管(25 mL、5 mL)碘量瓶(250 mL)酸式滴定管(50 mL)玻璃棒烧杯(250 mL、50 mL)2、试剂食盐样品碘化钾溶液(100 g/L)硫酸溶液(1 mol/L)淀粉溶液(5 g/L)硫代硫酸钠标准溶液(0002 mol/L)四、实验步骤1、硫代硫酸钠标准溶液的标定准确称取 015 g 左右基准重铬酸钾(K₂Cr₂O₇)于碘量瓶中,加入 25 mL 水使之溶解。
加入 2 g 碘化钾及 20 mL 硫酸溶液(1 mol/L),摇匀,于暗处放置10 分钟。
用硫代硫酸钠标准溶液滴定至溶液呈淡黄色,加入 3 mL 淀粉溶液(5 g/L),继续滴定至蓝色刚好消失,记录消耗硫代硫酸钠标准溶液的体积 V₁。
2、食盐中碘含量的测定准确称取 1000 g 食盐样品于 250 mL 烧杯中,加适量水溶解后,转入 250 mL 容量瓶中,用水定容至刻度,摇匀。
用移液管准确移取2500 mL 上述溶液于碘量瓶中,加入25 mL 水、5 mL 碘化钾溶液(100 g/L)及 5 mL 硫酸溶液(1 mol/L),摇匀,于暗处放置 5 分钟。
用硫代硫酸钠标准溶液滴定至溶液呈淡黄色,加入 3 mL 淀粉溶液(5 g/L),继续滴定至蓝色刚好消失,记录消耗硫代硫酸钠标准溶液的体积 V₂。
食盐中碘含量的测定
食盐中碘含量的测定是指对食盐中碘的含量进行测定的方法。
一、原理:
碘在酸性溶液中发生氧化还原反应,当电位调节到特定pH值时,碘由高价态I3-变为低价态I2,然后与高效毒标剂(如固定甲酸铵)发生毒标反应,得到黄色棕褐色沉淀,其色度强度可以用分光光度计直接测定。
二、试剂:
(1) 碘标准溶液(1000μg/mL);
(2) 0.1mol/L稀硝酸溶液;
(3) 0.1mol/L硫酸溶液;
(4) 高效毒标剂0.05mol/L固定甲酸铵溶液;
(5) 尿素溶液;
三、实验步骤:
1.将1.00g食盐放入50mL烧杯中加入20mL水,搅拌;
2.加入10mL 0.1mol/L稀硝酸,煮沸15min;
3.加入10mL 0.1mol/L硫酸,煮沸15min;
4.冷却,稀释至100mL;
5.滴入尿素溶液调节pH至
6.5;
6.滴入0.05mol/L固定甲酸铵溶液至暗褐色沉淀,搅拌;
7.用分光光度计测定其色度强度;
8.以碘标准溶液调校,计算结果。
实验报告食盐中碘含量的测定班级:应111-1一.【实验目的】1. 通过本实验了解碘对人体的作用,熟悉碘盐中碘的添加形式以及含量范围。
2. 准确,熟练掌握滴定的基本操作。
3. 熟练掌握碘量法测定碘含量的基本原理,方法。
4. 熟练掌握硫代硫酸钠的配置与标定,熟悉硫代硫酸钠与基准物重铬酸钾的反应条件。
二.【实验原理】在加碘盐的产品质量检验中,碘含量是一项重要的指标 按照GB5461-92的规定,加碘中碘酸钾的加入量应为20-50mg /kg .由于加碘食盐中碘元素绝大部分是以IO 3-存在,少量的是以I -形式存在。
本实验依据碘的性质对其进行定性和定量检测。
1.碘的测定:(1)I -的定性检测:通过NaNO 2在酸性环境下氧化I -生成I 2,遇淀粉呈蓝紫色而检验I -的存在。
(2)KIO 3的定性:在酸性条件下,IO 3-易被Na 2S 2O 3还原成I 2,遇淀粉呈现蓝紫色。
但Na 2S 2O 3浓度太高时,生成的I 2又和多余的Na 2S 2O 3反应,生成I -使蓝色消失。
因此实验中要使Na 2S 2O 3的酸度控制在一定范围。
测定范围是每克食盐含30ug 碘酸钾立即显浅蓝色,含50ug 显蓝色。
含碘越多颜色越深。
(3)定量测定:I -在酸性介质中能被饱和溴水还原成IO 3-,样品中原有及氧化生成的IO 3-于酸性条件下与I -成的I 2再用Na 2S 2O 3标准溶液滴定,以淀粉为指示剂,滴定至溶液的蓝色刚好消失为终点,从而求得加碘盐中的碘含量。
主要反应:I - +3Br 2+3H 23-+6H ++6Br - IO 3-+ 5I -+6H 2 +3H 2O I2 + 2S 2O 32-+ S 4O 62-故有 KIO 3~I ~ 3I 2 ~ 6Na 2S 2O 3 及 I ~KIO 3~ 3I 2 ~ 6Na 2S 2O 3 2.Na 2S 2O 3的标定:(1).结晶硫代硫酸钠含有杂质,不能采用直接法配制标准溶液,且Na 2S 2O 3溶液不稳定易分解。
食盐中碘含量测定问题的探讨
杨荣淇
碘是合成甲状腺激素的主要成分,适量的碘可供应人体合成生长发育所必需的甲状腺激素,如果缺乏碘,会产生地方性甲状腺肿和地方性克汀病,但碘过量则又可引起甲状腺功能低下和甲状腺肿大。
为了保障人民群众的健康,国家规定食用盐中必须加碘,且严格控制碘加入量,因而对于食用盐中碘含量的测定十分重要。
目前我国国家标准GB/T 13025.7—91《制盐工业通用试验方法碘离子的测定》(简称国标法)•采用的是溴水氧化法,即在酸性溶液中碘离子经溴氧化为碘酸根,再加碘化钾析出碘,而后用硫代硫酸钠标准溶液滴定,测定碘离子含量。
这种方法需消除过量氧化剂,否则将对结果数据产生影响,使试验数据不准确;另外,由于此法使用饱和溴水,对人体的危害和化验室环境的污染较为严重。
为此,本人查阅有关资料,设计了“双氧水氧化—吸光光度法”测定食盐中碘含量的试验方法,通过反复对比试验,认为采用该法能够达到精确度高、操作简便、不需消除过量氧化剂的影响且无污染的效果。
一、试验部分
1、原理
在酸性条件下,溶液中的碘离子经过过氧化氢(双氧水)氧化为碘,碘与淀粉反应使溶液变蓝,在一定条件下,颜色随碘浓度的增大而加深。
通过分光光度计测量溶液的吸光度后,在标准曲线上查出碘离子的含量。
2I-+H
2O
2
+2H+ → I2+2H2O
本试验采用在氯化钠溶液中加入已知浓度的碘化钾溶液来模拟加碘食盐溶液,通过测定出的碘含量与已知值比较,来判断试验的准确性与精确度。
2、试验
(1)主要仪器与试剂
721分光光度计(上海分析仪器厂)。
本法所有试剂和水未特别注明要求的,均使用分析纯试剂和蒸馏水。
碘化钾标准溶液:100ug/ml,准确称取碘化钾0.1000g溶于水,定容至1l (用时新配)。
碘化钾标准使用液:10ug/ml,准确移取10.00mL碘化钾标准溶液于100ml容量瓶中,用水定容至刻度。
氯化钠溶液:200g/l,称取氯化钠100.0g溶于水,定容至500ml。
淀粉溶液:10g/l,称取淀粉1g,加入水搅拌成糊状,再缓慢倒入沸水100mL,搅溶后再煮沸半分钟,冷却备用(用时新配)。
过氧化氢(双氧水)溶液:3%。
(2)试验方法
按一定的浓度,准确移取碘化钾标准使用液,加入氯化钠溶液35.0mL,用0.5mol/L盐酸2mL酸化1~2分钟,再加入3%过氧化氢溶液、2.5mL淀粉溶液1.0mL,加水至刻度,摇匀,10分钟后用分光光度计测定吸光度。
二、结果与讨论
由于现实试验条件下有各种影响因素存在,有些在原理上可行的方法在实际中未必可行。
在本试验中,本人通过改变试验条件,对各种可能存在的情况分别进行比较试验,找出有影响的因素,选择最佳的试验条件,保证数据的准确性。
在准确性有保证的情况下,选择简便、快速的试验方法。
对于吸光光度计,不仅要考虑光度计的误差(因为浓度与透光率之间存在对数关系),还要考虑校准曲线的误差。
在实际分析时,除了选用精度高的仪器之外,应尽可能提高校准曲线的精度,拓宽最佳工作范围;同时在取样时尽可能使测量信号落在均值以上的区域。
在试验过程中,通过对比试验得出以下结论:
1、比色皿的选择
按试验方法配制一组除碘化钾标准使用液加入量逐渐递增外,其它试剂加入量不变的溶液,用1.0cm、2.0cm两种比色皿,在固定吸收波长条件下测定吸光度。
结果发现采用1.0cm比色皿得出的吸光度数据偏小且数据之间间隔小,容易造成读数误差。
使用2.0cm比色皿能减少在数据处理过程中人为因素造成的误差,且绘出的曲线比用1.0cm的比色皿得出的曲线更为圆滑合理。
因此选用2.0 cm的比色皿。
2、吸收波长的确定
根据吸光光度法的有关规则,本法需采用可见光测定吸光度,而可见光波长在570~630nm范围内。
在试验中,本人采用每隔5nm测一次吸光度的方法,通过比较,发现在波长595 nm时,吸收曲线的线性最好,故选取最佳波长595nm。
3、溶液酸度的影响
因为本试验要在酸性条件下进行,那么不同的溶液酸度是否会对双氧水的氧化性产生影响以及溶液酸度为多少才为最佳呢?本人在试验中采用在其它试剂加入量不变的条件下,改变溶液的酸度,加入不同体积的0.5mol/l盐酸的方法,在0.5~10.0ml范围内,每隔0.5ml为一个试验点进行比较试验。
试验表明,加入盐酸1.5~4.0ml时,吸光度稳定不变。
为了试验的方便及减少系统误差,选取加入盐酸量为2.0ml。
4、显色剂用量的影响
显色剂用量的多少会影响反应后溶液的颜色,从而影响到吸光度,但是溶液颜色的深浅与显色剂的用量并非是一一对应的线性关系,在某个范围内溶液的颜色与显色剂用量无关。
为了减少试验操作中加入显色剂时移取量的误差,保证数据的准确,必须找出这个范围。
在其它条件不变的情况下,分别加入0.5、1.0、1.5、2.0~5.0mL的淀粉溶液,测定各自的吸光度。
结果发现在0.5~2.5mL范围内,溶液的吸光度稳定不变。
考虑操作的方便,选用1.0mL。
5、氧化剂的影响
在日常检验过程中,我们无法预先知道样品中的碘含量,而且不同的样品之间碘含量千差万别。
如果氧化剂用量的多少对试验结果有影响,则对于氧化剂加入量的选择将会是个难题,且还必须考虑加入其它试剂来消除过量的氧化剂。
众所周知,一个试验加入的试剂越多,则带来的各种影响因素也越多,可能造成误差的机会也越多。
化验室常用30%和3%的双氧水作为氧化剂,由于浓度大于30%的双氧水溶液会灼烧皮肤,如选择30%浓度的双氧水,则存在较大的危险性,并且食盐中碘的含量较少,选用30%的双氧水溶液,则所需的用量很少,这使得操作过程中人为因素(如看刻度)和试验仪器的精确度所造成的相对误差增大。
综上所述,故选用3%的双氧水作为氧化剂。
其它试验条件不变,改变双氧水的用量,结合国家规定的食盐中碘含量,选择试验范围:加入3%双氧水1.0~8.0ml,间隔梯度为0.5mL。
试验表明,加入量在2.0~4.5ml范围时,吸光度稳定,误差小。
从减少误差的角度考虑,选择加3%双氧水量为2.5ml。
6、显色时间的影响
显色时间是指加入显色剂淀粉后到测定吸光度之间的时间间隔。
其它试验条件不变,分别显色5、10、15、……、55、60分钟,测定相应的吸光度。
通过比较,结果表明用本法测定碘离子含量时,在30分解内显色稳定。
所以选择显色时间为10~20分钟。
7、吸收曲线的绘制和准确度
准确移取碘化钾标准使用液1.00、2.00、4.00…、8.00mL(即含碘化钾的量分别为10、20、40……、80ug) 于50mL的容量瓶中,加入氯化钠溶液35mL,按试验方法,在721分光光度计,用2.0cm比色皿,在595nm波长处测出吸光度A,以吸光度为纵坐标,碘化钾含量为横坐标绘制吸收曲线。
仿照加碘食盐,在已知重量为M1的氯化钠中加入一定量M2的碘化钾•(因碘化钾量很少,可先准确称取碘化钾,溶解定容后再准确移取),按此制作5个样品,分别求出标准值Q(Q= M2/ M1,因M2很小,故分母中M2忽略),然后分别按照本试验方法和GB/T13025.7—91的试验方法进行对比试验。
试验结果如下表:
从上表可以看出,本法较国标法的测量精确度更高。
本人认为主要是因为本法采用了最佳的试验条件,排除了各种影响因素,使得试验的系统误差减小,结果更为可信。
对生产企业而言,在实际生产加碘盐过程中只需粗略判定食盐中碘含量是否符合国家标准要求即可,则在采用此法时可不用分光光度计,直接采用目视比色,即事先做好两个标准管(碘化钾含量分别为20、50ug/g),通过将试样管与标准管比较,如颜色介于标准管之间即为合格,就能简便、快速地得出结果,确保产品质量。
这种方法对生产厂家在生产过程中监控食用盐的碘含量也很有应用价值。
(作者单位:福建三明市产品质量监督检验所)
欢迎您的下载,
资料仅供参考!
致力为企业和个人提供合同协议,策划案计划书,学习资料等等
打造全网一站式需求。