紫外分光光度法测定食盐中的碘含量
- 格式:ppt
- 大小:1.17 MB
- 文档页数:22

食盐中碘含量的光度分析法测定李继胜,朱自强,彭 滨 摘要: 目的 用较简单的方法测定食盐中碘的含量。
方法 试用分光光度法(波长为590nm)测定食盐中碘的含量。
结果 在30m in内测定其吸光度,碘浓度在0.3~1.6L g/ml范围内呈线性,碘标准曲线的相关系数r=0.992; 5次精密度测定标准偏差RSD s=0.425%;加标试验平均回收率=100.4%。
结论 试验表明:分光光度法测定食盐中微量碘酸钾含量的方法简单、快速,有较高的灵敏度和较好的准确性。
关键词: 碘酸钾;分光光度法;食盐 中图分类号:O657.3 文献标识码:ASpectrophotometer Determination Of Micro Amounts of Potassium Iodate in Edible Salt Li Jisheng,Zhu Ziqiang,Peng Bin (Dept.o f Chemistry,Wuyi University,Jiangmen529020,China) Abstract: Obj ective A m ethod for the determinati on of m icro amounts of potassium iodate in iodized salt by spec-trophotom eter was reported in this paper. Result The l inear range of the method was0.3~1.6L g/ml and r=0.992 ,the average recovery was100.4%,the RSDs were0.425%(n=5). Conclusion The method is pr oved to be sim-pl e,rapid and reliable with hi gher sensiti vity and better accuracy,and has been used for determination of potassium io-date in edible salt wi th satisfactory results. Key words: Potassium iodate;Spectrophotometer;Edible sal t 食盐加碘是防治碘缺乏病的根本措施,食盐的含碘量一般采用直接滴定方法检测。


结晶紫褪色分光光度法测定食盐中微量碘刘英红*,马卫兴,许兴友,何倩,沙鸥(淮海工学院化学工程学院,江苏连云港 222005摘要:在硫酸介质中和溴化钾存在下,碘酸根能使结晶紫氧化而褪色,且褪色的程度与碘酸根存在量成正比,从而建立了光度法测定碘的新方法。
方法的最大吸收波长为630nm。
碘酸根含量在5 ~42 g/10mL范围内符合比尔定律。
表观摩尔吸光系数为1.1 104L m ol 1 cm 1。
将该方法用于测定加碘食盐中的微量碘,结果满意。
关键词:结晶紫;碘;褪色作用;分光光度法中图分类号:T S365 文献标识码:B 文章编号:1000-9973(200907-0099-03 Spectrophotometric determination of iodine in salt adding iodineby decoloration of crystal violetLIU Ying hong*,M A Wei x ing,XU Xing you,H E Qian,SH A Ou (College of Chemical Engineering,Huaihai Institute of Technology,Lianyungang222005,China Abstract:In the medium o f H2SO4and in the pr esence of KBr,the co lor of crystal v iolet oxidized by iodide can be faded,and the deg ree of co lor fading is pro por tional to the concentration of io dide,and a new spectropho to metr ic metho d for determination of iodides repo rted.T he m ax ium abso rbance is at630nm.Beer s law is obeyed from5to42g of iodine per10mL of solution. The apparent molar absorptiv ity is1.1 104L m ol 1 cm1.T he metho d has been used in the determ inatio n of iodine in iodine spiked salt w ith satisfactory results.Key words:cry stal vio let;iodine;co lor fading reaction;spectrophotom etry碘是人体生长发育、提高智力必不可少的微量元素。


分光光度法测定食盐中碘含量方法的评述分光光度法测定食盐中碘含量方法的评述随着人们生活水平的提高,大多数居民都能吃上加碘盐。
而有些人为了防治甲状腺病而大量吃海带、紫菜等富含碘的食物,以至碘过量,引起机体一系列的不良反应,甚至危及健康。
因此,及时、准确地测定食盐中的碘含量具有重要意义。
目前常用的测定食盐中碘含量的方法有三种:碘量瓶直接测定法;碘溶液比色测定法和分光光度法。
①分光光度法是一种可以同时测定吸光度和相对强度的物理方法,适合于现场操作,且灵敏度高,准确性好。
但操作繁琐,只适合小批量检测。
②碘量瓶法是将固定在架子上的塑料量筒底部烧灼后磨去,再用铅笔填写被测样品的量,最后将瓶口磨平封死,作为碘的标准液。
然后用分光光度计进行比色测定。
这种方法操作简单,但由于反复磨损,量筒内壁附着大量的铅,会影响到比色的精密度。
另外,由于量筒的大小限制,也使它不能满足批量检测的要求。
③分光光度法是将玻璃比色皿或金属比色皿放在分光光度计下面,当入射光线经过单色器通过棱镜时发生折射和干涉现象,形成各种颜色的光谱。
根据这些光谱的强度和颜色,便可求出待测元素的含量。
该方法操作简单,测定快速,但受客观条件限制较多,比如量程选择不当,将造成假阳性;波长选择不当,会导致吸收峰的损失;样品浓度太低或太高,都将使检测误差增大。
(1)测定样品应用分光光度法,以铁为基准标准。
当仪器校正完毕并做好空白样品测定时,将空白液直接注入已调零的比色管中,关闭玻璃阀门,待其自然沉降后即可读取吸光度。
(2)测定过程要注意条件控制,样品的处理温度、试剂、反应时间以及比色管内的空气要一致。
并使用恒温加热装置,避免温度升得过快。
(3)读数需要借助检流计,仪器采用自动电位滴定器。
并将所用的仪器以及电极和相应的参比溶液全部校正到仪器所给定的参考点。
另外,还应记录仪器测定过程中出现的吸光度值、 A/D变化值、仪器误差等,并与计算值对比,作出检验结果。
(4)试验结束后,试验人员应首先检查结果的精密度和准确度。

分光光度法测定食盐中碘的含量
韦文业;施先义;谢玉艳
【期刊名称】《理化检验-化学分册》
【年(卷),期】2014(000)011
【摘要】碘是甲状腺合成甲状腺激素的主要成分,这种激素能促进人体的新陈代谢和生长发育。
人体缺碘易患缺碘性疾病,如地方性甲状腺肿、地方性克汀病等,我国是碘缺乏病流行严重的国家,目前主要是在食盐中加入碘(以碘酸钾形式加入)并且严格控制碘的加入量,为此,测定食盐中碘含量非常重要。
食盐中含碘量的测定常用的方法有滴定分析法[1]和萃取光度法[2]等,利用碘酸钾作氧化剂的氧化褪色光度法有较多的研究[3-4]。
【总页数】2页(P1453-1454)
【作者】韦文业;施先义;谢玉艳
【作者单位】广西现代职业技术学院资源工程系,河池 547000;广西现代职业技术学院资源工程系,河池 547000;广西现代职业技术学院资源工程系,河池547000
【正文语种】中文
【中图分类】O657.3
【相关文献】
1.邻氯酚红褪色分光光度法测定食盐中碘的含量
2.联苯胺分光光度法测定食盐中碘含量
3.酸性红褪色分光光度法测定食盐中碘的含量
4.分光光度法测定食盐中碘含量的最优条件研究
5.紫外分光光度法测定食盐中碘的含量
因版权原因,仅展示原文概要,查看原文内容请购买。

Ξ加碘酸钾食盐中碘含量的紫外分光光度法测定刘翠格, 默丽萍, 魏永巨(河北师范大学化学学院,河北石家庄 050016)摘 要:根据碘(I 2)、碘离子(I -)和碘三离子(I 3-)的紫外吸收光谱,拟订了加碘酸钾食盐中碘含量的光度测定方法.在p H 2.4,KI 浓度为0.01mol/L 的HCl 介质中,1mol 碘酸钾可定量转变为3mol I 3-,通过测量I 3-在288nm 或350nm 处的吸光度,可计算食盐样品中碘的含量.方法的加入回收率在96.8%~102.6%之间.本文中,笔者分析了2种市售碘盐样品,结果令人满意.关键词:碘;食盐;紫外分光光度法中图分类号:O 657.32 文献标识码:A 文章编号:100025854(2003)0520497203碘是人体内合成甲状腺素所必需的微量元素.适量的甲状腺素有促进机体生长、调节能量转换、稳定神经系统等作用.缺碘会影响机体代谢,引起甲状腺肿,严重者可致发育停滞、痴呆.按国际推荐标准,成人每日需碘0.1~0.3mg [1].防止碘缺乏的一个重要措施是推广食用加碘食盐.食盐中加碘的方法有2种,一是加入碘化钾,二是加入碘酸钾.1994年,国家规定在食盐中加入碘酸钾[2,3].目前市售加碘酸钾食盐中碘含量一般为(35±15)mg/kg.食盐含碘量的测定方法有多种[2],如滴定分析法、吸光光度法[3~6]、荧光及化学发光法[7]、离子选择电极法、极谱法、色谱法和专用测碘仪法[8]等.笔者在研究碘(I 2)、碘离子(I -)和碘三离子(I 3-)的紫外光谱时,观察到I 3-的紫外光谱与I 2和I -的紫外光谱有明显不同.根据这种光谱差异和碘的化学性质,拟订了加碘酸钾食盐中碘含量的测定方法,实验结果令人满意.1 原 理在酸性介质中,KIO 3与过量KI 反应生成I 2: IO 3-+5I -+6H +=3I 2+3H 2O.(1)I 2与I -结合生成I 3-: I 2+I -=I 3-.(2)反应完成后,溶液中含有I 3-和过量的I -.由于I 3-在260nm 以上有灵敏的光吸收,而I 2和I -在260nm 以上没有吸收(见图1),因而可以通过测定溶液的吸光度而得知I 3-的浓度,进而推算加碘酸钾食盐中碘的含量.2 实验部分2.1 仪器与试剂UV 2501PC 分光光度计(日本,岛津).I 2:分析纯,天津市天大化工实验厂出品,配制成0.500mmol/L 水溶液;KI :分析纯,中国医药公司进口分装,配制成0.050mol/L 水溶液,使用时适当稀释;KIO 3:化学纯,上海化学试剂总厂出品,配制成0.100mol/L 水溶液,使用时适当稀释;HCl :分析纯,配制成水溶液并标定其准确浓度;NaCl :分析纯,1.0mol/L 水溶液;实验用水为蒸馏水.2.2 实验方法在25mL 容量瓶中分别加入I 2,KI ,KIO 3,HCl ,NaCl 等溶液,用水稀释至刻度,摇匀,以水为参比,Ξ收稿日期:20030403;修回日期:20030531作者简介:刘翠格(1954),女,河北保定人,河北师范大学副教授,从事无机化学的教学与研究.第27卷第5期2003年 9月河北师范大学学报(自然科学版)Journal of Hebei Normal University (Natural Science Edition )Vol.27No.5Sep.20031cm 吸收池,扫描吸收光谱,或读取一定波长的吸光度.根据加入HCl 标准溶液的浓度和体积,计算显色溶液的p H 值,加入NaCl 溶液以控制离子强度.3 结果与讨论3.1 I 2,I -和I 3-的吸收光谱按实验方法测量I 2,I -和I 3-的吸收光谱,得图1.图1中I 2的吸收峰在202nm ,I -的吸收峰在193和226nm ,I 2和I -在260nm 以上没有吸收;I 3-的吸收峰在288和350nm ,摩尔吸光系数(ε)分别为3.52×104和2.33×104L/(mol ・cm ).根据反应式(1)和(2),1mol KIO 3可以定量转变为3mol I 3-,因此,KIO 3的反应是一个有倍增效应的高灵敏度显色反应.3.2 溶液酸度的影响溶液酸度对反应(1)有显著影响,实验表明在p H 1.4~3.4之间较为合适(见图2).在高酸度条件下(p H <1.4),I -可与溶解氧发生反应:4I -+4H ++O 2=2I 2+2H 2O ,产生正误差;而在低酸度条件下(p H >3.4),I 2发生歧化反应:3I 2+6OH -=5I -+IO 3-+3H 2O ,此时I 3-将不能生成.本实验控制p H为2.4.λ/nmI 2与I -的浓度均为0.060mmol/L ;I 3-为0.040mmol/L I 2+0.010mol/L KI图1 I 2,I -和I 3-的紫外吸收光谱p HKIO 3:5.0μmol/L ;KI :0.010mol/L ;0.2mol/L NaCl 介质图2 溶液酸度对显色反应的影响3.3 KI 用量的影响I 2:0.040mmol/L ;曲线1和2的测量波长分别为350,288nm图3 KI 用量对显色反应的影响由于I 3-的稳定常数较小(lg K =2.96)[9],为了保证反应(2)进行完全,必须加入过量的KI (见图3).本实验取KI 浓度为0.01mol/L.3.4 显色溶液的稳定性在过量KI 存在下,I 3-是相当稳定的.显色溶液在50min 内吸光度基本不变;时间再延长,溶液吸光度有所下降[5].3.5 共存物质的影响本方法基于氧化还原反应(1),只有氧化性离子如MnO 4,Cr 2O 72-,Cu 2+等才能产生干扰,但在食盐中,这些离子一般不存在,因此,本方法基本不存在干扰物质[4].3.6 工作曲线在p H 2.4,NaCl 浓度为0.2mol/L 的条件下,用KIO 3标准溶液制作工作曲线,回归方程分别如下:288nm :A =0.009+0.787c I ,r =0.99997;894河北师范大学学报(自然科学版)第27卷350nm :A =0.005+0.518c I ,r =0.99995.3.7 加入回收实验在碘盐样品溶液中定量加入KIO 3标准溶液,与样品溶液同时显色后,以样品显色溶液为参比,测量由于加入KIO 3所产生的吸光度增加值,再根据回归方程计算加入碘的浓度,进而计算回收率.以不同样品为基体,做了7次加入回收实验,分别在288和350nm 波长下测量,结果列于表1.表1中回收率在96.8%~102.6%之间,在光度分析允许误差范围内.表1 加入回收实验结果加入碘/(mg ・L -1)288nm吸光度增加值测得碘/(mg ・L -1)回收率/%350nm吸光度增加值测得碘/(mg ・L -1)回收率/%0.2540.20330.24797.20.13540.25299.20.2540.20230.24696.80.13490.25198.80.3810.30860.381100.00.20300.382100.30.3810.30410.37598.40.20000.37698.70.5080.41160.512100.80.27140.514101.20.3810.31430.388101.80.20760.391102.60.2540.20300.24797.20.13290.24797.23.8 样品分析称取市售加碘酸钾食盐10.00g ,溶解后转移至100mL 容量瓶中,以水定容.移取此溶液2.00~4.00mL 至25mL 容量瓶中,加入5.0mL 0.05mol/L KI ,1.0mL 0.1mol/L HCl ,用水稀释至刻度,摇匀,在288或350nm 测量吸光度,由工作曲线计算样品中碘的含量.笔者测定了2种市售加碘酸钾食盐样品,测量数据与计算结果列于表2.其中样品1为自然精制碘盐(执行标准QB 2446—99),样品2为碘盐洗粉(执行标准G B 5461—2000).这2种样品的含碘量标签值均为(35±15)mg/kg.由表2可见,样品2的含碘量平均值 x 与标签值一致,而样品1的含碘量平均值比标签值略低.表2 食盐样品碘含量的测定结果V /mL 样品1288nmAw /(mg ・kg -1)350nmAw /(mg ・kg -1)样品2288nmAw /(mg ・kg -1)350nmAw /(mg ・kg -1)2.000.136620.20.088320.00.243037.10.158837.03.000.189419.10.123219.00.344335.50.227035.74.000.248319.00.161818.90.461035.90.302635.9x ±s 19.4±0.719.3±0.636.2±0.836.2±0.8参考文献:[1] 周爱儒.生物化学[M ].第5版.北京:人民卫生出版社,2000.396.[2] 刘占广.碘盐含碘量分析综述[J ].海湖盐与化工,1999,28(6):33235.[3] 王彦,薛斌.分光光度法测定食盐中的碘含量[J ].辽宁化工,1996,(1):57258.[4] 胡章记.倍增反应紫外吸光光度法测定食盐中微量碘[J ].化学研究,2002,13(1):43244.[5] 马卫兴,薛婉立.紫外光度法测定食盐中的添加剂碘酸钾[J ].中国调味品,1997,(6):22224.[6] 王末肖,高磊红,刘春艳,等.吸光光度法测定碘酸钾的研究[J ].理化检验(化学分册),2002,38(5):2432244.[7] 张子红,杜凌云,王术皓,等.停流流动注射化学发光法测定碘盐中的碘酸根[J ].光谱实验室,2001,18(5):5842587.[8] 陈焕文,于爱民,韩松柏,等.手持式测碘仪现场测定食盐中的碘[J ].分析化学,2001,29(7):8552858.[9] 刘翠格,默丽萍.分光光度法测定I 3-的稳定常数[J ].化学通报,2003,66(3):2132214.(下转第530页)994第5期刘翠格等:加碘酸钾食盐中碘含量的紫外分光光度法测定035河北师范大学学报(自然科学版)第27卷界的物种多样性和遗传多样性的基因库.因此,在白洋淀建立湿地自然保护区,实施保护措施,防止湿地生态环境的破坏和生态功能的退化,无论是从保护湿地生态系统的特殊性、典型性和生物多样性的稀有性上,还是淡水湖泊资源本身所具有的社会经济价值上衡量,都具有十分重要的保护地位.但是,由于保护不力,白洋淀生态环境退化日益严重,已经给淀周边地区的经济和社会发展造成了巨大损失,并制约了淀区社会经济的发展,阻碍了人民生活水平的迅速提高,影响了社会的可持续发展战略的实施.因此,建议尽快建立白洋淀湿地自然保护区,以便使白洋淀能够迅速得到切实、有效的保护.白洋淀湿地自然保护区建立以后,应以生态学、生态经济学和可持续发展理论为指导,以保护湿地资源、生态环境和生物多样性为中心,以确保自然资源永续利用和生态系统的良性循环为目标,严格保护白洋淀湿地生态系统,大力改善和建设湿地生态环境,加大科技投入,积极开展科学研究,科学合理地利用自然资源,实现湿地生态系统的良性循环,促进区域社会经济的持续、稳定、健康发展,把白洋淀湿地自然保护区建设成为集自然保护、科研、宣传教育、生态旅游等多种功能于一体的综合效益显著的湿地类型自然保护区.参考文献:[1] 安新县地方志办公室.白洋淀志[M].北京:新华出版社,1996.[2] 安新县地方志编纂委员会.安新县志[M].北京:新华出版社,2000.On Establishing the N ature Preserve of B aiyangdian EvergladeWEN Zhi2guang(College of Resource and Environment Sciences,Hebei Normal University,Hebei Shijiazhuang 050016,China) Abstract:Illuminates the necessary of the nature preserve of Baiyangdian everglade through analyzing the worthiness of the ecological protect,economic and social benefits,and illuminates the urgent character of establishing the nature preserve of Baiyangdian everglade though analyzing the existent problems in the ecological protect,finally,advises establishing the nature preserve of Baiyangdian everglade as soon as possible and puts forward instructional thought and developmental direction of the constructing the nature preserve of Baiyangdian everglade.K ey w ords:Baiyangdian everglade;marsh;ecology;nature preserve(责任编辑 蔡丹英)(上接第499页)Determination of Iodine in Edible Salt AddedPotassium Iodate by U ltraviolet SpectrophotometryL IU Cui2ge, MO Li2ping, WEI Y ong2ju(College of Chemistry,Hebei Normal Universit y,Hebei Shijiazhuang 050016,China)Abstract:According to the ultraviolet absorption spectra of iodine,iodide ion and triiodide ion,a method for determination of iodine in edible salt added potassium iodate was proposed.In the medium of HCl with p H2.4,0.01mol/L KI,1mol potassium iodate may be quantitatively converted into3mol I3-. By measuring the absorbance of I3-at288or350nm,quantity of iodine in edible salt can be calculated.A recovery percent of this method was found to be96.8%~102.6%.Two samples of edible salt purchased from market were analyzed.The results were satisfactory.K ey w ords:iodine;edible salt;ultraviolet spectrophotometry(责任编辑 邱 丽)。
山 东 化 工 收稿日期:2020-06-04作者简介:赵俊英(1981—),女,山东德州人,讲师,从事分析测试工作。
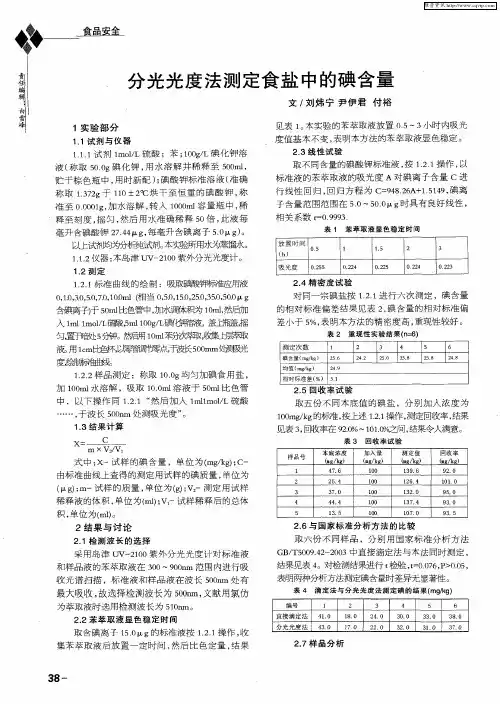
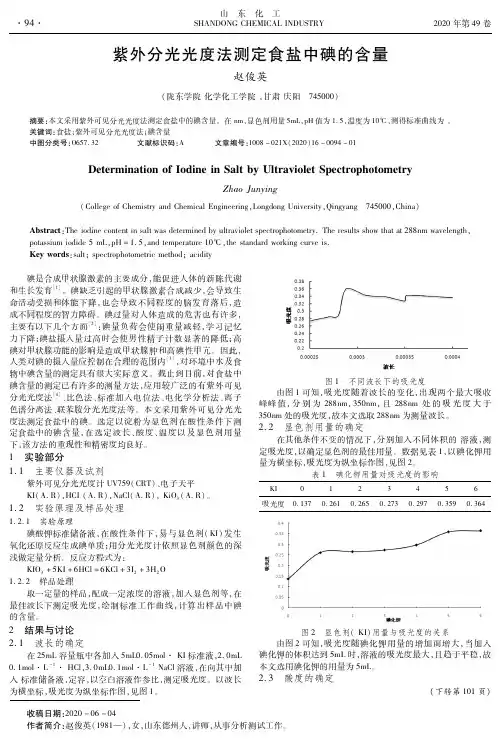
紫外分光光度法测定食盐中碘的含量赵俊英(陇东学院化学化工学院,甘肃庆阳 745000)摘要:本文采用紫外可见分光光度法测定食盐中的碘含量。
在nm,显色剂用量5mL,pH值为1.5,温度为10℃,测得标准曲线为。
关键词:食盐;紫外可见分光光度法;碘含量中图分类号:O657.32 文献标识码:A 文章编号:1008-021X(2020)16-0094-01DeterminationofIodineinSaltbyUltravioletSpectrophotometryZhaoJunying(CollegeofChemistryandChemicalEngineering,LongdongUniversity,Qingyang 745000,China)Abstract:Theiodinecontentinsaltwasdeterminedbyultravioletspectrophotometry.Theresultsshowthatat288nmwavelength,potassiumiodide5mL,pH=1.5,andtemperature10℃,thestandardworkingcurveis.Keywords:salt;spectrophotometricmethod;acidity 碘是合成甲状腺激素的主要成分,能促进人体的新陈代谢和生长发育[1]。
碘缺乏引起的甲状腺激素合成减少,会导致生命活动受损和体能下降,也会导致不同程度的脑发育落后,造成不同程度的智力障碍。
碘过量对人体造成的危害也有许多,主要有以下几个方面[2]:碘量负荷会使闹重量减轻,学习记忆力下降;碘盐摄入量过高时会使男性精子计数显著的降低;高碘对甲状腺功能的影响是造成甲状腺肿和高碘性甲亢。
因此,人类对碘的摄入量应控制在合理的范围内[3],对环境中水及食物中碘含量的测定具有很大实际意义。


浊点萃取—紫外光谱法测定食盐中碘含量高颖;方丽娟;李然海;朱良元;孙银龙;王红艳【摘要】建立了浊点萃取一紫外光谱法测定微量碘的新方法.利用表面活性剂Triton X-100和配位剂碘化钾对微量碘进行浊点萃取,并结合紫外光谱法进行测定.考察了平衡时间、水浴温度、离心时间、pH值、萃取剂用量等因素对萃取的影响,并得到最佳实验条件:pH为2.0,10%的TritonX-100用量2.0mL,水浴温度80C,平衡时间9 min,4 000 r/min转速下离心10 min.该方法应用于食盐中碘含量的测定,结果准确.【期刊名称】《宿州学院学报》【年(卷),期】2013(028)003【总页数】3页(P69-71)【关键词】浊点萃取;紫外光谱法;碘酸根;分离富集【作者】高颖;方丽娟;李然海;朱良元;孙银龙;王红艳【作者单位】宿州学院化学与生命科学学院,安徽宿州,234000;宿州学院化学与生命科学学院,安徽宿州,234000;宿州学院化学与生命科学学院,安徽宿州,234000;宿州学院化学与生命科学学院,安徽宿州,234000;宿州学院化学与生命科学学院,安徽宿州,234000;宿州学院化学与生命科学学院,安徽宿州,234000【正文语种】中文【中图分类】O657.32碘是人体的必需微量元素之一,健康的成人体内碘的总量在20~50 mg[1]。
碘在人体中起到促进生物氧化、调节蛋白质合成和分解、促进糖和脂肪代谢等作用。
值得注意的是,人体摄入过多的碘是有害的,饮食碘过量会引起“甲亢”。
在日常生活中,人们所食用的食盐中含有微量碘(加碘食盐中的碘元素以KIO3的形式存在),因此,食盐中碘的含量对人体至关重要。
我国卫生部规定食盐中碘含量的平均水平为20~30 mg/kg[2]。
食盐中碘含量的测定方法有滴定法[3]、原子发射光谱法[4]、原子吸收光谱法[5]、光度分析法[6]、电化学法[7]、色谱法[8]等。
本实验建立了浊点萃取-紫外光谱法测定微量碘的新方法。
分光光度法测定食盐中碘含量方法的评述在近几年的各类专业期刊上,常见“食盐中碘含量是否达到卫生标准”等相关内容。
本文主要对分光光度法测定食盐中碘含量方法的评述。
有关部门规定每人每天的食盐摄取量不能超过6克,目前我国国内市场销售的食盐均符合国家规定,其碘含量也符合国家规定。
5月22日,河南省科学院应用光谱技术研究所和河南省盐业总公司联合承担了河南省碘缺乏病防治专项资金的申报工作。
据该研究所李兰玉所长介绍,食盐中碘含量是检验食盐是否符合国家碘卫生标准的重要依据之一。
此次他们与河南省盐业总公司签订协议,将这一工作交给了河南省盐业总公司,目的就是让他们进行这方面的科学研究,探索出新的测定方法。
据了解,食盐碘含量如何测定一直是个难题。
李兰玉所长说:“该项目组成立后,他们先后经历了10多次试验,采用不同的方法对碘的测定值进行对比试验,最终选择了比较准确的“单一光程干涉法”,即用独特设计的可以消除非线性干扰的单色器、灵敏度高、稳定性好的光源、色散率低、响应速度快的单色仪和波长准确度高的分光光度计。
测定结果表明,采用分光光度法测定的碘含量的准确度和精密度均满足国家要求,不存在系统误差和随机误差,且具有操作简便、快速、灵敏度高等优点。
因此该方法既可用于质量监督、执法部门检测,又可用于食品加工企业对原料及产品进行卫生指标控制。
”11月25日,河南省卫生厅在郑州召开全省碘缺乏病防治新闻发布会,向媒体通报了省科学院应用光谱技术研究所承担的国家“九五”攻关课题——食盐中碘含量检测方法的研究情况。
据悉,由该研究所研制的国内首台碘含量分光光度计将于今年3月正式投入市场。
此仪器的研制成功,填补了我国此项检测的空白,为碘缺乏病防治提供了强有力的技术保证。
以该仪器为依托,他们还将致力于开发系列化食盐分析仪器,并将科研成果应用于生产实际。
同时,将科研成果转化为高新技术产品,带动当地经济的发展。
“该项目的完成,将使碘盐的检测时间由原来的24小时缩短为半小时,这不仅有利于全省广大碘缺乏病患者及时获得诊治,而且更有利于碘盐加工企业及时根据需求变化调整生产工艺,节约人力、物力和财力。
分光光度法测定食盐中碘含量的最优条件研究本文研究了使用分光光度法测定食盐中碘含量的最优条件,以确保测试结果的准确性。
首先,对测定过程进行了分析,分析了测定过程中所需要考虑的因素,指出了分光光度法测定食盐中碘含量的基本流程。
然后,通过实验验证,综合评估多个因素对测定结果的影响,最终确定了最优的测定条件,包括pH值、温度、时间、吸光度、测定场景以及延时等。
最后,将所确定的最优条件应用于实际检测,以确保检测结果的可靠性。
关键词:分光光度;食盐;碘含量;最优条件1.Introduction随着人们越来越关注饮食中的碘含量,如何检测食盐中碘含量变得越来越重要。
分光光度法是通过分析物质在不同波长的吸收强度,以测定物质的浓度而被广泛应用于食品中。
分光光度法测定食盐中碘含量的最优条件的研究是必不可少的,以确保测试结果的准确性和可靠性。
2.Factors for optimal conditions在进行分光光度法测定食盐中碘含量之前,应该考虑的因素有pH值、温度、时间、吸光度、测定场景以及延时等。
试验在pH 6.5的缓冲液中进行,以保证碘的稳定性;温度也应控制在25℃以下,以免各组分之间的反应,从而影响检测结果;光源波长应保持在364nm以上,源强度为80~90 %;吸光度应调节在0.1~0.3和2.4~3.0之间;可根据实验的需要,调整暴露时间;延时时间应为不少于2分钟。
3.Optimal conditions实验中,为了确保测定结果的可靠性,针对不同因素进行了实验,以确定最优条件:(1) pH值:pH值可以影响物质的稳定性,因此,本实验中,采用6.5的缓冲液,以确保碘的可检测性。
(2)度:本实验中,温度被控制在25℃以下,以免发生温度升高而对测试结果造成影响。
(3)源波长:光源波长必须大于364nm,以保证检测的准确性;(4)光度:本实验中,用0.1~0.3和2.4~3.0作为检测范围;(5)露时间:暴露时间可以根据实验的需要调整;(6)时时间:延时时间不低于2分钟,保证测试结果的可靠性。
紫外分光光度法测定食盐中碘酸钾含碘量
于海涛;李燕芹
【期刊名称】《中国公共卫生学报》
【年(卷),期】1995(014)004
【摘要】紫外分光光度法测定食盐中碘酸钾含碘量黑龙江省林口县卫生防疫站(157600)于海涛,李燕芹,申美艺,黄祖霖食盐中碘酸钾的测定,国标采用硫代硫酸钠滴定法。
本文根据在波长288nm处具有最大吸收峰的特性,利用紫外分光光度法测定,简便灵敏,回收率99.56...
【总页数】1页(P214)
【作者】于海涛;李燕芹
【作者单位】不详;不详
【正文语种】中文
【中图分类】R151.3
【相关文献】
1.胶束分光光度法测定食盐中的碘酸钾 [J], 马卫兴
2.山梨酸氧化紫外光度法测定食盐中碘酸钾 [J], 谢玉艳;施先义;陈海妮;曾柳婷
3.甲基紫分光光度法测定食盐中的添加剂碘酸钾 [J], 马卫兴
4.罗丹明6G分光光度法测定食盐中的碘酸钾 [J], 马卫光;张明星
5.加碘酸钾食盐中碘含量的紫外分光光度法测定 [J], 刘翠格;默丽萍;魏永巨
因版权原因,仅展示原文概要,查看原文内容请购买。