有机复习 (反应类型、鉴别、计算)2011.11
- 格式:ppt
- 大小:210.00 KB
- 文档页数:20

有机化合物的反应类型
有机化合物的反应类型主要包括以下几种:
1.加成反应(Addition Reaction):加成反应是指有机化合物中的不
饱和键(如双键或三键)与其他物质发生反应,形成新的化合物。
常见的加成反应包括加氢反应、加卤素反应、加水反应等。
2.消除反应(Elimination Reaction):消除反应是指有机化合物中的
两个原子或基团被移除,形成新的化合物。
常见的消除反应包括卤代烃的消除反应、醇的脱水反应等。
3.取代反应(Substitution Reaction):取代反应是指有机化合物中
的原子或基团被其他原子或基团所取代,形成新的化合物。
常见的取代反应包括烷烃的卤代反应、芳烃的硝化反应等。
4.氧化还原反应(Oxidation-Reduction Reaction):氧化还原反应是
指有机化合物中的原子或基团发生氧化或还原反应,形成新的化合物。
常见的氧化还原反应包括醇的氧化反应、醛酮的还原反应等。
5.缩合反应(Condensation Reaction):缩合反应是指两个或多个有
机化合物分子之间发生反应,形成一个新的分子。
常见的缩合反应包括酯化反应、酰胺化反应等。
6.重排反应(Rearrangement Reaction):重排反应是指有机化合物
分子中的原子或基团发生重新排列,形成新的化合物。
常见的重排反应包括醇的脱水重排反应、芳烃的亲电取代重排反应等。
这些反应类型是有机化学中最基本和常见的反应类型,通过这些
反应可以合成出各种有机化合物。


高三化学总复习二轮复习专题三有机反应类型知识点:一、有机反应基本类型有机反应的几种基本类型是:取代反应、加成反应、消去反应、聚合反应等,此外还有氧化反应、还原反应、裂化反应等。
其中酯化反应、酯的水解反应、硝化反应、磺化反应等都是取代反应的一些子类型。
二、注意的问题:1.同一反应的类型,从不同的角度看可有不同的名称,如:(1)卤代,硝化,磺化,酯化等均属于取代反应(2)卤代烃,酯,多肽和蛋白质的水解反应属于取代反应,二糖,多糖的水解反应一般认为不属于取代反应(3)油脂在碱性条件下的水解反应叫皂化反应,也是取代反应(4)醇与醇,羧酸与羧酸,氨基酸与氨基酸等分子间的脱水反应属于取代反应有关反应类型的关系可图示为: Array 2.把握官能团的反应特征掌握碳碳不饱和键、-OH、-CHO、-COOH、-COOR、C6H5-的特征反应,弄清官能团之间相互影响如-COOH、-COO-中的C=O不与H2加成。
3.掌握一些反应物间量的关系①烃基或苯环上的H被Br2取代时,不要误认为1个Br2取代2个H原子。
②要注意1mol酚酯RCOOC6H5发生水解反应最多可消耗2molNaOH:RCOOC6H5+2NaOH→RCOONa+C6H5ONa+H2O。
4.理清一些反应对结构的特殊要求。
醇消去反应要求邻碳有H、氧化反应要求本碳有H。
6、聚合反应:由小分子生成高分子的反应。
(1)加聚反应:由不饱和的单体加成聚合成高分子化合物的反应。
要求掌握乙烯式的加聚:(2)缩聚反应:指单体之间相互作用作用生成高分子,同时生成小分子(一般是水分子)的聚合反应。
常见的是:羟基与羟基(成醚结构)、羟基与羧基(形成高分子酯)、羧基与氨基(形成蛋白质)之间的缩聚。
练习:写出:乙二酸和乙二醇在浓硫酸存在的条件下发生的一系列反应:三、条件不同反应类型不同的例子 (1)温度不同,反应类型不同CH 3CH 2OH CH 2 CH 2 + H 2O2CH 3CH 2OH C 2H 5OC 2H 5 + H 2O(2)溶剂不同,反应类型不同CH 3CH 2Br +H 2O C 2H 5OH + HBrCH 3CH 2Br + NaOH CH 2 CH 2 + NaBr +H 2O(3)浓度不同,反应类型不同(C 6H 10O 5)n +n H 2O nC 6H 12O 6(C 6H 10O 5)n 6nC +5nH 2O典型例题:例1:某有机物的结构式为:它在一定条件下能发生的反应有:①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去( )A.②③④B.①③⑤⑥C.①③④⑤D.②③④⑤⑥例2:以下物质;(1) 甲烷;(2) 苯;(3) 聚乙烯;(4) 聚乙炔;(5) 2-丁炔;(6) 环己烷;(7) 邻二甲170℃ 浓硫酸140℃ 浓硫酸△NaOH△ 乙醇稀H 2SO 4浓H 2SO 4苯;(8) 苯乙烯。

高中有机化学反应类型总结常见有机反应类型有:取代反应、加成反应、消去反应、聚合反应、氧化反应、还原反应一、取代反应1.概念:有机物分子里某些原子或原子团被其它原子或原子团所代替的反应。
2.能发生取代反应的有:烷烃(卤代)、苯环(卤代、硝化、磺化)、醇羟基(-OH)(与卤化氢、成醚、酯化)、卤原子(-X)(水解)、羧基(-COOH)(酯化)、酯基(-COO-)(水解)、肽键(-CONH-)(水解)等。
二、加成反应1.能发生加成反应的有:双键、三键、苯环、羰基(醛、酮)等。
2.加成反应有两个特点:①反应发生在不饱和的键上,不饱和键中不稳定的共价键断,然后不饱和原子与其它原子或原子团以共价键结合。
②加成反应后生成物只有一种(不同于取代反应,还会有卤化氢生成)。
说明:1.羧基和酯基中的碳氧双键不能发生加成反应。
2.醛、酮的羰基只能与H2发生加成反应。
3.二烯烃有两种不同的加成形式(1,2-加成、1,4-加成)。
4.不对称烯烃加成时,要符合氢多加氢的原则为主要产物。
5.双键、三键只有和溴水中的溴加成时没有反应条件。
6.加成比例:烯烃1:1、炔烃和二烯烃1:2三、消去反应1.概念:有机物在适当的条件下,从一个分子中脱去一个小分子(如水、HX等),生成不饱和(双键或三键)化合物的反应。
如:实验室制乙烯。
2.能发生消去反应的物质:醇(反应条件为浓硫酸加热,乙烯的反应条件为浓硫酸170℃)、卤代烃(强碱水溶液加热)。
3.反应机理:消去官能团和邻碳氢。
4.有多种邻碳氢时产物有多种,要符合氢少去氢的原则为主要产物。
四、聚合反应聚合反应是指小分子互相作用生成高分子的反应。
聚合反应包括加聚和缩聚反应。
1.加聚反应:由不饱和的单体加成聚合成高分子化合物的反应。
反应是通过单体的自聚或共聚完成的。
能发生加聚反应的官能团是:碳碳双键、碳碳三键、甲醛。
聚反应的实质是:加成反应。
加聚反应的反应机理是:碳碳双键断裂后,小分子彼此拉起手来形成高分子化合物。

有机化学10种反应类型⼀、取代反应定义:有机物分⼦⾥的某些原⼦或原⼦团被其它原⼦或原⼦团所代替的反应称为取代反应。
在中学化学中,取代反应包括卤代、酯化、⽔解、硝化和磺化等很多具体的类型。
分例如下:1、与卤素单质的取代------发⽣该类反应的有机物包括:烷烃、烯烃、芳⾹烃、醇、酚等。
例如:2、与混酸的硝化反应(苯及其同系物、苯酚、烷烃等均能发⽣硝化反应)。
如:(3)注:环⼰烷对酸、碱⽐较稳定,与中等浓度的硝酸或混酸在低温下不发⽣反应,与稀硝酸在100℃以上的封管中发⽣硝化反应,⽣成硝基环⼰烷。
在铂或钯催化下,350℃以上发⽣脱氢反应⽣成苯。
环⼰烷与氧化铝、硫化钼、古、镍-铝⼀起于⾼温下发⽣异构化,⽣成甲基戌烷。
与三氯化铝在温和条件下则异构化为甲基环戊烷。
低碳硝基烷的⼯业应⽤⽇益⼴泛。
在使⽤原料上,以丙烷硝化来制取是合理的途径。
在⼯艺⽅⾯,国外较多的是以硝酸为硝化剂的⽓相硝化⼯艺,已积累了较丰富的⼯业经验。
有代表性的反应器则是多室斯登该尔反应器。
国内迄今有关硝基烷的⽣产和应⽤研究均进⾏得不多,这是应该引起我们充分注意的。
3、与硫酸的磺化反应(苯、苯的衍⽣物, ⼏乎均可磺化)。
如:4、羧酸和醇的酯化反应5、⽔解反应(卤代烃、酯、多糖、⼆糖、蛋⽩质都能在⼀定条件下发⽣⽔解反应)。
如:6、与活泼⾦属的反应:(醇、酚、羧酸等均能与活泼⾦属如钠反应⽣成氢⽓)。
如:7、醇与卤化氢(HX)的反应。
如:8、羧酸或醇的分⼦间脱⽔。
如:⼆、加成反应定义:有机物分⼦⾥不饱和碳原⼦跟其它原⼦或原⼦团直接结合⽣成化合物的反应叫加成反应。
在中学化学中,分⼦结构中含有“双键”或“叁键”的化合物均能发⽣加成反应。
如烯烃、⼆烯烃、炔烃、苯及其同系物、醛、酮、不饱和⾼级脂肪酸及其⽢油脂、单糖等。
通常参与加成反应的⽆机试剂包括H2、X2(X为Cl、Br、I)、HX、H2O、HCN等⼩分⼦(对称或不对称试剂)起加成反应。
说明:i.羧基和酯基中的碳氧双键不能发⽣加成反应。
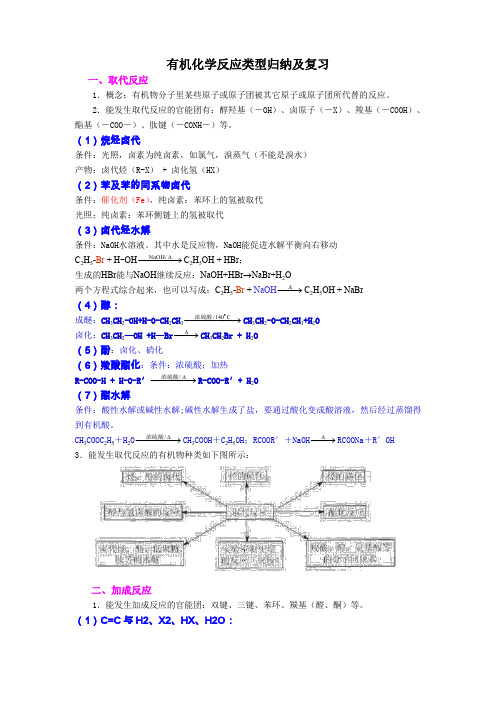
有机化学反应类型归纳及复习一、取代反应1.概念:有机物分子里某些原子或原子团被其它原子或原子团所代替的反应。
2.能发生取代反应的官能团有:醇羟基(-OH )、卤原子(-X )、羧基(-COOH )、酯基(-COO -)、肽键(-CONH -)等。
(1)烷烃卤代条件:光照,卤素为纯卤素,如氯气,溴蒸气(不能是溴水) 产物:卤代烃(R-X ) + 卤化氢(HX )(2)苯及苯的同系物卤代条件:催化剂(Fe ),纯卤素:苯环上的氢被取代 光照;纯卤素:苯环侧链上的氢被取代(3)卤代烃水解条件:NaOH 水溶液。
其中水是反应物,NaOH 能促进水解平衡向右移动C 2H 5-Br + H -OH −−−→−∆/NaOH C 2H 5OH + HBr ; 生成的HBr 能与NaOH 继续反应:NaOH+HBr →NaBr+H 2O两个方程式综合起来,也可以写成:C 2H 5-Br + NaOH −→−∆C 2H 5OH + NaBr (4)醇:成醚:CH 3CH 2-OH+H-O-CH 2CH 3−−−−→−C140/浓硫酸CH 3CH 2-O-CH 2CH 3+H 2O 卤化:CH 3CH 2—OH +H —Br −→−∆CH 3CH 2Br + H 2O (5)酚:卤化、硝化(6)羧酸酯化:条件:浓硫酸;加热R-COO-H + H-O-R ′−−−→−∆/浓硫酸R-COO-R ′+ H 2O (7)酯水解条件:酸性水解或碱性水解;碱性水解生成了盐,要通过酸化变成酸溶液,然后经过蒸馏得到有机酸。
CH 3COOC 2H 5+H 2O −−−→−∆/浓硫酸CH 3COOH +C 2H 5OH ;RCOOR ′+NaOH −→−∆RCOONa +R ′OH 3.能发生取代反应的有机物种类如下图所示:二、加成反应1.能发生加成反应的官能团:双键、三键、苯环、羰基(醛、酮)等。
(1)C=C 与H2、X2、HX 、H2O :(2)C ≡C 与H2、X2、HX 、H2O : (3)苯与H2(4)醛、酮与氢气加成: (5)油脂氢化:2.加成反应有两个特点:①反应发生在不饱和的键上,不饱和键中不稳定的共价键断裂,然后不饱和原子与其它原子或原子团以共价键结合。
高三化学有机反应类型2.条件不同产物不同的例子 (1)温度不同,产物不同 CH 3CH 2OH CH 2 2 + H 2O2CH 3CH 2OH C 2H 5OC 2H 5 + H 2O(2)溶剂不同,产物不同 CH 3CH 2Br +H 2O C 2H 5OH + HBrCH 3CH 2Br + NaOH CH 2 CH 2 + NaBr +H 2O(3)浓度不同,产物不同(C 6H 10O 5)n +n H 2O nC 6H 12O 6(C 6H 10O 5)n 6nC +5nH 2O170℃浓硫酸140℃浓硫酸△ NaOH △乙醇稀H 2SO 4浓H 2SO 4(4)条件不同,产物不同+ Br 2+ HBr+ Br 2+ HBr例1:有机化学中取代反应范畴很广。
下列五个反应中,属于取代反应的是________。
A .CH 3COONa + NaOH Na 2CO 3 + CH 4 ↑B .CH 3 CH 3CH 2CH CHCH 3 + H 2OC .2 CH 3CH 2OH CH 3CH 2OCH 2CH 3 + H 2OD .(CH 3)2CHCH CH 2 + HI (CH 33E .CH 3COOH + CH 3OH CH 3COOCH 3 + H 2O例2:由2-氯丙烷(CH 3CHClCH 3)制取1,2-丙二醇(CH 3CHOHCH 2OH )时,依次发生的反应是: ( ) A .加成→消去→取代 B .消去→加成→取代 C .取代→消去→加成 D .取代→加成→消去例3:某有机物的结构简式为,它在一定条件下可能发生的反应有:①加成 ②水解 ③酯化④氧化 ⑤中和 ⑥消去 ( ) A .②③④ B .①③⑤⑥ C .①③④⑤ D .②③④⑤⑥例4.现通过以下步骤由制取3光2Br 3 Fe3 62%浓硫95℃CaO△140℃浓硫酸浓硫酸△ CO OHCH 2 CHO OH—Cl —ClClClCl CClCl④⑤⑥(已知C C C不稳定)(1)从左到右依次每步反应所属的反应类型(a为取代,b为加成,c为消去,d为加聚,只填字母)。
有机反应类型有哪些有机反应即涉及有机化合物的化学反应,是有机合成的基础。
几种基本反应类型为:取代反应、加成反应、消除反应、周环反应、重排反应和氧化还原反应。
有机反应的类型1.取代反应:取代反应是指化合物或有机物分子中任何一个原子或原子团被试剂中同类型的其它原子或原子团所替代的反应,用通式表示为:R-L(反应基质)+A-B(进攻试剂)→R-A(取代产物)+L-B(离去基团)属于化学反应的一类。
2.加成反应:加成反应是不饱和化合物类的一种特征反应。
加成反应是反应物分子中以重键结合的或共轭不饱和体系末端的两个原子,在反应中分别与由试剂提供的基团或原子以σ键相结合,得到一种饱和的或比较饱和的加成产物。
这个加成产物可以是稳定的;也可以是不稳定的中间体,随即发生进一步变化而形成稳定产物。
3.消除反应:消除反应又称脱去反应或是消去反应,是指一种有机化合物分子和其他物质反应,失去部分原子或官能基(称为离去基)的有机反应。
消除反应发生后,生成反应的分子会产生多键,为不饱和有机化合物。
消除反应可使反应物分子失去两个基团(见基)或原子,从而提高其不饱和度。
4.周环反应:这类反应表明化学键的断裂和生成是同时发生的,它们都对过渡态作出贡献。
这种一步完成的多中心反应称为周环反应。
5.氧化还原反应:氧化-还原反应的实质是电子的得失或共用电子对的偏移。
反应中,发生氧化反应的物质,称为还原剂,生成氧化产物;发生还原反应的物质,称为氧化剂,生成还原产物。
氧化还原反应的方程式1.单质与氧气的反应①镁在空气中燃烧:2Mg+O2点燃2MgO②铁在氧气中燃烧:3Fe+2O2点燃Fe3O4③铜在空气中受热:2Cu+O2加热2CuO④铝在空气中燃烧:4Al+3O2点燃2Al2O3⑤氢气中空气中燃烧:2H2+O2点燃2H2O2.化合物与氧气的反应①一氧化碳在氧气中燃烧:2CO+O2点燃2CO2②甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O③酒精在空气中燃烧:C2H5OH+3O2点燃2CO2+3H2O。
一、有机反应归类有机反应官能团及类别反应条件重点反应方程式举例取代反应卤代反应烷烃(通式)光照苯(通式)及同系物光照催化剂苯酚(-OH)醇(-OH)加热硝化反应苯及同系物浓硫酸、加热酯化反应酸(-COOH)醇(-OH):浓硫酸、加热水解卤代烃(-X)NaOH、水加热|+ HClCH3COOH+ CH3CH2OH CH3COOCH2CH3+H2O浓硫酸△CH4+Cl2CH3Cl+HCl光CH2Cl2+Cl2CHCl3+HCl(CHCl3又叫氯仿)光C2H5—Br + H2OC2H5—OH + HBr△CH3|+Cl2光照CH2Cl反应酯稀硫酸,加热碱、加热糖类稀酸C12H22O11+H2O 2 C6H12O6分子间脱水醇浓硫酸,140℃加成反应与H2(还原反应)烯烃、炔烃:苯及同系物:醛:加热、Ni作催化剂与X2、HX与H2O烯烃:炔烃:加热消去反应卤代烃NaOH、醇加热CH3COOC2H5+H2O CH3COOH + C2H5OH无机酸△CH3COOC2H5+H2O CH3COOH + C2H5OH无机酸△CH3COOC2H5+H2O CH3COOH + C2H5OH无机酸△CH3—C—H +H2 CH3C H2OHO催化剂△CH2=CH2+Br2 CH2Br—CH2BrCH2=CH2+ H2CH3CH3催化剂△CH2=CH2+Br2 CH2Br—CH2BrCH2=CH2+ H2O CH3CH2OH高温高压催化剂催化剂△CH3COOC2H5+NaOH CH3COONa + C2H5OH△醇 浓硫酸,加热170℃氧化反应有机物大多都能燃烧,碳碳双键、碳碳三键、苯的同系物、醛基都能被酸性高锰酸钾溶液氧化,乙醇能使重铬酸钾溶液变色。
醇催化氧化醛催化氧化被其他氧化剂氧化聚合 反应加聚反应缩聚反应n HOOC-COOH +n HOCH 2-CH 2OH HO[ OC-COOCH 2CH 2O]n H +(2n-1)H 2O中和 反应苯酚羧酸CH 3COOHCH 3COO -+H +具有酸的通性CH 3CHO +2Ag(NH 3)2OHCH 3COONH 4+2Ag+3NH 3+H 2O△CH 3CH 2OHH 2C=CH 2↑+H 2O浓硫酸 170℃一定条件CH 2-CH 2n CH 2=CH 2n2CH 3—C —H+O 2 2CH 3COOH O催化剂 △CH 3CHO+2Cu(OH)2CH 3COOH+C△CH 3CHO+2Cu(OH)2+NaOHCH 3COONa+Cu 2O+3H 2O△中和反应CH3COOH +NaOH = CH3COONa+H2O氨基酸NH2-CH2-COOH + NaOH NH2-CH2-COONa + H2O置换反应醇有机实验(反应)制取乙烯1、石蜡油分解制取乙烯2、制取乙炔淀粉水解(C6H10O5)n + nH2O nC6H12O6苯酚弱酸性蛋白质盐析(可逆)、变性(不可逆)、颜色反应(遇浓硝酸变黄)、水解反应(最终氨基酸)二、烃基及其衍生物的相互转化CaC2 + 2H2O HC CH↑+Ca(OH)2CH3CH2OH H2C=CH2↑+H2O浓硫酸170℃烃的衍生物的重要类别和主要化学性质:类别通式代表物分子结构特点主要化学性质卤代烃R—X溴乙烷C2H5BrC—X键有极性,易断裂1.取代反应:与NaOH溶液发生取代反应,生成醇;2.消去反应:与强碱的醇溶液共热,生成烯烃。