微生物限度检查记录表格
- 格式:docx
- 大小:28.40 KB
- 文档页数:4
RF-08-099 A/0
第 1 页 共 1 页
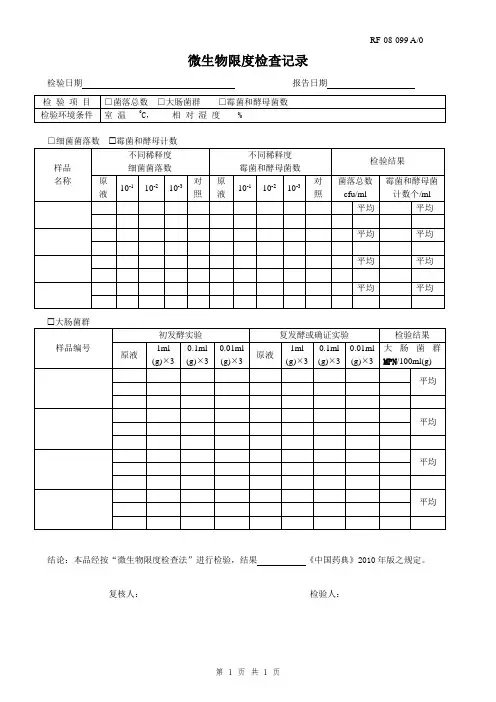
微生物限度检查记录
检验日期 报告日期 检 验 项 目
□菌落总数 □大肠菌群 □霉菌和酵母菌数
检验环境条件 室 温 0
C , 相 对 湿 度 %
□细菌菌落数 霉菌和酵母计数 样品 名称 不同稀释度 细菌菌落数
不同稀释度 霉菌和酵母菌数 检验结果
原液 10-1 10-2 10-3 对照 原液
10-1 10-2 10-3 对照
菌落总数cfu/ml 霉菌和酵母菌计数个/ml
平均 平均 平均 平均 平均 平均
平均
平均
大肠菌群
样品编号 初发酵实验
复发酵或确证实验 检验结果
原液
1ml (g) 3 0.1ml (g) 3 0.01ml (g) 3 原液 1ml (g) 3 0.1ml (g) 3 0.01ml (g) 3 大肠菌群MPN /100ml(g)
平均
平均
平均
平均
结论:本品经按“微生物限度检查法”进行检验,结果 《中国药典》2010年版之规定。
复核人: 检验人:。
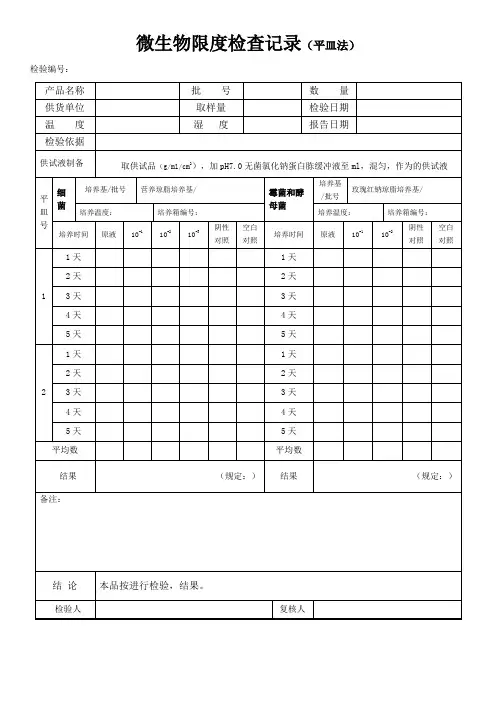

微生物限度检查记录(稀释法)文件编码:SOP-JHJY00301-07样品名称批号检验编号规格检验日期报告日期检验目的培养时间结束时间检验依据《中国药典》年版部供试液制备取供试品10g,加胰酪大豆胨液体培养基至 ml,用匀浆仪或其他适宜方法混匀,制成1:10供试液,进一步稀释成1:100,1:1000等适宜的稀释级。
一、需氧菌(30~35℃,3-5天);胰酪大豆胨琼脂,批号,温度:℃二、霉菌和酵母菌(20~25℃,5-7天);沙氏葡萄糖琼脂,批号,温度:℃培养时间1:10 1:100 1:1000 阴性对照1:10 1:100 1:1000 阴性对照皿1 1天2天3天4天5天6天/ / / / 7天/ / / /皿2 1天2天3天4天5天6天/ / / / 7天/ / / /皿3 1天2天3天4天5天6天/ / / / 7天/ / / /皿4 1天2天3天4天5天6天7天接下页样品名称批号1:10 1:100 1:1000 阴性对照1:10 1:100 1:1000 阴性对照皿5 1天2天3天4天5天6天/ / / / 7天/ / / /菌落总数结果计数: cfu/g;(规定:≦cfu/g)计数: cfu/g;(规定:≦cfu/g)三、大肠埃希菌培养内容胰酪大豆胨液体(30-35℃;18-24h)温度:℃,培养时间:h麦康凯液体(42-44℃;24-48h)温度:℃,培养时间:h麦康凯琼脂培(30-35℃;18-72h)温度:℃,培养时间:h供试品阳性对照阴性对照结果□检出□未检出大肠埃希菌(规定:不得检出cfu/g)四、耐胆盐革兰阴性菌培养内容肠道菌增菌液体培养基(30-35℃;24-48h)温度:℃,培养时间:h紫红胆盐葡萄糖琼脂(30-35℃;24-48h)温度:℃,培养时间:h供试品1:10 1:100 1:1000阳性对照阴性对照结果每1g为cfu (规定:≦ cfu/g)五、沙门菌检查培养内容胰酪大豆胨液体(30-35℃;18-24h)温度:℃,时间:hRV沙门菌增菌液体(30-35℃;18-24h)温度:℃,时间:h木糖赖氨酸脱氧胆酸盐琼脂(30-35℃;18-48h)温度:℃,时间:h三糖铁琼脂斜面(30-35℃;18-24h)温度:℃,时间:h供试品阳性对照阴性对照结果□检出□未检出沙门菌(规定:不得检出10g)结论本品按《中国药典》年版部检验,结果。


(2020版)药品片剂微生物限度检查法验证记录文件编号:XXX-XX-XXXXXX制药有限责任公司XX年XX月XX日XX片微生物限度检查法标准起草说明XX片由XXXXXXXX药材制成,有XXXXX作用。
根据其用药途径和处方,应进行需氧菌总数、霉菌数和酵母菌总数的测定及控制菌大肠埃希菌检查。
本品参照2015版药典进行过方法适用性验证没有发现抑菌性,所以确定需氧菌总数、霉菌数和酵菌总数及大肠埃希菌采用常规法测定。
经对所采用的方法适用性进行试验,符合《中国药典》2020版四部1105非无菌产品微生物限度检查的微生物计数法和1106非无菌产品微生物限度控制菌检查法与1107非无菌药品微生物限度标准,方法可行。
XX片微生物限度检查法标准正文微生物限度:按微生物限度检查法(《中国药典》2020版四部1105非无菌产品微生物限度检查的微生物计数法和1106非无菌产品微生物限度控制菌检查法与1107非无菌药品微生物限度标准。
取样品10克,加PH7.0无菌氯化钠蛋白胨缓冲液稀释至100ml,制备成溶解均匀的1:10供试液。
需氧菌总数、霉菌与酵母菌总数取本品1:10供试液1ml,注皿,平行制备平皿(2个平皿需氧菌总数和2个平皿霉菌与酵母菌总数),按平皿法测定。
大肠埃希菌取本品1:10供试液10ml直接接至100ml胰酪大豆胨液体培养基中,依法检查。
《中国药典》非无菌制剂项下标准规定:需氧菌总数103cfu/g ; 霉菌和酵母菌总数102cfu/g ; 不得检出大肠埃希菌(1g)。
XX片生物限度检查方法适用性试验1、样品名称:XX片批号XXX、XXX、XXX2、验证用菌种:铜绿假单胞菌CMCC﹙B﹚10104、、枯草杆菌CMCC﹙B﹚63501、金黄色葡萄球菌CMCC﹙B﹚26003、白色念珠菌CMCC﹙F﹚98001、黑曲霉CMCC ﹙F﹚98003 大肠埃希菌CMCC﹙B﹚44102.3.实验方法:《中国药典》2015版四部微生物限度方法适用性检查验证实验。
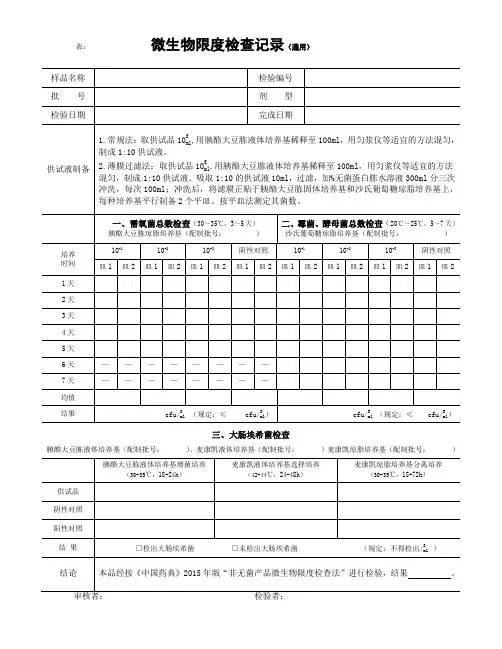
表:微生物限度检查记录(通用)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)微生物限度检查记录(30~35℃,3~5天)20℃~25℃,5~7天)沙氏葡萄糖琼脂培养基(配制批号:)三、控制菌检查(30-35℃)表:胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)(30℃~35℃)胰酪大豆胨液体培养基(配制批号:)、RV沙门增菌液体培养基(配制批号:),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:)五、耐胆盐革兰阴性菌检查胰酪大豆胨液体培养基(配制批号:)、肠道菌增菌液体培养基(配制批号:),紫红胆盐葡萄糖琼脂培养基(配制批号:)表:(含药材原粉的片剂)胰酪大豆胨液体培养基(配制批号: )、麦康凯液体培养基(配制批号: )麦康凯琼脂培养基(配制批号: )(30℃~35℃)胰酪大豆胨液体培养基(配制批号: )、RV 沙门增菌液体培养基(配制批号: ),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号: )、三糖铁琼脂(配制批号: )五、耐胆盐革兰阴性菌检查胰酪大豆胨液体培养基(配制批号: )、肠道菌增菌液体培养基(配制批号: ),紫红胆盐葡萄糖琼脂培养基(配制批号: )表:微生物限度检查记录(蛇胆川贝液)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、RV沙门增菌液体培养基(配制批号:),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:)表:微生物限度检查记录(30~35℃,3~5天)20℃~25℃,5~7天)沙氏葡萄糖琼脂培养基(配制批号:)胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)表:微生物限度检查记录(内包材)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)。
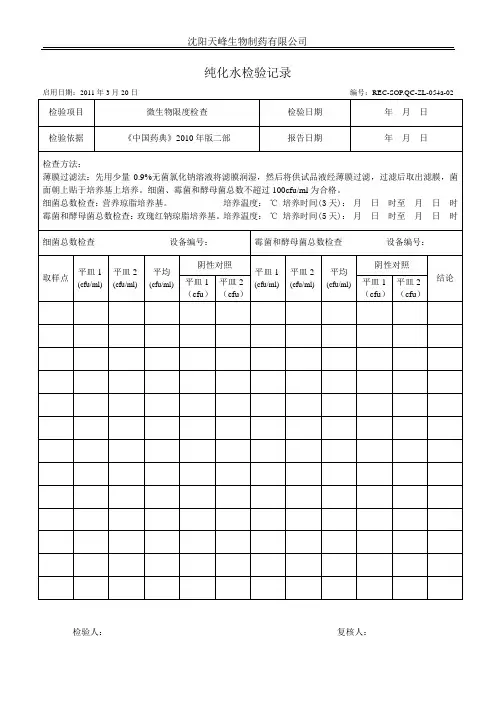

微生物限度检查记录(口服给药)
检验编号: 检品名称: 批号 第 页 共 页
检验者 月 日~ 月 日 校对者: 月 日
培养基名称: 营养琼脂培养基 (批号: 生产单位 )灵敏度
玫瑰红钠琼脂培养基 批号: 生产单位 )灵敏度
供试液制备 常规法 取供试品 g(ml),加PH7.0无菌氯化钠-蛋白胨缓冲液至 ml 。
①匀浆仪 转速 转/分钟 min ②研钵法 ③保温振摇法: ℃,保温 min,并适时振摇
细菌数:取本品1:10的供试液1 ml 注入2个平皿(0.5ml/皿),平行制备4个平皿
霉菌(酵母菌):取本品1:10的供试液1 ml 注入1个平皿,平行制备2个平皿
检查方法:照《中国药典2005年版一部》(附录XIII C )或二部(附录XI J )微生物限度检查法检查
细菌数: ℃, hr 霉菌(酵母菌)总数: ℃, hr
控制菌检查 培养温度 ℃
大肠埃希菌检查:对照菌: 大肠埃希菌[CMCC (B )44102] 沙门菌检查:对照菌: 乙型副伤寒沙门菌[ CMCC (B )50094]
结论: 本品按《中国药典2005年版 部》检查微生物限度,结果 规定。
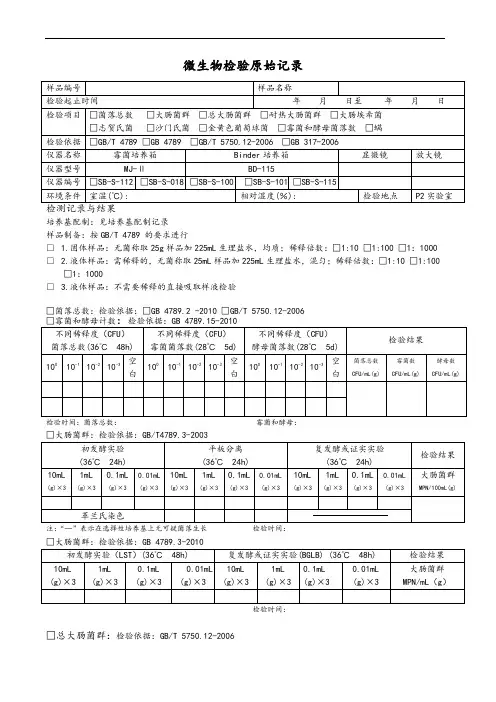
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人:复核人:
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
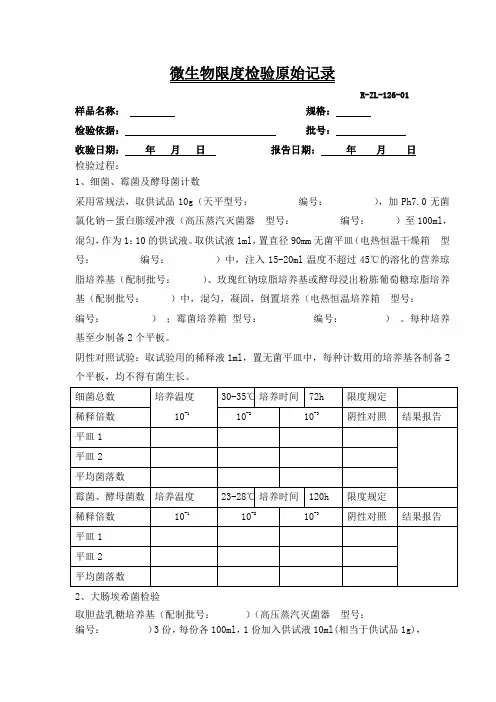
微生物限度检验原始记录R-ZL-126-01样品名称:规格:检验依据:批号:收验日期:年月日报告日期:年月日检验过程:1、细菌、霉菌及酵母菌计数采用常规法,取供试品10g(天平型号:编号:),加Ph7.0无菌氯化钠-蛋白胨缓冲液(高压蒸汽灭菌器型号:编号:)至100ml,混匀,作为1:10的供试液。
取供试液1ml,置直径90mm无菌平皿(电热恒温干燥箱型号:编号:)中,注入15-20ml温度不超过45℃的溶化的营养琼脂培养基(配制批号:)、玫瑰红钠琼脂培养基或酵母浸出粉胨葡萄糖琼脂培养基(配制批号:)中,混匀,凝固,倒置培养(电热恒温培养箱型号:编号:);霉菌培养箱型号:编号:)。
每种培养基至少制备2个平板。
阴性对照试验:取试验用的稀释液1ml,置无菌平皿中,每种计数用的培养基各制备2个平板,均不得有菌生长。
细菌总数培养温度30-35℃培养时间72h 限度规定稀释倍数 10-1 10-2 10-3阴性对照结果报告平皿1平皿2平均菌落数霉菌、酵母菌数培养温度23-28℃培养时间120h 限度规定稀释倍数10-1 10-2 10-3阴性对照结果报告平皿1平皿2平均菌落数2、大肠埃希菌检验取胆盐乳糖培养基(配制批号:)(高压蒸汽灭菌器型号:编号:)3份,每份各100ml,1份加入供试液10ml(相当于供试品1g),1份加入对照菌液作为阳性对照,第3份加入与供试液等量的稀释剂作为阴性对照。
均培养24小时(电热恒温培养箱型号:编号:)。
阴性对照应无菌生长。
必要时可延长至48小时。
取上述培养物0.2ml,接种至含5mlMUG培养基(配制批号:)(高压蒸汽灭菌器型号:编号:)的试管内,培养,于24小时在366nm紫外光下观察,(也可在5小时时进行观察,若无荧光则需延长培养,24小时时再进行观察),同时用未接种的MUG培养基作本底对照。
若管内培养物呈现荧光,为MUG阳性;不呈现荧光,为MUG阴性。
观察后,沿培养基的管壁加入数滴靛基质试液,液面呈玫瑰红色,为靛基质阳性;呈试剂本色,为靛基质阴性。
微生物限度检验记录式样名称:________________种类:________________生产批号:___________________检验日期:___________________检验项目:微生物限度检验检验目的:为了评估样品的微生物质量,保证产品的安全性和稳定性。
检验原理:根据国家标准方法,对样品进行微生物限度检验。
检验仪器和试剂:1.培养基:牛肉膏培养基、营养琼脂培养基等2.培养基固化器3.可灭菌离心管4.称量仪5.稀释液6.离心机7.干燥器8.显微镜9.微量移液器和移液枪10.注射器11.恒温培养箱12.培养基平板13.称重天平14.微生物限度试剂15.培养基扩展工具16.无菌培养皿检验步骤:1.样品准备将样品称量约10g,加入已经去离子水或生理盐水中,并使用搅拌棒搅拌均匀,使样品完全悬浮。
2.稀释取1mL悬浮样品加入9mL稀释液中,得到10倍稀释液。
依序对稀释液进行1/10、1/100,求得合适的稀释倍数。
3.培养基涂布取样品稀释液分别用无菌鉴别板扩展在牛肉膏培养基和营养琼脂培养基上,使用温度适宜的顶酵母、肠球菌染色和试纸进行培养基涂布。
4.培养将涂布后的培养基平板密封好,放置在恒温培养箱中,设置适宜的培养温度和时间。
5.细菌计数培养箱培养结束后,取出培养基平板,使用显微镜对每个培养基平板上的细菌进行计数。
计算每个培养基平板上的菌落形成单位(CFU)数目。
6.菌种鉴定依据菌落形态、生理生化反应、药敏试验等方法进行菌种的初步鉴定,记录鉴定结果。
7.结果记录将每个培养基平板上的菌落形成单位数目记录在表格中,并记录每个菌落的特征和形态。
8.结论与建议根据检验结果,评估样品的微生物质量,判断样品是否符合限度标准。
如果有异常菌落存在,则建议进行进一步检验、处理或采取相应的措施。
记录:检验项目,检测结果--------------,-------------------------菌落计数,牛肉膏培养基:__CFU/g营养琼脂培养基:__CFU/菌种鉴定--------------,-------------------------鉴定结果:1.菌种1:________2.菌种2:________3.菌种3:________结论:样品通过微生物限度检验,各指标符合国家标准。
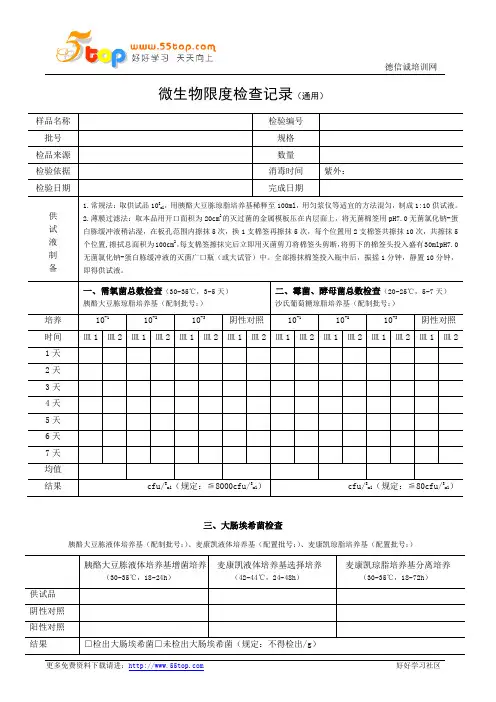
微生物限度检查记录(平皿法)--液体文件编码:SOP-JHJY00301-04样品名称批号检验编号规格检验日期报告日期检验目的培养时间结束时间检验依据《中国药典》年版部供试液制备取供试品10ml,加胰酪大豆胨液体培养基至 ml,用匀浆仪或其他适宜方法混匀,制成1:10供试液,进一步稀释成1:100,1:1000等适宜的稀释级。
一、需氧菌(30~35℃,3~5天);胰酪大豆胨琼脂培养基,批号,培养温度:℃二、霉菌和酵母菌(20~25℃,5~7天);沙氏葡萄糖琼脂培养基,批号,培养温度:℃培养时间1:10 1:100 1:1000阴性对照原液1:10 1:100阴性对照皿1 皿2 皿1 皿2 皿1 皿2 皿1 皿2 皿1 皿2 皿1 皿21天2天3天4天5天6天/ / / / / / / 7天/ / / / / / / 平均值结果计数: cfu/ml(规定:≦cfu/ml)计数: cfu/ml(规定:≦cfu/ml)三、大肠埃希菌供试液制备取供试品10ml,加胰酪大豆胨液体培养基100ml,用匀浆仪或其他适宜方法混匀,制成1:10供试液;取1:10的供试液10ml置ml胰酪大豆胨液体培养基中混匀,30~35℃培养18~24小时。
培养内容胰酪大豆胨液体(30~35℃;18~24h)温度:℃,培养时间:h麦康凯液体培养基(42~44℃;24~48h)温度:℃,培养时间:h麦康凯琼脂培养基(30~35℃;18~72h)温度:℃,培养时间:h供试品阳性对照阴性对照结果□检出□未检出大肠埃希菌(规定:不得检出cfu/ml)结论本品按《中国药典》年版部检验,结果。
检验人:复核人:。