微生物限度检查记录(2015年版)
- 格式:pdf
- 大小:127.31 KB
- 文档页数:7

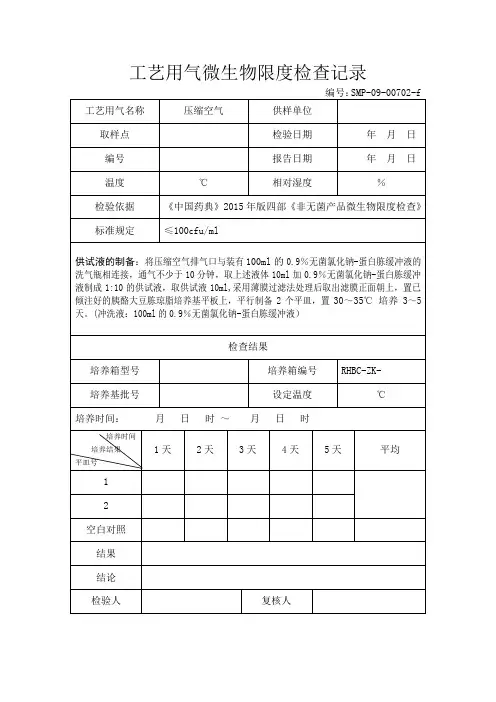
工艺用气微生物限度检查记录
编号:SMP-09-00702-f 工艺用气名称压缩空气供样单位
取样点检验日期年月日
编号报告日期年月日
温度℃相对湿度%检验依据《中国药典》2015年版四部《非无菌产品微生物限度检查》标准规定≤100cfu/ml
供试液的制备:将压缩空气排气口与装有100ml的0.9%无菌氯化钠-蛋白胨缓冲液的洗气瓶相连接,通气不少于10分钟,取上述液体10ml加0.9%无菌氯化钠-蛋白胨缓冲液制成1:10的供试液,取供试液10ml,采用薄膜过滤法处理后取出滤膜正面朝上,置已倾注好的胰酪大豆胨琼脂培养基平板上,平行制备2个平皿,置30~35℃培养3~5天。
(冲洗液:100ml的0.9%无菌氯化钠-蛋白胨缓冲液)
检查结果
培养箱型号培养箱编号RHBC-ZK-
培养基批号设定温度℃
培养时间:月日时~月日时
培养时间
1天2天3天4天5天平均培养结果
平皿号
1
2
空白对照
结果
结论
检验人复核人。



2015年版中国药典微生物限度检查方法验证方案佛山市华普生药业有限公司文件编码:TS-VP-4201-00页数:1/56 人工牛黄甲哨唑胶囊微生物限度检查方法验证方案人工牛黄甲硝唑胶囊微生物限度检查方法验证方案起草部门:QC组签名:日期:审核部门:QC组签名:日期:部门:质量部签名:日期:批准质量负责人签名:日期:质量部颁发本文件根据需要应分发于以下部门:01 质量部下表用于记录修订/变更主要内容及历史。
佛山市华普生药业有限公司文件编码:TS-VP-4201-00页数:2/56 人工牛黄甲哨唑胶囊微生物限度检查方法验证方案文件编号修订原因修订日期TS-VP-4201-00 按GMP(2010年修订版)要求新制定2015.10.22佛山市华普生药业有限公司文件编码:TS-VP-4201-00页数:3/56 人工牛黄甲哨唑胶囊微生物限度检查方法验证方案目录1. 概述2. 验证目的和范围3. 组织及职责4. 验证进度计划表5. 验证所需要的仪器设备及相关文件的确认6. 验证所需要的菌种、培养基、检验样品的确认7.验证项目和验证方法7.1试验菌株7.2需氧菌总数检查、霉菌和酵母菌总数检查方法验证的菌液制备7.3需氧菌总数检查、霉菌和酵母菌总数检查方法验证--常规倾注平皿法7.4需氧菌总数检查方法验证—离心沉淀-薄膜过滤法7.5控制菌检查方法验证—离心沉淀-薄膜过滤法8.偏差与漏项控制佛山市华普生药业有限公司文件编码:TS-VP-4201-00页数:4/56 人工牛黄甲哨唑胶囊微生物限度检查方法验证方案9.验证报告会审佛山市华普生药业有限公司文件编码:TS-VP-4201-00页数:5/56 人工牛黄甲哨唑胶囊微生物限度检查方法验证方案1. 概述我公司生产品种人工牛黄甲硝唑胶囊,产品微生物限度检查项目为需氧菌总数、霉菌和酵母菌总数、以及大肠埃希菌检查和沙门菌检查。
参照《中国药典》2015版四部附录1105:微生物计数法,以及1106:控制菌检查法的规定,本公司对该产品的微生物限度检查方法予以验证。
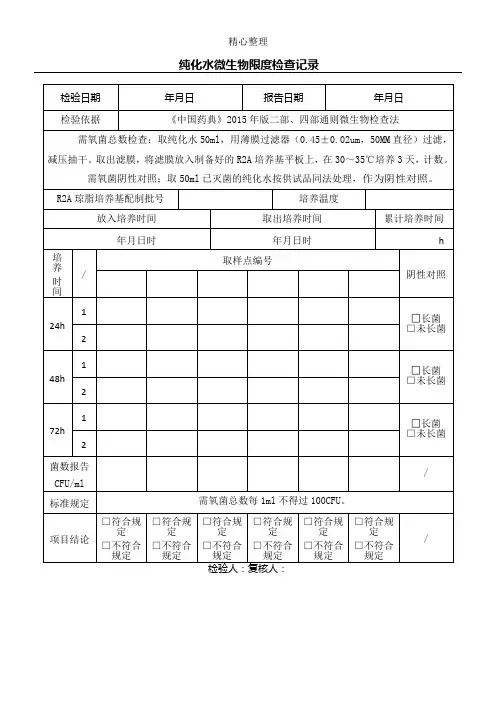
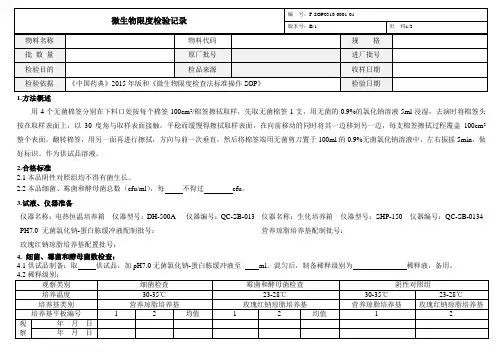
1.方法概述
用4个无菌棉签分别在下料口处按每个棉签100cm2/棉签擦拭取样,先取无菌棉签1支,用无菌的0.9%的氯化钠溶液5ml浸湿,去演时将棉签头按在取样表面上,以30度角与取样表面接触,平稳而缓慢得擦拭取样表面,在向前移动的同时将其一边移到另一边,每支棉签擦拭过程覆盖100cm2整个表面,翻转棉签,用另一面再进行擦拭,方向与前一次垂直,然后将棉签端用无菌剪刀置于100ml的0.9%无菌氯化钠溶液中,左右振摇5min,做好标识。
作为供试品溶液。
2.合格标准
2.1本品阴性对照组均不得有菌生长。
2.2本品细菌、霉菌和酵母菌总数(cfu/ml),每不得过cfu。
3.试液、仪器准备
仪器名称:电热恒温培养箱仪器型号:DH-500A 仪器编号:QC-SB-013 仪器名称:生化培养箱仪器型号:SHP-150 仪器编号:QC-SB-0134 PH7.0 无菌氯化钠-蛋白胨缓冲液配制批号:营养琼脂培养基配制批号:
玫瑰红钠琼脂培养基配置批号:
4. 细菌、霉菌和酵母菌数检查:
4.1供试品制备:取供试品,加pH7.0无菌氯化钠-蛋白胨缓冲液至ml。
混匀后,制备稀释级别为稀释液,备用。
4.5检验结果:本品菌落总数数为。
检验人:复核人:年月日。

青岛**有限公司文件目的建立微生物限度检查操作规程,规范操作,保证结果的准确性。
范围成品、辅料、内包装袋及纯化水的检验。
责任品管部微生物限度检验人员内容概述:本检验操作规程依据中国药典2015年版四部《通则1105 非无菌产品微生物限度检查:微生物计数法》和《通则1106 非无菌产品微生物限度检查:控制菌检查法》进行检查。
微生物计数法一、计数方法1.微生物计数法系用于能在有氧条件下生长的嗜温细菌和真菌的计数。
2、计数方法本法包括平皿法、薄膜过滤法。
3、计数培养基适用性检查和供试品计数方法适用性检查供试品微生物计数中所使用的培养基应进行适用性检查。
供试品的微生物计数方法应进行方法适用性试验,以确定采用的方法适合于该产品的微生物计数。
4、菌种及菌液的制备4.1试验用菌株的传代次数不得超过5代(从菌种保藏中心获得的干燥菌种为第0袋),并采用适宜的菌种保藏技术进行保藏。
计数培养基适用性检查和计数方法适用性试验见表1。
4.2菌液制备按表1规定培养各试验菌株。
取金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌的新鲜培养物,用PH7.0无菌氯化钠-蛋白胨缓冲液或0.9%无菌氯化钠溶液制成适宜浓度的菌悬液;取黑曲霉的新鲜培养物加入3-5ml含0.05%(ml/ml)聚山梨酯80的PH7.0无菌氯化钠-蛋白胨缓冲液或0.9%无菌氯化钠溶液,将孢子洗脱。
采用适宜的方法吸出孢子悬液至无菌试管中,用含0.05%(ml/ml)聚山梨酯80的PH7.0无菌氯化钠-蛋白胨缓冲液或0.9%无菌氯化钠溶液制成适宜浓度的黑曲霉孢子悬液。
菌液制备后若在室温下放置,应在2小时内使用;若保存在2-8℃,可在24小时内使用。
黑曲霉孢子悬液可保存在2-8℃,在验证过的贮存期内使用。
表1 试验菌液的制备和使用4.3阴性对照为确认试验条件是否符合要求,应进行对照试验,阴性对照试验应无菌生长。
4.4培养基适用性检查按照表1规定,接种不大于100cfu的菌液至胰酪大豆胨液体培养基或胰酪大豆胨琼脂培养基平板或沙氏葡萄糖琼脂培养基平板,置规定的条件下培养。
表:2.1-024微生物限度检查记录(通用)1. 常规法:取供试品10為1,用胰酪大豆胨液体培养基稀释至 100ml ,用匀浆仪等适宜的方法混匀,制成1:10供试液。
2. 薄膜过滤法:取供试品10mi ,用胰酪大豆胨液体培养基稀释至 100ml ,用匀浆仪等适宜的方法混匀,制成1:10供试液。
吸取1:10的供试液10ml ,过滤,加0.1%无菌蛋白胨水溶液 300ml 分 三次冲洗,每次100ml ;冲洗后,将滤膜正贴于胰酪大豆胨固体培养基和沙氏葡萄糖琼脂培养基 上,每种培养基平行制备 2个平皿。
按平皿法测定其菌数。
胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批)麦康凯琼脂培养基(配制批号: )供试液制备微生物限度检查记录、需氧菌总数检查30〜353〜5)、霉菌、酵母菌总数检查20C〜25C,5〜7天)三糖铁琼脂斜面穿刺接种 (18〜24h )三、控制菌检查 (30-35 C )检验者:表:2.1-024号:结论本品经按《中国药典》2015年版“非无菌产品微生物限度检查法”进行检验,结果审核者:微生物限度检查记录(丸剂)供试液制备供试液。
胰酪大豆胨增菌 (18〜24h )RV 沙门选择培养木糖赖氨酸脱氧胆酸分离培养(18〜48h )胰酪大豆胨液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)四、沙门菌检查 (30 °C 〜35C ) 胰酪大豆胨液体培养基(配制批号: )、RV 沙门增菌液体培养基(配制批号: ),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:五、耐胆盐革兰阴性菌检杳胰酪大豆胨液体培养基(配制批号:)、肠道菌增菌液体培养基(配制批号:),紫红胆盐葡萄糖琼脂培养基(配制批号:审核者:检验者: 表:2.1-024阴性对照阳性对照三、大肠埃希菌检查)、麦康凯液体培养基(配制批结果□检出大肠埃希菌□未检出大肠埃希菌(规定:不得检出/g)四、沙门菌检查(30°C〜35C)胰酪大豆东液体培养基(配制批号:)、肠道菌增菌液体培养基(配制批号:),紫红胆盐葡萄糖琼脂培养基(配制批号:、表: 2.1-024 微生物限度检查记录(蛇胆川贝液)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)胰酪大豆胨液体培养基(配制批号:)、RV沙门增菌液体培养基(配制批号:),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:)审核者:检验者:表:2.1-024 微生物限度检查记录(30〜353〜5天)、霉菌、酵母菌总数检查20C〜25C, 5〜7天)1、 口服液体药用聚酯瓶:取数个试瓶,加入1/2标示容量的氯化钠注射液,将盖旋紧,振摇1分钟,即得供试液。
霉菌与酵母菌总数、控制菌得检查。
二、引用标准:《中国药典》2015年版(通则1105-1106)三、目录1。
微生物限度标准2.设备、仪器及用具3。
消毒液、稀释剂、试液及培养基4。
检查总则(通则1105:非无菌产品微生物限度检查:微生物计数法,通则1106非无菌产品微生物限度检查:控制菌检查法)5。
微生物计数法检查6.控制菌检查法7.实验技术8、附件1.微生物限度标准非无菌药用原料及辅料得微生物限度标准(2).目测霉变者以不合格论。
(3)。
“无”为标准依据或无相应规定。
准依据或无相应规定.2.设施、仪器及用具2、1、设施:2、1、1.微生物限度检查室及相关设施:微生物计数试验环境应符合微生物限度检查得要求。
检验全过程必须严格遵守无菌操作,防止再污染,防止污染得措施不得影响供试品中微生物得检出。
单向流空气区域、工作台面及环境应定期进行监测。
2、1、2.其她设备:高压蒸汽灭菌器;细菌培养箱(30~35℃);霉菌培养箱(25~28℃);电炉(或其她适宜得加热装置);恒温水浴;电热干燥箱(250~300℃);电冰箱。
生化试剂储存箱。
2、2仪器及器皿2、2、1。
菌落计数器;显微镜(1500X);电子天平或药物天平(感量0、1g);pH 系列比色计。
2、2、2.玻璃器皿:锥形瓶(250~300ml,内装玻璃珠若干)、研钵(玻璃或陶瓷制,∮10~12cm)、培养皿(∮9 cm)、量筒(100ml)、试管(18×180mm)及塞、吸管(1ml分度0、01,10ml分度0、1)、载玻片、盖玻片、玻璃消毒缸(带盖)。
2、2、3新购得玻璃器皿得清洁:先用流水冲洗,浸泡于1%~2%盐酸(工业用)液中约2~6小时,除去游离碱质,再用流水冲洗.用于化学分析得玻璃仪器,需用重铬酸钾清洁液浸泡数分钟后,再用流水冲洗,最后以纯化水涮洗2~3次,晾干备用。
2、3用过得玻璃器皿:2、3、1未被病原微生物污染得器皿:可随时洗涤.用清水冲洗(或浸泡),除容量仪器外,可用毛刷与肥皂粉,内外刷洗,再用清水涮洗干净,晾干备用.容量仪器宜用清洁液浸泡或涮洗,再用流水冲洗,最后以纯化水涮洗2~3次.试管及培养皿:先正放或直立于高压蒸汽灭菌器内,经121℃灭菌30 分钟.趁热倾出培养物,再以清水或用毛刷及肥皂粉刷洗,最后以流水涮净。