微生物限度检查原始记录表
- 格式:doc
- 大小:78.50 KB
- 文档页数:1
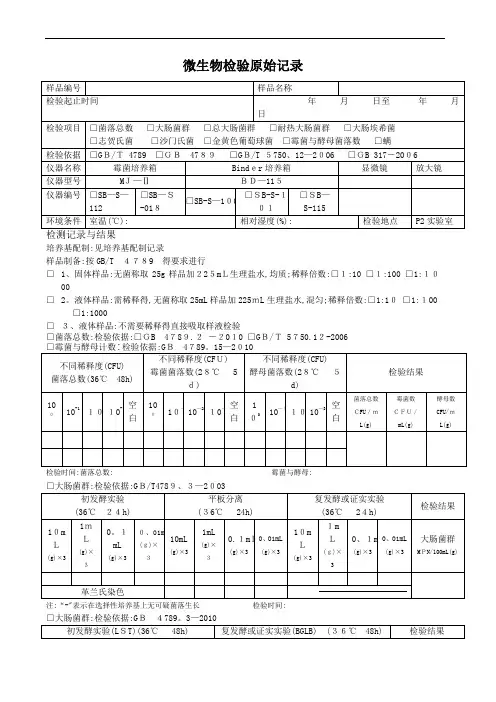
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 得要求进行
□1、固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:10
00
□2。
液体样品:需稀释得,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10□1:100 □1:1000
□3、液体样品:不需要稀释得直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2-2010 □GB/T 5750.12-2006
检验时间:菌落总数: 霉菌与酵母:
注:“-"表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
注:“-”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨: 检验依据GB 317、4-、10-2006
ﻬ微生物限度检验记录(复合膜)
检验人: 复核人:
微生物限度检验记录(辅料)
检验人: 复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人: 复核人:
ﻬ微生物限度检验记录(半成品、成品)
检验人: 复核人:
ﻬ微生物限度检验记录(辅料)
检验人: 复核人:。
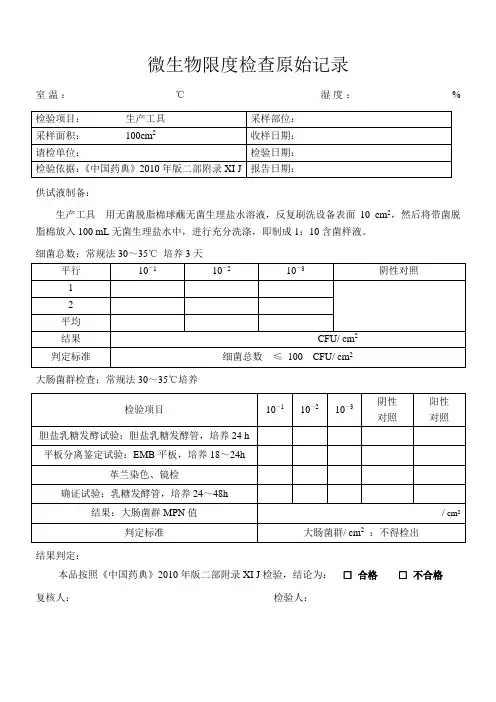
室温:℃湿度:%
供试液制备:
生产工具用无菌脱脂棉球蘸无菌生理盐水溶液,反复刷洗设备表面10 cm2,然后将带菌脱脂棉放入100 mL无菌生理盐水中,进行充分洗涤,即制成1:10含菌样液。
细菌总数:常规法30~35℃培养3天
大肠菌群检查:常规法30~35℃培养
结果判定:
本品按照《中国药典》2010年版二部附录XI J检验,结论为:□合格□不合格
复核人:检验人:
室温:℃湿度:%
供试液制备:
用无菌镊子取无菌脱脂棉签蘸无菌生理盐水溶液,反复刷洗人员手部和衣服表面10 cm2,然后将带菌脱脂棉放入100 mL无菌生理盐水中,进行充分洗涤,即制成含菌样液。
细菌总数:常规法30~35℃培养3天
大肠菌群检查:常规法30~35 ℃培养
结果判定:
本品按照《中国药典》2010年版二部附录XI J检验,结论为:□合格□不合格复核人:检验人:。
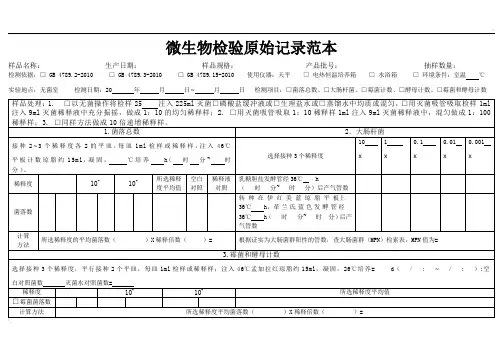

微生物原始记录表填写
微生物原始记录表是用来记录微生物培养实验过程中所观察到的各项
指标数据的一种表格形式。
下面是一个示范的微生物原始记录表,包括了
实验的基本信息以及观察到的各项指标数据。
请注意,根据实际情况,可
以根据需要添加或修改记录表的字段。
实验名称:微生物培养实验
实验日期:2024年1月1日
序号培养基组分(g/L)pH值温度(℃)培养时间(h)观察时间(h)观察指标A观察指标B观察指标C
1107.03724000
2107.0372411015
3107.0372421525
4107.0372432030
5107.0372442535
【说明】
1.序号:按照培养时间的顺序进行编号,方便对实验结果进行分析和
比较。
2.培养基组分:记录培养基的成分,以便后续对不同成分的培养基进
行比较。
3.pH值:记录培养基的酸碱性。
4.温度:记录培养的温度条件。
5.培养时间:记录培养的总时间,单位为小时。
6.观察时间:记录每次观察的时间点,以小时为单位。
7.观察指标A/B/C:根据实验需要,可以添加相应的观察指标,例如微生物生长曲线中的菌落数、菌液的浊度、菌液的酸碱度等等。
以上示范的记录表仅仅是一个参考样例,具体的填写内容和形式取决于实验的目的和方法。
实际操作中,可以根据具体的实验内容进行添加或修改。
在填写微生物原始记录表时应注意实验的准确性和可重复性,记录下实验过程中的每一个重要环节和观察结果,以便后续对实验结果进行分析和验证。
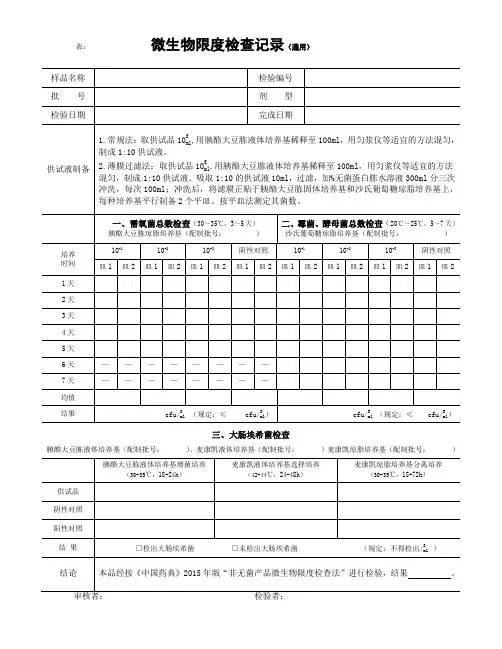
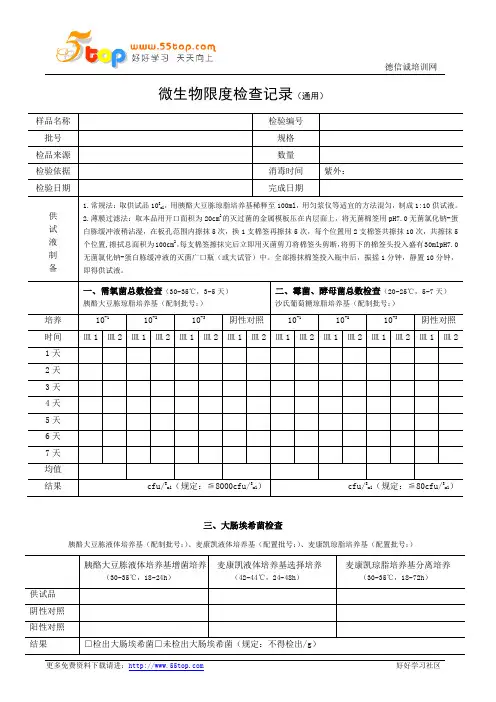
表:微生物限度检查记录(通用)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)微生物限度检查记录(30~35℃,3~5天)20℃~25℃,5~7天)沙氏葡萄糖琼脂培养基(配制批号:)三、控制菌检查(30-35℃)表:胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)(30℃~35℃)胰酪大豆胨液体培养基(配制批号:)、RV沙门增菌液体培养基(配制批号:),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:)五、耐胆盐革兰阴性菌检查胰酪大豆胨液体培养基(配制批号:)、肠道菌增菌液体培养基(配制批号:),紫红胆盐葡萄糖琼脂培养基(配制批号:)表:(含药材原粉的片剂)胰酪大豆胨液体培养基(配制批号: )、麦康凯液体培养基(配制批号: )麦康凯琼脂培养基(配制批号: )(30℃~35℃)胰酪大豆胨液体培养基(配制批号: )、RV 沙门增菌液体培养基(配制批号: ),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号: )、三糖铁琼脂(配制批号: )五、耐胆盐革兰阴性菌检查胰酪大豆胨液体培养基(配制批号: )、肠道菌增菌液体培养基(配制批号: ),紫红胆盐葡萄糖琼脂培养基(配制批号: )表:微生物限度检查记录(蛇胆川贝液)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、RV沙门增菌液体培养基(配制批号:),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:)表:微生物限度检查记录(30~35℃,3~5天)20℃~25℃,5~7天)沙氏葡萄糖琼脂培养基(配制批号:)胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)表:微生物限度检查记录(内包材)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)。
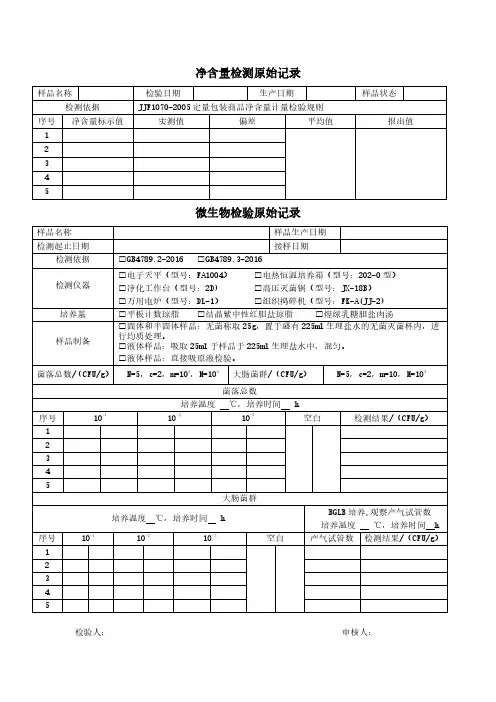
净含量检测原始记录
样品名称检验日期生产日期样品状态检测依据JJF1070-2005定量包装商品净含量计量检验规则
序号净含量标示值实测值偏差平均值报出值1
2
3
4
5
微生物检验原始记录
样品名称样品生产日期
检测起止日期接样日期
检测依据□GB4789.2-2016□GB4789.3-2016
检测仪器□电子天平(型号:FA1004)□电热恒温培养箱(型号:202-0型)□净化工作台(型号:2D)□高压灭菌锅(型号:JX-18B)
□万用电炉(型号:DL-1)□组织捣碎机(型号:FK-A(JJ-2)
培养基□平板计数琼脂□结晶紫中性红胆盐琼脂□煌绿乳糖胆盐肉汤
样品制备□固体和半固体样品:无菌称取25g,置于盛有225ml生理盐水的无菌灭菌杯内,进行均质处理。
□液体样品:吸取25ml于样品于225ml生理盐水中,混匀。
□液体样品:直接吸原液检验。
菌落总数/(CFU/g)N=5,c=2,m=104,M=105大肠菌群/(CFU/g)N=5,c=2,m=10,M=102
菌落总数
培养温度℃,培养时间h
序号10-110-210-3空白检测结果/(CFU/g)1
2
3
4
5
大肠菌群
培养温度℃,培养时间h
BGLB培养,观察产气试管数培养温度℃,培养时间h
序号10-110-210-3空白产气试管数检测结果/(CFU/g)1
2
3
4
5
检验人:审核人:。
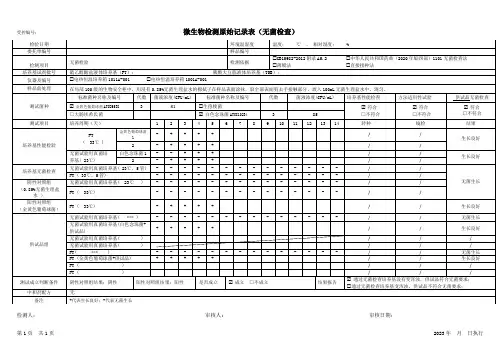
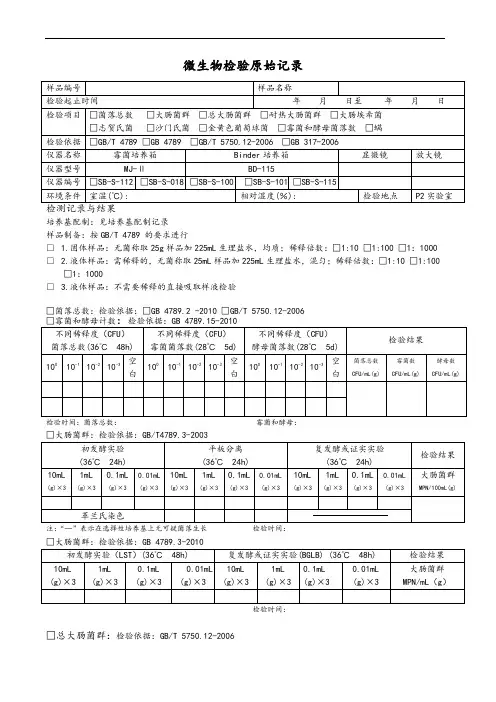
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人:复核人:
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
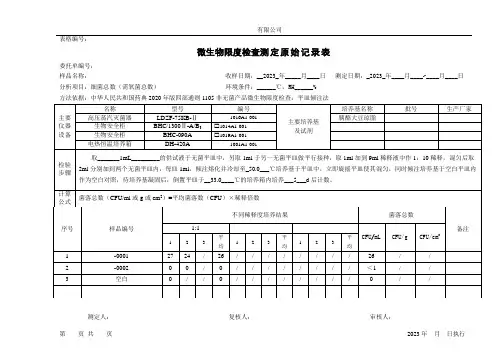
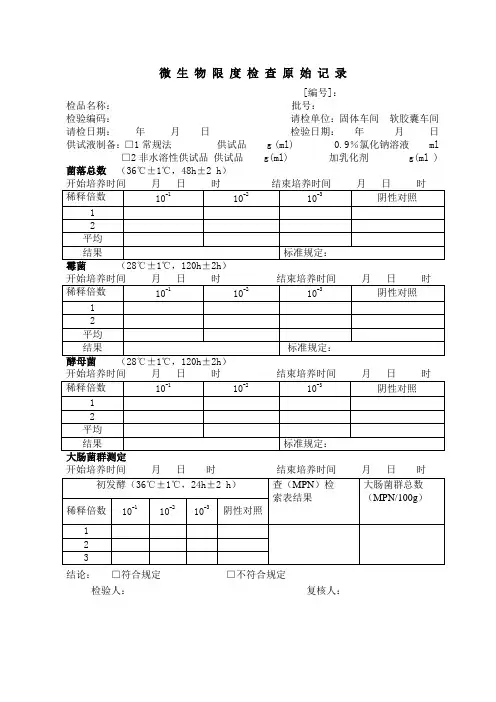
菌落总数与大肠菌群检验原始记录
主检:年月日校核:年月日
菌落总数和大肠菌群检测原始记录
主检:年月日校核:年月日
水质微生物检验原始记录
主检:年月日校核:年月日
乳酸菌与大肠菌群检测记录
主检:年月日校核:年月日
致病菌检验原始记录
主检:年月日校核:年月日
XXXX检测有限公司
霉菌和酵母菌检验原始记录
菌落计数:
培养温度:28±1℃培养时间:年月日时--- 年月日时
主检:年月日校核:年月日
XXXX检测有限公司
商业无菌检验原始记录
共页第页
主检:日期:校核:日期:。