吉林大学大学物理气体作业答案
- 格式:ppt
- 大小:729.00 KB
- 文档页数:22

吉林大学化学学院2002~2003学年第2学期期末考试物理化学 试题 2003年7月3日说明:1、全部答案写在答题纸上,标明题号,不抄题。
2、考试时间为2.5小时。
3、考试结束时,请将试题、答题纸、草纸上交。
注意: 答题时要列出详细运算步骤并计算出中间运算数值和最终计算结果.(玻兹曼常数k B =1.3806×10-23 J.K -1; 普朗克常数h = 6.6262×10-34 J.s;N A =6.023×1023; F=96500; 摩尔质量: O 16.00; Kr 83.80; He 4.0026)一、计算题 ( 共10题 100分 )(1). 10 分 (1636)已知 N 2分子的转动惯量 I = 13.9×10-47kg ⋅m 2,求1mol N 2分子在 25℃时各转动热力学函数G m (r ),F m (r ),H m (r ),U m (r ),S m (r )。
(2). 10 分 (1570)有1 mol Kr ,温度为300 K 、体积为V ,有1 mol He 具有同样的体积V ,如要使这两种气体具有相同的熵值(忽略电子运动的贡献),则He 的温度应多高?并用熵的统计意义解释此结果。
(M r (Kr) = 83.8, M r (He) = 4.0026)(3). 10 分 (5447)含有相同物质量的A, B 溶液,等体积相混合,发生反应 A+B=C, 在反应 1 h 后, A 的75%已反应掉, 当反应时间为2 h 时, 在下列情况下, A 有多少未反应?[1] 当该反应对A 为一级, 对B 为零级[2] 当对A, B 均为一级[3] 当A, B 均为零级(4). 10 分 (5416)碳的放射性同位素14C ,在自然界树木中的分布基本保持为总碳量的1.10×10-13%。
某考古队在一山洞中,发现一些古代木头燃烧的灰烬, 经分析14C 的含量为总碳量的9.57×10-14%, 已知14C 的半衰期为 5700 a (年), 试计算这灰距今约有多少年?(5). 10 分 (5371)300 K 时,研究反应 A 2+ 2B = 2C + 2D 有下列实验事实:[1] 当按化学计量比进料时,测得下列数据t / s 0 90 217[B] /mol ·dm -3 0.02 0.010 0.0050[2] 当二次实验中 [B]0相同,[A]0增加一倍时,反应速率增大至 1.4 倍,假设反应速率方程为 r = k [A 2]x [B]y ,请求 x ,y ,并求算反应速率常数。


吉大物理化学试题及答案一、选择题(每题5分,共20分)1. 下列关于理想气体的描述,正确的是:A. 理想气体分子间无相互作用力B. 理想气体分子体积可以忽略不计C. 理想气体分子间存在相互作用力D. 理想气体分子体积不可忽略答案:AB2. 根据热力学第二定律,下列说法错误的是:A. 不可能从单一热源吸热全部转化为功B. 不可能使热量从低温物体自发地传到高温物体C. 可以不产生其他影响而将热量从低温物体传到高温物体D. 不可能使热量从低温物体传到高温物体答案:C3. 根据吉布斯自由能的定义,下列说法正确的是:A. 在恒温恒压下,系统自发进行的过程吉布斯自由能会减小B. 吉布斯自由能的单位是焦耳C. 吉布斯自由能是温度和压力的函数D. 吉布斯自由能是温度和体积的函数答案:AC4. 下列关于电化学的描述,正确的是:A. 原电池的总反应是氧化还原反应B. 电解池的总反应是氧化还原反应C. 原电池和电解池的总反应都是氧化还原反应D. 原电池和电解池的总反应都不是氧化还原反应答案:A二、填空题(每题5分,共20分)1. 理想气体状态方程为_______。
答案:PV=nRT2. 热力学第一定律的数学表达式为_______。
答案:ΔU=Q+W3. 根据吉布斯自由能的公式,当温度和压力不变时,系统自发进行的过程满足_______。
答案:ΔG<04. 电化学中,电势差的定义是_______。
答案:E=ΔG/nF三、简答题(每题10分,共20分)1. 简述热力学第二定律的开尔文表述和克劳修斯表述。
答案:开尔文表述:不可能从单一热源吸热全部转化为功而不产生其他影响。
克劳修斯表述:不可能使热量从低温物体自发地传到高温物体。
2. 描述电化学中的法拉第定律。
答案:法拉第定律指出,电解过程中通过电极的电量与电极上发生氧化还原反应的物质的量成正比,比例常数为法拉第常数。
四、计算题(每题20分,共40分)1. 假设有一理想气体,其初始状态为P1=100kPa,V1=2m³,T1=300K。
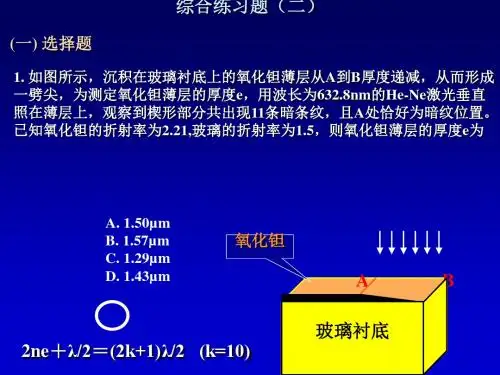

第十一章气体动理论习题详细答案一、选择题1、答案:B解:根据速率分布函数()f v的统计意义即可得出。
()f v表示速率以v为中心的单位速率区间内的气体分子数占总分子数的比例,而dvvNf)(表示速率以v为中心的dv速率区间内的气体分子数,故本题答案为B。
2、答案:A解:根据()f v的统计意义和pv的定义知,后面三个选项的说法都是对的,而只有A不正确,气体分子可能具有的最大速率不是pv,而可能是趋于无穷大,所以答案A正确。
3、答案:Armsv=据题意得222222221,16H O H HH O O OT T T MM M T M===,所以答案A正确。
4、由理想气体分子的压强公式23kp nε=可得压强之比为:Ap∶Bp∶Cp=n A kAε∶n B kBε∶n C kCε=1∶1∶15、氧气和氦气均在标准状态下,二者温度和压强都相同,而氧气的自由度数为5,氦气的自由度数为3,将物态方程pV RTν=代入内能公式2iE RTν=可得2iE pV=,所以氧气和氦气的内能之比为5 : 6,故答案选C。
6、解:理想气体状态方程PV RTν=,内能2iU RTν=(0mMν=)。
由两式得2U iPV=,A、B两种容积两种气体的压强相同,A中,3i=;B中,5i=,所以答案A正确。
7、由理想气体物态方程'mpV RTM=可知正确答案选D。
8、由理想气体物态方程pV NkT=可得气体的分子总数可以表示为PVNkT=,故答案选C。
9、理想气体温度公式21322k m kTευ==给出了温度与分子平均平动动能的关系,表明温度是气体分子的平均平动动能的量度。
温度越高,分子的平均平动动能越大,分子热运动越剧烈。
因此,温度反映的是气体分子无规则热运动的剧烈程度。
由于k ε是统计平均值,因而温度具有统计意义,是大量分子无规则热运动的集体表现,对个别分子或少数分子是没有意义的。
故答案选B 。
10、因摩尔数相同的氢气和氦气自由度数不同,所以由理想气体的内能公式2i E RT ν=可知内能不相等;又由理想气体温度公式21322k m kT ευ==可知分子的平均平动动能必然相同,故答案选C 。



物理化学期末试题(共4页)学院 姓名 班级与学号 卡号 得分一、 填空(每空1分,共10分)1.纯物质完美晶体在 0K 时的熵值为零。
2.在-10℃、101325Pa 下,纯水化学势u 1与冰的化学势u 2的大小关系为u 1 > u 2 。
3.温度T 时将纯NH 4HS (S )置于真空容器中,发生分解反应:NH 4HS(s)=NH 3(g)+H 2S(g), 测得平衡时系统的总压力为p ,则K Θ= p 2/(2p )2 。
4.某系统经历一不可逆循环后,则系统、环境及总的熵变ΔS 系 = 0,ΔS 环 > ,ΔS 总 > 0。
5. 完全互溶的双液系中,在x B =0.6处,平衡蒸气压有最高值,那么组成为x B =0.4的溶液在气液平衡时,x B (g )、 x B (l )、x B (总)的大小顺序为 x B (g ) > x B (总) > x B (l ) 。
6.某理想气体进行绝热恒外压膨胀,其热力学能变化ΔU < 0与其焓变ΔH < 0﹝填>,< 或== 。
7. 若Cu 2﹢+2e -→ Cu 的E Θ=0.34V ,则1/2Cu → 1/2 Cu 2﹢+e -的E Θ= 0.34V 。
二、选择(1分×15=15分)1.实际气体的节流膨胀过程中,哪一组的描述是正确的?( A ) A. Q =0 ΔH =0 Δp <0 B. Q =0 ΔH <0 Δp >0 C. Q <0 ΔH =0 Δp <0 D. Q >0 ΔH =0 Δp <02.工作在100℃和30℃的两个大热源间的卡诺机,其效率是( A ) A. 19% B. 23% C. 70% D. 30%3.热力学基本公式d A = -S d T -p d V 可适用下述哪一个过程?( B ) A. 293K 、p Θ的水蒸发过程 B.理想气体真空膨胀C. 电解水制取氢D. N 2+3H 2 →2NH 3未达平衡 4.理想气体经绝热真空膨胀后,其温度怎样变化( C ) A. 上升 B.下降 C.不变 D .不能确定 5.下列各式中不是化学势的是( C )A. C n p,T,)/(B n G ∂∂B. C n V,T,)/(B n A ∂∂C. C n S,T,)/(B n U ∂∂D.C n p,S,)/(B n H ∂∂6.盐碱地的农作物长势不良,甚至枯萎,主要原因是( D )A. 天气太热 B . 很少下雨 C .肥料不足 D . 水分倒流 7.p Θ下,C (石墨)+O 2(g) =CO 2(g)的反应热为Δr H m Θ,下列说法中错误的是 ( D ) A .Δr H m Θ就是CO 2(g)的生成焓Δf H m ΘB . Δr H m Θ是C (石墨)的燃烧焓 C . Δr H m Θ=Δr U m ΘD . Δr H m Θ>Δr U m Θ8.已知反应 H 2O(g)=H 2(g)+1/2 O 2(g)的平衡常数为K 1Θ及反应 CO 2(g)=CO(g)+1/2 O 2(g)的K 2Θ,则同温度下反应 CO(g)+ H 2O(g)= CO 2(g)+ H 2(g)的K 3Θ为 ( D )· a A. K 3Θ= K 1Θ+ K 2ΘB. K 3Θ= K 1Θ× K 2ΘC. K 3Θ= K 2Θ/ K 1ΘD. K 3Θ= K 1Θ/ K 2Θ9.已知在298K 时,液体A 的饱和蒸气压为90KPa ,液体B 的饱和蒸气压为30KPa 。

大学物理(气体动理论)习题答案8-1 目前可获得的极限真空为Pa 1033.111-⨯,,求此真空度下3cm 1体积内有多少个分子?(设温度为27℃)[解] 由理想气体状态方程nkT P =得 kT V NP =,kT PV N =故 323611102133001038110110331⨯=⨯⨯⨯⨯⨯=---...N (个)8-2 使一定质量的理想气体的状态按V p -图中的曲线沿箭头所示的方向发生变化,图线的BC 段是以横轴和纵轴为渐近线的双曲线。
(1)已知气体在状态A 时的温度是K 300=A T ,求气体在B 、C 、D 时的温度。
(2)将上述状态变化过程在 T V -图(T 为横轴)中画出来,并标出状态变化的方向。
[解] (1)由理想气体状态方程PV /T =恒量,可得:由A →B 这一等压过程中BBA A T V T V = 则 6003001020=⋅=⋅=A AB B T V V T (K) 因BC 段为等轴双曲线,所以B →C 为等温过程,则==B C T T 600 (K)C →D 为等压过程,则CCD D T V T V = 3006004020=⋅=⋅=C CD D T V V T (K) (2)8-3 有容积为V 的容器,中间用隔板分成体积相等的两部分,两部分分别装有质量为m 的分子1N 和2N 个, 它们的方均根速率都是0υ,求: (1)两部分的分子数密度和压强各是多少?(2)取出隔板平衡后最终的分子数密度和压强是多少?010203040[解] (1) 分子数密度 VNV N n VN V N n 2222111122====由压强公式:231V nm P =, 可得两部分气体的压强为 VV mN V m n P VV mN V m n P 3231323120220222012011====(2) 取出隔板达到平衡后,气体分子数密度为 VN N V N n 21+==混合后的气体,由于温度和摩尔质量不变,所以方均根速率不变,于是压强为:VV m N N V nm P 3)(31202120+==8-4 在容积为33m 105.2-⨯的容器中,储有15101⨯个氧分子,15104⨯个氮分子,g 103.37-⨯氢分子混合气体,试求混合气体在K 433时的压强。


1010 气体动理论班号 学号 姓名 成绩一、选择题(在下列各题中,均给出了4个~5个答案,其中有的只有1个是正确答案,有的则有几个是正确答案,请把正确答案的英文字母序号填在题后的括号内)1. 两种摩尔质量不同的理想气体,它们的压强、温度相同,体积不同,则下列表述中正确的是:A. 单位体积内的分子数相同;B. 单位体积中气体的质量相同;C. 单位体积内气体的内能相同;D. 单位体积内气体分子的总平均平动动能相同。
(A 、D )[知识点] 理想气体状态方程nkT p =及内能公式RT i E 2=。
[分析与解答] 根据理想气体状态方程nkT p =,当气体的压强与温度相同时,单位体积内的分子数n 相同。
由理想气体状态方程RT Mm pV =,得RTpM V m =,即当气体压强与温度相同,但摩尔质量不同时,单位体积中气体的质量不相同。
又由理想气体内能公式RT i M m E 2=,结合状态方程,得pV i E 2=,则有p i V E 2=,可见当压强相同的两种理想气体的自由度相同(即为同结构分子)时,单位体积内气体的内能才会相同。
理想气体分子的平均平动动能kT k 23=ε,则有p n E k k 23==ε,则当气体的压强相同时,单位体积内的气体分子的总平均平动动能相同。
2. 以a 代表气体分子的方均根速率,ρ 表示气体的质量体密度。
则由气体动理论可知,理想气体的压强p 为:A. 2a p ρ=; B. a p ρ31=; C. 231a p ρ=; D. (C )[知识点] RT Mm pV =,MRT 32=v[分析与解答] 由方均根速率的定义和题意有a MRT ==32v(1)由理想气体状态方程 RT Mm pV = (2)由题意 Vm ρ=(3)联立以上三式,则有 23ρa p =3. 对处于平衡状态下的一定量某种理想气体,在关于内能的下述表述中,正确的是: A. 内能是所有分子平均平动动能的总和; B. 气体处于一定状态,就相应有一定的内能; C. 当理想气体状态改变时,内能一定随着变化;D. 不同的理想气体,只要温度相同,其内能也相同。
综合练习(一)一.选择题1.物质的量为n 的理想气体,该气体的哪一组物理量确定后,其他状态函数都有定值(1)p (2)V (3)T ,U √(4)T ,p 2.公式p p H Q ∆=适用于下列哪个过程(1)理想气体从1013。
25kPa 反抗恒定外压101.325kPa 膨胀 √(2)273。
2K ,101。
325k Pa 下,冰融化成水 (3) 298。
2K,101.325k Pa 下,电解CuSO 4水溶液 (4)理想气体从状态A 变化到状态B3.某化学反应若在300K, p 下在试管中进行时放热6×104J ,若在相同条件下通过可逆电池进行反应,则吸热6×103J ,该化学反应的熵变为(1) —200J ﹒K —1 (2) 200 J ﹒K —1 (3) -20 J ﹒K —1 √ (4) 20 J ﹒K -14.上题反应在试管中进行时其环境的熵变√(1) 200J ﹒K —1 (2) -200 J ﹒K -1 (3) —180J ﹒K -1 (4) 180 J ﹒K -1 5.第3题中系统可能做的最大非体积功为(1) -66000J √(2) 66000 J (3) -54000 J (4) 54000 J 6.在通常情况下,对于二组分系统能平衡共存的最多相 (1) 1 (2) 2 (3) 3 √(4) 4 7.下列各式哪个表示了偏摩尔量 √(1)()C TPn B U n ∂∂ (2)()c TVn BA n ∂∂ (3)()C SPnB Hn ∂∂ (4)()C B TPn B n μ∂∂ 8.298K ,当H 2SO 4溶液的浓度从0.01mol ﹒kg -1增加到0.1 mol ﹒kg —1时,其电导率和摩尔电导率将(1)m κΛ减小,增加 (2)m κΛ增加,增加 (3)m κΛ减小,减小 √ (4)m κΛ增加,减小 9.在化学动力学中,质量作用定律只适用于(1)反应基数为正整数的反应 (2)恒温恒容反应 √(3)基元反应 (4)理想气体反应 10.兰格缪尔等温吸附理论中,最重要的基本假设是(1)吸附质为理想气体 (2)中压条件 √(3)单分子层吸附 (4)多分子层吸附二.填空1.在一个绝热箱内装有浓硫酸和水,开始中间用隔膜分开,然后弄破隔膜,使水和浓硫酸混合,以水和浓硫酸为系统,则:Q( = )0, W ( = ),△U ( = )0。