- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Pt H2O Pt
草酸
3
Cቤተ መጻሕፍቲ ባይዱ
二氨二氯合铂的可能构型 两种不同的二氨二氯合铂异构体的不同的化学性质
4-2-3 对映异构 M(AABBCC)的异构体 的异构体
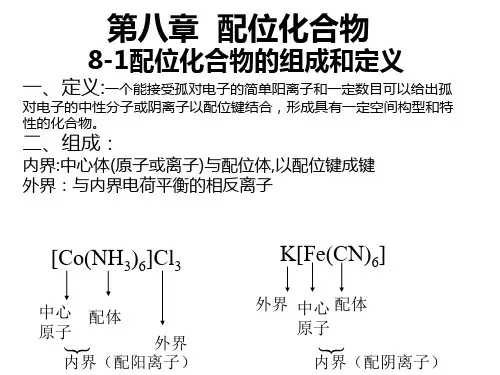
4-1-1 配合物的定义 1. 配合物的定义 由一定数量的可以供出孤对电子或π电子的离子或 由一定数量的可以供出孤对电子或 电子的离子或 分子(统称配体)与接受孤对电子或 统称配体 与接受孤对电子或π电子的原子或离子 分子 统称配体 与接受孤对电子或 电子的原子或离子 (统称中心原子或离子 以配位键结合形成的化合物。 统称中心原子或离子 结合形成的化合物。 统称中心原子或离子)以配位键结合形成的化合物 2. 配合物的组成 配合物的组成: (1) 内界和外界 内界和外界: 配合物一般有内界和外界组成, 配合物一般有内界和外界组成 [Cu(NH3)4] SO4
内界 外界
具有一定稳定性的结构单元称为配合物的内界, 具有一定稳定性的结构单元称为配合物的内界 用 中括号表示出来, 其余部分为外界. 中括号表示出来 其余部分为外界 K3[Fe(CN)6]
外界 内界
配合物的内界和外界以离子键结合 配合物的内界和外界以离子键结合. 如果配合物的 界和外界以离子键结合 内界是中性分子 无外界, 如[PtCl2(NH3)2], Ni(CO)4]. 内界是中性分子, 无外界 中性分子 (2) 中心原子 中心离子)或形成体 中心原子(中心离子 或形成体 中心离子 中心原子是配合物的核心部分. 中心原子是配合物的核心部分 [Cu(NH3)4]2+: Cu2+ [PtCl2(NH3)2]: Pt2+ Ni(CO)4]: Ni [S9]2-: S2中心原子不一定是阳离子, 可以是中性原子, 中心原子不一定是阳离子 可以是中性原子 也可是 阴离子. 阴离子 (3) 配体和配位原子 在配体中, 在配体中,直接与中心离子或原子相结合的原子称 为配位原子, 为配位原子,如NH3中N,CN-中C。 , 。
4-1 配合物基本概念
硫酸铜水溶液天蓝色: [Cu(H2O)4]2+; 向硫酸铜溶液 硫酸铜水溶液天蓝色 滴加过量氨水,形成深蓝色的透明溶液: 滴加过量氨水,形成深蓝色的透明溶液 [Cu(NH3)4]2+;向 向 其中滴加过量浓盐酸,得到黄色透明溶液: [CuCl4]2-。 其中滴加过量浓盐酸,得到黄色透明溶液 这样的由金 像[Cu(H2O)4]2+、[Cu(NH3)4]2+、[CuCl4]2-这样的由金 属原子与中性分子或者阴离子结合形成的复杂离子叫做 配离子(络离子 其中的金属原子是配离子形成体 络离子), 形成体或 配离子 络离子 ,其中的金属原子是配离子形成体或中 心原子,其中的H2O、NH3、Cl-等叫做配体。 心原子,其中的 、 等叫做配体。 配体 中心离子与配体之间的化学作用力叫做配位键, 中心离子与配体之间的化学作用力叫做配位键,一 般是中心原子接受配体中的某原子的孤对电子形成的。 般是中心原子接受配体中的某原子的孤对电子形成的。 中心原子周围的配位原子的个数叫做配位数 配位原子的个数叫做配位数。 中心原子周围的配位原子的个数叫做配位数。
4-2-2 几何异构 几何异构是立体异构之一, 几何异构是立体异构之一 是配体在中心原子周 围因排列方式不同而产生的异构现象 而产生的异构现象。 围因排列方式不同而产生的异构现象。 顺式 顺式 顺式 见教材MA4B2型(图4-5): 反式和顺式 cis见教材 图 cis- 反式和顺式. cisMA3B3型(图4-6):N 面式和经式. Cl NH3 图 H3 面式和经式 O OH HN O
第4章 配位化合物
基 本 概 念 配 合 物 的 命 名 杂 化 理 论 晶 体 场 理 论 配 合 物 的 立 体 异 构 作 业
基本要求
1. 掌握配位化合物的组成及有关的概念。 掌握配位化合物的组成及有关的概念。 2. 掌握配位化合物价键理论的主要论点,并能用此 掌握配位化合物价键理论的主要论点, 解释一些实例。 解释一些实例。 3. 理解晶体场理论,并能解释双峰图、配合物的稳 理解晶体场理论,并能解释双峰图、 定性及配离子的颜色。 定性及配离子的颜色。
4. 如果外界是氢氧根离子,称氢氧化某。 如果外界是氢氧根离子 称氢氧化某。 氢氧根离子, [Cu(NH3)4](OH)2: 氢氧化四胺合铜 氢氧化四胺合铜(II) 5. 处于配合物内界的配离子,其命名方法一般地依照如 处于配合物内界的配离子, 下顺序:配位体数、配位体的名称(不同配位体名称之间 下顺序:配位体数、配位体的名称 不同配位体名称之间 以中圆点(·)分开 分开), 中心离子名称, 以中圆点 分开 ,“合”,中心离子名称,中心离子氧 化态(加括号 用罗马数字注明)。 加括号:用罗马数字注明 化态 加括号 用罗马数字注明 。 Cu2[SiF6]: 六氟合硅 六氟合硅(IV)酸亚铜 酸亚铜 K3[Fe(CN)6]: 六氰合铁 六氰合铁(III)酸钾 酸钾 若配离子中的配位体不止一种, 若配离子中的配位体不止一种,在命名时配体列出的 顺序按如下规定: 顺序按如下规定: 6. 配位体中既有无机配体又有有机配体,无机配体排列 配位体中既有无机配体又有有机配体, 在前, 有机配体排列在后。 在前 有机配体排列在后。 二氯·二 三苯基膦 合铂(II) 三苯基膦)合铂 cis-PtCl2(Ph3P)2]: 顺-二氯 二(三苯基膦 合铂 二氯 -
(4) 配位数 配合物中心原子周围的配位原子的个数, 配合物中心原子周围的配位原子的个数 称为配位 数. 配位数不一定等于配体的数目, 只有是单齿配体时 配位数不一定等于配体的数目 才相等. 才相等 [Fe(CN)6]3-: Fe3+配位数为 配位数为6. [Cu(en)2]2+: Cu2+配位数为4. 配位数为4. (5) 多核化合物 含有多个中心原子的配合物称为多核配合物(图4含有多个中心原子的配合物称为多核配合物 图 4). (6) π-配合物 配合物 配体中没有孤电子对,而是提供π 配体中没有孤电子对,而是提供π电子与中心原 子形成π配键 配键. 年发现的蔡斯盐K[Pt(C2H4)Cl3] 子形成 配键 如1825年发现的蔡斯盐 年发现的蔡斯盐 [图4-15]. 图
K2[PtCl4]加氨水得棕黄色配合物, 组成为[PtCl2(NH3)2], 有 Pt 加氨水得棕黄色 棕黄色配合物 Cl NH3 Cl C H3N OH H3N O O 极性, 水中溶解度0.26g/100g. Cl NH3 Cl NH3 反式 反式 Pt 将其用氯化氢处理或热至250℃, 转变为浅黄色, 组成仍为 Pt 转变为浅黄色 Pt trans-) ], NH3 transCl [PtCl2(NH3 2 但极性消失, 水中溶解度减至0.037g/100g.Cl ? Cl NH3 NH3 H3N Cl NH3 草酸 HO NH3 H2O 四配位配合物的几何构型不是四面体而是平面四边形;如 四配位配合物的几何构型不是四面体而是平面四边形; Pt 反式 四面体构型 Pt 顺式 H3N Cl 果是四面体, [PtCl2(NH33N2]不可能出现异构现象, 而平面四边形 H ) trans不可能有立体异构体 OHcis不能反应 则可以有两种异构体 的[PtCl2(NH3)2]则可以有两种异构体(图4-8).
4-2 配合物的异构现象与立体结构
化学式相同而结构不同的化合物称为同分异构体。 化学式相同而结构不同的化合物称为同分异构体。 同分异构体 4-2-1 结构异构 1. 结构异构:组成相同而结构不同的异构现象 结构异构:组成相同而结构不同的异构现象. 紫色), CrCl3·6H2O: [Cr(H2O)6]Cl3(紫色 紫色 [CrCl(H2O)5]Cl2·H2O(灰绿色 灰绿色), 灰绿色 [CrCl2(H2O)4]Cl·2H2O(深绿色 深绿色) 深绿色 键合异构: 2. 键合异构 由于同一种配体以两种不同配位原子 配位引起的异构. 配位引起的异构 都可作为配位原子: 硫氰根), 如: SCN-中S和N都可作为配位原子 SCN-(硫氰根 和 都可作为配位原子 硫氰根 异硫氰根); 硝基), 亚硝酸根). NCS-(异硫氰根 NO2-(硝基 ONO-(亚硝酸根 异硫氰根 硝基 亚硝酸根
H[PtCl3(NH3)]: 三氯 一胺合铂 酸 三氯·一胺合铂 一胺合铂(II)酸 7. 有多种无机配体和有机配体时,先列出阴离子的名 有多种无机配体和有机配体时, 称后列出中性分子的名称。 称后列出中性分子的名称。 [Pt(en)Cl2]: 二氯 一(乙二胺 合铂 二氯·一 乙二胺 合铂(II) 乙二胺)合铂 8. 同类配体 按配位原子元素符号的英文字母顺序列出 同类配体, 配位原子元素符号的英文字母顺序列出 列出. [Co(NH3)5(H2O)]Cl3: 三氯化五胺 一水合钴 三氯化五胺·一水合钴 一水合钴(III) 9. 同类配体, 配位原子也相同时, 将含原子个数少的配 同类配体, 配位原子也相同时, 将含原子个数少的配 体排在前面, 较多的排在后面. 体排在前面 较多的排在后面 [PtNO2NH3(NH2OH)(py)]Cl: 一氯化硝基 胺·羟胺 吡啶 一氯化硝基·胺 羟胺 羟胺·吡啶 合铂(II) 合铂 10. 如果配位原子相同 配体含的原子个数也相同 按配 如果配位原子相同, 配体含的原子个数也相同, 体结构式中与配位原子相连的原子的元素符号的字母 顺序列出. 顺序列出 氨基·硝基 二胺合铂(II) 硝基·二胺合铂 [PtNH2NO2(NH3)2]: 氨基 硝基 二胺合铂
按配位原子种类分为: 按配位原子种类分为: a. 含N配位:NH3, NO(亚硝酰 NO2(硝基 NCS-(异硫 配位: 亚硝酰), 硝基), 亚硝酰 硝基 异硫 配位 氰根). 氰根 b. 含O配体 H2O, OH-(羟基 CO32-, ONO-(亚硝酸根 配体: 羟基), 亚硝酸根). 配体 羟基 亚硝酸根 c. 含C配体 CN-(氰), CO(羰基 配体: 羰基). 配体 氰 羰基 d. 含S配体 S2-, SCN-(硫氰根 SH-(巯). 配体: 硫氰根), 配体 硫氰根 巯 e. 含P配体 PH3, PR3(膦). 配体: 配体 膦 f. 卤素配体 F-, Cl-. 卤素配体: 按配体所含配位原子的数目分为: 按配体所含配位原子的数目分为 单齿配体: 配体中只有一个配位原子, 单齿配体 配体中只有一个配位原子 F-, OH-, NH3. 多齿配体(双齿 三齿、四齿等等): 双齿、 多齿配体 双齿、三齿、四齿等等 配体中有多个配位 原子, 乙二胺四乙酸) 原子 en, EDTA(乙二胺四乙酸 (图4-1,4-2). 乙二胺四乙酸 图 多齿配体形成的配合物又被形象地叫做螯合物。 多齿配体形成的配合物又被形象地叫做螯合物。 螯合物