高一化学非金属及其化合物复习
- 格式:doc
- 大小:420.00 KB
- 文档页数:4
《非金属及其化合物》全章复习与巩固【学习目标】1.总结几种常见非金属(碳、硅、氯、硫、氮)及其化合物的主要性质,理解浓硫酸及硝酸的氧化性。
2. 掌握氯离子、铵根离子的检验方法。
3. 学会氨气、二氧化硫、二氧化碳的检验方法。
4. 掌握氯气、氨气的实验室制法。
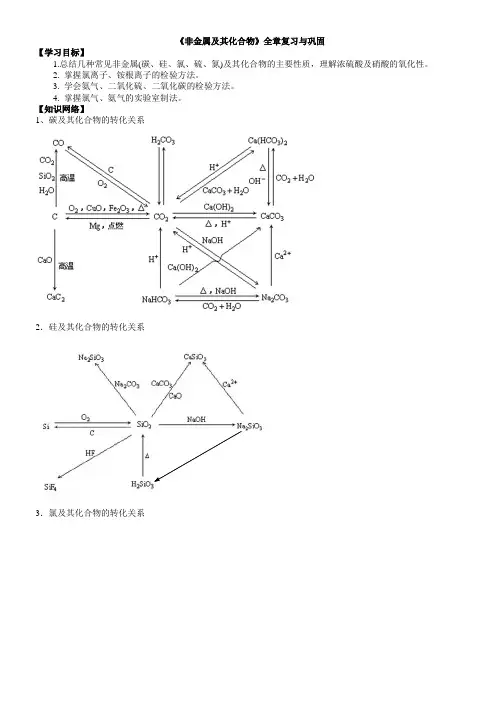
【知识网络】1、碳及其化合物的转化关系2.硅及其化合物的转化关系3.氯及其化合物的转化关系4.硫及其化合物的转化关系5.氮及其化合物的转化关系【要点梳理】要点一、碳、硅及化合物1.碳碳在常温下非常稳定,但在高温条件下活动性增强,主要表现为还原性。
(1)与非金属单质反应2C+O22CO C+O2CO2(2)与某些氧化物反应C+CO22CO C+H2O(g)CO+H22C+SiO2Si+2CO↑C+2CuO2Cu+CO2↑(3)与氧化性酸反应C+2H2SO4(浓)CO2↑+2SO2↑+2H2OC+4HNO3(浓)CO2↑+4NO2↑+2H2O2.碳的氧化物(1)CO:主要表现还原性2CO+O22CO23CO+Fe2O32Fe+3CO2CO+H2O CO2+H2(2)CO2①弱氧化性:CO2+C2COCO2+2Mg C+2MgO②酸性氧化物的三点通性CO2+H2O H2CO3CO2+Ca(OH)2=CaCO3↓+H2OCO2+CaO CaCO3其它性质:CO2+H2O+CaCO3=Ca(HCO3)22CO2+Ca(OH)2=Ca(HCO3)2Na2SiO3 +CO2 +H2O ==H2SiO3↓+ Na2CO3 (CO2少量)Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO2Na2O2+2CO2=2Na2CO3+O23.碳酸盐(1)溶解性正盐中只有碱金属的碳酸盐和铵盐溶于水,所有酸式盐均溶于水。
一般酸式盐比相应正盐易溶,但碱金属的碳酸氢盐比碳酸盐的溶解度小。
(2)热稳定性一般规律:可溶性碳酸正盐>不溶性碳酸正盐>酸式碳酸盐。
如:Na2CO3>CaCO3>NaHCO3(3)正盐与酸式盐的相互转化4.硅单质地壳中含量最高的两种元素分别是氧和硅。

实用精品文献资料分享高一化学必修一?非金属及其化合物?知识点汇总2.高一化学必修一?非金属及其化合物?知识点汇总第一节无机非金属材料的主角―硅3.硅及硅的化合物的相互关系(涉及到的方程式要求每位同学都要4.过关)5.一、硅单质6.物理性质7.单质硅有游离态和化合态两种。
熔点高、硬度大、是良好的半导8.体材料,可用来制造集成电路、晶体管、硅整流器、半导体器件,太阳能电池。
硅的原子结构示意图为9._____。
10.化学性质11.硅在常温下化学性质稳定。
一定条件下,可发生化学反响。
写出12.以下变化的化学方程式:13.①硅和非金属反响:和O2:14.②和NaOH溶液反响:。
15.③和氢氟酸反响:。
16.二、二氧化硅和硅酸盐17.二氧化硅18.①硅是一种亲氧元素,在自然界中总是与氧相互化合,所以在氧化气氛包围的地球上,硅主要以熔点很高的是SiO2和硅酸盐形式存在。
SiO2是硅最重要的化合物。
二氧化硅具有空间网状结构。
密度和硬度都大。
19.③化学性质。
写出以下变化的化学方程式。
20. a.和强碱反响(NaOH):;21.玻璃的组成成分中含有二氧化硅,故存放碱性试剂的玻璃试剂瓶不能用玻璃塞。
22. b.和碱性氧化物反响:;23. c.和HF酸反响:。
玻璃的组成成分中含有二氧化硅,故氢氟酸不24.能存放在玻璃试剂瓶中。
氢氟酸可用塑料瓶盛装。
25.硅酸和硅酸盐实用精品文献资料分享①H2SiO3酸性比碳酸弱,溶解度小。
可由硅酸盐和强酸反响来制备。
如:向Na2SiO3溶液中滴加HCl,可发生反响:得到硅酸。
硅酸凝胶经枯燥脱水形成硅酸干胶,称为“硅胶〞。
它是优良的吸附剂,也可作催化剂的载体。
②碳化硅俗称金刚砂,具有金刚石结构,有很大的硬度。
工业上金刚砂的制备原理(用化学方程式表示)为:SiO2+3CSiC+2CO。
在这个反响中,氧化剂是__________,复原剂是__________,氧化剂与复原剂的物质的量之比为__________。

非金属及其化合物重难点归纳一、硅二、氯1、性质2、实验室制取氯气:制取原理:MnO2 + 4HCl(浓) 加热MnCl2 + Cl2↑+2H2O 气体成分:Cl2 (HCl、H2O)3、漂白粉:①制:2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O②有效成分:Ca(ClO)2 成分:CaCl2 和 Ca(ClO)2③漂白原理:Ca(ClO)2 + CO2 + H2O = CaCO3↓ + 2HClO (在溶液中)漂白慢Ca(ClO)2 + 2HCl = CaCl2 + 2HClO 漂白快④久置失效发生的反应:Ca(ClO)2 + CO2 + H2O = CaO3 + 2HClO2HClO 2HCl + O2↑4、Br2 、I2在不同溶剂中的颜色三、氮1、氮的氧化物NO:无色气体、有毒(同CO)、难溶与水NO2:红棕色气体、有毒、与水反应反应:2NO + O2 = 2NO2 3NO2 + 2H2O = 2HNO3 + NO 2、硝酸意比溶于水化学性质的通性强氧化性与金属氧化物3FeO + 10HNO3 = 3Fe(NO3)3 + NO↑+ 5H2O与金属3Cu + 8HNO3(稀) = 3Cu(NO3)2 +2NO↑+ 4H2OCu + 4HNO3(浓) = Cu(NO3)2 +2NO2↑+ 2H2O与非金属C + 4HNO3(浓)加热CO2↑+ 4NO2↑+2H2O不稳定性4HNO3光照或加热4NO2↑ + O2↑+ H2O3、氨()物理性质无色气体、有刺激性气味、密度小于空气、1:700溶于水化学性质与H2O NH3 + H2O NH3·H2O NH4++ OH- 与酸NH3 + HCl = NH4Cl氨的催化氧化4NH3 + 5O2催化剂加热4NO + 6H2O实验室制取原理NH4+ + OH- 加热 NH3↑+ H2O2NH4Cl +Ca(OH )2 加热2NH3↑+ CaCl2 + 2H2O4、实验室制取干燥的方法制取原理: 2NH4Cl +Ca(OH )2 加热2NH3↑+ CaCl2 + 2H2O气体成分: NH3( H2O )除水用试剂:碱石灰(不用浓H2SO4 、 CaCl2原因是:2NH3 + H2SO4 = (NH4)2SO4;CaCl2 + 8NH3 = CaCl2·8NH3 )5、受热易分解:NH3·H2O加热NH3↑+ H2O NH4HCO3加热NH3↑+ CO2↑+ H2O四、硫1、的性质2、3、浓4、C与浓反应产物的鉴别:5、用原理制取的中含有Hcl和,如何除去:五、知识点比较总结1、二氧化硅和二氧化碳的比较2、液氯、新制氯水和久置氯水的比较3、浓硫酸和浓硝酸的比较4、氨气、氨水与铵盐的性质【素材积累】1、2019年,文野31岁那年,买房后第二年,完成了人生中最重要的一次转变。

非金属及其化合物化学方程式汇总1.硅的化学性质:Si + O2 SiO2Si + 2NaOH + H2O === Na2SiO3 + 2 H2↑Si + 4HF === SiF4↑+ 2 H2↑2.二氧化硅的化学性质:①酸性氧化物的通性:SiO2+ 2NaOH == Na2SiO3+ H2OSiO2+ CaO △CaSiO3②弱氧化性:SiO2+2C 高温2CO+Si③与酸(只与氢氟酸)反应——腐蚀玻璃4HF+SiO2==SiF4↑+2H2O3.氯气的化学性质:2Fe+3Cl2点燃2FeCl3Cu+Cl2点燃CuCl2注意:Cl2的氧化性强,和可变价金属反应生成高价的金属氯化物!2Na+ Cl2点燃2NaClH2+ Cl2点燃2HClCl2+ H2O ==== HCl + HClO2HClO ==== 2HCl + O2 ↑Cl2 + 2NaOH ===== NaCl + NaClO + H2OCl2 + 2Ca(OH)2 ===== CaCl2 + Ca(ClO)2 + H2O Ca(ClO)2+2HCl==CaCl2+2HClO注意:①Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO②2HClO==2HCl +O2↑③Ca(ClO)2+2HCl==CaCl2+2HClO①漂白原理;①②在空气中变质;③工业上应用4.卤素的性质:①与氢气反应:H2+F2==2HFH2+ Cl2点燃2HClH2+ Br2加热2H BrH2+ I2加热2HI②与水反应:2H2O+2F2==4HF+O2Cl2+ H2O HCl + HClOBr2+ H2O HBr+ HBrO③与碱反应:Cl2 + 2NaOH ===== NaCl + NaClO + H2O Br2+ 2NaOH ===== NaBr + NaBrO + H2O ④置换反应:Cl2 + 2NaBr===== 2NaCl + Br2Cl2 + 2NaI===== 2NaCl + I2Br2 + 2NaI===== 2NaBr + I25.硫的化学性质:①还原性:S+O2点燃SO2②氧化性:S+H2△H2S2Cu+S △Cu2SFe+S △FeS注意:S的氧化性较弱,和可变价金属反应生成低价的金属硫化物!2Na+ S == 2Na2S③3S+6NaOH △2Na2S+Na2SO3+3H2O④硫的特性:S+2Hg==HgS(用硫粉除去洒落的Hg珠)2Ag+S==Ag2S6.二氧化硫的化学性质:①酸性氧化物的通性:SO2+H2O H2SO3SO2+ 2NaOH == Na2SO3+ H2OSO2+ NaOH == NaHSO3SO2+ CaO == CaSO3②还原性:SO2+2H2O+Cl2== H2SO4+2HClSO2+2H2O+Br2== H2SO4+2HBrSO2+2H2O+X2== H2SO4+2HX (X= Cl、Br、I)③氧化性:SO2+2H2S== 3S↓+2H2O7.硫酸的化学性质:①酸的通性:H2SO4+Zn== ZnSO4+ H2↑CuO +H2SO4== CuSO4 + H2O2NaOH +H2SO4==Na2SO4 +H2ONa2CO3 +H2SO4==Na2SO4 +H2O +CO2↑②浓硫酸具有强氧化性:S+2H2SO4(浓)△↑+2H2OC+2H2SO4(浓)△CO2↑+2SO2↑+2H2O(浓H2SO4与非金属反应时只作氧化剂)Cu+2H2SO4(浓)△CuSO4+SO2↑+2H2O(浓H2SO4与金属反应既表现出氧化剂有表现出酸性)③吸水性:④脱水性:8. 硝酸的化学性质:①酸的通性:CuO +2HNO3== Cu(NO3)2 + H2ONaOH +HNO3==NaNO3 +H2ONa2CO3 + 2HNO3==2NaNO3 +H2O +CO2↑②浓硝酸具有强氧化性:S+6HNO3(浓)△H2SO4+6NO2↑+2H2OC+4HNO3(浓)△CO2↑+4NO2↑+2H2O(浓H2SO4与非金属反应时只作氧化剂)Cu+2H2SO4(浓)△CuSO4+SO2↑+2H2OCu+4HNO3(浓)△Cu(NO3)2+2NO2↑+2H2O(浓HNO3与金属反应既作氧化剂又作酸)9. H2S、HI通入浓硫酸中H2S+H2SO4(浓)==SO2↑+S↓+2H2O2H2S+H2SO4(浓)==3S↓+4H2O2HI+H2SO4(浓)==SO2↑+I2+H2O 10.工业上用接触法制硫酸:4FeS2+11O2催化剂△2Fe2O3+8SO22SO2+O2催化剂高温高压2SO3SO3+H2O==H2SO4 11.工业上生产HNO3:4NH3+5O2催化剂△4NO+6H2O2NO+O2==2NO23NO2+H2O==2HNO3+NO12.工业上生产晶体硅/玻璃:①晶体硅:SiO2+2C==2CO+Si(粗硅,后两步用于提纯)Si+2Cl2==SiCl4(g)SiCl4+2H2==Si+4HCl②玻璃:Na2CO3+SiO2高温Na2SiO3+CO2↑CaCO3+SiO2高温CaSiO3+CO2↑(CaSiO3的热稳定性比CaCO3强)13.实验室制NH3、Cl2:①制取NH3:2NH4Cl(固)+Ca(OH)2(固)△CaCl2+2NH3↑+2H2O(此方程式不能写离子反应方程式。

最新高中化学非金属及其化合物总复习知识点考点总结范文归纳非金属及其化合物1.(09年山东理综·10)下列关于氯的说法正确的是A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂B.若3517Cl、3717若Cl为不同的核素,有不同的化学性质学科C.实验室制备Cl2,可用排放和食盐水集气法收集D.1.12LCl2含有1.7NA个质子(NA表示阿伏伽德罗常数)答案:C2.(09年宁夏理综·7)将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为A.NO2B.N2O2C.N2OD.N2O4答案:A3.(09年广东理基·22)下列关于硅单质及其化合物的说法正确的是①硅是构成一些岩石和矿物的基本元素②水泥、玻璃、水晶饰物都是硅酸盐制品③高纯度的硅单质广泛用于制作光导纤维④陶瓷是人类应用很早的硅酸盐材料A.①②B.②③C.①④D.③④答案:C4.(08年海南化学·13)下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。
化合物B在常温常压下为气体,B和C的相对分子质量之比为4︰5,化合物D是重要的工业原料(1)写出A在加热条件下与H2反应的化学方程式_______________________________。
(2)写出E与A的氢化物反应生成A的化学方程式___________________________。
(3)写出一个由D生成B的化学方程式____________________________________。
(4)将5mL0.10mol·L—1的E溶液与10mL0.10mol·L—1的NaOH溶液混合。
①写出反应的离子方程式__________________________________________;②反应后溶液的pH____7(填“大于”、“小于”或“等于”),理由是;③加热反应后的溶液,其pH_____(填“增大”、“不变”或“减小”),理由是_______________。

【最新】高一化学必修一第四章非金属及其化合物(硅、氯)知识点总结高一化学必修一第四章非金属及其化合物(硅.氯)知识点总结非金属及其化合物〔一〕一.硅Si1.硅单质存在结构:化合态〔自然界〕,在地壳中的含量第二〔仅次于氧〕物理性质:灰黑色,金属光泽,硬度大,有脆性,熔沸点高的固体,是良好的半导体材料〔硅芯片.光电池〕性质化学性质〔常温下化学性质稳定〕以下关于硅的说法不正确的选项是〔〕A.硅是非金属元素,它的单质是灰黑色有金属光泽的固体B.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料C.硅的化学性质不活泼,常温下不与任何物质反响D.加热到一定温度时硅能与H2.O2等非金属反响答案:C2.二氧化硅其化学性质很不活泼,氢氟酸HF是唯一能与之反响的酸!!!天然二氧化硅的存在形式:结晶形和无定形应用:石英光导纤维,石英坩埚,玛瑙饰品类别晶体结构熔沸点与水反响方程式与酸反响方程式与烧碱反响方程式与CaO反响方程式存在状态二氧化硅酸性氧化物原子晶体〔四面体网状结构〕高不反响SiO2+4HF==SiF4↑+2H2OSiO2+2NaOH==Na2SiO3+H2OSiO2+CaO高温[来源:学.科.网Z._._.K]CaSiO3水晶.玛瑙.石英.硅石.沙子1.以下物质的主要成分不是SiO2的是〔〕A.石英B.水晶C.金刚砂D.玛瑙答案:C2.以下说法正确的选项是〔〕A.SiO2溶于水显酸性B.CO2通入水玻璃可得硅酸C.SiO2是酸性氧化物,它不溶于任何酸D.SiO2晶体中不存在单个SiO2分子答案:BD3.硅酸1.特点:溶解度很小,酸性很弱〔比碳酸弱〕2.什么是〝硅胶〞?硅胶的用途:多孔.吸水能力强,故可做枯燥剂;也做催化剂的载体1.将足量的CO2通入以下溶液中,能产生沉淀的是〔〕A.硅酸钠溶液B.石灰水C.氯化钡溶液D.氯化钙溶液答案:A2.碳化钛〔TiC〕.碳化硼〔B4C3〕.氮化硅〔Si3N4〕等非氧化物陶瓷是新型无机非金属材料,合成这些物质需在高温条件下进行,在合成它们的过程中必须注意〔〕答案:BA.通入足量氧气B.防止与氧气接触C.通入少量氯气D.通入少量氧气3.以下物质属于酸性氧化物但不溶于水的是A.二氧化碳B.二氧化硅C.二氧化硫D.氧化铁答案:B4.以下说法正确的选项是〔〕A.硅是良好的半导体材料,能与盐酸或氢氧化钠溶液反响B.二氧化硅不导电,能与盐酸或氢氧化钠溶液反响C.硅酸具有多孔性结构,可用作吸附剂或催化剂的载体D.二氧化硅是酸性氧化物,能与氢氟酸反响,也能与氢氧化钠溶液反响答案:D4.硅酸盐1.大多硅酸盐不溶于水,化学性质稳定2.硅酸钠Na2SiO3性质:可溶于水,其水溶液俗称水玻璃用途:制备硅胶和木材防火剂的原料Na2SiO3+H2O+CO2=Na2CO3+H2SiO3或Na2SiO3+2HCl=H2SiO3+2NaCl产品:陶瓷.玻璃.水泥小练:写出以SiO2为原料制备H2SiO3的化学方程式答案:SiO2+2NaOH====Na2SiO3+H2ONa2SiO3+2HCl====2NaCl+H2SiO3↓或Na2SiO3+CO2+H2O====Na2CO3+H2SiO3↓Na2SiO3+2CO2+2H2O====2NaHCO3+H2SiO3↓二.氯Cl1.氯气很强的氧化性!!!有毒气体!!!重要性质与金属钠反响方程式与金属铁反响方程式与金属铜反响方程式与氢气反响方程式与水反响方程式制漂白液反响方程式制漂白粉反响方程式实验室制法氯离子的检验试剂以及反响方程式2Na+Cl22Fe+3Cl2Cu+Cl2点燃2NaCl2FeCl3CuCl22HCl点燃点燃H2+Cl22HCl;H2+Cl2H2O+Cl2==HCl+HClOCl2+2NaOH==NaCl+NaClO+H2O2Cl2+2Ca(O H)2==CaCl2+Ca(ClO)2+2H2OMnO2+4HCl〔浓〕△MnCl2+Cl2↑+2H2OAgN O3溶液:Ag ++Cl—==AgCl1.以下气体,被当作化学武器首次使用于战争的是〔〕A.氯气 B.一氧化碳C.芥子气D.沙林答案:A—2.检验Na2SO4溶液中含有Cl的方法是〔〕A.先加BaCl2溶液,再加AgNO3溶液B.先加AgNO3溶液,再加稀HNO3C.先加足量的Ba〔NO3〕2溶液,再加AgNO3溶液D.先加足量Ba〔OH〕2溶液,再加AgNO3溶液答案:C3.以下气体,既有颜色又有毒性的是〔〕A.N2B.COC.Cl2D.CO2答案:C4.以下说法正确的选项是〔〕A.用鼻子对着盛有氯气的瓶口,就可以嗅到氯气的气味[来源:Z#__#]B.用排水集气法便可以收集到纯洁的氯气C.氯气有漂白性D.自来水常用氯气来杀菌.消毒答案:D5.欲除去Cl2中的少量HCl气体,可选用〔〕A.NaOH溶液B.AgNO3溶液[来源:学科网Z__K]C.饱和食盐水D.石灰水答案:C2.氯水〔混合物〕〔1〕溶液中含H+:具有酸性〔2〕溶液中含Cl2.HClO:具有强氧化性(3)溶液中含Cl—:具有Cl—的性质〔4〕溶液中含HClO:具有漂白性分类颜色成分性质液氯纯洁物黄绿色Cl2氧化性新制氯水混合物黄绿色Cl2.H2O.HClO.H +.Cl—.ClO—.极少量的为OH—氧化性.酸性.漂白性久置氯水混合物[来源:Z__]无色H+.Cl—.H2O.极少量的OH—稀盐酸酸性氯水在保存是要密封,避光保存.因为氯水不稳定,见光易分解.3.次氯酸〔1〕弱酸性:比碳酸弱〔2〕见光容易分解:2HClO==2HCl+O2↑(3)强氧化性:杀菌消毒,漂白漂白性的思考:起漂白作用的物质有哪些?枯燥氯气能否漂白物质???1.氯气可用来杀菌消毒,又可作漂白剂,其中起作用的是〔〕A.Cl2B.HClOC.HCl 答案:B2.以下物质不能作漂白剂的是A.SO2B.Ca(ClO)2C.NaClOD.H2SO4(浓)答案:D3.以下物质中,既含有氯分子,又含有氯离子的是〔〕A.氯化钠溶液 B.新制氯水C.漂白粉D.液氯答案:B4.以下物质能使枯燥的有色布条褪色的是〔〕A.氯水B.液氯C.氯气D.次氯酸答案:AD5.以下表达能证明次氯酸是一种弱酸的是〔〕A.次氯酸不稳定,易分解B.次氯酸是一种强氧化剂C.次氯酸钙能与碳酸作用生成碳酸钙和次氯酸D.次氯酸能使染料和有机色质褪色答案:C6.有一包白色固体,它可能是KCl.K2CO3.KNO3中的一种或几种,进行以下实验:①溶于水,得无色溶液;[来源:学科网]②在所得溶液中滴入AgNO3溶液,生成白色沉淀〔说明:Ag2CO3为白色沉淀〕;③再滴加稀硝酸,沉淀量减少但不完全消失,同时有气泡生成.根据上述现象判断: 〔1〕白色固体一定含有的成分是_______________,可能含有的成分是_______________.〔2〕请写出上述实验中有关反响的离子方程式______________________________________.思路解析:由②产生白色沉淀知,可能含有K2CO3和KCl中的一种或两种;由③沉淀量减少且有气泡生成知,一定含有K2CO3;又由沉淀不完全消失可知,一定含有KCl.答案:〔1〕KCl和K2CO3KNO3 2〔2〕Ag++Cl-====AgCl↓,2Ag++CO3====Ag2CO3↓,D.O2Ag2CO3+2H+====2Ag++H2O+CO2↑扩展阅读:高中化学必修一第四章__非金属及其化合物知识点总结第四章非金属及其化合物【内容结构】氧化性:与金属及其他非金属反响Cl2与水.碱反响:消毒剂.漂白剂(漂白液与漂白粉)单S可燃性:生成SO2质N2稳定性:空气的主要成分Si亲氧性:以SiO2及硅酸盐的形式存在半导体性:信息技术与光电技术材料非金属SO与水反响:酸雨2.NO2及与环境的关系:大气污染与防治氧化物其化与强碱反响:制NaSiO2SiO32合硅酸盐材料的根底物与水反响:制氨水氢化物与酸反响:制铵盐化NH3合液化:制冷剂物H2SO4.HNO3.HClO氧化性含氧酸H不溶性2SiO3胶体性质:制硅胶NaClO.Ca(ClO)2消毒剂.漂白粉含氧酸盐Na2SiO3黏胶剂(水玻璃).防火剂复杂硅酸盐陶瓷.玻璃.水泥【知识要点】一.硅及其化合物的相互转化SiF4SiSiO2H2SiO3Na2SiO3二.氯及其化合物的相互转化CuCl2NaClNaClOHClCl2HClOFeCl2FeCl3Ca(ClO)2三.硫及其化合物的相互转化 H2SSSO2SO3H2SO4FeSNa2SNa2SO3CaSO3BaSO4四.氮及其化合物的相互转化NH4HCO3NH3H2ONH3N2NONO2HNO3NH4ClNaNO3二.本章知识结构梳理(一)硅及其化合物1.二氧化硅和二氧化碳比拟类别晶体结构熔沸点与水反响方程式与酸反响方程式与烧碱反响方程式与CaO反响方程式存在状态高不反响SiO2+4HF==SiF4↑+2H2OSiO2+2NaOH==Na2SiO3+H2O高温二氧化硅酸性氧化物原子晶体二氧化碳_酸性氧化物分子晶体低CO2+H2OH2CO3不反响少:2NaOH+CO2==Na2CO3+H2O过:NaOH+CO2==NaHCO3CaO+CO2==CaCO3人和动物排放SiO2+CaOCaSiO3水晶.玛瑙.石英.硅石.沙子2.硅以及硅的化合物的用途物质硅单质SiO2硅酸钠SiC用途半导体材料.光电池〔计算器.人造卫星.登月车.探测器〕饰物.仪器.光导纤维.玻璃矿物胶砂纸.砂轮的磨料(二)氯1.液氯.新制的氯水和久置的氯水比拟分类颜色液氯纯洁物黄绿色新制氯水混合物黄绿色Cl2.H2O.HClO.H +.Cl—.ClO—.极少量的为OH—氧化性.酸性.漂白性久置氯水混合物无色H +.Cl—.H2O.极少量的OH—稀盐酸酸性成分Cl2性质氧化性2.氯气的性质与金属钠反响方程式与金属铁反响方程式2Na+Cl2点燃2NaCl2FeCl32Fe+3Cl2点燃与金属铜反响方程式与氢气反响方程式与水反响方程式制漂白液反响方程式制漂白粉反响方程式实验室制法氯离子的检验试剂以及反响方程式H2+Cl2Cu+Cl2点燃CuCl22HCl2HCl;H2+Cl2H2O+Cl2==HCl+HClOCl2+2NaOH==NaCl+NaClO+H2O2Cl2+2C a(OH)2==CaCl2+Ca(ClO)2+2H2OMnO2+4HCl〔浓〕△MnCl2+Cl2↑+2H2OAgNO3溶液Ag++Cl—==AgCl(三)硫.氮1.二氧化硫的性质物理性质颜色状态黄绿色密度比空气___大___毒性有毒SO2+H2OH2SO3SO2+2NaOH==Na2SO3+H2O与烧碱反响方程式Na2SO3+SO2+H2O==2NaHSO3SO2+NaOH==NaHSO3化学性质漂白性复原性氧化性漂白原理:由于它能跟某些有色物质生成:无色物质曾学过的具有漂白性的物质与氧气反响方程式与氯水反响方程式吸附漂白:活性炭氧化漂白:HClO.O3.Na2O22SO2+O2===2SO3SO2+Cl2+2H2O==H2SO4+2HCl与水反响方程式酸性与硫化氢反响方程式SO2+2H2S==3S↓+2H2O2.浓硫酸和浓硝酸的性质相同点与Cu浓硫酸Cu+2H2SO4(浓)△浓硝酸CuSO4+Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O反响SO2↑+2H2O与木炭反响与铁铝反响异同点C+2H2SO4(浓)△CO2↑C+4HNO3(浓)△CO2↑+4NO2↑+2H2O+2SO2↑+2H2O发生钝化现象,所以可以用铁制或铝制容器来存放冷的浓硫酸和浓硝酸①吸水性枯燥剂②脱水性蔗糖变黑王水:浓硝酸和浓盐酸〔__1__:3___〕3.氨气.氨水与铵盐的性质氨气颜色状态的物无色有刺理性激性气味质的气体NH3+H2O密度比空气__小___水溶性易溶〔1:_700_〕可以形成喷泉,水溶液呈_碱_性.氨气与水反响的化方程式学性与盐酸反质应方程式实验室制法氨水NH3H2ONH4++OH—NH3+HCl==NH4Cl△Ca(OH)2+2NH4ClCaCl2+2NH3↑+2H2ONNH3.成分NH3H2O.H2O.NH4+.OH—.极少量的H+铵盐物理性质:铵盐都是_无色_色晶体,____能_____溶于水化学性质氯化铵分解反响方程式碳酸氢铵分解反响方程式NH4Cl△NH3+HClNH4HCO3△NH3↑+H2O+CO2↑高中化学必修一第四章非金属及其化合物二氧化硅1结构:二氧化硅晶体是由氧原子和硅原子构成的,在二氧化硅晶体中无二氧化硅晶体.在晶体中每个硅原子与四个氧原子结合,每个氧原子与两个硅原子结合,向空间网状结构,即二氧化硅晶体由硅原子和氧原子按1:2的比例组成的空间网状结构晶体2物理性质:二氧化硅具有硬度大.熔点高.不溶于水.不导电等性质,纯洁的二氧化硅晶体无色透明3化学性质:①二氧化硅是酸性氧化物,能与碱和碱性氧化物反响,如:②弱氧化性:③特性二氧化硅是酸性氧化物,却能与氢氟酸发生反响: 4用途:制备高性能通讯材料光导纤维;制备石英玻璃.石英钟;制造电子工业中的重要部件.光学仪器.精密仪器.轴承.耐磨器皿;装饰品硅酸:硅酸是一种弱酸,比碳酸还弱,切难溶于水.通过复分解反响制的硅酸形成胶体溶液,进一步形成凝胶,硅酸凝胶经枯燥脱水可形成常用作枯燥剂的〝硅胶〞硅酸的制备:硅酸盐1硅酸盐是由硅.氧和金属组成的化合物的总称.硅酸盐是一类结构复杂的物质,一般都不溶于水.化学性质稳定,是地壳岩石的主要成分2最简单最常用的硅酸盐是硅酸钠,其水溶液熟称水玻璃,其化学性质稳定,不能燃烧,不易被腐蚀,热稳定性强,有粘性.可用作建筑材料.纸张粘合剂,木材织物的防腐剂.防火剂3硅酸盐由于组成比拟复杂,通常用二氧化硅和金属氧化物的形式表示其组成.如:Na2SiO3→Na2O.SiO2氯气氯气通常状况下呈黄绿色,是一种具有强烈刺激性气味的有毒气体,化学性质活泼,具有较强的氧化性1氯气与金属反响〔除金.铂外〕①产生黄色的火焰和大量白烟②产生大量棕色气体③产生大量棕色的烟2氯气与氢气反响方程式:氢气在氯气中燃烧,发出苍白火焰.氢气燃烧结束后,抽去盖在集气瓶口处的毛玻璃片,及其瓶口处有白雾3氯气和水反响氯气的水溶液叫氯水.氯气与水反响生成盐酸和次氯酸,氯气既是氧化剂又是复原剂方程式:①氯水的成分:三分子〔水分子,氯气.次氯酸分子〕四离子〔氢离子.氯离子.次氯酸根离子.少量氢氧根离子〕②颜色:新制的饱和的氯水呈浅黄绿色③因含有盐酸和次氯酸而成酸性,但主要是由于盐酸④沉淀性:与银离子反响生成沉淀⑤强氧化性因含有次氯酸和氯气而呈强氧化性,但氧化性主要由次氯酸决定,氯气的强氧化性决定它具有漂白性⑥不稳定性:由于次氯酸:4氯气与碱反响:方程式:①吸收多余的氯气用氢氧化钠②漂白粉的有效成分是次氯酸钙5氯气与某些复原性物质的反响氯气具有强氧化性,可与二氧化硫,亚硫酸根,硫离子.溴离子.碘离子.亚铁离子等具有复原性的微粒发生氧化复原反响6氯气的用途:自来水杀菌;制造盐酸;制造漂白剂;合成塑料.橡胶.人造纤维;农药.燃料.药品.氯气的实验室制法方程式:制得的气体含有盐酸和水,因此分别通过饱和食盐水.浓硫酸〔氯化钙〕等进行除杂.气体用向上排空气法或排饱和食盐水法收集.尾气用氢氧化钠吸收.卤素1卤素包括氟氯溴碘2卤素均具有强氧化性,并且氟>氯>溴>碘>爱3化学性质:①与金属反响:卤素都能与金属反响生成金属卤化物②都与氢气反响生成对应的酸③与水反响:④与碱反响:二氧化硫:1物理性质:无色.有刺激性气味的有毒气体,密度比空气大,易于液化2化学性质:①与水反响生成显酸性的物质,具有漂白作用,但漂白后新物质不稳定,受热易恢复原色②常见的能被二氧化硫漂白的物质有:品红溶液.白纸浆.毛.丝.草帽辫.但二氧化硫不能漂白酸碱指示剂③二氧化硫的氧化性和复原性与氧气反响:与氯气反响:与溴反响:与碘反响:与硫化氢反响:亚硫酸根与氯气反响:亚硫酸与氯气反响:亚硫酸根与氧气反响:亚硫酸与氧气反响:氮的重要氧化物NO和NO21一氧化氮:无色无味气体,不溶于水,易被氧气氧化,方程式:(反响现象:无色气体变成红棕色有刺激性气味的气体),有毒,能与血红蛋白结合2二氧化氮:红棕色气体,有刺激性气味,有毒,刺激呼吸器官导致呼吸道.肺部病变,浓度大时引起死亡化学性质:与水反响方程式:雷雨发庄稼的化学原理:氨1物理性质:无色有刺激性气味气体,密度较小,极易溶于水,易液化2化学性质:①与水反响:②与氯化氢反响:3氨的实验室制备方程式:收集方法:向下排空气法尾气处理:用稀硫酸吸收验满方法:用湿润的红色石蕊试纸检验:试纸变蓝;用浓盐酸检验:产生大量白烟枯燥方法:碱石灰枯燥氨的用途:肥料.化工合成.制冷剂铵盐1物理性质:晶体,易溶于水2化学性质:①受热易分解:氯化铵分解:碳酸铵分解:碳酸氢铵分解:硝酸铵分解:②铵盐与碱反响:〔铵盐的特征反响〕硫酸铵与氢氧化钠反响:硝酸铵与氢氧化钠反响:硝酸1硝酸与金属铜反响铜与稀硝酸反响:铜与浓硝酸反响:硝酸是一种强氧化剂,几乎能与所有金属反响〔金.铂〕除外,但是与铝.铁在冷的浓硝酸中会发生钝化现象.浓度越大,氧化性越大.一旦沾在皮肤上,用小苏打水或肥皂水洗涤2硝酸与非金属反响硝酸与碳反响:硫酸1浓硫酸的物理性质纯洁的硫酸是无色粘稠油状液体,沸点较高,不易挥发,密度大于水,溶于水时放出大量的热2浓硫酸的三大特性:吸水性.脱水性.强氧化性①浓硫酸的吸水性:由于浓硫酸有吸水性常可以作为枯燥剂,但是浓硫酸不能枯燥碱性气体,氨,复原性气体,如:硫化氢.溴化氢.碘化氢②浓硫酸的脱水性:脱水性是化学变化③浓硫酸的氧化性:a浓硫酸具有很强的氧化性,可以把复原性很弱的银氧化,但遇到铝.铁发生钝化b在做氧化剂时一般会复原为二氧化硫浓硫酸与碳反响:。

非金属及其化合物的复习怀集县第一中学沈小莲【考纲要求】1.掌握常见的非金属元素(如:H、O、C、Si 、Cl、S、N、)单质、氢化物、氧化物、最高价氧化物对应水化物等重要性质,并进行比较。
2.从原子的核外电子排布,理解元素(单质、化合物)性质的相似性和递变性。
重点掌握典型非金属(如卤族元素)在周期表中的位置及与其性质的关系。
【知识梳理】这部分知识在高考题中更多演变为解决基本概念、基本理论、化学实验或化学计算题的基石,几乎出现在所有的高考题型中,如选择题中的离子共存、氧化还原反应等概念,离子反应方程式的书写和判断,药品的保存和仪器的洗涤,填空题的化工流程题,实验题,计算题等都是高考的热点。
1.同主族元素性质的比较。
(1)同主族元素原子结构的比较:(相同点和不同点)(2)同主族元素化学性质的比较:(从上向下)如:非金属性、氧化性、还原性、得电子能力、失电子能力、元素的主要化合价、元素最高价氧化物、最高价氧化物对应的水化物等。
2.同周期不同族元素非金属性比较:单质与氢气化合的能力、气态氢化物的稳定性、气态氢化物的还原性、最高价氧化物对应水化物的酸性、单质的氧化性、对应阴离子的还原能力等等。
3.各族元素的单质及其化合物知识网络【复习建议】一、运用理论,统领全局化学基本理论源于元素及其化合物知识,是从大量的元素及其化合物的知识中提炼出来的规律性的知识。
它对于元素及其化合物的学习具有很强的指导作用。
中学化学所学的基本理论有:结构理论、周期律理论、电离理论、平衡理论、氧化还原理论等。
在元素及其化合物的复习中,我们要注意将理论与元素化合物知识结合起来,利用理论指导学习,抓住问题的实质,掌握规律性的问题。
①“结构”指导复习结构决定性质。
在复习中要学会善于运用结构理论解决实际问题。
例如根据:原子半径大小原子决定原子得失决定元素的电子的能力化学性质最外层电子数多少我们可以解释为什么卤族元素的非金属性强于氧族元素,在通常情况下碳族元素的化学性质稳定这一问题。

专题:非金属元素及其化合物重要非金属元素及其化合物一、卤族元素(1).卤族元素物理性质比较:化学性质与Cl2相似,都具有典型的非金属性,都可以与金属作用生成金属卤化物,都可以与非金属反应,都可与水发生反应,都可以与强碱作用。
递变性:与金属、非金属反应时条件不同。
例如:卤素单质与H2的反应H2+F2═_______,H2+Cl2______,H2+I22HI,与H2化合时,无论从反应条件、反应的剧烈程度以及生成气态氢化物的稳定性(HF>HCl>HBr>HI),都说明卤素单质的递变性。
____。
和_____,其中______是有效成分。
漂白粉的漂白原理是:————————————————————检验氯气收集时是否集满______________________ 概述:从氟元素到碘元素,其单质颜色逐渐___,水溶性逐渐_____,熔沸点逐渐___和H2反应逐渐____,1mol单质和H2反应放出的热量逐渐_____,气态氢化物的热稳定性逐渐_____,氢化物酸性逐渐____2、碘1)、海洋植物中提取碘①从海洋植物中得到碘离子:将海带晒干,灼烧成灰,用水溶解浸泡,使I―进入水中,过滤,除灰渣。
蒸氯气通入碳酸氢钠溶液中:______________________(2)ClO-是一种弱酸的酸根离子,能发生水解反应:_____________,所以次氯酸钙溶液显碱性。
若遇到铁盐、铝盐易发生双水解:__________________________(3)HClO和ClO-都具有_______,无论酸性、碱性条件下都可以跟亚铁盐、碘化物、硫化物等发生氧化还原反应,但不能使品红溶液褪色。
如:硫酸亚铁溶液遇漂白粉:__________________漂白粉遇亚硫酸酸盐:__________________(4)HClO见光易分解:__________(5)次氯酸钙中的Ca2+、ClO-可以表现出一些综合性质。
1.【解析】氯酸钾与浓盐酸反应放出氯气,并且带出氯化氢气体,在①中看到黄绿色的氯气,氯气使②中的Br-变成橙色的溴水,与③中I-反应生成I2,使淀粉变蓝,NaOH溶液可以吸收氯气,棉球的颜色没有变化。

高中化学复习——非金属及其化合物知识点总结一、卤族元素1、包括:元素名称:元素符号:卤族元素最外层有个电子,位于元素周期表第族,气态氢化物的通式为;除氟元素外,其它元素的最高价氧化物的通式为,最高价氧化物对应的水化物的通式为。
2、卤族元素随着原子序数的递增,电子层数逐渐,原子半径,得电子的能力逐渐,非金属性,最高价氧化物对应的水化物酸性,气态氢化物的稳定性。
气态氢化物的水溶液酸性。
3、4、F2有性,它与H2相遇即爆炸,写出该反响的化学方程式,它与水反响的方程式为。
5、氯气的性质①Cl2密度空气,有气味,毒。
氯气的电子式为,是一种常见的剂。
②Cl2与H2在或条件下都可发生反响,写出其反响的化学方程式;③Cl2能在条件下,与钠、镁、铝、铁、铜等金属发生反响,写出铁在氯气中反响的化学方程式,该反响的实验现象为,把得到的色固体溶于水中,可配制成色的溶液;写出铜在氯气中反响的化学方程式,该反响的实验现象为,把得到的色固体溶于水中,可配制成色的溶液。
④氯气溶于水,且能和水反响生成两种酸:和,其中有漂白性,一旦漂白有色织物,颜色不能复现。
写出氯气与水反响的离子方程式,在该反响中,氯气起到了剂的作用。
假设有1mol氯气参与反响,有mol电子发生转移。
⑤氯气的水溶液叫做,包括的微粒有。
其中使氯水有酸性,使氯水有强氧化性。
⑥氯气与强碱溶液可发生反响,类似于氯气与水的反响,在反响中能生成两种盐。
写出氯气与NaOH溶液反响的离子方程式,该反响的产物中,是家庭常用的“84”消毒液的主要成分。
氯气与熟石灰反响可以用来制漂白粉,写出该反响的化学方程式,在产物中起到漂白作用的有效成分是。
⑦当把氯气通入FeCl2溶液中一段时间后,溶液颜色变化为,写出该反响的离子方程式;把氯气通入FeBr2溶液中,写出该反响的离子方程式。
在以上的两个反响中,氯气都作剂。
⑧工业上可以通过电解饱和食盐水的方法来制取氯气,该生产过程又叫做,写出该反响的化学方程式。


高中化学必修一非金属与其化合物知识点归纳(精华版)1. 常见的非金属元素及其特性氢(H)•最轻的元素;•在常温常压下为气体,不易液化和固化;•与氧等元素发生反应时,易形成水化合物。
卤素(F、Cl、Br、I)•在自由状态下为单质;•电负性较高,能轻易地从其他元素中夺去电子,形成阴离子;•与金属反应时,能形成离子化合物,如NaCl、KBr等。
硫(S)•在自由状态下为单质;•没有明显的金属或非金属特性;•可形成多种氧化物,如SO2、SO3等。
碳(C)•最重要的非金属元素之一;•有多种同素异形体,如石墨、金刚石等;•与氧和氢等元素反应时,可形成多种化合物,如CO、CO2、CH4等。
2. 常见的非金属化合物及其性质酸(包括无机酸和有机酸)•在水溶液中呈酸性;•可与碱反应,生成盐和水;•可与金属反应,发生置换反应,并释放氢气。
氯化物•在水溶液中呈碱性;•可与银盐反应,生成白色沉淀;•可与铁盐反应,生成深绿色或暗红色溶液。
硫酸盐•在水溶液中呈酸性;•可与钡盐反应,生成白色沉淀;•可与铵盐反应,释放氨气。
有机化合物•与水不易混溶;•可分为烷类、烯类、炔类等不同类型;•具有独特的化学性质,如燃烧、酸碱中和等。
3. 非金属的应用氧•常用于焊接、氧化、脱硫等工业领域;•用于呼吸机、氧气袋等生命救治领域。
氮•用于制造氨气、硝酸等工业产品;•用于控制食品腐败、保持新鲜等食品保存领域。
卤素•用于消毒、药品等领域;•用于电子产品等高科技领域。
碳•用于生产炭黑、活性炭等工业产品;•用于生产石墨电极等高科技领域。
4. 非金属与环境问题相关污染物•SO2:主要来源于燃煤、燃油等化石燃料的燃烧;•NOx:主要来源于汽车尾气、化石燃料的燃烧等;•CO2:主要来源于工业生产、能源消耗等。
影响•酸雨:由于SO2、NOx等气体在大气中与水蒸气反应而形成的酸性物质,对环境和人类健康产生负面影响;•温室效应:由于大量CO2等气体的排放,导致地球气温升高,进而产生如海平面上升等严重后果;•其他:如空气污染、水资源短缺等也与非金属元素和化合物有关。
《非金属及其化合物》全章复习与巩固【学习目标】1. 总结几种常见非金属(碳、硅、氯、硫、氮)及其化合物的主要性质,理解浓硫酸及硝酸的氧化性。
2. 掌握氯离子、铵根离子的检验方法。
3. 学会氨气、二氧化硫、二氧化碳的检验方法。
4. 掌握氯气、氨气的实验室制法。
【知识网络】1、碳及其化合物的转化关系2 •硅及其化合物的转化关系3 .氯及其化合物的转化关系OH ACO3+H2O 上c«co3CftO高温CaC】COCO66 »CuO.兰十Ca(OH)3+ HjO△• H+NaOHCi(OH)△, N^OHNaH°°3“ CO^H^O上f BCuC\tCaCO,CO.HQ■ HC 汁HC1ONMH •NaCUNaClO 6(QH打y心心go} —~~ i tF恥_»FeCt.+Br,4 .硫及其化合物的转化关系5. 氮及其化合物的转化关系【要点梳理】要点一、碳、硅及化合物1 .碳碳在常温下非常稳定,但在高温条件下活动性增强,主要表现为还原性。
(1) 与非金属单质反应_小点燃_ - C点燃—2C+Q _____ 2CO C+O 2 ________ CO(2)与某些氧化物反应C+CO 2CO C+H2C+SiQ2 汩Si+2COf2O(g)吉*日冋CO+HF&CljAgNO,NaOH IICI ------%芫全憊烽reb Ha^O) K^O|C+2CuQ 2Cu+CQf (3)与氧化性酸反应C+2H 2SQ(浓) _ CQ 1+2SQf+2H 2O C+4HNQ 浓)^- CQl+4NQf+2HQ 2 •碳的氧化物(1) C0 :主要表现还原性 am2CQ+Q2CQ 3CO+FeC3^CO+HO I — CQ+H 2 ② 酸性氧化物的三点通性CQ+HQ H 2CQ CQ+CaQH^CaCQ 阳Q硅是一种重要的非金属单质,用途非常广泛,作为良好的半导体材料,硅可用来制造集成电路、晶体管、 硅整流器、半导体器件。
高一化学非金属及其化合物知识点总结一、硅元素无机非金属材料中的主角,在地壳中含量26.3%,次于氧.是一种亲氧元素,以熔点很高的氧化物及硅酸盐形式存在于岩石、沙子和土壤中,占地壳质量90%以上.位于第3周期,第ⅣA族碳的下方.Si对比C最外层有4个电子,主要形成四价的化合物.二、二氧化硅(SiO2)天然存在的二氧化硅称为硅石,包括结晶形和无定形.石英是常见的结晶形二氧化硅,其中无色透明的就是水晶,具有彩色环带状或层状的是玛瑙.二氧化硅晶体为立体网状结构,基本单元是[SiO4],因此有良好的物理和化学性质被广泛应用.(玛瑙饰物,石英坩埚,光导纤维)物理:熔点高、硬度大、不溶于水、洁净的SiO2无色透光性好化学:化学稳定性好、除HF外一般不与其他酸反应,可以与强碱(NaOH)反应,是酸性氧化物,在一定的条件下能与碱性氧化物反应SiO2+4HF==SiF4↑+2H2OSiO2+CaO===(高温)CaSiO3SiO2+2NaOH==Na2SiO3+H2O不能用玻璃瓶装HF,装碱性溶液的试剂瓶应用木塞或胶塞.三、硅酸(H2SiO3)酸性很弱(弱于碳酸)溶解度很小,由于SiO2不溶于水,硅酸应用可溶性硅酸盐和其他酸性比硅酸强的酸反应制得.Na2SiO3+2HCl==H2SiO3↓+2NaCl硅胶多孔疏松,可作干燥剂,催化剂的载体.四、硅酸盐硅酸盐是由硅、氧、金属元素组成的化合物的总称,分布广,结构复杂化学性质稳定.一般不溶于水.(Na2SiO3、K2SiO3除外)最典型的代表是硅酸钠Na2SiO3:可溶,其水溶液称作水玻璃和泡花碱,可作肥皂填料、木材防火剂和黏胶剂.常用硅酸盐产品:玻璃、陶瓷、水泥五、硅单质与碳相似,有晶体和无定形两种.晶体硅结构类似于金刚石,有金属光泽的灰黑色固体,熔点高(1410℃),硬度大,较脆,常温下化学性质不活泼.是良好的半导体,应用:半导体晶体管及芯片、光电池、六、氯元素:位于第三周期第ⅦA族,原子结构:容易得到一个电子形成氯离子Cl-,为典型的非金属元素,在自然界中以化合态存在.七、氯气物理性质:黄绿色气体,有刺激性气味、可溶于水、加压和降温条件下可变为液态(液氯)和固态.制法:MnO2+4HCl(浓)MnCl2+2H2O+Cl2闻法:用手在瓶口轻轻扇动,使少量氯气进入鼻孔.化学性质:很活泼,有毒,有氧化性,能与大多数金属化合生成金属氯化物(盐).也能与非金属反应:2Na+Cl2===(点燃)2NaCl2Fe+3Cl2===(点燃)2FeCl3Cu+Cl2===(点燃)CuCl2Cl2+H2===(点燃)2HCl现象:发出苍白色火焰,生成大量白雾.燃烧不一定有氧气参加,物质并不是只有在氧气中才可以燃烧.燃烧的本质是剧烈的氧化还原反应,所有发光放热的剧烈化学反应都称为燃烧.Cl2的用途:①自来水杀菌消毒Cl2+H2O==HCl+HClO2HClO===(光照)2HCl+O2↑1体积的水溶解2体积的氯气形成的溶液为氯水,为浅黄绿色.其中次氯酸HClO有强氧化性和漂泊性,起主要的消毒漂白作用.次氯酸有弱酸性,不稳定,光照或加热分解,因此久置氯水会失效.②制漂白液、漂白粉和漂粉精制漂白液Cl2+2NaOH=NaCl+NaClO+H2O,其有效成分NaClO比HClO稳定多,可长期存放制漂白粉(有效氯35%)和漂粉精(充分反应有效氯70%)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O③与有机物反应,是重要的化学工业物质.④用于提纯Si、Ge、Ti等半导体和钛⑤有机化工:合成塑料、橡胶、人造纤维、农药、染料和药品八、氯离子的检验使用硝酸银溶液,并用稀硝酸排除干扰离子(CO32-、SO32-)HCl+AgNO3==AgCl↓+HNO3NaCl+AgNO3==AgCl↓+NaNO3Na2CO3+2AgNO3==Ag2CO?3↓+2NaNO3Ag2CO?3+2HNO3==2Ag NO3+CO2↑+H2OCl-+Ag+==AgCl↓九、二氧化硫制法(形成):硫黄或含硫的燃料燃烧得到(硫俗称硫磺,是黄色粉末)S+O2===(点燃)SO2物理性质:无色、刺激性气味、容易液化,易溶于水(1:40体积比)化学性质:有毒,溶于水与水反应生成亚硫酸H2SO3,形成的溶液酸性,有漂白作用,遇热会变回原来颜色.这是因为H2SO3不稳定,会分解回水和SO2SO2+H2OH2SO3因此这个化合和分解的过程可以同时进行,为可逆反应.可逆反应——在同一条件下,既可以往正反应方向发生,又可以向逆反应方向发生的化学反应称作可逆反应,用可逆箭头符号连接.十、一氧化氮和二氧化氮一氧化氮在自然界形成条件为高温或放电:N2+O2(浓H2SO4)12C+11H2O放热2H2SO4(浓)+CCO2↑+2H2O+SO2↑还能氧化排在氢后面的金属,但不放出氢气.2H2SO4(浓)+CuCuSO4+2H2O+SO2↑稀硫酸:与活泼金属反应放出H2,使酸碱指示剂紫色石蕊变红,与某些盐反应,与碱性氧化物反应,与碱中和十一、硝酸物理性质:无色液体,易挥发,沸点较低,密度比水大.化学性质:具有一般酸的通性,浓硝酸和稀硝酸都是强氧化剂.还能氧化排在氢后面的金属,但不放出氢气.4HNO3(浓)+Cu==Cu(NO3)2+2NO2↑+4H2O8HNO3(稀)+3Cu3Cu(NO3)2+2NO↑+4H2O反应条件不同,硝酸被还原得到的产物不同,可以有以下产物:N(+4)O2,HN(+3)O2,N(+2)O,N(+1)2O,N(0)2,N(-3)H3△硫酸和硝酸:浓硫酸和浓硝酸都能钝化某些金属(如铁和铝)使表面生成一层致密的氧化保护膜,隔绝内层金属与酸,阻止反应进一步发生.因此,铁铝容器可以盛装冷的浓硫酸和浓硝酸.硝酸和硫酸都是重要的化工原料和实验室必备的重要试剂.可用于制化肥、农药、炸药、染料、盐类等.硫酸还用于精炼石油、金属加工前的酸洗及制取各种挥发性酸.十二、氨气及铵盐氨气的性质:无色气体,刺激性气味、密度小于空气、极易溶于水(且快)1:700体积比.溶于水发生以下反应使水溶液呈碱性:NH3+H2ONH3?H2ONH4++OH-可作红色喷泉实验.生成的一水合氨NH3?H2O是一种弱碱,很不稳定,会分解,受热更不稳定:NH3.H2O===(△)NH3↑+H2O浓氨水易挥发除氨气,有刺激难闻的气味.氨气能跟酸反应生成铵盐:NH3+HCl==NH4Cl(晶体)氨是重要的化工产品,氮肥工业、有机合成工业及制造硝酸、铵盐和纯碱都离不开它.氨气容易液化为液氨,液氨气化时吸收大量的热,因此还可以用作制冷剂.铵盐的性质:易溶于水(很多化肥都是铵盐),受热易分解,放出氨气:NH4ClNH3↑+HCl↑NH4HCO3NH3↑+H2O↑+CO2↑。
高中化学必修一非金属及其化合物知识点总结 HUA system office room 【HUA16H-TTMS2A-HUAS8Q8-HUAH1688】第四章 非金属及其化合物四、氮及其化合物的相互转化二、本章知识结构梳理(一)硅及其化合物1、二氧化硅和二氧化碳比较(漂白液与漂白粉)Na 2SiO 3)、32、硅以及硅的化合物的用途(二) 氯1、液氯、新制的氯水和久置的氯水比较稀盐酸性质氧化性氧化性、酸性、漂白性酸性2、氯气的性质与金属钠反应方程式2Na+Cl2点燃2NaCl与金属铁反应方程式2Fe+3Cl2点燃2FeCl3与金属铜反应方程式Cu+Cl2点燃CuCl2与氢气反应方程式H2+Cl22HCl;H2+Cl22HCl与水反应方程式H2O +Cl2==HCl+HClO制漂白液反应方程式Cl2+2NaOH==NaCl+NaClO+H2O制漂白粉反应方程式2Cl2 +2C a(O H)2==CaCl2+C a(C l O)2+2H2O实验室制法MnO2+4HCl(浓)△MnCl2+Cl2↑+2H2O(三) 硫、氮1、二氧化硫的性质2、浓硫酸和浓硝酸的性质3、氨气、氨水与铵盐的性质N高中化学必修一第四章非金属及其化合物二氧化硅1结构:二氧化硅晶体是由氧原子和硅原子构成的,在二氧化硅晶体中无二氧化硅晶体。
在晶体中每个硅原子与四个氧原子结合,每个氧原子与两个硅原子结合,向空间网状结构,即二氧化硅晶体由硅原子和氧原子按1:2的比例组成的空间网状结构晶体2物理性质:二氧化硅具有硬度大、熔点高、不溶于水、不导电等性质,纯净的二氧化硅晶体无色透明3化学性质:①二氧化硅是酸性氧化物,能与碱和碱性氧化物反应,如:②弱氧化性:③特性二氧化硅是酸性氧化物,却能与氢氟酸发生反应:4用途:制备高性能通讯材料光导纤维;制备石英玻璃、石英钟;制造电子工业中的重要部件、光学仪器、精密仪器、轴承、耐磨器皿;装饰品硅酸:硅酸是一种弱酸,比碳酸还弱,切难溶于水。
必修1第四章《非金属及其化合物》复习提纲本章知识结构第一部分硅A等级(识别“是什么”):知道:SiO2是硅最重要的化合物,占地壳质量约12%,其存在形态有结晶型和无定型两大类,统称硅石。
SiO2基本结构单元为四面体结构:高温 Si 与O 按1:2的比例组成立体网状结构。
B 等级(明确“是什么”): 二氧化硅和二氧化碳性质比较 物质二氧化硅 二氧化碳 熔沸点、硬度、状态很高、硬度大、固态 低、硬度小、气态化 学 性 质与水 不反应CO 2+H 2O=H 2CO 3 与氢氟酸 SiO 2+4HF=SiF 4↑+2H 2O 用HF 来腐蚀和雕刻玻璃。
不反应 与碱溶液 SiO 2+2NaOH=Na 2SiO 3+H 2O 盛装NaOH 溶液的试剂瓶用橡皮塞,而不用玻璃塞。
CO 2+2NaOH=Na 2CO 3+H 2O 与碱性氧化物SiO 2+CaO=CaSiO 3CO 2+CaO=CaCO 3异同点相同点都是酸性氧化物,都与碱或碱性氧化物反应。
不同点①CO 2与水反应生成H 2CO 3;SiO 2不与水反应; ②SiO 2溶于氢氟酸,CO 2不与氢氟酸反应;③SiO 2须在高温下与碱性氧化物反应,而CO 2可在常温常压下进行。
硅酸和碳酸的性质比较物质 硅酸 碳酸 化学式 H 2SiO 3 H 2CO 3 酸酐 SiO 2CO 2 制法硅酸胶体的制备:Na 2SiO 3+2HCl=2NaCl+H 2SiO 3↓CO 2+H 2O=H 2CO 3颜色与状态 白色、固体 无纯态,只存在于水溶液中水溶性 不溶于水只存在于水溶液中酸性比较H 2CO 3 >H 2SiO 3向硅酸钠饱和溶液中通入二氧化碳,同样可得到硅酸凝胶,说明硅酸是一种酸性比碳酸还弱的弱酸。
A等级(识别“是什么”):硅单质物性:①存在和形态:自然界中无游离态,主要以硅酸盐和二氧化硅形式存在。
②晶体硅是灰黑色、有金属光泽、硬而脆的固体。
③导电性:半导体材料,介于导体和半导体之间。
文科班必修1第四章《非金属及其化合物》复习提纲
本章知识结构
第一部分 硅
知道:SiO 2是硅最重要的化合物,占地壳质量约12%,其存在形态有结晶型和无定型两大类,统称硅石。
SiO 2基本结构单元为四面体结构:
Si 与O 按1:2的比例组成立体网状结构。
硅酸和碳酸的性质比较
点燃 点燃
点燃
硅单质物性:
①存在和形态:自然界中无游离态,主要以硅酸盐和二氧化硅形式存在。
②晶体硅是灰黑色、有金属光泽、硬而脆的固体。
③导电性:半导体材料,介于导体和半导体之间。
硅酸盐材料:水泥、玻璃、陶瓷、水玻璃(Na 2SiO 3的水溶液)等 硅酸盐组成的表示:
例如,Na 2SiO 3→Na 2O ·SiO 2
Al 2Si 2O 5(OH)4→Al 2O 3·2SiO 2·2H 2O
新型无机非金属材料:高温结构陶瓷、光导纤维等
传统无机非金属材料的优缺点:抗腐蚀、耐高温,质脆、经不起冲击。
新型无机非金属材料的特性:强度高,耐高温;
①具有电学特性:绝缘体、半导体、导体等;
②具有光学特性:发光、透光(可见光、红外光、射线); ③具有生物功能。
第二部分 氯 氯及其化合物:
氯气的物理性质:黄绿色气体,密度比空气大,能溶于水,有刺激性气
味,有毒。
氯气的化学性质:
(1)与金属:一般将金属氧化到最高价态。
Cu + Cl 2 = CuCl 2 2Fe +3Cl 2 = 2FeCl 3 (变价金属被氧化为最高价) (2)与非金属反应
H 2 + Cl 2 = 2HCl (苍白色火焰 白雾)
(3)与水反应 Cl 2 + H 2O = HCl + HClO HClO 性质: 弱酸(弱于H 2CO 3),具有强氧化性(漂白、杀菌、消毒)。
不稳定性 2HClO = 2HCl + O 2↑ (4)与碱反应
吸收尾气:Cl 2 + 2NaOH = NaClO + NaCl + H 2O 制漂白粉:Cl 2 +2Ca(OH)2 = Ca(ClO)2 + CaCl 2 + 2H 2O 漂白粉主
点燃
要成分:
Ca(ClO)2 + CaCl 2 漂白粉有效成分
: Ca(ClO)2
第三部分
硫及其化合物
硫(俗称硫磺):黄色粉末,不溶于水,微溶于酒精,易溶于CS 2 。
S +O 2 = SO 2
浓硫酸的氧化性:(稀硫酸为非氧化性酸,不与铜和碳反应)
第四部分 氮及其化合物
工业合成氨:
氨及其铵盐: 1、物理性质:
氨是一种无色、有刺激性气味的气体;极易溶于水(1:700),水溶液叫“氨水”;氨易液化“液氨”,常作致冷剂。
2、化学性质:
(1)氨水呈弱碱性,能使酚酞变红或使湿润的红色石蕊试纸变蓝色:
△
△
△
△
△
NH 3 + H 2O = NH 3·H 2O (呈弱碱性)
氨水不稳定,易分解。
NH 3·H 2O = NH 3↑+ H 2O (2)氨与酸的反应(生成相应的铵盐)
HCl + NH 3 = NH 4Cl H 2SO 4 + 2NH 3 = (NH 4)2SO 4 NH 3+HNO 3 = NH 4NO 3 3、铵盐性质:都易溶于水,受热易分解,与碱反应放出氨气。
NH 4Cl = HCl ↑ + NH 3↑
NH 4HCO 3 = NH 3↑+ H 2O + CO 2↑ NH 4NO 3 + NaOH = NaNO 3 + H 2O + NH 3↑ 4、氨的实验室制法:加热铵盐与碱的混合物
重要的氮氧化物 :2NH 4Cl + Ca(OH)2 = CaCl 2 + 2H 2O + 2NH 3↑
自然界中即存在: N 2+O 2
2NO (无色有毒的气体,难溶于水)
2NO+O 2 = 2NO 2(红棕色刺激性气味有毒气体,密度比空气大,易液化,易溶于水)
在工业生产硝酸时,应使用稍过量的空气,经过多次循环氧化吸收,可充分利用原料,并减少NO 的排放以保护环境:
重要的导出方程式:
硝酸的氧化性:Cu + 4HNO 3(浓)== Cu(NO 3)2 + 2H 2O + 2NO 2↑
3Cu + 8HNO 3(稀)== 3Cu(NO 3)2 + 4H 2O + 2NO ↑
常温下(冷的)浓H 2SO 4或浓HNO 3会使活泼金属钝化(如铝、铁),因此可用铁制槽车运输浓H 2SO 4或浓HNO 3。