硝酸和氮气反应
- 格式:doc
- 大小:12.40 KB
- 文档页数:2

氮及其化合物1、氮气物理性质:氮气是一种无色无味的气体,密度比空气略小,难溶于水。
2、氮气化学性质:化学性质很稳定,只有在一定条件(如高温、高压、放电等)下,才能跟 H2、O2等物质发生化学反应。
3、与氧气反应 N2 + O2 ===放电或高温 === 2NO4、与氮气反应:工业合成氨 N2 + 3H2==2NH3用途;氮气的用途广泛,工业上,氮气是制硝酸、氮肥的原料,含氮化合物是重要的化工原料。
氮气还常被用作保护气;在医学上,常用液氮作医疗麻醉。
氮的固定指的是将游离态的氮(即氮气)转化为化合态的氮的过程。
氮的固定方式可分为工业固氮、闪电固氮、生物固氮三种。
“雷雨发庄稼”就是一个闪电固氮的过程。
5、NO 物理性质:无色、难溶于水的、有毒气体,大气污染物之一,化学性质:极易在空气里被氧化成 NO2。
6、NO2 物理性质:红棕色、有刺激性气味的、有毒气体,易溶于水,易液化。
7、化学性质:空气中的 NO2在一定条件下易形成光化学烟雾,并且对臭氧层中臭氧的分解起到催化作用。
8、和氧气反应:2NO + O2 == 2NO2与 H2O 的反应: 3NO2 + H2O === 2HNO3 + NO工业上利用这一原理来生产硝酸。
9、与碱的反应 2NO2 + 2NaOH === NaNO3 + NaNO2 + H2O 实验室常用 NaOH 来吸收二氧化氮10、用途及危害:空气中的NO2与水作用生成HNO3,随雨水落下形成酸雨,工业制硝酸最后也是用水吸收生成的 NO2 制得硝酸。
11、氨物理性质:无色、有刺激性气味的气体,密度比空气小,易液化,极易溶于水,用氨气做喷泉实验。
12、氮化学性质:氨气具有还原性: 4NH3 + 5O2 4NO + 6H2O氨与水反应 NH3 + H2O=NH3·H2O 氨水是弱碱。
NH3·H2O =NH4+ + OH—氨水中存在的分子有 NH3 、NH3·H2O 、H2O ;存在的离子有 NH4+、OH-、H+(极少量);氨水密度小于水,氨水越浓氨水的密度越小。

氮及其化合物方程式总结氮气是一种无色、无臭的气体,它是大气中最主要的成分之一、氮的化学式为N2,它是由两个氮原子组成的。
氮气在常温下是稳定的,不易与其他物质反应,但是在一些特殊的条件下,氮与其他元素形成氮化物或氮氧化物。
氮气可以与氧气反应生成氮氧化物,在工业生产中,氮气与氧气的混合物是可以燃烧的,反应生成氮氧化物和燃烧产物,其中最主要的产物是二氧化氮(NO2)和一氧化氮(NO)。
氧化氮可以与大气中的水反应生成硝酸(HNO3),形成酸性雨。
氮气也可以与氢反应生成氨气(NH3),这个反应通常称为哈伯-博什过程(Haber-Bosch process),是工业上合成氨气的重要方法。
该反应的方程式为:N2+3H2→2NH3氨气在工业上广泛应用于制造化肥,它是植物生长所必需的营养物质之一在自然界中,土壤中的一些细菌可以利用氮气,通过固氮作用将氮气转化为能被植物吸收利用的形式。
这个过程被称为生物固氮作用,其中一种常见的细菌是根瘤菌。
根瘤菌与豆科植物共生,根瘤菌能够与植物共同形成根瘤,菌根瘤中的根瘤菌利用空气中的氮气形成是细菌能够通过酶将氮气转化为氨气,植物则能够通过氨气获得氮元素。
氮化物是氮的化合物之一、典型的氮化物有氨(NH3)、硝酸(HNO3)和亚硝酸(HNO2)。
氨是一种气体,具有刺激性的气味。
它是制造化肥的重要原料,也可以用于制造合成纤维、颜料等。
氨的化学式为NH3,氨气加水会生成氢氧化铵(NH4OH)。
硝酸和亚硝酸是氮的氧化物化合物。
它们在环境中重要,因为它们可以与其他化合物反应生成酸性雨,对环境造成危害。
硝酸的化学式为HNO3,亚硝酸的化学式为HNO2在工业上,氮还可以与其他元素形成各种氮化物。
例如,氮可以与钙、硅等元素反应生成氮化钙(Ca3N2)和氮化硅(Si3N4)。
氮化钙在火柴生产和炮火制造中有应用,氮化硅是一种硬度很高的陶瓷材料,可以用于制造刀具和机械零件。
综上所述,氮及其化合物在自然界和工业中都具有重要的应用。

硝酸与金属反应的一般规律
硝酸与金属的反应是相当复杂的。
在这类氧化还原反应中,包括许多平行反应。
因此,可以得到多种还原产物,而且在还原产物之间还进行氧化还原反应。
某些金属(如镁、锌)与小于2 mol/L的硝酸反应时,还会产生一定量的氢气。
硝酸的还原产物,除取决于硝酸的浓度、还原剂的还原能力外,还与反应温度和反应中间产物(HNO2、NO2)的催化作用有关,反应虽复杂,但硝酸与金属的反应是有规律的。
(1)在金属活动性顺序中,位于氢后面的金属如铜、汞、银等,与浓硝酸反应时,主要得到NO2,与稀硝酸反应时,主要得到NO。
(2)在常温下Fe、Co、Ni、Al等金属在浓硝酸中发生“钝化”,在金属表面覆盖一层致密的金属氧化物薄膜,阻止反应进一步发生。
这些金属与稀硝酸作用主要生成N2O(有的认为是NO),这是由于它们的还原性较强,能将硝酸还原成较低价的N2O。
如与更稀的硝酸反应则生成氨(钴在同样条件下则生成氮气)。
(3)镁、锌等金属与不同浓度的硝酸作用能得到氮的不同低价态的还原产物。
例如,当硝酸中HNO3的质量分数为9%~33%(密度为~g/cm3)时,反应按下式进行:
4Zn+10HNO3=4Zn(NO3)2+5H2O+N2O↑
若硝酸更稀,反应会生成氨,氨与过量的硝酸进一步反应生成硝酸铵。
4Zn+10HNO3=4Zn(NO3)2+NH4NO3+3H2O
(4)Au、Pt、Ir、Rh等重金属与浓、稀硝酸都不反应,因为它们特别稳定,不易被氧化。
(5)Sn、Sb、W、V等金属与浓硝酸作用,生成金属氧化物,而不是硝酸盐(因为这些金属氧化物不溶于硝酸,反应不再继续发生)。

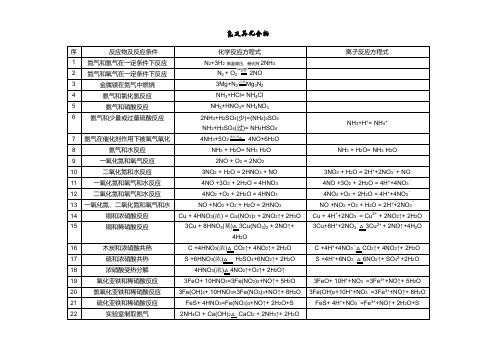
氮及其化合物序反应物及反应条件化学反应方程式离子反应方程式1 氮气和氢气在一定条件下反应N2+3H2 高温高压、催化剂2NH3×2 氮气和氧气在一定条件下反应N2 + O2放电2NO ×3 金属镁在氮气中燃烧3Mg+N2点燃Mg3N2 ×4 氨气和氯化氢反应NH3+HCl= NH4Cl ×5 氨气和硝酸反应NH3+HNO3= NH4NO3×6 氨气和少量或过量硫酸反应2NH3+H2SO4(少)=(NH4)2SO4NH3+H+= NH4+NH3+H2SO4(过)= NH4HSO47 氨气在催化剂作用下被氧气氧化4NH3+5O2催化剂△4NO+6H2O ×8 氨气和水反应NH3 + H2O= NH3·H2O NH3 + H2O= NH3·H2O9 一氧化氮和氧气反应2NO + O2 = 2NO2×10 二氧化氮和水反应3NO2 + H2O = 2HNO3 + NO 3NO2 + H2O = 2H++2NO3-+ NO11 一氧化氮和氧气和水反应4NO +3O2 + 2H2O = 4HNO34NO +3O2 + 2H2O = 4H++4NO3-12 二氧化氮和氧气和水反应4NO2 +O2 + 2H2O = 4HNO34NO2 +O2 + 2H2O = 4H++4NO3-13 一氧化氮、二氧化氮和氧气和水NO +NO2 +O2 + H2O = 2HNO3NO +NO2 +O2 + H2O = 2H++2NO3-14 铜和浓硝酸反应Cu + 4HNO3(浓) = Cu(NO3)2 + 2NO2↑+ 2H2O Cu + 4H++2NO3-= Cu2+ + 2NO2↑+ 2H2O3Cu+8H++2NO3-△3Cu2+ + 2NO↑+4H2O 15 铜和稀硝酸反应3Cu + 8HNO3(稀)△3Cu(NO3)2+ 2NO↑+4H2O16 木炭和浓硝酸共热 C +4HNO3(浓)△CO2↑+ 4NO2↑+ 2H2O C +4H++4NO3-△CO2↑+ 4NO2↑+ 2H2O17 硫和浓硝酸共热S +6HNO3(浓)△H2SO4+6NO2↑+ 2H2O S +4H++6NO3-△6NO2↑+ SO42-+2H2O18 浓硝酸受热分解4HNO3(浓)△4NO2↑+O2↑+ 2H2O↑×19 氧化亚铁和稀硝酸反应3FeO+ 10HNO3=3Fe(NO3)3+NO↑+ 5H2O 3FeO+ 10H++NO3-=3Fe3++NO↑+ 5H2O20 氢氧化亚铁和稀硝酸反应3Fe(OH)2+ 10HNO3=3Fe(NO3)3+NO↑+ 8H2O 3Fe(OH)2+10H++NO3-=3Fe3++NO↑+ 8H2O21 硫化亚铁和稀硝酸反应FeS+ 4HNO3=Fe(NO3)3+NO↑+ 2H2O+S FeS+ 4H++NO3-=Fe3++NO↑+ 2H2O+S22 实验室制取氨气2NH4Cl + Ca(OH)2△ CaCl2 + 2NH3↑+ 2H2O ×。

电弧法硝酸-概述说明以及解释1.引言1.1 概述概述:电弧法是一种重要的化学实验室技术,用于制备硝酸。
它是通过利用弧光加热和高温氧化的原理,将氮气与氧气反应生成硝酸。
电弧法以其高效、快速和低能耗的特点,广泛应用于化工领域。
在电弧法中,通过两根电极间形成的电弧产生高温和高能量,将空气中的氮气分子激发到高能级,并与氧气分子发生碰撞反应。
在这个过程中,氮氧化合物以及硝酸的中间产物被形成。
接着,通过将中间产物经过一系列的反应和加工步骤,最终得到纯净的硝酸。
电弧法在化学工业中有着广泛的应用。
首先,它是制备硝酸的主要方法之一,在农业、医药和化肥生产中扮演着至关重要的角色。
其次,电弧法还可用于制备其他硝酸盐,如硫酸铵和硝酸钾等。
此外,通过调整电弧发生时的电流和电压,还可控制反应的速率和产物的纯度,从而适应不同的工业需求。
然而,电弧法也存在一些不足之处。
首先,电弧法操作复杂,需要较高的技术水平和设备要求。
其次,电弧法的能耗较大,对电力资源的消耗较高。
此外,电弧法还存在一定的安全隐患和环境污染问题,需要采取相应的措施来保护操作人员和环境。
随着科学技术的不断发展,电弧法在未来还有更大的发展潜力。
例如,利用新材料和先进的设备,可以进一步提高电弧法的效率和纯度,减少能耗和安全风险。
同时,与其他化学制备方法相结合,还可以实现更加绿色和可持续的硝酸生产过程。
总而言之,电弧法是一种重要的化学实验室技术,用于制备硝酸。
它具有高效、快速和广泛应用的特点,但也存在一些不足之处。
随着科学技术的发展,电弧法在未来仍有更大的发展空间,为硝酸生产提供更加可持续和环保的解决方案。
文章结构部分的内容可以着重介绍本文的组织架构,说明各个章节或部分的内容和目的,以帮助读者更好地理解整篇文章的逻辑和主题。
以下是文章结构部分的内容示例:【1.2 文章结构】本文主要从电弧法的定义、原理、应用领域、优缺点以及发展趋势等方面进行探讨。
为了更好地展示这些内容,本文按照以下结构进行组织。
氮及其化合物一、氮气2.3Mg+N 2Mg3N2N2+O22NON2+3H 2催化剂高温高压2NH3二、氨气1、氨的催化氧化:4NH3+5O24NO +6H2O2、氨气与盐酸反应:NH3+HCl NH4Cl(白烟,检验氨气)3、少量氨在氯气中燃烧:2NH3+3Cl 2N2+6HCl足量的氨和氯气反应:8NH3+3Cl2N2+6NH4Cl4、氨气通过灼热的氧化铜:2NH3+3CuO N2+3Cu+3H2O5、氨气和水反应:NH3+H2O NH3·H2ONH3·H2O NH4++OH-6、氨水与盐酸反应:NH3·H2O+HCl NH4Cl+H 2O7、Al2(SO4)3+6NH3·H2O2Al(OH)3↓+3(NH4)2SO4Al3++3NH3·H2O Al(OH)3↓+3NH4+8、向氯化铁溶液中加入氨水:FeCl3+3NH3·H2O Fe(OH)3↓+3NH4ClFe3++3NH3·H2O Fe(OH)3↓+3NH4+9、向氯化亚铁溶液中加入氨水:FeCl2+2NH 3·H2O Fe(OH)2↓+2NH4ClFe2++2NH3·H2O Fe(OH)2↓+2NH4+放电10、硫酸铜溶液中加入氨水:CuSO4+2NH3·H2O Cu(OH)2↓+(NH4)2SO4Cu2++2NH3·H2O Cu(OH)2↓+2NH4+11、氨气在催化剂、加热的条件下和一氧化氮反应:4NH3+6NO5N2+6H2O氨气在催化剂、加热的条件下和二氧化氮反应:8NH3+6NO27N2+12H2O三、铵盐1、向氯化铵溶液加入氢氧化钠溶液并加热: NH4Cl+NaOH NaCl+NH3↑+H2ONH4++OH-NH3↑+H2O3、加热氯化铵:NH4Cl NH3↑+HCl↑(不能用于制氨气)4、加热碳酸氢铵:NH4HCO3NH3↑+CO2↑+H2O5、加热硝酸铵:5NH4NO34N2↑+2HNO3+9H2O(易爆炸)6、向四羟基合铝酸钠溶液中加入氯化铵溶液:Na[Al(OH)4]+NH4Cl Al(OH)3↓+NaCl+NH3↑+H2O[Al(OH)4]-+NH4+Al(OH)3+NH3↑7、氯化铵固体和消石灰共热:2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O装置:固——固反应加热装置(与制取O2装置相同)四、一氧化氮1、一氧化氮和氧气反应:2NO+O22NO2现象:无色气体变为红棕色2、一氧化氮、二氧化氮和氢氧化钠溶液反应(尾气处理):NO+NO2+2NaOH2NaNO2+H2O NO+NO2+2OH-2NO2-+H2O五、二氧化氮:1、二氧化氮与水反应:3NO2+H2O2HNO3+NO2、二氧化氮和氢氧化钠溶液反应(尾气处理):2NO2+2NaOH NaNO2+NaNO3+H2O2NO2+2OH-NO2-+NO3-+H2O六、硝酸:1、浓硝酸受热或见光分解:4HNO34NO2↑+O2↑+2H2O2、铜与浓硝酸反应:Cu+4HNO3(浓)Cu(NO3)2+2NO2↑+2H2OCu+4H++2NO3-Cu2++2NO2↑+2H2O3、铜和稀硝酸反应:3Cu+8HNO3(稀)3Cu(NO3)2+2NO ↑+4H2O3Cu+8H++2NO3-3Cu2++2NO ↑+4H2O4、碳与浓硝酸共热:C+4HNO3(浓)CO2↑+4NO2↑+2H2O6、银与浓硝酸反应:Ag+2HNO3(浓)AgNO3+NO2↑+H2OAg+2H++NO3-Ag++NO2↑+H2O7、银与稀硝酸反应:3Ag+4HNO3(稀)3AgNO3+NO ↑+2H2O3Ag+4H++NO3-3Ag++NO↑+2H2O8、少量的铁与稀硝酸反应:Fe+4HNO3(稀)Fe(NO3)3+NO↑+2H2OFe+4H++NO3-Fe3++NO ↑+2H2O9、过量的铁与稀硝酸反应:3Fe+8HNO3(稀)3Fe(NO3)2+2NO ↑+4H2O3Fe+8H++2NO3-3Fe2++2NO ↑+4H2O 13、氧化亚铁与稀硝酸反应:3FeO+10HNO33Fe(NO3)3+NO ↑+5H2O3FeO+10H++NO3-3Fe3++NO ↑+5H2O14、四氧化三铁溶于稀硝酸:3Fe3O4+28HNO39Fe(NO3)3+NO ↑+14H2O3Fe3O4+28H++NO3-9Fe3++NO ↑+14H2O*16、氢硫酸与浓硝酸反应:H2S+2HNO3(浓)S↓+2NO2↑+2H2OH2S+2H++2NO3-S ↓+2NO2↑+H2O*17、氢硫酸与稀硝酸反应:3H2S+2HNO3(稀)3S↓+2NO ↑+4H2O3H2S+2H++2NO3-3S↓+2NO↑+4H2O*18、亚硫酸与稀硝酸反应:3H2SO3+2HNO3(稀)3H2SO4+2NO↑+H2O3H2SO3+2H++2NO3-6H++3SO42-+2NO↑+H2O*19、氢碘酸与稀硝酸反应:6HI+2HNO3(稀)3I2+2NO +4H2O8H++2I-+2NO3-3I2+2NO+4H2O*20、氢氧化亚铁与稀硝酸反应:3Fe(OH)2+10HNO3(稀)3Fe(NO3)3+NO↑+8H2O3Fe(OH)2+10H++NO3-3Fe3++NO↑+8H2O21、硫化钠溶液与稀硝酸反应:3Na2S+8HNO36NaNO3+3S↓+2NO ↑+4H2O3S2-+8H++2NO3-3S↓+2NO↑+4H2O*22、亚硫酸钠与稀硝酸反应:3Na2SO3+2HNO33Na2SO4+2NO↑+H2O3SO42-+2H++2NO3-3SO42-+2NO↑+H2O。
氮及其化合物【考点要求】考点 1 氮及其重要化合物的主要物理性质,知道氮单质的主要用途考点 2 二氧化氮和水的反应考点 3 氨气和水、酸的反应,认识氨水的成分及氨水的不牢固性,铵盐易溶于水、受热易分解、与碱反应等性质考点 4硝酸的强氧化性,认识硝酸分别于Cu 、 C 反应,认识常温下铁、铝在浓硝酸中的钝化现象考点 5 氮循环对生态平衡的重要作用。
认识氮氧化物、二氧化硫等污染物的本源和危害,认识非金属及其重要化合物在生产生活中的应用和对生态环境的影响,渐渐形成可连续发展的思想。
【考点梳理】1、氮气物理性质:氮气是一种无色无味的气体,密度比空气略小,难溶于水。
化学性质:化学性质很牢固,只有在必然条件(如高温、高压、放电等)下,才能跟H2、O2等物质发生化学反应。
与氧气反应N2 + O2 ===== 放电或高温== 2NO与氮气反应工业合成氨N 2 + 3H 2 2NH 3用途;氮气的用途广泛,工业上,氮气是制硝酸、氮肥的原料,含氮化合物是重要的化工原料。
氮气还常被用作保护气;在医学上,常用液氮作医疗麻醉。
氮的固定指的是将游离态的氮(即氮气)转变成化合态的氮的过程。
氮的固定方式可分为工业固氮、闪电固氮、生物固氮三种。
“雷雨发庄稼”就是一个闪电固氮的过程。
2、 NO物理性质:无色难溶于水的有毒气体,大气污染物之一,化学性质:极易在空气里被氧化成NO 2。
3. NO2物理性质:红棕色有刺激性气味的有毒气体,易溶于水,易液化。
化学性质:空气中的NO 2在必然条件下易形成光化学烟雾,并且对臭氧层中臭氧的分解起到催化作用。
和氧气反应:2NO + O2 == 2NO 2与 H 2O 的反应:3NO2 + H 2O === 2HNO 3 + NO 工业上利用这一原理来生产硝酸。
与碱的反应2NO 2+2NaOH===NaNO 3+NaNO 2+H2O 实验室常用NaOH来吸取二氧化氮用途及危害空气中的 NO 2与水作用生成 HNO 3,随雨水落下形成酸雨,工业制硝酸最后也是用水吸取生成的 NO2制得硝酸。
氮及其化合物的化学方程式和离子方程式(注:带*的不要求记住,但要求能理解)一、氮气1、镁在氮气中燃烧:3Mg+N2Mg3N22、氮气在放电的条件下与氧气反应:N2+O22NO放电3、合成氨反应:N2+3H2催化剂高温高压2NH3二、氨气1、氨的催化氧化:4NH3+5O24NO+6H2O*2、少量氨在氯气中燃烧:2NH3+3Cl2N2+6HCl*3、足量的氨和氯气反应:8NH3+3Cl2N2+6NH4Cl*4、氨气在纯净的氧气中燃烧:4NH3+3O22N2+6H2O*5、氨气通过灼热的氧化铜:2NH3+3CuO N2+3Cu+3H2O6、氨气和水反应:NH3+H2O NH3·H2O NH4++OH-7、氨水与盐酸反应:NH3·H2O+HCl NH4Cl+H2ONH3·H2O+H+NH4++H2O8、氨水与醋酸反应:NH3·H2O+CH3COOH CH3COONH4+H2ONH3·H2O+CH3COOH CH3COO-+NH4++H2O9、氯化镁溶液加入氨水:MgCl2+2NH3·H2O Mg(OH)2↓+2NH4ClMg2++2NH3·H2O Mg(OH)2↓+2NH4+10、向硫酸铝溶液中加入氨水:Al2(SO4)3+6NH3·H2O2Al(OH)3↓+3(NH4)2SO4Al3++3NH3·H2O Al(OH)3↓+3NH4+11、氯化亚铁溶液中加入氨水:FeCl2+2NH3·H2O Fe(OH)2↓+2NH4ClFe2++2NH3·H2O Fe(OH)2↓+2NH4+12、向氯化铁溶液中加入氨水:FeCl3+3NH3·H2O Fe(OH)3↓+3NH4ClFe3++3NH3·H2O Fe(OH)3↓+3NH4+13、硫酸铜溶液中加入氨水:CuSO4+2NH3·H2O Cu(OH)2↓+(NH4)2SO4Cu2++2NH3·H2O Cu(OH)2↓+2NH4+*14、硝酸银溶液中加入少量氨水:AgNO3+NH3·H2O AgOH↓+NH4NO3Ag++NH3·H2O AgOH↓+NH4+*15、硝酸银溶液加入过量氨水:AgNO3+3NH3·H2O[Ag(NH3)2]OH+NH4NO3+2H2OAg++3NH3·H2O Ag(NH3)2++OH-+2H2O*16、氨气在催化剂、加热的条件下和一氧化氮反应:4NH3+6NO5N2+6H2O*17、氨气在催化剂、加热的条件下和二氧化氮反应:8NH3+6NO27N2+12H2O18、氨气和氯化氢气体产生白烟:NH3+HCl NH4Cl三、氯化铵1、氯化铵溶液与硝酸银溶液反应:NH4Cl+AgNO3AgCl↓+NH4NO3Cl-+Ag+AgCl↓2、氯化铵溶液呈酸性:NH4Cl+H2O NH3·H2O+HClNH4++H2O NH3·H2O+H+3、向氯化铵溶液加入氢氧化钠溶液并加热:NH4Cl+NaOH NaCl+NH3↑+H2ONH4++OH-NH3↑+H2O4、氯化铵固体和消石灰共热:2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O*5、氢氧化镁溶于氯化铵溶液中:Mg(OH)2+2NH4Cl MgCl2+2NH3↑+2H2OMg(OH)2+2NH4+Mg2++2NH3↑+2H2O*6、向四羟基合铝酸钠溶液中加入氯化铵溶液:Na[Al(OH)4]+NH4Cl Al(OH)3↓+NaCl+NH3↑+H2O[Al(OH)4]-+NH4+Al(OH)3+NH3↑*7、硅酸钠溶液与氯化铵溶液混合:Na2SiO3+2NH4Cl2NaCl+H2SiO3↓+2NH3↑SiO32-+2NH4+H2SiO3↓+2NH3↑*8、饱和氯化铵溶液和亚硝酸钠溶液共热:NH4Cl+NaNO2N2↑+NaCl+2H2ONH4++NO2-N2↑+2H2O9、加热氯化铵:NH4Cl NH3↑+HCl↑10、加热碳酸氢铵:NH4HCO3NH3↑+CO2↑+H2O*11、加热硝酸铵:5NH4NO34N2↑+2HNO3+9H2O*12、强热硫酸铵:3(NH4)2SO4N2↑+3SO2↑+4NH3↑+6H2O四、一氧化氮1、一氧化氮和氧气反应:2NO+O22NO22、一氧化氮和氧气的混合气体通入水中的总反应:4NO+3O2+2H2O4HNO3*3、氨气在催化剂、加热的条件下和一氧化氮反应:4NH3+6NO5N2+6H2O*4、一氧化氮、二氧化氮和氢氧化钠溶液反应:NO+NO2+2NaOH2NaNO2+H2ONO+NO2+2OH-2NO2-+H2O 五、二氧化氮1、二氧化氮与水反应:3NO2+H2O2HNO3+NO3NO2+H2O2H++NO3-+NO2、二氧化氮和氧气的混合气体通入水中的总反应:4NO2+O2+2H2O4HNO3*3、二氧化氮和氢氧化钠溶液反应:2NO2+2NaOH NaNO2+NaNO3+H2O2NO2+2OH-NO2-+NO3-+H2O六、硝酸*1、锌与浓硝酸反应:Zn+4HNO3(浓)Zn(NO3)2+2NO2↑+2H2OZn+4H++2NO3-Zn2++2NO2↑+2H2O*2、锌和稀硝酸反应:3Zn+8HNO33Zn(NO3)2+2NO ↑+4H2O3Zn+8H++2NO3-3Zn2++2NO ↑+4H2O3、银与浓硝酸反应:Ag+2HNO3(浓)AgNO3+NO2↑+H2OAg+2H++NO3-Ag++NO2↑+H2O4、银与稀硝酸反应:3Ag+4HNO33AgNO3+NO ↑+2H2O3Ag+4H++NO3-3Ag++NO↑+2H2O5、铜与浓硝酸反应:Cu+4HNO3(浓)Cu(NO3)2+2NO2↑+2H2OCu+4H++2NO3-Cu2++2NO2↑+2H2O6、铜和稀硝酸反应:3Cu+8HNO3(浓)3Cu(NO3)2+2NO ↑+4H2O3Cu+8H++2NO3-3Cu2++2NO ↑+4H2O7、少量的铁与浓硝酸共热:Fe+6HNO3(浓)Fe(NO3)3+3NO2↑+3H2OFe+6H++3NO3-Fe3++3NO2↑+3H2O8、少量的铁与稀硝酸反应:Fe+4HNO3Fe(NO3)3+NO↑+2H2OFe+4H++NO3-Fe3++NO ↑+2H2O9、过量的铁与稀硝酸反应:3Fe+8HNO33Fe(NO3)2+2NO ↑+4H2O3Fe+8H++2NO3-3Fe2++2NO ↑+4H2O10、碳与浓硝酸共热:C+4HNO3(浓)CO2↑+4NO2↑+2H2O*11、硫与浓硝酸共热:S+6HNO3(浓)H2SO4+6NO2↑+2H2O*12、磷与浓硝酸共热:P+5HNO3(浓)H3PO4+5NO2+H2O↑13、氧化钠溶于硝酸:Na2O+2HNO32NaNO3+H2ONa2O+2H+2Na++H2O14、氧化铜与硝酸反应:CuO+2HNO3Cu(NO3)2+H2OCuO+2H+Cu2++H2O15、氧化铁溶于硝酸:Fe2O3+6HNO32Fe(NO3)3+3H2OFe2O3+6H+2Fe3++3H2O*16、氧化亚铁与浓硝酸反应:FeO+4HNO3(浓)Fe(NO3)3+NO2↑+2H2OFeO+4H++NO3-Fe3++NO2↑+2H2O*17、氧化亚铁与稀硝酸反应:3FeO+10HNO33Fe(NO3)3+NO ↑+5H2O3FeO+10H++NO3-3Fe3++NO ↑+5H2O*18、四氧化三铁溶于浓硝酸:Fe3O4+10HNO3(浓)3Fe(NO3)3+NO2↑+5H2OFe3O4+1OH++NO3-3Fe3++NO2↑+5H2O*19、四氧化三铁溶于稀硝酸:3Fe3O4+28HNO39Fe(NO3)3+NO ↑+14H2O3Fe3O4+28H++NO3-9Fe3++NO ↑+14H2O*20、二氧化硫通入浓硝酸中:SO2+2HNO3H2SO4+2NO2↑SO2+2NO3-SO42-+2NO2↑*21、二氧化硫通入稀硝酸中:3SO2+2HNO3+2H2O3H2SO4+2NO↑3SO2+2NO3-+2H2O4H++3SO42-+2NO↑*22、氢硫酸与浓硝酸反应:H2S+2HNO3(浓)S↓+2NO2↑+2H2OH2S+2H++2NO3-S ↓+2NO2↑+H2O*23、氢硫酸与稀硝酸反应:3H2S+2HNO33S↓+2NO ↑+4H2O3H2S+2H++2NO3-3S↓+2NO↑+4H2O*24、亚硫酸与与浓硝酸反应:H2SO3+2HNO3H2SO4+2NO2↑+H2OH2SO3+2NO3-SO42-+2NO2↑+H2O*25、亚硫酸与稀硝酸反应:3H2SO3+2HNO33H2SO4+2NO↑+H2O3H2SO3+2H++2NO3-6H++3SO42-+2NO↑+H2O *26、氢碘酸与浓硝酸反应:2HI+2HNO3(浓)I2+2NO2↑+2H2O4H++2I-+2NO3-I2+2NO2↑+2H2O*27、氢碘酸与稀硝酸反应:6HI+2HNO33I2+2NO +4H2O8H++2I-+2NO3-3I2+2NO+4H2O28、氢氧化钠溶液与硝酸反应:NaOH+HNO3NaNO3+H2OH++OH-H2O29、氢氧化镁与硝酸反应:Mg(OH)2+2HNO3Mg(NO3)2+2H2OMg(OH)2+2H+Mg2++2H2O30、氢氧化铝与硝酸反应:Al(OH)3+3HNO3Al(NO3)3+3H2OAI(OH)3+3H+Al3++3H2O31、氨水与硝酸反应:NH3·H2O+HNO3NH4NO3+H2ONH3·H2O+H+NH4++H2O*32、氢氧化亚铁与浓硝酸反应:Fe(OH)2+4HNO3(浓)Fe(NO3)3+NO2↑+3H2OFe(OH)2+4H++NO3-Fe3++NO2↑+3H2O*33、氢氧化亚铁与稀硝酸反应:3Fe(OH)2+10HNO33Fe(NO3)3+NO↑+8H2O3Fe(OH)2+10H++NO3-3Fe3++NO↑+8H2O*34、硝酸亚铁溶液与浓硝酸反应:Fe(NO3)2+2HNO3(浓)Fe(NO3)3+NO2↑+H2OFe2++2H++NO3-Fe3++H2O+NO2↑*35、硝酸亚铁溶液与稀硝酸反应:3Fe(NO3)2+10HNO33Fe(NO3)3+NO ↑+5H2O3Fe2++10H++NO3-3Fe3++NO↑+5H2O*36、硫化钠与浓硝酸反应:Na2S+4HNO32NaNO3+S↓+2NO2↑+2H2OS2-+4H++2NO3-S↓+2NO2↑+2H2O*37、硫化钠溶液与稀硝酸反应:3Na2S+8HNO36NaNO3+3S↓+2NO ↑+4H2O3S2-+8H++2NO3-3S↓+2NO↑+4H2O*38、碘化钾溶液与浓硝酸混合:2KI+4HNO3(浓)2KNO3+I2+2NO2↑+2H2O2I-+4H++2NO3-I2+2NO2↑+2H2O*39、碘化钾与稀硝酸反应:6KI+8HNO36KNO3+I2+2NO↑+4H2O6I-+8H++2NO3-3I2+2NO↑+4H2O*40、亚硫酸钠与浓硝酸反应:Na2SO3+2HNO3(浓)Na2SO4+2NO2↑+H2OSO32-+2H++2NO3-SO42-+2NO2↑+H2O*41、亚硫酸钠与稀硝酸反应:3Na2SO3+2HNO33Na2SO4+2NO↑+H2O3SO42-+2H++2NO3-3SO42-+2NO↑+H2O42、浓硝酸受热或见光分解:4HNO34NO2↑+O2↑+2H2O七、硝酸钠*1、实验室用硝酸钠固体与浓硫酸微热制备硝酸:NaNO3+H2SO4NaHSO4+HNO3↑*2、硝酸钠受热分解:2NaNO32NaNO2+O2↑3、铜和硝酸钠的酸化溶液反应:3Cu+2NaNO3+4H2SO43CuSO4+Na2SO4+2NO↑+4H2O3Cu+8H++2NO3-3Cu2++2NO↑+4H2O*4、加热硝酸铜固体:2Cu(NO3)22CuO+2NO2↑+O2↑*5、加热硝酸银固体:2AgNO32Ag+2NO2↑+O2↑。
污水处理—硝化与反硝化反硝化反应过程:在缺氧条件下,硝酸盐被反硝化细菌还原成为氮气和氧气。
反硝化细菌利用硝酸盐作为电子受体,有机物或者无机物作为电子供体,从而获得能量。
反硝化反应过程需要在缺氧(n)条件下进行,其相应的反应式为:1.反硝化反应方程式:C5H7O2N+5H2O+4NO3-→5NO2-+CO2+7H2O2.反硝化过程总反应式:C5H7O2N+2.5NO3-+3.5H2O→0.5N2+CO2+5H2O通过上述反应过程的物料衡算可知,在反硝化反应过程中,将1克硝酸盐氮还原为氮气需缺氧2.86克,同时产生0.57克有机物或无机物作为电子供体。
在反硝化反应过程中,氮元素的转化经历了以下几个过程:硝酸盐NO3-→亚硝酸盐NO2-→一氧化氮NO→氮气N2.三、硝化反硝化反应过程硝化反硝化反应过程:硝化反应和反硝化反应是一个连续的过程,需要在好氧条件下进行硝化反应,然后在缺氧条件下进行反硝化反应。
硝化反应将氨氮转化为硝酸盐氮,反硝化反应将硝酸盐氮还原为氮气。
硝化反硝化反应过程是一种高效的污水微生物脱氮方法,可以有效地去除污水中的氮元素。
四、污水硝化反硝化脱氮处理技术的应用污水硝化反硝化脱氮处理技术是一种成熟的污水处理方法,已经被广泛应用于城市污水处理厂和工业污水处理厂中。
该技术可以有效地去除污水中的氮元素,降低氮污染物排放,保护水环境。
同时,该技术具有工艺简单、运行成本低等优点,适用于不同规模的污水处理厂。
好氧池是指充氧池,其溶解氧浓度一般不小于2mg/L。
其主要功能是降解有机物和进行硝化反应。
当除磷为主要目标时,应采用厌氧/好氧工艺。
其基本工艺流程如下:当除氮为主要目标时,宜采用缺氧/好氧工艺。
其基本工艺流程如下:如果需要同时脱氮除磷,则应采用厌氧/缺氧/好氧(A/A/O)工艺。
在厌氧条件下,VFA(挥发性脂肪酸)、PHA(聚羟基脂肪酸)、PO(磷酸盐)和PP(多聚磷酸盐)可以被PAOs吸收和转化为PHA。
硝酸和氮气反应
硝酸是一种常见的无机化合物,由氮气和氧气组成,是可以产生氮排放的潜在源,也可以用作有机化合物的氮源,在氮化工业中排列重要的地位。
已经有许多研究表明,硝酸可以与氮气反应,从而产生能量,这种反应也被称为硝酸氮气反应,它可以改善能源利用率,减少碳排放。
首先,硝酸和氮气可以实现化学反应。
这种反应一般以HNO3(以硝酸)和N2O(以氮气)为基础,它们可以经过合成型反应,产生一种叫做 NOX物质,同时还会释放出大量的能量,以及质子和氧离子
被释放出来。
这种反应的最终产物是 NO2氧化物,该物质可以进一
步反应,生成氮排放物。
其次,硝酸和氮气反应也是一种可以实现能源利用率改善的方法。
这种反应的最终产物是 NO2氧化物,这种物质可以进一步用于合成
有机化合物以及实现化学转换,从而将储存的化学能量释放出来,用于发电和 in power generation and other process.样就可以大大
提高能源利用率,把储存在硝酸中的能量充分利用起来。
此外,硝酸和氮气反应也可以减少碳排放。
硝酸和氮气的反应产生的最终产物是一氧化二氮,这种物质可以作为碳排放的终结物,而不是温室气体排放,因此可以有效地减少温室效应。
总之,硝酸和氮气可以发生反应,能够产生大量的能量,而且还可以改善能源利用率和减少碳排放。
因此,硝酸和氮气反应有助于改善能源利用情况,减少碳排放,并有助于我们改善人类和环境的生活
质量。