第11章 配位化学-2
- 格式:ppt
- 大小:1.23 MB
- 文档页数:53



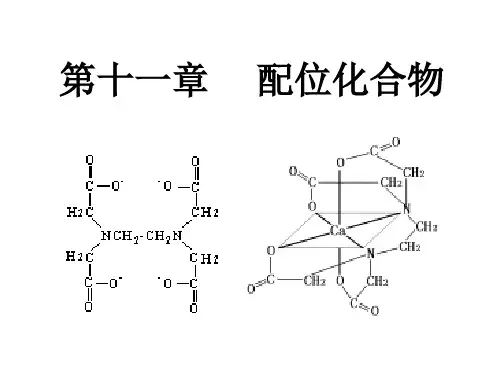
有环状结构,被称为螯合物或内配合物。
2+同一配体的两个或两个以上的配位原子间有一个原子,这样才能形成比较配位化合物金属有机配合物SO4科学家鲍林CN -为强配体,使Co 3个d 电子重排中心采取d 2sp 3 杂化,配离子Co(CN)为正八面体构型。
3d4s4p d 2sp 3杂化过渡金属Ni 的d轨道与CO的π*能量相近,对称性一致,可以成键。
按重叠后的(C2H4) ]·H2Oσ配键d-pπ配键在八面体场中,六个配体沿x,y,z轴的个方向分布,以形成八面体场。
正八面体场中配体与d z2 轨道的相对位置,轨道的波瓣与六个配体正相对,d x 2-y 2d z 2球形场正八面体场中配体与d xy 轨道的相对位置,,轨道的波瓣不与配体相对,能量升高的少,低于球形场。
d xy d xz d yz 球形场坐标原点为正六面体的中心,三轴分别沿与三边平行的方向伸展。
4 个配体的位置如图所示,形成四面体场。
正四面体场中配体与d x 2-y 2 轨道的相对位置正四面体场中配体与d xy 轨道的相对位置d d d 球形场(d )球形场(d )坐标原点位于正方形中心,坐标轴沿正方形对角线方向伸展。
4个配位原子位于正方形的顶点,形成正方形电场。
yx-++--y 2d x 2-y 2轨道的波瓣与配体一一相对,受电场作用最大,能量最高。
d xy 轨道处于y 平面内,受电场作用较大,能量居第二位。
++--d xy yx轨道的环形波瓣在x O y 平面内,列第三位。
d z 2yx能量最低的是轨道和轨道d xz d yz ++--z d yzyz++--d xzxz2.影响分裂能大小的因素弱场强场 小大-----光谱化学序列弱场强场 小大X -,OH -等弱场配体△小,常有△< P ,取高自旋光谱化学序列中NO 2-,CN -,CO 等强场配体△大,常导致△> P ,取低自旋方式,强场低自旋。
高自旋排布(dε)4 (dγ)2 低自旋排布(dε)6 (dγ)05个d轨道的能量为零点。





配位化学教学大纲预览说明:预览图片所展示的格式为文档的源格式展示,下载源文件没有水印,内容可编辑和复制中国海洋大学本科生课程大纲课程属性:学科基础课程性质:选修一、课程介绍1.课程描述:配位化学是高等院校化学化工类专业的一门选修课程,配位化学是无机化学领域中一个重要分支,具有边缘科学的性质,它已经成为沟通无机化学与有机化学、无机化学与生命科学等学科的重要渠道。
通过本课程的学习,使学生获得配位化学的基本概念和基本理论以及配位化合物的相关应用,扩大学生的知识面并提高知识水平。
本课程的教学着重讲述配位化学的基本理论和基本方法,同时在教学中也注意介绍正在发展中的一些较新的理论、方法和应用以激发学生的学习热情。
2.设计思路:配位化学是在无机化学基础上发展起来的一门重要的学科,发展至今,配位化学已经具有了一整套完善的理论体系;另一方面配位化学与物理化学、有机化学、生物化学、固体化学、材料化学和环境科学等学科相互渗透,使配位化学已成为众多学科的交叉点。
因此,本课程在系统讲解配位化学的基础理论知识之外,在教学过程中将结合学科前沿和试验测试结果,把配位化学与各学科交叉发展的最新动态和最新成果介绍给学生,提高学生学习的新鲜感和趣味性。
课程内容包括两个模块:基础理论知识和交叉学科介绍。
基础理论知识讲包括:配位化合物的基本知识,配位化合物的化学键理论,配合物的表征方法,配合物的反应动力学和反应机理,配合物在水溶液中的稳定性。
交叉学科介绍包括:金属有机配合物,金属原子簇化合物,特殊类型的配合物,配位催化,海洋配位化学,配合物合成化学,生物配位化学,配位化学的最新发展领域与动态。
3. 课程与其他课程的关系:配位化学是在无机化学的基础上发展起来的一门独立的、同时也与化学各分支学科等互相渗透的具有综合性的学科。
配位化学几乎渗透到化学及相关学科的各个领域,例如分析化学、有机金属化学、生物无机化学、结构化学、催化化学、配位光化学、界面配位化学、纳米配位化学、以及配位超分子化学等等。

第十一章配位化合物11.1 基本概念 (1)11.2 化学键理论 (6)11.3 晶体场理论 (11)11.4 螯合物 (18)11.5 配位平衡 (19)11.1 基本概念11.1.1 配位化合物的基本概念前言配位化合物是一类由中心金属原子(离子)和配位体组成的化合物。
第一个配合物是1704年普鲁士人在染料作坊中为寻找蓝色染料,而将兽皮、兽血同碳酸钠在铁锅中强烈煮沸而得到的,即KFe[Fe(CN)6]。
配合物的形成对元素和配位体都产生很大的影响,以及配合物的独特性质,使人们对配位化学的研究更深入、广泛,它不仅是现代无机化学学科的中心课题,而且对分析化学、生物化学、催化动力学、电化学、量子化学等方面的研究都有重要的意义。
1.配位化合物的定义配合物是由中心原子(或离子)和配位体(阴离子或分子)以配位键的形式结合而成的复杂离子或分子,通常称这种复杂离子或分子为配位单元。
凡是含有配位单元的化合物都称配合物。
如:[Co(NH3)6]3+、[HgI4]2-、Ni(CO)4等复杂离子或分子,其中都含配位键,所以它们都是配位单元。
由它们组成的相应化合物则为配合物。
如:[Co(NH3)6]Cl3、k2[HgI4]、Ni(CO)411.1.2 组成2.配位化合物的组成图11-01表11-01 常见的配体表11.1.3 命名3.配位化合物的命名对于整个配合物的命名,与一般无机化合物的命名原则相同,如配合物外界酸根为简单离子,命名为某化某;如配合物外界酸根为复杂阴离子,命名为某酸某;如配合物外界为OH-,则命名为氢氧化某。
但配合物因为存在较为复杂的内界,其命名要比一般无机化合物复杂。
内界的命名顺序为:例如:11.1.4 配合物的类型4.配位化合物的类型(1).简单配位化合物简单配位化合物是指由单基配位体与中心离子配位而成的配合物。
这类配合物通常配位体较多,在溶液中逐级离解成一系列配位数不同的配离子。
例如:这种现象叫逐级离解现象。
第十一章配位化合物配位化合物简称配合物,也称络合物,是一类复杂的化合物,它的存在和应用都很广泛,生物体内的金属元素多以配合物的形式存在。
例如植物中的叶绿素是镁的配合物,植物的光合作用靠它来完成。
又如动物血液中的血红蛋白是铁的配合物,在血液中起着输送氧气的作用;动物体内的各种酶几乎都是以金属配合物形式存在的。
当今配合物广泛地渗透到分析化学、生物化学等领域。
发展成为一门独立的学科──配位化学。
本章将对配合物的基本概念、组成、性质等作一初步介绍。
§11-1 配合物的基本概念一、配合物及其组成配位化合物是一类复杂的化合物,含有复杂的配位单元。
配位单元是由中心离子(或原子)与一定数目的分子或离子以配合键结合而成的。
例如在硫酸铜溶液中加入氨水,开始时有蓝色Cu2(OH)2SO4沉淀生成,当继续加氨水过量时,蓝色沉淀溶解变成深蓝色溶液。
总反应为:CuSO4 + 4NH3ƒ[Cu(NH3)4]SO4 (深蓝色)此时在溶液中,除SO42-和[Cu(NH3)4]2+外,几乎检查不出Cu2+的存在。
再如,在HgCl2溶液中加入KI,开始形成桔黄色HgI2沉淀,继续加KI过量时,沉淀消失,变成无色的溶液。
HgCl2 + 2KI ƒHgI2↓+ 2KCl HgI2 + 2KI ƒK2[HgI4]象[Cu(NH3)4]SO4和K2[HgI4]这类较复杂的化合物就是配合物。
配合物的定义可归纳为:由一个中心离子(或原子)和几个配体(阴离子或分子)以配位键相结合形成复杂离子(或分子),通常称这种复杂离子为配离子。
由配离子组成的化合物叫配合物。
在实际工作中一般把配离子也称配合物。
经研究表明,在[Cu(NH3)4]SO4中,Cu2+占据中心位置,称中心离子(或形成体);中心离子Cu2+的周围,以配位键结合着4个NH3分子,称为配体;中心离子与配体构成配合物的内界(配离子),通常把内界写在方括号内;SO 42-被称为外界,内界与外界之间是离子键,在水中全部离解。