高考领航2015届高考化学新一轮总复习 课时作业:17第五章第二讲.pptx
- 格式:pptx
- 大小:68.00 KB
- 文档页数:8
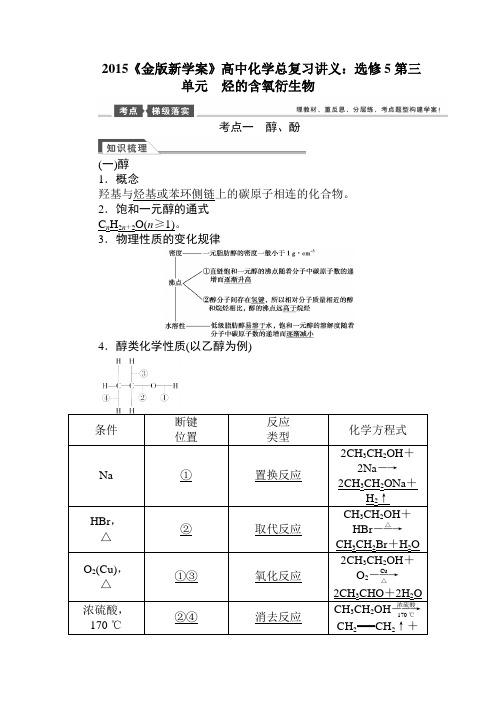
2015《金版新学案》高中化学总复习讲义:选修5第三单元烃的含氧衍生物考点一醇、酚(一)醇1.概念羟基与烃基或苯环侧链上的碳原子相连的化合物。
2.饱和一元醇的通式CnH2n+2O(n≥1)。
3.物理性质的变化规律4.醇类化学性质(以乙醇为例)条件断键位置反应类型化学方程式Na ①置换反应2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑HBr,△②取代反应CH3CH2OH+HBr――→△CH3CH2Br+H2O O2(Cu),△①③氧化反应2CH3CH2OH+O2――→Cu△2CH3CHO+2H2O 浓硫酸,170 ℃②④消去反应CH3CH2OH――→浓硫酸170 ℃CH2===CH2↑+CH3CH2OH+CH3COOH浓硫酸△CH3COOC2H5+H2O(二)酚1.苯酚的组成与结构2.物理性质(1)颜色状态:无色晶体,露置在空气中会因部分被氧化而显粉红色;(2)溶解性:常温下在水中溶解度不大,高于65 ℃时与水混溶;(3)毒性:有毒,对皮肤有强烈的腐蚀作用。
皮肤上不慎沾有苯酚应立即用酒精清洗。
3.化学性质(1)羟基中氢原子的反应①弱酸性电离方程式为:C6H5OH C6H5O-+H+,俗称石炭酸,但酸性很弱,不能使石蕊试液变红。
②与活泼金属反应与Na反应的化学方程式为:2C6H5OH+2Na―→2C6H5ONa+H2↑。
③与碱的反应加入NaOH溶液现象为:液体变澄清苯酚的浑浊液中――→再通入CO2气体现象为:溶液又变浑浊。
――→该过程中发生反应的化学方程式分别为:(2)苯环上氢原子的取代反应苯酚与浓溴水反应的化学方程式为:此反应常用于苯酚的定性检验和定量测定。
(3)显色反应苯酚跟FeCl3溶液作用显紫色,利用这一反应可以检验苯酚的存在。
(4)加成反应(5)氧化反应苯酚易被空气中的氧气氧化而显粉红色;易被酸性高锰酸钾溶液氧化;容易燃烧。
(6)缩聚反应◎思考与探究(1)其中属于脂肪醇的有哪些?属于芳香醇的有哪些?属于酚类的有哪些?(2)其中物质的水溶液显酸性的有哪些?(3)其中互为同分异构体的有哪些?(4)你能列举出⑤所能发生反应的类型吗?提示:(1)①②③⑤④⑤(2)④⑤(3)③④(4)取代反应,氧化反应,消去反应,加成反应,显色反应。





第五章 化学反应中的能量的转化第一节 化学反应与能量的转化梳理基础一、焓变与反应热1.焓变。
(1)焓(H ):描述物质所具有的________的物理量。
单位:________(或________)。
(2)焓变(ΔH ):反应________的总焓与________的总焓之差。
(3)焓变(ΔH )与反应热(Q )的关系。
对于等压条件下的化学反应,如果反应中物质的能量全部转化为________,则ΔH =________。
(4)表现形式:燃烧热、中和热、溶解热等。
(5)计算方法。
①ΔH =________物总能量-________物总能量; ②ΔH =________物总键能-________物总键能。
答案:1.(1)内能 kJ/mol kJ·mol -1 (2)产物 反应物(3)热能 Q p (5)①生成 反应 ②反应 生成2.化学反应的实质与特征。
1.了解化学反应中能量转化的原因,能说出常见的能量转化形式。
2.了解化学能与热能的相互转化。
了解吸热反应、放热反应、反应热等概念。
3.了解热化学方程式的含义,能用盖斯定律进行有关反应热的简单计算。
4.了解能源是人类生存和社会发展的重要基础。
了解化学在解决能源危机中的重要作用。
(1)实质:________断裂和________形成。
(2)特征:既有________生成,又有________的变化。
答案:2.(1)旧化学键 新化学键 (2)新物质 能量3.反应热。
(1)定义:在恒压条件下进行反应的________。
符号:______,单位:________或kJ·mol -1。
(2)产生原因。
吸收能量E 1↓反应物―――――――――→旧化学键断裂新化学键形成生成物⇒⎩⎨⎧ E 1>E 2, 反应,ΔH E 1<E 2, 反应,ΔH↓放出能量E 2答案:3.(1)热效应 ΔH kJ/mol (2)吸热 >0 放热 <0 (3)燃烧 化合 分解二、热化学方程式1.概念:表明反应所________或________热量的化学方程式。