动物源性食品中磺胺类药物残留量LCMSMS分析方法
- 格式:pdf
- 大小:1.76 MB
- 文档页数:5

动物组织中磺胺类抗生素残留量检测方法(二)3.4.1 控制液的配制 3.4.1.1 阴性控制液的配制:取2 mL组织阴性对比溶液(3.2.2.1),加入到6 mL MSU提取缓冲溶液(3.2.2.3)中制成阴性基准液,在室温下混合匀称,该基准液可在室温下放置不超过6h。
用于分析仪和试剂的性能监测。
3.4.1.2 阳性控制液的配制:取0.3mL 抗生素标准溶液(3.2.2.2),加6 mL组织阴性对比溶液(3.2.2.1),混匀后从中取2 mL溶液加入到6 mL MSU提取缓冲溶液(3.2.2.3)中制成阳性基准液,在室温下混合匀称,该基准液可在室温下放置不超过6h。
用于分析仪性能监测和阳性确认。
3.4.2 提取称取试样约10g(精确到0.1g)于50 mL离心管中,加入30 mL MSU提取缓冲液(3.2.2.3)。
于高速组织捣碎匀质器中匀质30s~60s。
然后将离心管放置在80℃±2℃的电热恒温器中,保温30 min后,将管取出放置在冰水浴中冷却10 min;于3300 r/min下离心10 min,倒出上清液,注重除去浮在表层的脂肪粒。
用M2缓冲液(3.2.2.3)或0.1mol/L调整提取液pH,每次加入300 uL M2缓冲液或0.1 mol/L盐酸直至pH达到7.5左右。
须要时取适量上清液用等体积举行脱脂。
提取液复原到室温后立刻举行受体分析。
3.4.3 测定 3.4.3.1 将一磺胺受体试剂(3.2.2.4)加入到硅硼酸盐玻璃试管中,用微量移液器加入300 uL水,置于旋涡振荡器上混匀10 s 将试剂溶解。
3.4.3.2 加入 4 mL 样品提取液(3.4.2)或阴性控制液(3.4.1.1)或阳性控制液(3.4.1.2)分离用于测试样本、阴性对比和阳性对比。
3.4.3.3 将一磺胺氘标志物试剂(3.2.2.5)加入试管,混合15 s,65℃±1℃温育3 min。

动物组织中磺胺类抗生素残留量检测方法(一)1 范围本标准规定了动物组织中磺胺类抗生素残留的发射免疫受体筛选测定办法。
本标准适用于动物(牛、猪、家禽和鱼虾等)组织中磺胺类抗生素残留的发射免疫受体筛选测定。
2 试样制备和保存 2.1 试样制备从混合原始样品中取出部分代表性样品,剔除脂肪组织后将可食部分放入搅拌器中绞碎,充分混匀,用四分法缩分出不少于500 g,均分两份,装入洁净容器内作为试样,加封并标明标志。
制样过程中必需防止样品受到微生物或化学物的污染或发生残留物含量的变幻。
2.2 试样保存样品于-18℃冷冻保存。
新奇或冷冻的组织样品可在2℃~6℃储藏72h。
3 测定办法 3.1 办法提要样品中的磺胺类抗生素残留经提取、稀释后与[3H]标志的互相竞争结合细菌细胞中的磺胺特异性受体。
在一定温度下举行竞争性结合反应后,将磺胺-受体复合物的沉淀重新用水溶解,加入闪耀液后测定[3H]衰变发出的R粒子发射性计数cpm(count per minute)。
液体闪耀计数仪测得的cpm与样品中磺胺残留量成反比。
3.2 试剂和材料 3.2.1 水,试验用水为重蒸馏水。
3.2.2 Charm Ⅱ竞争性受体结合组织磺胺测试试剂盒每批新试剂盒用法前须举行性能监测。
试剂盒主要由以下部分构成: 3.2.2.1 肉类组织阴性对比浓缩干粉,储藏于2℃~6℃。
用法时取浓缩干粉按标签配制成组织阴性对比溶液,此溶液可在2℃~6℃冰箱或冰浴中保存48 h,或可将所有或部分溶液保存于-15℃以下的冰箱中,用法时将其置于室温下解冻,解冻后的溶液在2℃~6℃冰箱或冰浴中保存24 h。
3.2.2.2 多种抗生素混合标准品干粉,含,储藏于2℃~6℃。
用法时按标签配制成抗生素标准溶液,浓度为1000 ug/L。
溶液的保存办法同3. 2.2.1。
3.2.2.3 缓冲液:包括肉类组织提取缓冲溶液(MSU提取缓冲液)干粉和调整pH值的M2缓冲液干粉,2℃~6℃储藏。



猪粪便沼液中多种抗生素残留量的LC—MSMS检测引言:
抗生素的广泛使用不仅在医学领域发挥了重要作用,也在农业领域发挥了重要作用,但是同时也带来了一系列问题,其中之一是抗生素在动物排泄物中的残留。
猪粪便沼液是农业领域中常见的肥料来源,其中可能含有多种抗生素残留。
为了保障人类健康和环境的安全,有必要对猪粪便沼液中多种抗生素残留的情况进行检测。
材料与方法:
1. 样品收集:从不同养殖场收集猪粪便沼液样品,尽量覆盖不同地区和养殖方式,确保样品的代表性。
2. 样品处理:将收集到的样品通过离心操作分离出沉淀物,然后通过过滤操作获得过滤液。
过滤液即为待测样品。
3. 标准品制备:购买市售的多种抗生素标准品,然后按照规定浓度配制成不同浓度的标准溶液。
4. 样品提取:将待测样品进行提取,常用的提取方法有液液萃取、固相萃取等。
本实验中选择固相萃取法提取待测样品中的抗生素残留物。
5. 分析仪器:使用液相色谱-串联质谱联用技术(LC-MS/MS)进行抗生素残留物的检测。
LC-MS/MS检测技术具有灵敏度高、选择性好、重复性好等优点,是目前常用的抗生素残留检测方法之一。
6. 数据分析:通过分析仪器产生的色谱图和质谱图,结合标准品的定量曲线,可以得到待测样品中抗生素残留物的浓度。
结果与讨论:
通过以上的实验步骤,我们可以获得猪粪便沼液中多种抗生素残留物的检测结果。
根据实验结果,我们可以评估不同养殖场的猪粪便沼液样品中抗生素残留的程度,进一步了解抗生素在农业领域的使用情况和可能对环境和人类健康带来的潜在风险。


LCMSMS农药一齐分析法简介:LC-MS/MS是一种基于液相色谱联用串联质谱的分析技术,广泛应用于农药残留监测领域。
它具有高灵敏度、高选择性和高效率的优点,可以实现多种目标物同时检测和定量。
LC-MS/MS农药一齐分析法的原理:该分析方法首先通过液相色谱将样品中的目标物进行分离,然后经过串联质谱仪的产物离子扫描模式进行检测和定量。
在这种分析方法中,每个目标物都有一个特定的质谱图,通过与事先建立的质谱库中的标准谱进行比对,可以确定每个目标物的含量。
方法的步骤:1.样品的制备:将样品加入适量的溶剂中,并通过固相萃取或液-液萃取等方法将目标物提取出来。
然后使用气相色谱或高效液相色谱等方法对提取物进行净化和预处理。
2.样品的进样:将制备好的样品注入液相色谱系统中,通过自动进样器进行进样。
3.液相色谱的分离:使用液相色谱系统进行目标物的分离。
选择合适的色谱柱和流动相进行优化,以达到理想的分离效果。
4.串联质谱的检测:将液相色谱分离得到的目标物进入串联质谱仪进行检测和定量。
在质谱检测中,使用多反应监测(MRM)模式进行目标物的筛选和定量。
5.数据处理和结果分析:使用专业的数据处理软件对得到的质谱数据进行处理和分析,计算出每个目标物的浓度,并与质谱库中的标准谱进行比对确定目标物的含量。
LC-MS/MS农药一齐分析法的优点:1.高灵敏度:LC-MS/MS技术可以在低浓度下检测和定量目标物,其灵敏度通常比传统的色谱方法高几个数量级。
2.高选择性:通过质谱仪的选择离子模式和多反应监测模式,可以有效地排除样品中的干扰物,提高分析的选择性。
3.高效率:LC-MS/MS技术可以实现多种目标物的一齐分析,大大提高分析效率和样品通量。
4.宽线性范围:LC-MS/MS技术的线性范围通常较宽,可以适应不同浓度范围内目标物的测定需求。
总结:LC-MS/MS农药一齐分析法是一种高效、高灵敏度和高选择性的分析技术,在农药残留监测和食品安全领域具有重要的应用价值。
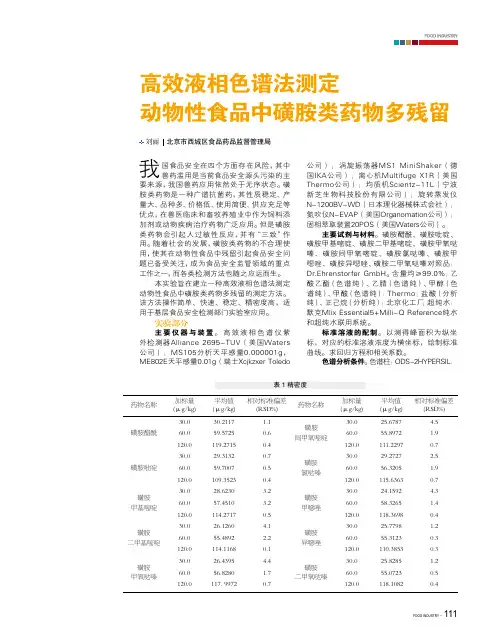
高效液相色谱法测定动物性食品中磺胺类药物多残留 刘丽 北京市西城区食品药品监督管理局我国食品安全在四个方面存在风险,其中兽药滥用是当前食品安全源头污染的主要来源,我国兽药应用依然处于无序状态。
磺胺类药物是一种广谱抗菌药,其性质稳定、产量大、品种多、价格低、使用简便、供应充足等优点,在兽医临床和畜牧养殖业中作为饲料添加剂或动物疾病治疗药物广泛应用。
但是磺胺类药物会引起人过敏性反应,并有“三致”作用。
随着社会的发展,磺胺类药物的不合理使用,使其在动物性食品中残留引起食品安全问题已备受关注,成为食品安全监管领域的重点工作之一,而各类检测方法也随之应运而生。
本实验旨在建立一种高效液相色谱法测定动物性食品中磺胺类药物多残留的测定方法。
该方法操作简单、快速、稳定、精密度高,适用于基层食品安全检测部门实验室应用。
实验部分主要仪器与装置。
高效液相色谱仪紫外检测器Alliance 2695-TUV(美国Waters 公司);MS105分析天平感量0.000001g,ME802E天平感量0.01g(瑞士Xcjkzxer Toledo 公司);涡旋振荡器MS1 MiniShaker(德国IKA公司);离心机Multifuge X1R(美国Thermo公司);均质机Scientz-11L(宁波新芝生物科技股份有限公司);旋转蒸发仪N-1200BV-WD(日本理化器械株式会社);氮吹仪N-EVAP(美国Organomation公司);固相萃取装置20POS(美国Waters公司)。
主要试剂与材料。
磺胺醋酰、磺胺吡啶、磺胺甲基嘧啶、磺胺二甲基嘧啶、磺胺甲氧哒嗪、磺胺间甲氧嘧啶、磺胺氯哒嗪、磺胺甲噁唑、磺胺异噁唑、磺胺二甲氧哒嗪对照品:Dr.Ehrenstorfer GmbH。
含量均≥99.0%;乙酸乙酯(色谱纯)、乙腈(色谱纯)、甲醇(色谱纯)、甲酸(色谱纯):Thermo;盐酸(分析纯)、正己烷(分析纯):北京化工厂;超纯水:默克Mlix Essential5+Milli-Q Reference纯水和超纯水联用系统。

T logy科技分析与检测磺胺类药物作为一种合成的抗菌药物,其对于治疗禽畜细菌性疾病有着较好的效果。
但是在禽畜养殖期间,长期使用磺胺类药物,会在禽畜体内发生堆积,食用有磺胺类药物残留的动物性食品,会对人的健康造成危害,因此,要采取合理的方式对动物性食品中磺胺类药物的残留情况进行 检测。
1 磺胺类药物的危害人如果食用含有磺胺类药物的食物,药物则会在人的身体内发生积累,将会损伤泌尿系统,导致人体内血小板减少,出现过敏反应等,同时,还会致使细菌出现耐药性等。
目前,我国已经将磺胺类药物列为了动物养殖期间的限制使用药物,明确规定磺胺类药物的残留量不得超过 0.1 mg/kg。
2 动物性食品中磺胺类药物残留的原因2.1 没有依据规定生产药物现代一些饲料、药厂企业在实际经营期间,违背了《兽药管理条例》中的相关规定。
在标签中应当对兽药中的关键成分,以及具体含量情况进行明确标识,但是,商检发现,药物生产厂家受利益驱使,并未对这些内容进行明确,从而导致部分养殖者滥用药物,不规范用药,导致动物性食品中药物残留过高[1]。
2.2 未严格依据规范用药养殖户为了获取更高的经济效益,经常会滥用药物,这也是导致动物性食品中磺胺类药物残留过高的主要原因。
养殖者为了提高经济效益,在屠宰畜禽时,会通过给畜禽服用药物的方式,对畜禽出现的一些临床症状进行掩盖,并未严格的依据休药规定用药,这也是造成动物性食品中药物残留过高的一项关键原因。
3 检测动物性食品中磺胺类药物残留的方法3.1 实验室检测磺胺类药物残留3.1.1 毛细管电泳分析法该方法是在高压直流电的作用下,让食物样品依据电性在石英毛细管中分离,从而完成检测的一种方法。
该方法在具体应用过程中消耗的试剂和样品都较少,具有较高的经济效益,并且有着较高的分离效率,能够实现对不同种药物残留的同时检测[2]。
例如,在实际检测过程中,将毛细血管电泳法与质谱法进行联合应用,通过该方法完成对肉类样品中磺胺类药物残留情况的检测,该方法在具体应用过程中的检测上限能够达到10 μg/L,精度高,能够满足检测需求。


磺胺类药物在动物性食品中的残留与检测核心提示:摘要:磺胺类药物是一类广谱抗菌药,临床上主要用于预防和治疗细菌感染性疾病,还常作为饲料添加剂在动物生产中长期应用。
然而,磺胺药会引起人过敏性反应,且可能有致癌性。
因此,磺胺类药物的不合理使用,使其在摘要:磺胺类药物是一类广谱抗菌药,临床上主要用于预防和治疗细菌感染性疾病,还常作为饲料添加剂在动物生产中长期应用。
然而,磺胺药会引起人过敏性反应,且可能有致癌性。
因此,磺胺类药物的不合理使用,使其在动物性食品中残留引起生态环境污染和人类健康危害的潜在威胁已倍受关注。
因此,研究出一种操作简便、快速、灵敏的磺胺类药物残留检测方法,对于畜产品的安全具有实际意义。
酶联免疫吸附法(ELISA)作为一种免疫学检测技术不仅具有上述优点,而且准确性好、特异性强、检测成本低,还可用于大批量样品的检测。
而单抗在试剂的标准化及抗体的大量供应上明显优于多抗,所以单克隆抗体技术的应用在药残检测上是主要的发展方向。
关键词:磺胺;动物性食品;残留;免疫学;检测磺胺类药物(sulfnaides ,SAs)是一类具有对氨基苯磺酰胺结构的化学治疗药物,是畜禽抗感染治疗中使用的重要药物之一。
SAs的作用机理是干扰细菌酶系统对氨基苯甲酸(PABA)的利用,影响细胞核蛋白质的合成,抑制细菌的繁殖。
其抗菌谱广,能抑制大多数革兰氏阳性菌和阴性菌。
因具有性质稳定、价格低廉、使用方便,联合抗菌增效剂效果可提高数倍,常以亚治疗浓度的药物做为饲料添加剂来预防疾病的发生,提高饲料的转化率,促进动物生长,常用的SAs有十几种。
但不合理的使用会造成过敏、脑神经损害,耐药菌株增加等危害。
为了保证食品安全,欧盟对牛奶和肉类食品中的磺胺类药物制定了最高允许量,即单个磺胺类药物的浓度不得超过25 μg/kg,磺胺类药物总量不得超过100 μg/kg[1]。
1 SAs性质概述1.1 理化性质磺胺类药物的母核结构式如图1,N1含有磺酰胺基,有弱酸性。
色谱法检测动物源食品中磺胺类药物残留研究进展作者:龙举李佩佩龙位等来源:《安徽农业科学》2015年第26期摘要磺胺类药物是一类可限量使用于水产养殖和畜禽业的广谱高效抗菌药物,且被广泛应用。
磺胺类在动物源性食品中会有残留,通过任何途径摄入磺胺都有可能在人体内蓄积而对人造成危害。
目前,动物源性食品中磺胺类药物多残留的定量检测主要有高效液相色谱法(HPLC)以及高效液相串联质谱法(HPLCMSMS)。
色谱法检测磺胺类药物的主要步骤为提取、浓缩、净化和进色谱柱分析。
简要综述了色谱法检测动物源食品中磺胺类药物的方法研究进展,以期为动物源性食品中磺胺类药物多残留检测提供参考。
关键词磺胺类;残留;检测;动物源食品;高效液相色谱;质谱中图分类号S851.34+7文献标识码A文章编号0517-6611(2015)26-330-03磺胺类药物(Sulfonamides,SAs)是指具有对氨基苯磺酰胺结构的一类药物的总称,被广泛应用于水产养殖和畜禽业,主要作为化学治疗药物用于预防和治疗细菌感染性疾病[1]。
磺胺类药物有较广的抗菌谱,对大多数革兰氏阳性菌、革兰氏阴性菌的抑制作用明显[2]。
可限量使用的磺胺类药物是目前水产养殖业中最常使用的抗生素之一,多用于养殖类水生生物的烂鳃病、肠炎病、弧菌病、疖疮病、细菌性败血病等。
在生物体内,磺胺类药物有着比较长的作用时间和代谢时间,通过食物链等途径摄入的磺胺类药物都有可能蓄积在人体内并富集,磺胺二甲嘧啶等甚至有引起潜在致癌性的可能[3]。
人类造血系统会遭受磺胺类药物残留的破环,从而引发粒细胞缺乏症、血小板减少症、溶血性贫血症等[4];磺胺类药物残留也会引起人体过敏反应,轻则出现荨麻诊或皮肤瘙痒,严重时则引起血管性水肿,甚至导致死亡[5]。
世界上一些地区或国家对动物源性食品中的磺胺类药物最高残留限量要求不断提高[6],欧盟、美国等地区或国家规定了动物源性食品中单个磺胺以及总磺胺的最高残留限量(MRLs)为100 μg/kg,而潜在致癌的磺胺二甲基嘧啶(SM2)最高残留限量(MRLs)为25 μg/kg[7]。
动物源性食品中氯霉素类药物残留量的测定1. 引言1.1 研究背景动物源性食品中的氯霉素类药物残留一直是一个备受关注的问题。
氯霉素类药物是一类广泛应用于动物兽药中的抗菌药物,其在畜禽养殖中被广泛使用以预防和治疗各种疾病。
长期过量使用氯霉素类药物可能导致其在动物体内残留过多,进而通过动物食物链传播到人类食品中,对人体健康造成潜在风险。
近年来,随着人们对食品安全和质量的重视,检测动物源性食品中氯霉素类药物残留量的需求逐渐增加。
当前的检测方法主要是基于高效液相色谱-质谱联用技术(HPLC-MS/MS)或气相色谱-质谱联用技术(GC-MS/MS),这些方法具有高灵敏度、高选择性和高准确性,可以有效地检测动物源性食品中微量的氯霉素类药物残留。
本研究旨在深入探讨动物源性食品中氯霉素类药物残留量的测定方法及技术,为相关检测工作提供参考和支持。
通过分析检测结果和提出建议,希望能够为今后的研究和监管工作提供一定的指导和借鉴。
部分结束。
1.2 研究目的本研究的目的是为了建立一种准确、快速、简便的方法来测定动物源性食品中氯霉素类药物残留量,以保障人们的食品安全和健康。
当前,氯霉素类药物在畜禽养殖中的广泛应用,容易导致其在动物体内残留并通过食品链进入人体,对人体健康产生潜在威胁。
有必要对动物源性食品中氯霉素类药物残留量进行有效监测和控制。
本研究旨在探讨氯霉素类药物在动物源性食品中的危害程度,分析氯霉素类药物残留的检测方法及技术,在此基础上建立一种可靠的氯霉素类药物残留量测定技术,并探讨其在实际监测中的应用及意义。
通过本研究的开展,旨在为提高食品安全水平、促进食品监管工作的科学化和规范化提供参考和支撑。
2. 正文2.1 氯霉素类药物简介氯霉素(Chloramphenicol)是一种广谱抗生素,能够抑制细菌的蛋白质合成,因其广谱性和毒力适中而广泛应用于兽医学和临床医学领域。
氯霉素类药物包括氯霉素、磺胺类药物等,它们在动物源性食品中的残留问题备受关注。
高效液相色谱-串联质谱法检测虾中9种磺胺类药物的残留目的:建立虾中9种磺胺类抗生素残留的高效液相色谱-串联质谱同时测定方法。
方法:样品经乙腈提取,经脱脂、净化、浓缩后,以A相为甲醇、B相0.50 mmol/L乙酸铵溶液为流动相,采用HPLC-MS/MS多反应监测(MRM)正离子模式测定。
结果:9种磺胺类药物在0~100 ng/ml范围内线性关系良好(γ>0.999 0),加标回收率为75.3%~95.6%,相对标准偏差(RSD)为4.5%~13.5%。
结论:该方法准确、可靠、灵敏度好,适用于磺胺类药物残留的检测。
[Abstract] Objective: To develop the method for the simultaneous determination of 9 sulfonamides (SAs) residues in shrimps by high performance liquid chromatography and tandem mass spectrometry (HPLC-MS/MS). Methods: The sample was extracted with acetonitrile, defatted and purified and then concentrated by evaporation. The 9 analytes were separated with a mobile phase composed of methanol and 0.50 mmol/L aqueous ammonium acetate solution. The mass spectrometer was operated using multiple reaction monitoring (MRM). Results: The 9 drugs showed good linear correlation in the range of 0-100 ng/ml (γ>0.999 0). The average recovery rate was 75.3% to 95.6% at two concentration levels. The relative standard deviation was 4.5% to 13.5%. Conclusion: The results indicate that the HPLC-MS/MS assay is accurate, reliable, and sensitive, thus it is suitable for the determination of SAs in aquatic products.[Key words] High performance liquid chromatography-tandem mass spectrometry (HPLC-MS/MS); Sulfonamides; Drug residue; Shrimp磺胺类药物(SAs)是具有对氨基苯磺酰胺结构的一类药物的总称,是常用的广谱抗生素。
51一、背景磺胺类药物(Sulfonamides,SAs)是指一类具有对氨基苯磺酰胺结构、用于预防和治疗细菌感染性疾病的化学药物,是当前畜禽生产中常用的抗菌、抗原虫药物,具有抗菌谱广、价格低、化学性质稳定、使用方便等优点。但是摄入大量磺胺类药物会破坏正常免疫机能,破坏人的造血系统,造成溶血性贫血症、粒血细胞缺乏症等症状。并且人体长期摄入含磺胺类药物的动物性食品后,药物不断在人体内蓄积,当积累到一定程度后,就会对人体产生毒性作用,同样可引起肾损害,所以针对磺胺类药物的监控是一项刻不容缓的工作。
目前关于磺胺类药物的标准已出台《GB/T 20759-2006 畜禽肉中十六种磺胺类药物残留量的测定 液相色谱-串联质谱法》、《GB/T 21316-2007动物源性食品中磺胺类药物残留量的测定 高效液相色谱-质谱-质谱法》,方法中涉及肌肉、内脏、鱼、虾和肠衣、牛奶中磺胺脒、甲氧苄啶、磺胺醋酰、磺胺嘧啶等几十种磺胺类药物的前处理方法及液质检测方法。本文中将详细介绍采用AB SCIEX API 4000™ LC-MS/MS检测磺胺类药物分析10种磺胺类药物,并且经实验证实AB SCIEX API 4000+™、4000 QTRAP®、API 5000™以及TRIPLE
QUAD™ 5500、QTRAP® 5500同样适用与该方法。
二、化合物信息
动物源性食品中磺胺类药物残留量LC-MS/MS分析方法
表1. 化合物基本信息化合物 英文通用名 分子量 CAS 分子式磺胺嘧啶 Sulfadiazine 250.3 68-35-9 C
10H10N4O2
S
磺胺吡啶 Sulfapyridine 249.3 144-83-2 C
11H11N3O2
S
磺胺噻唑 Sulfathiazole 255.3 72-14-0 C
9H9N3O2S2
磺胺甲基嘧啶 Sulfamerazine 264.3 127-79-7 C
11H12N4O2
S
磺胺二甲嘧啶 Sulfadimidine 278.3 57-68-1 C
12H14N4O2
S
磺胺甲氧哒嗪 Sulfamethoxypyridazine 280.3 80-35-3 C
11H12N4O3
S
磺胺间二甲氧嘧啶 Sulfadimethoxine 310.3 155-91-9 C
12H14N4O4
S
磺胺氯达嗪 Sulfachlorpyridazine 284.7 80-32-0 C
10H9ClN4O2
S
磺胺邻二甲氧嘧啶 Sulfadoxine 310.3 2447-57-6 C
12H14N4O4
S
磺胺甲基异恶唑 sulfamethoxazole 253.3 723-46-6 C
10H11N3O3
S
磺胺苯吡唑 Sulfaphonazole 314.4 526-08-9 C
15H14N4O2
S
三、前处理方法(GB/T21311-2007)3.1提取3.1.1 肌肉、内脏、鱼虾和肠衣称取2 g(精确至0.01 g)试样置于玻璃研钵内,再称取约6 g(精确至0.01 g)C18填料加至试样上用玻璃杵轻轻研磨,使样品与填料混合均匀(色泽均一,状态分散),装于50 mL具螺旋盖聚四氟乙烯离心管中,加入25 mL乙腈-水溶液,涡旋振荡1 min,放入家用微波炉中在光波模式下微波辐照30 s,3000 r/min离心5 min,将乙腈层移入100 mL棕色分液漏斗中。离心后的沉淀物再加入25 mL乙腈摇匀,微波辅助提取30 s,3000 r/min离心5 min,合并已经提取液,待净化。
动物源性食品中磺胺类药物残留量LC-MS/MS分析方法52
3.1.2 牛奶称取2 g(精确至0.01 g)试样置于玻璃研钵内,加入6 g(精确至0.01 g)硅藻土,另加入6 g(精确至0.01 g)C18填料,用玻璃杵轻轻研磨30 s,使样品与填料混合均匀(色泽均一,状态分散),装于50 mL具螺旋盖聚四氟乙烯离心管中,加入25 mL乙腈-水溶液,涡旋振荡1 min,放入家用微波炉中在光波模式下微波辐照30 s,3000 r/min离心5 min,将乙腈层移入100 mL棕色分液漏斗中。离心后的沉淀物再加入25 mL乙腈摇匀,微波辅助提取30 s,3000 r/min离心5 min,合并已经提取液,待净化。
3.2净化提取液中加入25 mL乙腈饱和正己烷溶液,振摇5 min,将底层乙腈溶液移入150 mL棕色鸡心瓶中,加入10 mL正丙醇,用旋转蒸发仪于45℃水浴中加压蒸发至近干,氮气流吹干,准确加入1 mL乙腈-水溶液,超声30 s溶解残渣,将溶解液移入10 mL棕色离心管中,加入0.5 mL乙腈饱和正己烷,涡旋振荡2 min,于3000 r/min离心5 min,弃去正己烷溶液,取底层乙腈-水溶液过0.22 µm微孔滤膜后,供高效液相色谱-质谱/质谱测定。
四、实验方法4.1液相条件色谱柱:Agilent Zorbax Eclipse XDB-C18, 3.0×100mm, 3.5 µm;柱温:40℃,流速:300 µL/min;流动相:A:水(含1mM甲酸铵及0.1%甲酸),B:乙腈;梯度洗脱,洗脱条件见表2: 表2. 液相色谱条件时间(min) 流速( µL/min) A(%) B(%) 0 300 90 10 2.5 300 10 90 4.8 300 10 90 4.9 300 90 10 10 300 90 10
4.2质谱条件离子源:Turbo V™ 离子源;扫描模式:正离子;采集模式:多反应监测MRM;表3. 磺胺类药物代谢物MRM离子对
化合物名称 母离子 定量子离子 定性子离子 扫描模式磺胺氯哒嗪 285 156 108 正离子磺胺嘧啶 251 156 108 正离子磺胺甲基异恶唑 254 156 108 正离子磺胺噻唑 256 156 108 正离子磺胺甲基嘧啶 265 156 172 正离子53
动物源性食品中磺胺类药物残留量LC-MS/MS分析方法磺胺邻二甲氧嘧啶 311 156 108 正离子磺胺吡啶 250 156 184 正离子磺胺甲氧哒秦 281 156 108 正离子磺胺二甲嘧啶 279 124 186 正离子磺胺苯吡唑 315 156 222 正离子磺胺间二甲氧嘧啶 311 156 108 正离子
五、定量质谱数据5.1化合物保留时间及灵敏度
表4. 各化合物色谱图中保留时间及对应浓度信噪比化合物名称 检测离子对(m/z) 保留时间(min) 浓度(ng/mL) 信噪比*
磺胺氯哒嗪 285/156 4.00 0.001 6.3
磺胺嘧啶 251/156 3.57 0.002 12.9
磺胺甲基异恶唑 254/156 4.07 0.001 5.9
磺胺噻唑 256/156 3.58 0.001 12.6
磺胺甲基嘧啶 265/156 3.75 0.001 12.8
磺胺邻二甲氧嘧啶 311/156 4.07 0.001 53.1
磺胺吡啶 250/156 3.68 0.001 19.5
磺胺甲氧哒嗪 281/156 3.92 0.001 13.8
磺胺二甲嘧啶 279/186 3.87 0.001 14.9
磺胺苯吡唑 315/158 4.24 0.001 13.6
磺胺间二甲氧嘧啶 311/156 4.23 0.001 75.4
*:信噪比按照3倍标准偏差计算。
图1. 磺胺类药物色谱峰54
在标准《GB/T 21316-2007动物源性食品中磺胺类药物残留量的测定 高效液相色谱-质谱-质谱法》中规定该方法磺胺类药物的最低残留量为10 µg/kg,在本实验中完全能够满足检测要求。
5.2重现性数据
图2. 化合物灵敏度及对应空白色谱图
图3. 添加基质样品连续采集7针得到对应峰面积图3中以磺胺氯达嗪为例,添加基质样品在方法LOQ浓度下连续采集7次,得到方法相对标准偏差CV%。图4中以部分化合物为例,列举磺胺类药物检测方法的标准偏差。可以看到化合物的CV%均小于5%,满足方法中“在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的15%”要求。55
图4. 连续7针得到的相对标准偏差六、结论6.1 采用AB SCIEX API 4000™灵敏度完全可满足磺胺类药物在动物源性食品安全法规要求;6.2 AB SCIEX API 4000™可精确定量分析,特别是在分析复杂基质样品中磺胺类药物时,实验结果可看到低浓度同样具有良好的重现性以及准确性;
动物源性食品中磺胺类药物残留量LC-MS/MS分析方法