凯基抗酒石酸酸性磷酸酶染液试剂盒
- 格式:pdf
- 大小:173.10 KB
- 文档页数:3

碱性磷酸酶(ALP)测定试剂盒(NPP底物-AMP缓冲液法)适用范围:本试剂盒用于体外定量测定人血清中的碱性磷酸酶(ALP)的活性。
1.1包装规格1.2主要组成成分试剂1主要组分:AMP缓冲液 42 0mmol/L试剂2主要组分:4-硝基苯磷酸二钠 56mmol/L2.1外观2.1.1试剂1应为无色或淡黄色透明溶液,无混浊,无未溶解物。
2.1.2试剂2应为无色或淡黄色透明溶液,无混浊,无未溶解物。
2.2装量液体试剂的净含量应不少于标示值。
2.3试剂空白2.3.1试剂空白吸光度:ALP试剂盒在波长395~415nm处测定试剂的空白吸光度值,应不大于0.8。
2.3.2试剂空白吸光度变化率:ALP试剂盒在波长395~415nm处测定试剂的空白吸光度变化率,应不大于0.0050。
2.4分析灵敏度测试120U/L碱性磷酸酶时,吸光度变化率应不小于0.01。
2.5准确度用本公司ALP试剂盒和已上市ALP试剂盒同时测定40个临床样本,相关系数r2应不小于0.95,在[20,100]U/L区间内,线性绝对偏差应不超过±10U/L;在(100,800]U/L区间内,线性相对偏差应不超过±10%。
2.6精密度2.6.1重复性重复测试(120±12)U/L的样本,所得结果的变异系数CV应不大于5%;2.6.2批间差测试(120±12)U/L的样本,所得结果的批间相对极差应不大于10%。
2.7线性范围ALP试剂盒在[20,800]U/L范围内,线性相关系数(r)应不小于0.990;在[20,100]U/L区间内,线性绝对偏差应不超过±10U/L;在(100,800]U/L区间内,线性相对偏差应不超过±10%。
2.8稳定性原包装的ALP试剂盒在2℃~8℃避光保存,有效期为12个月。
在ALP试剂盒有效期满后2个月内,分别检测2.1、2.3、2.4、2.5、2.6.1、2.7项,结果应符合各项目的要求。

7-AAD染色试剂盒凯基7-AAD染色试剂盒(Cell Apoptosis 7-AAD Detection Kit)Cat number:KGA For Research Use OnlyStore at4℃for one yearExpire date:A.试剂盒说明7-AAD (7-amino-actinomycin D)是一种核酸染料,它不能通过正常质膜,随着细胞凋亡、细胞死亡过程,质膜对7-AAD的通透性逐渐增加,结合细胞凋亡中DNA的有控降解,在合适波长激发光的激发下可发出明亮的红色荧光,通过7-AAD标记DNA的强弱,将细胞分为三群:7-AAD强为死亡细胞,7-AAD弱是凋亡细胞,7-AAD-为正常活力细胞。
7-AAD同PI 有着相似的荧光特性,但其发射波谱较PI窄,对其他检测通道的干扰更小,在多色荧光分析中是PI 的最佳替代品,可与Annexin V-EGFP/FITC/PE联合使用。
本试剂盒适用于培养的细胞染色,可应用于荧光显微镜、激光共聚焦计或流式细胞仪检测。
二、储存条件组分KGA219(100 assays)7-AAD染液0.5 mL 4℃,避光10×Assays Buffer 5 mL4℃1×10倍。
三、试剂盒以外自备仪器和试剂流式细胞仪、激光共聚焦或荧光显微镜:激发波长546nm,发射波长647 nm微量移液器、1.5m L Microtube、载玻片四、使用注意事项1.微量试剂取用前请离心集液。
2.7-AAD避光保存及使用。
3.7-AAD为潜在致癌物,操作时请采取防护措施,穿防护服、戴手套等。
4.本试剂盒适用于检测活细胞,流式细胞仪检测时,细胞数量不以应低于1×105,,不推荐用于检测组织样本。
五、操作方法1.悬浮细胞离心(2000rpm离心5min)收集;贴壁细胞用胰酶消化收集用PBS洗涤细胞二次(2000rpm离心5min)收集1~5×105细胞;2.加入5μL 7-AAD染液,混匀;室温、避光、反应5~15min;3.加入500μL的1×Assays Buffer悬浮细胞;4.请在1 hour内,进行下述荧光显微镜或流式细胞仪的观察和检测。

土壤碱性磷酸酶活性测定试剂盒使用说明货号:BC0280规格:50T/48S产品简介:土壤磷酸酶是一类催化土壤有机磷化合物矿化的酶,其活性的高低直接影响着土壤中有机磷的分解转化及其生物有效性,是评价土壤磷素生物转化方向与强度的指标。
土壤磷酸酶受到土壤碳、氮含量、有效磷含量和pH显著影响。
通常按照其最适pH范围,分为碱性、中性和酸性三种类型磷酸酶。
碱性环境中,S-AKP/ALP催化磷酸苯二钠水解生成苯酚和磷酸氢二钠,通过测定酚的生成量即可计算出S-AKP/ALP活性。
产品内容:试剂一:液体×1瓶,4℃避光保存。
试剂二:粉剂×1瓶,4℃保存。
用前加50mL蒸馏水充分溶解。
试剂三:液体×1瓶,4℃保存。
试剂四:粉剂×1瓶,4℃避光保存。
临用前加1152μL无水乙醇(自备),48μL蒸馏水充分溶解。
(变褐色后不能再使用)标准品:液体×1瓶,0.5μmol/mL苯酚标准液,4℃保存。
操作步骤:催化反应:称取风干混匀土壤约0.1g,加入0.05mL甲苯(自备),轻摇15min;加0.4mL试剂一并且摇匀后,置于37℃恒温培养箱,开始计时,催化反应24h;到时后迅速加入1mL试剂二充分混匀,以终止酶催化的反应。
10000rpm室温离心10min,取上清液置于冰上待测。
显色反应:1.分光光度计预热30min以上,调节波长到660nm,蒸馏水调零。
2.空白管:取1mL玻璃比色皿,加入50μL蒸馏水,100μL试剂三,20μL试剂四,充分混匀,显色后再加蒸馏水830μL,混匀后室温静置30min,于660nm测定吸光度,记为A空白管。
3.标准管:取1mL玻璃比色皿,加入50μL标准液,100μL试剂三,20μL试剂四,充分混匀,显色后再加蒸馏水830μL,混匀后室温静置30min,于660nm测定吸光度,记为A标准管。
4.测定管:取1mL玻璃比色皿,加入50μL上清液,100μL试剂三,20μL试剂四,充分混匀,显色后再加蒸馏水830μL,混匀后室温静置30min,于660nm测定吸光度,记为A测定管。


2019-2020学年湖南省四校高三(下)联考生物试卷(2月份)副标题题号一二总分得分一、单选题(本大题共6小题,共6.0分)1.抗酒石酸酸性磷酸酶(TRACP)是一种含铁蛋白,在破骨细胞和活化的吞噬细胞中表达。
测定血清中TRACP浓度,有助于了解骨代谢状况。
下列相关叙述正确的是()A. 可用双缩脲试剂来检测破骨细胞中TRACP的氨基酸含量B. 重金属盐作用可直接使TRACP的氨基酸排列顺序发生改变C. TRACP基因及相关mRNA只存在于吞噬细胞、破骨细胞中D. 细胞中内质网、高尔基体的参与使TRACP具有特定的功能2.因发现控制“昼夜节律”分子机制,三位美国科学家获诺贝尔生理学奖。
PER、TIM基因是控制生命体昼夜节律的基因,PER基因编码的蛋白质在细胞核中夜间累积,而白天降解。
下列叙述错误的是()A. PER蛋白是大脑皮层作为自动节律性中枢选择性表达的产物B. 细胞核的核孔对于通过的物质既有大小限制也有选择透过性C. 若抑制TIM蛋白的合成,则PER蛋白不能在细胞核中积累D. PER蛋白的含量升高抑制PER基因的表达实现生物节律性3.下列关于生命活动调节与人体内环境及稳态关系的叙述,正确的是()A. 内环境中的血浆、淋巴、组织液等成分稳定→机体达到稳态B. 饮水不足,内环境渗透压升高,抗利尿激素增加→机体稳态失调C. 组织细胞的代谢活动减弱时→生成与回流的组织液中CO2的含量相等D. 注射等渗透压的5%的葡萄糖溶液→血浆中胰岛素/胰高血糖素的比值增大4.免疫系统通过多个检查点或“免疫刹车”来避免免疫系统的过度激活,CTLA4和PD-1是T细胞上的两个重要的检查点。
CTLA4检查点的功能(阻止T细胞被激活)类似于不让汽车发动起来,而PD-1检查点的功能(抑制T细胞的活性)类似于让跑动的汽车停下来。
下列有关说法错误的是()A. CTLA4检查点和PD-1检查点对T细胞的作用机理不同B. CILA4检査点和PD-1检查点的存在能一定程度上避免引起自身免疫性疾病C. 通过调节免疫细胞活性的免疫检查点疗法治疗癌症无副作用D. 机体对癌细胞进行特异性免疫主要通过T细胞来完成5.2022年北京冬奥会吉祥物“冰墩墩”,大熊猫是其设计原型。

碱性磷酸酶(ALP)测定标准操作程序1.摘要碱性磷酸酶(ALP)存在于成骨细胞、干细胞、白细胞、肾、脾、胎盘、前列腺和小肠内。
测定血清或肝素化血浆中的碱性磷酸酶活力,做临床辅助诊断用。
2.适用范围程序适用于日立7600自动生化分析仪检测血清、血浆中碱性磷酸酶(ALP)的活力。
3.职责使用日立7600自动生化分析仪进行测定碱性磷酸酶(ALP)活力的工作人员要严格按照本SOP程序进行,室负责人监督管理;本SOP的改动,可由任一使用本SOP的工作人员提出,并报经生化室负责人、科主任签字批准生效。
4.检测方法上海科华生物工程股份有限公司生产的碱性磷酸酶(ALP)试剂盒采用的是AMP缓冲液法。
5.原理在AMP的缓冲环境下,磷酸对硝基苯在碱性磷酸酶的作用下,可以水解成磷酸盐和对硝基苯酚。
在一定底物浓度范围内,磷酸对硝基苯的水解产物对硝基苯酚会引起405nm处吸光度的上升,其上升速率与血清中碱性磷酸酶的活力成正比。
−→−+OH−−磷酸盐对硝基苯酚磷酸对硝基苯碱性磷酸酶+26.仪器日立7600自动生化分析仪7.试剂7.1试剂来源:上海科华生物工程股份有限公司提供7.2试剂瓶内主要成分:R1:AMP缓冲液(PH10.50)、乙酸镁;R2:AMP缓冲液(PH8.85)、磷酸对硝基苯、乙酸镁。
AMP:2-氨基-2-甲基-1-丙醇7.3试剂稳定性:试剂在2-8℃避光保存,有效期1年。
试剂工作液在2-8℃避光保存,可稳定4周,15-25℃可保存稳定4天。
7.4试剂准备:试剂为即用式。
8.标准品和质量控制8.1校准程序:使用某某公司提供的标准品对自动分析仪进行校准。
按照公司标准品使用要求,并以9g/L氯化钠溶液或去离子水为空白,经校准测定,仪器自动对标准品响应量通过合适的数学模型绘制校准曲线。
8.2质控品某某公司提供的生化复合定值质控血清做为室内质控品。
每日在测定前做一次质控。
该质控品为干粉包装,在2-8℃冰箱可稳定到失效期,使用前用5ml去离子水复溶,待质控物充分溶解(大约30分钟)后使用。


绝经后骨质疏松症相关骨代谢指标的分析杨立顺;袁海生;沈兴娅;康建华;王艾云【摘要】目的观察调控破骨细胞活性的主要因子和骨吸收及骨形成标志物在绝经后骨质疏松症(PMOP)患者体内水平的变化,为临床早期防治骨质疏松提供依据.方法测定38例PMOP患者、50例骨量减低患者及94名绝经后骨量正常者(正常对照组)血清骨保护素(OPG)、核因子-kβ受体活化因子配体(RANKL)、骨源性碱性磷酸酶(BAP)、血清抗酒石酸酸性磷酸酶(TRACP)-5b、雌二醇(E2)、血浆同型半胱氨酸(Hcy)水平.剔除年龄、E2因素后对部分指标进行偏相关分析;对所有指标进行独立危险因素分析及二分类Logistic回归分析;采用受试者工作特征(ROC)曲线评价诊断准确度.结果 PMOP组、骨量减低组与正常对照组之间E2、Hcy、OPG、RANKL、TRACP-5b、BAP水平差异有统计学意义(P<0.05、P<0.01、P<0.001);PMOP组BAP水平明显高于骨量减低组及正常对照组(P<0.001),E2水平则明显低于骨量减低组(P<0.001)及正常对照组(P<0.05).正常对照组与骨量减低组之间E2、BAP水平无明显差异(P>0.05).控制年龄因素后,E2与TRACP-5b、BAP呈负相关[r值分别为-0.198(P=0.007)、-0.157(P=0.035)];控制年龄、E2因素后,Hcy与RANKL、TRACP-5b、BAP呈正相关(r值分别为0.368(P<0.001)、0.193(P=0.009)、0.224(P=0.002)],与OPG呈负相关(r值=-0.330,P<0.001).OPG与TRACP-5b呈负相关(r=-0.458,P=0.008),RANKL与BAP呈正相关(r=0.228,P=0.044).E2、Hcy、OPG、RANKL、TRACP-5b、BAP 诊断骨质疏松的ROC曲线下面积分别为0.819、0.686、0.803、0.776、0.731和0.719.骨质疏松影响因素的Logistic回归分析表明,独立于年龄,E2、OPG、TRACP-5b、Hcy对骨质疏松有显著影响,优势比(OR)分别为0.901、0.046、4.165、9.112.结论 TRACP-5b、Hcy和BAP对骨质疏松症的诊断准确度较好,可以作为临床早期防治PMOP的依据.【期刊名称】《检验医学》【年(卷),期】2013(028)008【总页数】5页(P685-689)【关键词】骨保护素;核因子-kβ受体活化因子配体;骨源性碱性磷酸酶;抗酒石酸酸性磷酸酶;雌二醇;同型半胱氨酸;骨代谢;绝经后骨质疏松症【作者】杨立顺;袁海生;沈兴娅;康建华;王艾云【作者单位】天津市中医药大学附属北辰中医医院检验科,天津,300400;天津市中医药大学附属北辰中医医院检验科,天津,300400;天津市中医药大学附属北辰中医医院检验科,天津,300400;天津市中医药大学附属北辰中医医院检验科,天津,300400;天津市中医药大学附属北辰中医医院检验科,天津,300400【正文语种】中文【中图分类】R446.1绝经后骨质疏松症(postmenopausal osteoporosis,PMOP)为高转换型骨质疏松症。
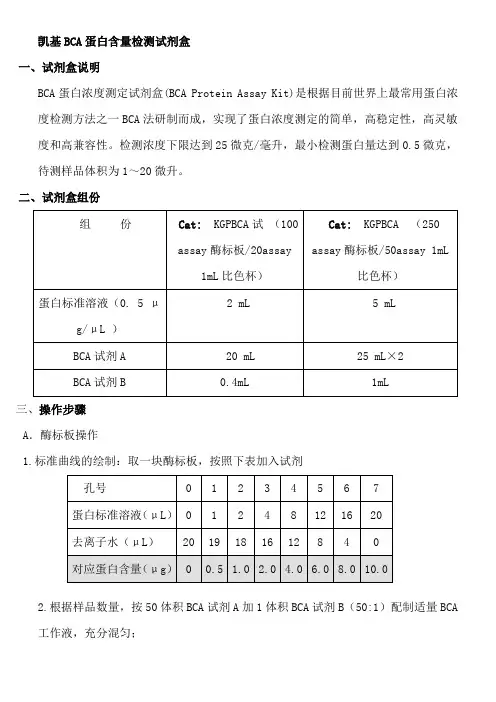
凯基BCA蛋白含量检测试剂盒一、试剂盒说明BCA蛋白浓度测定试剂盒(BCA Protein Assay Kit)是根据目前世界上最常用蛋白浓度检测方法之一BCA法研制而成,实现了蛋白浓度测定的简单,高稳定性,高灵敏度和高兼容性。
检测浓度下限达到25微克/毫升,最小检测蛋白量达到0.5微克,待测样品体积为1~20微升。
三、操作步骤2.根据样品数量,按50体积BCA试剂A加1体积BCA试剂B(50:1)配制适量BCA工作液,充分混匀;3. 各孔加入200μL BCA工作液;4. 把酶标板放在振荡器上振荡30sec,37℃放置30分钟,然后在562nm下比色测定。
以蛋白含量(μg)为横坐标,吸光值为纵坐标,绘出标准曲线;5.稀释待测样品至合适浓度,使样品稀释液总体积为20μL,加入BCA工作液200μL,充分混匀,37℃放置30分钟后,以标准曲线0号管做参比,在562nm波长下比色,记录吸光值;6.根据所测样品的吸光值,在标准曲线上即可查得相应的蛋白含量(μg),除以样品稀释液总体积(20μL),乘以样品稀释倍数即为样品实际浓度(单位:μg/μL)。
B.分光光度计测定2.根据样品数量,按50体积BCA试剂A加1体积BCA试剂B(50:1)配制适量BCA工作液,充分混匀;3.各管加入1000μL BCA工作液;4.各管充分混匀,37℃放置30分钟,然后在562nm下比色测定。
以蛋白含量(μg)为横坐标,吸光值为纵坐标,绘出标准曲线;5.稀释待测样品至合适浓度,样品稀释液总体积为100μL,加入BCA工作液1000μL,充分混匀,37℃放置30分钟后,以标准曲线0号管做参比,在562nm波长下比色,记录吸光值;6.根据所测样品的吸光值,在标准曲线上即可查得相应的蛋白含量(μg),除以样品稀释液总体积(100μL),乘以样品稀释倍数即为样品实际浓度(单位:μg/μL)。
、注意事项1.配制好的混合BCA工作液室温24小时内稳定。

凯基Annexin V-EGFP细胞凋亡检测试剂盒(Annexin V-EGFP Apoptosis Detection Kit)Cat number:KGA For Research Use OnlyStore at4℃ for one yearExpire date:一、 试剂盒说明在正常细胞中,磷脂酰丝氨酸(PS)只分布在细胞膜脂质双层的内侧,而在细胞凋亡早期,细胞膜中的磷脂酰丝氨酸(PS)由脂膜内侧翻向外侧。
Annexin V是一种分子量为35~36kD的Ca2+依赖性磷脂结合蛋白,与磷脂酰丝氨酸有高度亲和力,故可通过细胞外侧暴露的磷脂酰丝氨酸与凋亡早期细胞的胞膜结合。
因此Annexin V被作为检测细胞早期凋亡的灵敏指标之一。
将Annexin V进行荧光素(EGFP、FITC)标记,以标记了的Annexin V作为荧光探针,利用荧光显微镜或流式细胞仪可检测细胞凋亡的发生。
与FITC的绿色荧光信号相比,EGFP的绿色荧光信号具有信号强,不易淬灭,稳定性高等优点,故本试剂盒采用EGFP作为荧光标记探针。
碘化丙啶(Propidium Iodide, PI)是一种核酸染料,它不能透过完整的细胞膜,但对凋亡中晚期的细胞和死细胞,PI能够透过细胞膜而使细胞核染红。
因此将Annexin V与PI匹配使用,就可以将处于不同凋亡时期的细胞区分开来。
本试剂盒可应用于培养细胞凋亡检测(不推荐用于检测组织样本)。
二、 试剂盒组份组份Cat: KGA10110 assays Cat: KGA10220 assaysCat: KGA10350 assaysCat: KGA104100 assays储存条件AnnexinV-EGFP 50μL 100μL 250μL 500μL 4℃避光Propidium Iodide 50μL 100μL 250μL 500μL 4℃避光Binding Buffer 5 mL 10.0 mL 25 mL 50 mL 4℃三、 试剂盒以外自备仪器和试剂流式细胞仪或荧光显微镜、低速离心机、微量移液器1.5m L Microtube、载玻片、盖玻片(荧光显微镜观察需用)、PBS、不含EDTA的胰酶消化液四、 使用注意事项1.微量试剂取用前请离心集液。

广东药科大学学报Journal of Guangdong Pharmaceutical University Mar.2024,40(2)基于STING/NF-κB信号通路探讨茯苓酸对去卵巢小鼠骨质疏松的作用黄成硕1,陈驹2,吴晓静3,郑锦畅1,梁振1,郭伟雄1,陈继铭1(1.广东医科大学附属医院骨科中心,广东湛江524001;2.广东医科大学附属医院药学部,广东湛江524001;3.广东医科大学附属医院培训部,广东湛江524001)摘要:目的评价茯苓酸通过调控STING/NF-κB信号通路对去卵巢小鼠骨质疏松的影响。
方法取40只SPF级雌,10µg/kg)和茯苓酸组(FL,5mg/kg),性C57BL/6小鼠随机分为假手术组(Sham)、模型组(OVX)、17β-雌二醇组(E2通过切除双侧卵巢建立小鼠骨质疏松模型。
8周实验结束后分别检测血清碱性磷酸酶(ALP)和抗酒石酸酸性磷酸酶(StrACP)水平,观察股骨远端形态学和胫骨(皮质骨)骨形成动态变化,测定右侧股骨的生物力学和STING/NF-κB通路关键蛋白表达水平。
结果与OVX组比较,E组和FL组小鼠血清StrACP和ALP水平明显降低(P<0.01),2股骨远端骨小梁面积百分数明显增加(P<0.01),皮质骨双荧光间距明显减少(P<0.01),股骨最大载荷和断裂载荷明显升高(P<0.01),股骨STING和p-NF-κB p65/NF-κB p65蛋白表达水平明显降低(P<0.01)。
结论茯苓酸通过调控STING/NF-κB信号通路抑制骨吸收和促进骨形成,从而有效减少去卵巢小鼠骨丢失。
关键词:茯苓酸;小鼠;卵巢摘除;骨质疏松;17β-雌二醇中图分类号:R285.5文献标识码:A文章编号:2096-3653(2024)02-0119-05DOI:10.16809/ki.2096-3653.2023122001Effect of pachymoic acid on osteoporosis in ovariectomized mice based on STING/NF-κB signaling pathwayHUANG Chengshuo1,CHEN Ju2,WU Xiaojing3,ZHENG Jinchang1,LIANG Zhen1,GUO Weixiong1,CHEN Jiming1*(1.Orthopaedic Center,Affiliated Hospital of Guangdong Medical University,Zhanjiang524001,China;2.Department of Pharmacy,Affiliated Hospital of Guangdong Medical University,Zhanjiang524001,China;3.Training department,Affiliated Hospital of Guangdong Medical University,Zhanjiang524001,China)*Corresponding author Email:**************Abstract:Objective To evaluate the effect of pachymoic acid on osteoporosis in ovariectomized mice by regulatingSTINGNF-κB signaling pathway.Methods Forty SPF female C57BL/6mice were divided into sham operation,10µg/kg)and pachymoic acid group(FL,5mg/kg),and group(Sham),model group(OVX),17β-estradiol group(E2the osteoporosis model of mice was established by bilateral ovariectomy.After8weeks,the levels of serum alkalinephosphatase(ALP)and tartrate-resistant acid phosphatase(StrACP)were detected,the morphology of distal femurand the dynamic changes of tibia(cortical bone)bone formation were observed,and the biomechanics of the rightfemur and the expression levels of key proteins in STING/NF-κB pathway were determined.Results Compared withgroup and FL group were significantly lowered(P<0.01),the OVX group,the levels of serum StrACP and ALP in E2area percentage of trabecular bone in distal femur was increased(P<0.01),and the double-fluorescence distancebetween cortical bones was decreased(P<0.01).The maximum load and fracture load of femur were significantlyelevated(P<0.01),and the expression levels of STING and p-NF-κB p65/NF-κB p65protein in femur weresignificantly increased(P<0.01).Conclusion Pachymoic acid can inhibit bone resorption and promote boneformation by regulating STING/NF-κB signaling pathway,thereby effectively reducing bone loss in ovariectomized mice.Key words:pachymoic acid;mice;ovariectomization;osteoporosis;17β-estradiol收稿日期:2023-12-20基金项目:广东省医学科学技术研究基金项目(B2021148);2021年度广东省科技专项资金(“大专项+任务清单”)竞争性分配项目(2021A05234);湛江市非资助课题(2020B01275)作者简介:黄成硕(1986-),男,副主任医师,主要从事骨科疾病诊治,Email:*****************通信作者:陈继铭(1980-),男,主任医师,主要从事骨科疾病诊治,Email:**************。
土壤磷酸酶测定(酸性、中性和碱性磷酸酶)1. 分析意义土壤有机磷转化受多种因子制约,尤其是磷酸酶的参与,可加速有机磷的脱磷速度。
在pH4-9的土壤中均有磷酸酶。
积累的磷酸酶对土壤磷素的有效性具有重要作用。
研究证明,磷酸酶与土壤碳、氮含量呈正相关,与有效磷含量及pH也有关。
磷酸酶活性是评价土壤磷素生物转化方向与强度的指标。
2. 试验原理Kroll等(1955)最早提出用苯基磷酸盐作基质,以酚的释放量表示磷酸酶活性。
测定磷酸酶主要根据酶促作用生成的有机基团量或无机磷量计算磷酸酶活性。
前一种通称为有机基团含量法,是目前较为常用的测定磷酸酶的方法。
后一种称为无机磷含量法。
研究证明,磷酸酶有三种最适pH:4-5,6-7和8-10。
所以,测定酸性、中性和碱性反应土壤的磷酸酶,要提供相应的pH缓冲液才能测出该土壤的磷酸酶最大活性。
测定磷酸酶常采用的pH缓冲体系有醋酸盐缓冲液(pH5.0-5.4),柠檬酸盐缓冲液(pH7.0),三羟甲基氨基甲烷缓冲液(pH7.0-8.5),硼酸缓冲液(pH9-10)。
测定磷酸酶时,用各种磷酸一酯作为基质。
常用的基质有苯磷酸二钠、酚酞磷酸钠、甘油磷酸钠、α或β萘酚磷酸钠、ρ-硝基苯磷酸钠等。
3. 试剂配制a. 0.5%磷酸苯二钠(用缓冲液配制);b. pH5醋酸盐缓冲液、pH7柠檬酸盐缓冲液、pH9.4硼酸盐缓冲液;c. 氯代二溴对苯醌亚胺试剂:取0.125g 2.6-二溴苯醌氯酰亚胺,用10mL 96%乙醇溶解,贮于棕色瓶中,存放在冰箱里。
保存的黄色溶液未变褐色之前均可使用;d. 酚的标准溶液:酚原液-取1g重蒸酚溶于蒸馏水中,稀释至1L,贮于棕色瓶中;酚工作液-取10mL 酚原液稀释至1L(每毫升含0.01毫克酚);e. 甲苯;f. 0.3%硫酸铝溶液。
4. 标准曲线绘制:取1、3、5、7、9、11和13mL酚工作液,置于50mL容量瓶中,每瓶加入5mL缓冲液和4滴氯代二溴对苯醌亚胺试剂,显色后稀释至刻度,即得0.0002、0.0006、0.0010、0.0014、0.0018、0.0022和0.0026mg ·g -1浓度的酚标准溶液梯度。
补肾壮骨丸抗骨质疏松的药效学作用及机制探讨邢爽;康学【摘要】目的:探讨北京积水潭医院院内制剂补肾壮骨丸抗骨质疏松的药效学作用及其机制。
方法6个月龄雌性SD大鼠60只,随机分为正常对照组、模型对照组、补肾壮骨丸低(1.2 g/kg)、中(2.4 g/kg)、高(4.8 g/kg)剂量组以及阳性药雷洛昔芬组,每组10只。
双侧卵巢摘除术建立大鼠骨质疏松模型,去势手术1周后,补肾壮骨丸低、中、高剂量组及阳性药组分别灌胃给予不同剂量补肾壮骨丸混悬液及雷洛昔芬混悬液治疗12周,正常及模型对照组灌服等体积的生理盐水。
分别检测血清碱性磷酸酶(ALP)、抗酒石酸酸性磷酸酶(TRAP)、甲状旁腺激素(PTH)、促甲状腺激素(CT)以及垂体-性腺轴相关激素雌二醇(E2)、睾酮(T)、黄体生成素(LH)、卵泡刺激素(FSH)含量;测定骨密度、骨生物力学性能。
结果去势后,模型对照组血清ALP、TRAP、PTH活性显著升高(P<0.05或P<0.01),含量分别为(16.347±2.957)U/100 mL、(27.691±7.042)U/L、(45.829±17.007)pg/mL,CT水平显著下降,含量为(20.469±7.343)pg/mL,全股骨和股骨头骨密度为(0.1859±0.0137)、(0.1871±0.0193)g/cm2,股骨最大载荷为(63.448±17.540)N,最大挠度为(0.5848±0.1595)mm,均较正常对照组显著降低(P<0.05或P<0.01);性激素E2和T含量显著降低(P<0.01),分别为(5.935±1.621)pg/mL、(3.382±1.405)ng/mL,促性腺激素LH和FSH水平明显上调(P<0.05),含量分别为(12.549±2.376)、(15.841±1.896)mU/mL;与模型对照组比较,补肾壮骨丸中、高剂量组ALP含量为(13.619±2.881)、(12.720±3.044)U/100 mL,TRAP含量为(20.904±6.454)、(19.933±5.988)U/L,PTH含量为(26.753±13.013)、(25.630±15.618)pg/mL,三者活性均显著下调(P<0.05或P<0.01);高剂量组CT含量显著升高,为(28.350±7.827)pg/mL,中、高剂量组全股骨密度及高剂量组股骨头密度显著升高,分别为(0.2081±0.0113)、(0.2135±0.0139)、(0.2304±0.0290)g/cm2,高剂量组股骨最大载荷及挠度分别为(81.314±16.413)N、(0.7358±0.1488)mm,较模型组显著升高(P<0.05);高剂量组E2、T显著升高(P<0.05或P<0.01),含量为(8.799±2.204)pg/mL、(5.086±1.668)ng/mL;中、高LH含量分别为(10.740±1.652)、(10.575±0.886)mU/mL,FSH含量分别为(13.244±2.089)、(13.348±2.170)mU/mL,二者水平均显著下调(均P<0.05)。
凯基质粒大提试剂盒说明书修改日期:20200706Cat Number:KGA1710Store at RT/-20℃ for 12 monthsFor Research Use Only一、产品简介凯基质粒大提试剂盒是将硅胶薄膜的优点与经典的强碱-SDS裂解细菌法结合,可在1h 获取高质量的质粒DNA。
本试剂盒利用特制的纯化柱简化了结合、洗涤和洗脱步骤,可同时处理多种样品。
获得的纯化质粒为高纯度级别,适用于酶切、PCR、测序及转化等要求。
二、产品组分三、操作步骤使用前请先在Washing buffer加入90 mL无水乙醇(10 assays),其余规格加入无水乙醇的体积请参照瓶身标签。
Solution I在使用前请将提供的全部RNase A加入,混匀,置于4℃保存。
如非特别指明,所有离心步骤均在室温下操作。
1. 接种新鲜的单个菌落到LB培养基(含适量抗生素),37℃震荡培养14-16小时。
收集菌液,10000 rpm离心3min,尽量吸除上清。
注意:残留的液体培养基容易导致菌液裂解不充分,第5步离心后沉淀较松,不能有效吸取上清。
2. 向留有菌体沉淀的离心管中加入10 mL Solution I (确保已加入RNaseA),使用移液器或涡旋振荡器彻底悬浮细菌细胞沉淀。
注意:如果菌块未彻底混匀,会影响菌体裂解,导致质粒提取量和纯度偏低。
3. 向离心管中加入10 mL Solution II,温和地上下翻转5-10次室温放置2-4min。
注意:混匀一定要温和,以免污染细菌基因组DNA,此时菌液应变得清亮粘稠,作用时间不要超过5 min,以免质粒受到破坏。
4.向离心管中加入14 mL Solution III,温和地上下翻转5-10次,室温放置3-5min,此时会出现白色絮状沉淀。
5.12000 rpm离心15 min,用移液器小心地将上清转移到干净离心管中,尽量不要吸出沉淀(若上清中还有白色沉淀,可再次离心后取上清)。
凯基抗酒石酸酸性磷酸酶染液试剂盒
KEYGEN tartrate-resistant acid phosohate stain,TRAP stain
说明书修订日期:2016.01.14 Cat number:KGA221
Store at4℃for3months
For Research Use Only(科研专用)
一、检验原理
在酸性的缓冲液中,细胞内酸性磷酸酶催化底物水解,其生成物进而与一种稳定的重氮盐偶联,生成不溶性的偶氮染料沉淀,当底物中存在酒石酸时,该反应只出现在特异性细胞中。
二、试剂组成及配制
*简明试剂组成表
试剂组成试剂编号包装规格
一、固定液40ml×1瓶
二、底物液底物反应液(一)甲液①A粉×1支
②B液500μL×1支
乙液③C粉×1支
④D液,500μL×1支底物反应液(二)①E粉×1支
②F液,500μL×1支
底物反应液(三)G液,1ml×1支
底物反应液(四)①H粉×1支
②I液,500μL×1支
三、复染液苏木素10ml×1瓶
甲基绿10ml×1瓶
*具体试剂配制及操作
一、固定液:液体,40ml×1瓶
新鲜血涂片、细胞涂片或爬片、冰冻切片用固定液固定5~10min,石蜡包埋的切片经脱蜡后不需要再固定。
二、底物反应液(一)、(二)、(三)、(四)的组成及配制:
底物反应液(一)组成及配制:
组成:(1)A粉×1支(2)B液500μL×1支
(3)C粉×1支(4)D液500μL×1支
配制:临用前用移液器将B液吸入A粉中充分溶解配成甲液,备用。
再用移液器将D液吸入C粉中充分溶
解配成乙液,备用。
最后将甲液与乙液混合成底物反应液(一),现用现配
底物反应液(二)组成及配制:
组成:(1)E粉×1支(2)F液500μL×1支
配制:临用前用移液器将F液吸入E粉中充分溶解配成底物反应液(二),备用。
底物反应液(三):
G液1ml×1支
底物反应液(四)组成及配制:
组成:(1)H粉×1支(2)I液1ml×1支
配制:临用前用移液器将I液吸入H粉中充分溶解配成底物反应液(四),备用。
底物孵育液的配制
染缸孵育液的准备:
(1)将底物反应物(一),(二),(三),(四)的备用液混合并充分混匀,
(2)先在染缸内加30ml蒸馏水,37℃水浴10分钟,
(3)将底物反应物(一),(二),(三),(四)依次加入已预温的蒸馏水中,
(4)然后将样本玻片固定,水洗后还未完全干,立即放入已经准备好的反应孵育液中,避光孵育60分钟。
注:配置好的孵育液需现用现配,一次性用完,不可反复使用。
三、复染液:
苏木素液,10ml×1瓶
甲基绿液,10ml×1瓶
孵育完后,取出样本玻片水洗1~2分钟,在玻片尚未完全干之前进行复染。
可用苏木素复染1~2分钟,或用甲基绿复染2~3分钟,两者取其一。
三、染色结果
阳性反应为鲜红色或深红色颗粒,定位胞浆中。
四、玻片保存
样本玻片如需长期保存,苏木素复染可用中性树胶封片,甲基绿复染可用水性的甘油明胶封片。
五、所需仪器设备
光学显微镜、染缸、玻片、滴管、秒表、记号笔等。
六、样本染色前准备
血涂片及骨髓涂片的样本前处理
1、推片:取全血或骨髓3微升左右置载玻片上,将推玻片保持与载玻片30度角,置于血滴正前方,稍往后移与血滴接触,血滴沿推片下缘散开,再匀速沿载玻片平面平稳向前滑动,至血液铺完血膜为止。
满意效果为不太薄,以免细胞太少,也不要太厚,以免太重叠。
2、晾干:使涂片在空气中自然晾干,再放入本试剂盒中的固定液内固定2~3分钟,水洗约30~60秒。
3、水洗后注意在不要太干时放入底物孵育液中37℃避光孵育60分钟(太干后染色效果欠佳)
石蜡切片的样本前处理
1、脱蜡:二甲苯中脱蜡5~10分钟,再换用新鲜的二甲苯,脱蜡5~10分钟。
2、下行入水:无水乙醇5分钟,再用90%、70%乙醇、蒸馏水各2分钟。
特殊样本的前处理
例如骨切片作TRACP染色前的脱钙处理,不可用硝酸等进行脱钙,否则会破坏酶及蛋白类物质,从而影响染色效果,为保证染色质量,应该用专用脱钙剂进行脱钙,凯基均有供应,欢迎来电咨询。
冰冻切片的样本前处理
1、回温:将预先制作好的并保存在-20℃冰箱中的冰冻切片放置到切片架上回温约5~10分钟。
[注]:①可放到37℃孵箱中进行回温。
②在37℃水浴箱中放置一个小盒子,再将从冰箱中取出的切片放到小盒当中,目的是让冰冻切片回温到37℃
2、水合:将回温好的切片,水中浸泡1~2分钟。
七、产品用途
存在于正常人肺泡巨噬细胞等部位的TRAP和存在于细胞白血病人脾脏的TRAP均在细胞滤泡中,并不释放入血液,血液中TRAP绝大部分来源于破骨细胞。
因而测量血液中TRAP可以了解破骨细胞的功能状态。
本染液可用于石蜡切片、血液、骨髓涂片、细胞爬片、以及冰冻切片中破骨细胞染色。
八、注意事项
1、如样本为骨片的石蜡切片,要注意不可用硝酸脱钙,酸脱钙的方法对蛋白质(酶类)伤害较大,从而
影响特异性酶染色,会使细胞中的特异性酶失活,导致酶不能跟底物结合,从而导致染色失败。
建议使用抗酒石酸酸性磷酸酶专用的试剂进行脱钙。
2、用底物孵育液进行孵育时要注意避光。
九、储存条件及有效期
本试剂盒应置2~8℃密封避光保存,有效期3个月。
配置后要立即使用,一次用完。