双线桥和单线桥
- 格式:ppt
- 大小:300.50 KB
- 文档页数:6
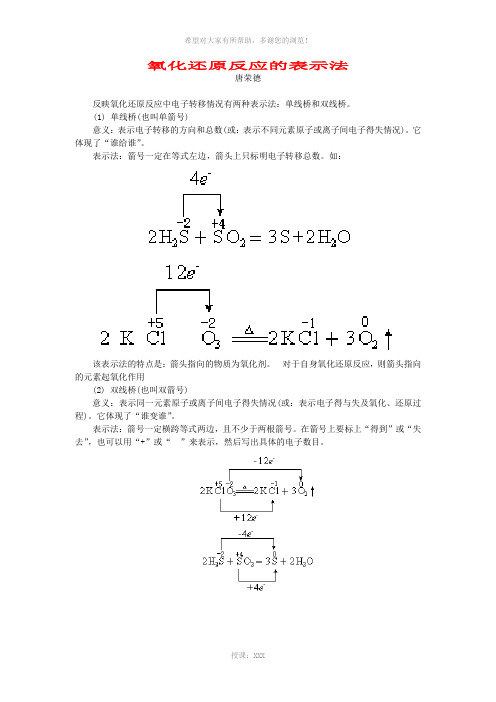
氧化还原反应的表示法唐荣德反映氧化还原反应中电子转移情况有两种表示法:单线桥和双线桥。
(1) 单线桥(也叫单箭号)意义:表示电子转移的方向和总数(或:表示不同元素原子或离子间电子得失情况)。
它体现了“谁给谁”。
表示法:箭号一定在等式左边,箭头上只标明电子转移总数。
如:该表示法的特点是:箭头指向的物质为氧化剂。
对于自身氧化还原反应,则箭头指向的元素起氧化作用(2) 双线桥(也叫双箭号)意义:表示同一元素原子或离子间电子得失情况(或:表示电子得与失及氧化、还原过程)。
它体现了“谁变谁”。
表示法:箭号一定横跨等式两边,且不少于两根箭号。
在箭号上要标上“得到”或“失去”,也可以用“+”或“”来表示,然后写出具体的电子数目。
对于分子内的氧化还原反应,特别是歧化反应,使用单线桥不方便,用双线桥好。
双线桥易画,但麻烦;单线桥简单,能看出氧化剂。
双线桥可用在氧化还原反应方程式配平上。
在考试评分中,回答表示氧化还原反应的电子转移方向和数目或总数时,使用任一种表示法都算正确。
其实,单线桥和双线桥并不以线桥的多少来划分,有两根或三根线桥的不一定是单线桥,但双线桥却不可能只有一根线桥。
因此,要判断是哪种线桥,关键是看线桥是在等式的左边,还是横跨了等式的两边。
如:双线桥单线桥双线桥单线桥两种表示法也有多种形式,如硫铁矿燃烧的氧化还原反应方程式:以上分析可以看出,双线桥是分析法,可理解为是微观的;单线桥是综合法,可理解为宏观的。
要注意,以下容易标错的氧化还原反应方程式。
如铝与NaOH溶液反应,把NaOH当成氧化剂,且标示如下是错的:因为该化学方程式是总反应方程式,反应过程是铝先与水反应生成氢氧化铝和氢气,然后氢氧化铝和碱反应生成偏铝酸钠和水,前者是置换反应,水是氧化剂;后者是复分解反应,NaOH作为碱与酸反应,并不是氧化剂。
正确的应是如下表示法:又如浓硫酸与硫化氢反应,如下表示是错的:因为氧化还原反应是逐步氧化和逐步还原的,即2价的S首先变成0价的S,再氧化才升高到+4价的S,直到氧化为+6价的S;同理,+6价的S首先被还原,变成+4价的S,再还原降到0价的S,直至还原到2价的S。


1、氧化还原反应的表示方法(1)双线桥法双线桥法是用两条线桥来表示氧化还原反应中化合价变化或电子转移方向和数目的方法。
方法如下:双线桥的箭头始于________有关元素,箭头指向发生________变化后生成物中对应元素。
在线上要标明“失去”或“得到”电子总数,化合价的升降以及该元素“被氧化”或“被还原”。
例如:(2)单线桥法单线桥法是用一条线桥来表示氧化还原反应中电子转移的方向和数目的方法。
箭号起点为________(失电子)元素,终点为________(得电子)元素,在线上只标转移电子总数,不标得与失。
例如:2、氧化剂和还原剂(1)氧化剂和还原剂的概念①从化合价角度定义:在氧化还原反应中,所含元素的化合价降低的反应物,称为氧化剂;所含元素的化合价升高的反应物称还原剂。
②从电子转移角度定义:在氧化还原反应中,得到电子(或电子偏向)的反应物,称为氧化剂;失去电子(或电子偏离)的反应物,称为还原剂。
(2)常见的氧化剂氧化剂是在化学反应中化合价容易________(或容易________)的物质。
常见的氧化剂有:①典型的非金属单质,如:F2、O2、Cl2、Br2(非金属活动性超强其氧化性就超强)。
②有变价元素的高价态化合物或离子,如:KMnO4、浓H2SO4、HNO3、H+。
③金属阳离子,如:Fe3+、Cu2+。
(3)常见的还原剂还原剂是在化学反应中化合价容易________(或容易_________)的物质。
常见的还原剂有:①典型的金属单质,如:K、Ca、Na、Mg(金属活动性超强其还原性就超强)。
②某些非金属单质及其化合物。
如:H2、C、CO。
③有变价元素的最低价态化合物或离子,如:H2S、HI、HBr、S2-、I-、Br-。
3、氧化产物和还原产物在氧化还原反应中,氧化剂得电子具有氧化性,起氧化作用,本身被还原后的生成物叫还原产物。
还原剂失电子具有还原性,起还原作用,本身被氧化,氧化后的生成物叫氧化产物。



1.氧化还原反应基本概念复习1.氧化还原反应的本质:,氧化还原反应的特征:。
2.如何判断一个化学反应是否为氧化还原反应?。
3.四大基本反应与氧化还原反应之间的关系是什么?。
4.反应Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O是不是氧化还原反应?,原因:。
5.口诀:升失氧,降得还。
化合价升高,电子,被,发生反应,本身作剂,变成产物。
化合价降低,电子,被,发生反应,本身作剂,变成产物。
7.氧化性和还原性的比较:规律为氧化性:〉还原性:〉6.双线桥和单线桥(双)(单)(1)置换反应型:Fe + 2HCl = FeCl2 + H2↑Fe + 2HCl = FeCl2 + H2↑是氧化剂,是还原剂,是氧化产物,是还原产物,电子转移的总数是,氧化性〉,还原性〉。
(2)置换反应型:Cu + 2Ag+ ==Cu2+ + 2Ag Cu + 2Ag+ ==Cu2+ + 2Ag是氧化剂,是还原剂,是氧化产物,是还原产物,电子转移的总数是,氧化性〉,还原性〉。
(3)置换反应型:2 Y-+ W2 = 2 W-+ Y2 2 Y-+ W2 = 2 W-+ Y2是氧化剂,是还原剂,是氧化产物,是还原产物,电子转移的总数是,氧化性〉,还原性〉。
(4)化合反应型:2Na+ Cl2 = 2NaCl2Na+ Cl2 = 2NaCl是氧化剂,是还原剂,是氧化产物,是还原产物,电子转移的总数是,氧化性〉,还原性〉。
(5)分解反应:2KClO32KCl + 3O2↑2KClO32KCl + 3O2↑是氧化剂,是还原剂,是氧化产物,是还原产物,电子转移的总数是,氧化性〉,还原性〉。
6部分氧化还原型:MnO2 +4HCl(浓)MnCl2 +Cl2↑+2H2O MnO2 +4HCl(浓)MnCl2 +Cl2↑+2H2O是氧化剂,是还原剂,是氧化产物,是还原产物,电子转移的总数是,氧化性〉,还原性〉。
(7)歧化反应型:3S+6NaOH = 2Na2S +Na2SO3 +3H2O 3S+6NaOH = 2Na2S +Na2SO3 +3H2O是氧化剂,是还原剂,是氧化产物,是还原产物,电子转移的总数是,氧化性〉,还原性〉。
反映氧化还原反应中电子转移情况有两种表示法:单线桥和双线桥。
(1) 单线桥(也叫单箭号)意义:表示电子转移的方向和总数(或:表示不同元素原子或离子间电子得失情况)。
它体现了“谁给谁”。
表示法:箭号一定在等式左边,箭头上只标明电子转移总数。
如:该表示法的特点是:箭头指向的物质为氧化剂。
(对于自身氧化还原反应,则箭头指向的元素起氧化作用)(2) 双线桥(也叫双箭号)意义:表示同一元素原子或离子间电子得失情况(或:表示电子得与失及氧化、还原过程)。
它体现了“谁变谁”。
表示法:箭号一定横跨等式两边,且不少于两根箭号。
在箭号上要标上“得到”或“失去”,也可以用“+”或“-”来表示,然后写出具体的电子数目。
对于分子内的氧化还原反应,特别是歧化反应,使用单线桥不方便,用双线桥好。
双线桥易画,但麻烦;单线桥简单,能看出氧化剂。
双线桥可用在氧化还原反应方程式配平上。
在考试评分中,回答表示氧化还原反应的电子转移方向和数目(或总数)时,使用任一种表示法都算正确。
其实,单线桥和双线桥并不以线桥的多少来划分,有两根或三根线桥的不一定是单线桥,但双线桥却不可能只有一根线桥。
因此,要判断是哪种线桥,关键是看线桥是在等式的左边,还是横跨了等式的两边。
如:双线桥单线桥双线桥单线桥两种表示法也有多种形式,如硫铁矿燃烧的氧化还原反应方程式:以上分析可以看出,双线桥是分析法,可理解为是微观的;单线桥是综合法,可理解为宏观的。
要注意,以下容易标错的氧化还原反应方程式。
如铝与NaOH溶液反应,把NaOH当成氧化剂,且标示如下是错的:因为该化学方程式是总反应方程式,反应过程是铝先与水反应生成氢氧化铝和氢气,然后氢氧化铝和碱反应生成偏铝酸钠和水,前者是置换反应,水是氧化剂;后者是复分解反应,NaOH作为碱与酸反应,并不是氧化剂。
正确的应是如下表示法:又如浓硫酸与硫化氢反应,如下表示是错的:因为氧化还原反应是逐步氧化和逐步还原的,即-2价的S首先变成0价的S,再氧化才升高到+4价的S,直到氧化为+6价的S;同理,+6价的S首先被还原,变成+4价的S,再还原降到0价的S,直至还原到-2价的S。