食品中防腐剂苯甲酸(钠)和山梨酸(钾)的测定.
- 格式:doc
- 大小:14.50 KB
- 文档页数:4

项目五用高效液相色谱法检测物质任务一食品中山梨酸、苯甲酸、糖精钠的测定(液相色谱法)单元一液相色谱分离原理和液相色谱仪的基本组成教学内容苯甲酸和山梨酸是我国目前最常用的食品防腐剂,广泛应用于各种果汁饮料中,以防止其变质。
但如果防腐剂的含量超过标准限度,或者长期饮用含有防腐剂的饮料,则会对人体健康造成不得影响,因此检测果汁中的苯甲酸和山梨酸含量是非常有必要的。
表GB2760-2007国家食品添加剂使用卫生标准抑制物质腐败的药剂。
即对以腐败物质为代谢底物的微生物的生长具有持续的抑制作用。
重要的是它能在不同情况下抑制最易发生的腐败作用,特别是在一般灭菌作用不充分时仍具有持续性的效果。
对纤维和木材的防腐用矿油、煤焦油、丹宁,对生物标本用甲醛、升汞、甲苯、对羟基苯甲酸丁酯、硝基糠腙衍生物或香脂类树脂。
在食品中使用防腐剂受到限制,因此多靠干燥、腌制等一些物理的方法。
特殊的防腐剂有乙酸等有机酸、以油酸脂为成分的植物油、芥子等特殊的精油成分。
对于生物体的局部(如人体表面或消化道),可以根据具体条件采用各种防腐剂(如碘仿、水杨酸苯酯、苯胺染料或吖啶类色素等)。
我国规定使用的防腐剂有苯甲酸、苯甲酸钠、山梨酸、山梨酸钾、丙酸钙等25种。
防腐剂应具备的几个条件:1、性质较稳定:加入到食品中后在一定的时期内有效,在食品中有很好的稳定性2、低浓度下具有较强的抑菌作用3、本身不应具有刺激气味和异味4、不应阻碍消化酶的作用,不应影响肠道内有益菌的作用5、价格合理,使用较方便。
防腐剂的作用机理:1、能使微生物的蛋白质凝固或变性,从而干扰其生长和繁殖。
2、防腐剂对微生物细胞壁、细胞膜产生作用。
由于能破坏或损伤细胞壁,或能干扰细胞壁合成的机理,致使胞内物质外泄,或影响与膜有关的呼吸链电子传递系统,从而具有抗微生物的作用。
3、作用于遗传物质或遗传微粒结构,进而影响到遗传物质的复制、转录、蛋白质的翻译等。
4、作用于微生物体内的酶系,抑制酶的活性,干扰其正常代谢。
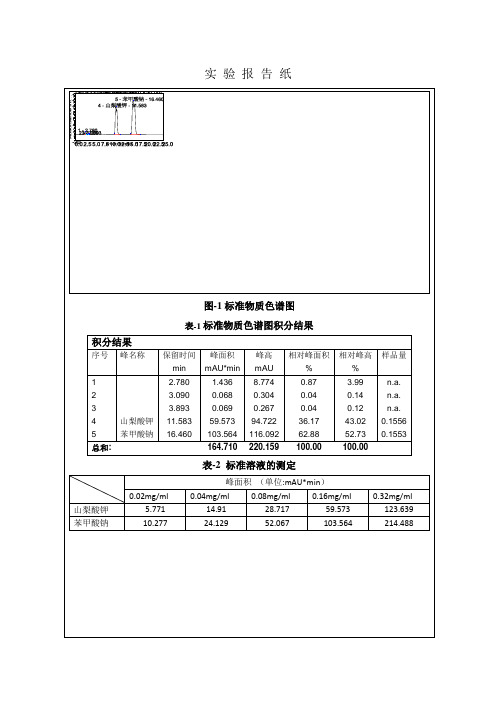
图-1标准物质色谱图表-1标准物质色谱图积分结果积分结果序号峰名称保留时间峰面积峰高相对峰面积相对峰高样品量min mAU*min mAU % %1 2.780 1.436 8.774 0.87 3.99 n.a.2 3.090 0.068 0.304 0.04 0.14 n.a.3 3.893 0.069 0.267 0.04 0.12 n.a.4 山梨酸钾11.583 59.573 94.722 36.17 43.02 0.15565 苯甲酸钠16.460 103.564 116.092 62.88 52.73 0.1553总和: 164.710 220.159 100.00 100.00表-2 标准溶液的测定峰面积(单位:mAU*min)0.02mg/ml 0.04mg/ml 0.08mg/ml 0.16mg/ml 0.32mg/ml 山梨酸钾 5.771 14.91 28.717 59.573 123.639 苯甲酸钠10.277 24.129 52.067 103.564 214.488山梨酸钾图-3 待测物质色谱图表-4 待测物质积分结果分析积分结果序号峰名称保留时间峰面积峰高相对峰面积相对峰高样品量min mAU*min mAU % %1 1.683 2.843 3.058 4.00 0.57 n.a.2 2.243 5.267 93.777 7.41 17.38 n.a.3 2.290 14.124 174.078 19.88 32.27 n.a.4 2.360 13.416 115.601 18.89 21.43 n.a.5 2.630 1.363 17.059 1.92 3.16 n.a.6 2.697 0.562 11.160 0.79 2.07 n.a.7 2.830 0.243 3.887 0.34 0.72 n.a.8 2.933 1.076 10.714 1.51 1.99 n.a.9 2.980 0.959 9.079 1.35 1.68 n.a. 10 3.467 2.141 5.633 3.01 1.04 n.a. 11 3.980 0.660 4.566 0.93 0.85 n.a. 12 4.0674.6204.666 6.50 0.86 n.a. 13 山梨酸钾 11.397 11.04838.135 15.55 7.07 0.0289 14 11.640 12.716 48.085 17.90 8.91 n.a. n.a.苯甲酸钠n.a. n.a.n.a.n.a.n.a.n.a. 总和:71.037 539.499 100.00 100.00待测物质的积分结果中,保留时间为11.397min 有检测信号,与标准物质的积分结果进行对比,此处为山梨酸钾的检测信号,说明待测物质中含有山梨酸钾。

气相色谱法测定食品中苯甲酸、苯甲酸钠、山梨酸、山梨酸钾及注意事项吴惠丽【期刊名称】《食品安全导刊》【年(卷),期】2016(000)021【总页数】1页(P79-79)【作者】吴惠丽【作者单位】焉耆回族自治县质量与计量检测所【正文语种】中文食品试样酸化后,利用苯甲酸、山梨酸易溶于乙醚的性质,用乙醚将食品中的苯甲酸、山梨酸提取出来,在气相色谱仪上进行分离测定,根据标准曲线求出食品中苯甲酸、苯甲酸钠、山梨酸和山梨酸钾的含量。
乙醚:不含过氧化物;石油醚:沸程30~60 ℃;盐酸;无水硫酸钠;盐酸(1∶1):量取100 mL水,一边摇动,一边缓缓加入100 mL盐酸,混匀,冷却至室温备用。
氯化钠酸性溶液(40 g/L):称取4.0 g氯化钠,加水溶解,并定容至100 mL,然后加数滴盐酸(1∶1)酸化。
色谱柱:固定液AT添加剂玻璃毛细柱,柱长15 m,内径0.53 mm,液膜厚度:1.00 μm;柱温:150 ℃、汽化温度:250 ℃、检测温度260 ℃。
苯甲酸、山梨酸溶液标准物质食品防腐剂苯甲酸溶液标准物质,标准值1.00 mg/mL。
食品防腐剂山梨酸溶液标准物质,标准值1.00 mg/mL。
制备苯甲酸、山梨酸混合标准使用液分别准确吸取0.4 mL苯甲酸溶液标准物质和0.4 mL山梨酸溶液标准物质混合置于1个10 mL容量瓶中,用石油醚_乙醚(3∶1)混合溶剂稀释至刻度,此标准混合使用液含苯甲酸或山梨酸为40 μg/mL。
以此类推,再分别准确吸取0.8、1.2、1.6、2.0 mL和2.4 mL苯甲酸溶液标准物质和山梨酸溶液标准物质,混合后置于一组10 mL容量瓶中,用石油醚_乙醚(3∶1)混合溶剂稀释并定容至刻度,混匀备用。
盖好瓶塞,防止溶剂挥发造成浓度变化,同时控制实验室温度为20 ℃。
此标准混合使用液系列中,苯甲酸或山梨酸的浓度分别为40、80、 120、160、200μg/mL和240μg/mL。

高效液相色谱法测定食醋和酱油中苯甲酸钠和山梨酸钾含量实验报告【专业版】(文档可以直接使用,也可根据实际需要修订后使用,可编辑放心下载)高效液相色谱法测定食醋和酱油中苯甲酸钠和山梨酸钾含量摘要:【目的】用高效液相色谱法测定食醋和酱油中苯甲酸钠和山梨酸钾含量。
【方法】以Hyperclone BDS C18柱(150×4.60 mm,5μm,phenomenex)为色谱柱;检测波长215~230nm,进样量10μL,流动相:甲醇:0.02mol/L 乙酸铵(35:65),流量0.8mL/min,柱温30℃【结果】:食醋中的苯甲酸钠含量为127.15899ug/mol,酱油中的苯甲酸钠含量为723.60033ug/mol,未见则出山梨酸钾。
????【结论】:高效液相色谱法具有高速、高效、高灵敏度的优点,所以数据准确,用外标法计算结果操作简单,计算方便,得出样品中苯甲酸钠的含量。
关键词:高效液相色谱法外标法苯甲酸钠山梨酸钾一、前言苯甲酸钠,化学式:C6H5O2Na,是苯甲酸的钠盐,苯甲酸钠是很常用的防腐剂,有防止变质,延长保质期的效果。
山梨酸钾别名2,4-己二烯酸钾,是山梨酸的钾盐,也是防腐剂。
本实验采用高效液相色谱法对酱油和醋中的苯甲酸钠和山梨酸钾的含量测定,方法简便快速,实用于苯甲酸钠和山梨酸钾的定量分析。
苯甲酸结构式:山梨酸钾结构式:二、实验目的和实验原理2.1.实验目的:(1)了解高效液相色谱仪基本结构和工作原理,以及初步掌握其操作技能;(2)学习高效液相色谱保留值定性方法和外标法的标准曲线定量方法;(3)掌握RP-HPLC法对食品中苯甲酸钠和山梨酸钾的测定方法;2.2.实验原理:将样品加热去除其中的二氧化碳和乙醇,用(1+1)氨水调pH值近中性,过滤后进高效液相色谱仪,进行反相色谱C18柱分离后,根据保留时间和峰面积进行定性定量分析。
三、仪器与试剂及试剂处理3.1. 仪器:高效液相色谱仪【高压输液泵LC-6A,检测器SPD-10A,保温箱CPD-10AS,进样阀7725I】;电子天平;纯水仪;离心机;超声波清洗机。

食醋和酱油中苯甲酸钠和山梨酸钾含量的测定专业:食品科学与工程教育姓名:蒋翠莲学号:20105494 指导老师:白绮摘要:[目的]用高效液相色谱法测酱油和食醋中山梨酸钾和苯甲酸钠的含量。
【方法】采用RP-HPLC法以C-18不锈钢柱(150mm)为色谱柱;流动相:甲醇:乙酸铵溶液(0.02mol/L)=5:95;柱温30℃;流速1.0mol/min ;检测波长230nm;进样量(标准进样量:2.5 ,5 ,7.5 ,10 ,15 ,20ul;样品进样量:5 ul)。
【结果】酱油中的山梨酸钾含浓度为0.069mg/ml;苯甲酸钠为0.0146mg/ml;醋中的山梨酸钾为0.00141mg/ml苯甲酸钠为0.00155mg/ml。
结论:高效液相色谱法具有高速、高效、高灵敏度的优点 所以数据准确 用外标法计算结果操作简单 计算方便 得出样品中苯甲酸钠的含量。
关键词:高效液相色谱法苯甲酸钠山梨酸钾前言:苯甲酸钠,化学式:C6H5O2Na,是苯甲酸的钠盐,苯甲酸钠是很常用的防腐剂,有防止变质,延长保质期的效果。
山梨酸钾别名2,4-己二烯酸钾,是山梨酸的钾盐,也是防腐剂。
本实验采用RP-HPLC法对酱油和醋中的苯甲酸钠和山梨酸钾的含量测定,方法简便,快速,实用于苯甲酸钠和山梨酸钾的定量分析。
1 实验部分1.1实验目的了解高效液相色谱仪基本结构和使用原理,操作过程。
学习高效液相色谱保留值定性方法和外标法的标准曲线测定方法。
学习RP-HPLC法对食品中苯甲酸钠和山梨酸钾的含量的测定方法。
1.2 仪器与试剂LC-6A/10A 高效液相色谱处理系统:由日本岛津公司提供;Milli-Q超纯水处理器;HS6150D型超声波处理器;2XZ-1型旋片真空泵,由浙江黄岩求精真空泵厂制造。
甲醇:HPLC,500ml,由Guangdong Ghuanghua Sol-Techco,Led提供;氨水:AR,500ml,由成都市科龙化工厂提供;碳酸氢钠(优级纯)纯度99.5%,500g 由成都市科龙化工厂提供;苯甲酸钠:AR 纯度99.5%,250g 由成都科龙化工厂提供;山梨酸钾:AR 纯度98.0%,由成都市科隆化工厂提供。

食品中苯甲酸和山梨酸的检测摘要:近年来食品安全卫生已成为社会、政府关注的焦点之一。
食品安全已越来越引起广大消费者的密切关注和担忧。
目前我国每年食物中毒报告例数约2万人,但据专家估计实际数量要比这个数字大10倍左右。
食品安全问题不仅涉及广大消费者的健康,还涉及相关企业的经济效益和市场空间,关系到整个食品行业的发展。
苯甲酸可与人体内的氨基乙酸结合生成马尿酸而随尿液排出体外。
如过量摄入苯甲酸和苯甲酸钠,将会影响肝脏酶对脂肪酸的作用,其次苯甲酸钠中过量的钠对人体血压、心脏、肾功能也会产生影响。
特别是对心脏、肝、肾功能弱的人群而言,苯甲酸和苯甲酸钠的摄食是不适合的嘲。
另外还会出现代谢性酸中毒、惊厥和气喘等病症。
在体外测定中还可以测到一些弱断裂剂的放射性。
苯甲酸及其钠盐因为有叠加中毒现象的报道,在使用上有争议,虽仍为各国允许使用,但应用范围愈来愈窄。
日本的进口食品中就限制使用,甚至部分禁止使用,日本已停止生产。
但因价值低廉,在中国仍作为主要防腐剂使用。
山梨酸具有较低的毒性,是迄今为止国际公认的最好的防腐剂,已经成为了西方发达国家的主流防腐剂。
但事实上,现在已经报道了许多案例(荨麻疹和假过敏)说明人体中对过多的山梨酸所带来的危害。
由于山梨酸和苯甲酸在食品中的广泛使用,所以在此讨论苯甲酸和山梨酸的检测以技术及以及各种检测技术的利弊。
1防腐剂的检测在食品工业中,作为防腐剂,不能影响人体正常的生理功能,一般说来,在正常规定的使用范围内使用食品防腐剂对人体没有毒害或毒性极小。
因此,食品防腐剂的定性与定量的检测在食品安全性方面是非常重要的。
目前,测定防腐剂的方法主要有:薄层色谱法、高效液相色谱法、毛细管电泳法、气相气谱法等1.1苯甲酸和山梨酸各种检测方法1.1.1高效薄层色谱法和高效液相色谱法M.Thomassin等人曾经采用高效薄层色谱法和高效液相色谱法对尼泊金酯类作过检测,实验发现高效薄层色谱法的相对标准偏差要大于高效液相色谱法,但是高效薄层色谱法对于尼泊金酯类的定量就更为快速。
超高效液相色谱法同时测定糕点中苯甲酸(钠)、山梨酸(钾)和糖精钠的含量发表时间:2018-07-09T17:23:54.363Z 来源:《基层建设》2018年第14期作者:钟锐文[导读] 摘要:糕点中的苯甲酸(钠)、山梨酸(钾)和脱氢乙酸(钠)、安赛蜜和糖精钠经水提取,脱脂、沉淀蛋白、离心、过滤后,采用超高效液相色谱法同时测定,样品标准加入平均回收率分别为99.01%~99.36%、99.51%~101.58%、98.90%~99.73%。
广州市澳键丰泽生物科技有限公司广东广州 510760摘要:糕点中的苯甲酸(钠)、山梨酸(钾)和脱氢乙酸(钠)、安赛蜜和糖精钠经水提取,脱脂、沉淀蛋白、离心、过滤后,采用超高效液相色谱法同时测定,样品标准加入平均回收率分别为99.01%~99.36%、99.51%~101.58%、98.90%~99.73%。
关键词:超高效液相;糕点;苯甲酸(钠);山梨酸(钾);糖精钠Simultaneous Determination of Benzoic Acid(Sodium),Sorbic Acid(Potassium),and Saccharin Sodium in Cakes by Ultra Performance Liquid ChromatographyRuiwen Zhong(Guangzhou Alchemy Biotechnology Co.,Ltd.,Guangzhou,Guangdong 510760,China) Abstract:The benzoic acid(sodium),sorbic acid(potassium),dehydroacetic acid(sodium),acesulfame potassium,and sodium saccharin in the cake are extracted with water,delipidated,precipitated protein,centrifuged,and filtered,followed by ultra-high performance liquid chromatography.The average recoveries of the standard samples were 99.01%~99.36%,99.51%~101.58%,and 98.90%~99.73%,respectively.Key words:Ultra high performance liquid phase;Pastry;Benzoic acid(sodium);Sorbic acid(potassium);Sodium saccharin食品安全是当今关系民生的重大问题,直接关系到广大人民群众的身体健康,而食品的色香味取决于在食品加工过程中使用的适量的食品添加剂。
液相色谱法检测苯甲酸、山梨酸、糖精钠的疑难详解苯甲酸、山梨酸、糖精钠是衡量食品卫生质量的重要指标,苯甲酸、山梨酸的检测参照GB/,糖精钠的检测参照GB/T,即可开展实验。
苯甲酸、山梨酸、糖精钠虽是较常见的检测项目,但是要得到一个准确可靠的结果,也存在一定的难度,许多新手常出现因对方法理解发生偏差而检测出错的事故。
笔者根据自己多年该方面工作的实际经验出发,以苯甲酸、山梨酸为着重点,从样品前处理、检测仪器的选择、超标时的判断等几个易出问题的方面,进行了详细的阐述。
2样品前处理的注意事项GB/和GB/在文字结构上有缺陷,在涉及用仪器法测定苯甲酸、山梨酸、糖精钠时,只讲述了液体样品的前处理方法,没有涉及对固体样品的前处理。
食品样品往往含有大量的油脂、蛋白质,对提取极为不利;如处理不干净也会污染色谱柱,影响检测工作。
这类样品处理的关键在于如何找到一种较理想的沉淀剂,尽量排除待测样品中的油脂、蛋白质,且不影响待测物组分的回收率。
GB/使用5%硫酸铜溶液沉淀蛋白,对于蛋白质含量较低的食品尚可,对于豆粉、奶粉、月饼等高油脂、高蛋白样品则沉淀效果不理想。
如用10%钨酸钠溶液作为沉淀剂,效果好些;如用10%亚铁氰化钾溶液和20%醋酸锌溶液则效果更理想(这是笔者目前用过最理想的沉淀剂)。
具体操作步骤如下:取一定量样品,捣碎,利用四分法原理称取样品克于50ml比色管中,加水20ml,浸泡、振荡均匀,加入氢氧化钠溶液(1mol/L) ml,加入%亚铁氰化钾溶液,20%乙酸锌溶液,定容,振荡使其充分混匀后,用滤纸初滤除去沉淀物,初滤液过μm微孔滤膜,收集滤液于样品瓶中,样品处理液和标准有溶液各进样5uL 测定。
用这种方法简单易行,接触有机试剂少,重复性和回收率都令人满意;缺点是一定要用液相色谱法检测,有一定局限。
3检测仪器的选择虽然液相色谱仪操作起来比气相色谱仪要复杂,但笔者建议如条件许可仍尽量用液相色谱法检测。
原因如下:液相色谱法所用的样品处理方法远比气相色谱法简单,且不需使用有机试剂。
食品中苯甲酸、山梨酸和糖精钠的测定液相色谱法测定食品中苯甲酸、山梨酸和糖精钠的液相色谱法是一种常用的分析方法,由于其操作简便、分离效果好以及分析结果准确可靠而得到广泛应用。
下面将详细介绍该方法的原理、仪器设备、操作步骤以及常见问题及解决方法。
一、方法原理:该方法采用液相色谱法进行分析,根据待测样品中的目标化合物与色谱柱之间的相互作用来实现物质的分离和定量。
主要包括样品的预处理、色谱分离、定量检测和数据分析等步骤。
二、仪器设备:液相色谱仪是该方法的主要仪器设备,其中包括色谱柱、检测器和数据处理系统等,常用的色谱柱有C18反相色谱柱、正相色谱柱等。
常用的检测器有紫外检测器、荧光检测器等。
三、操作步骤:1. 样品的预处理:将待测食品样品取适量加入提取溶剂中,超声或搅拌混合,静置一段时间使目标化合物溶解。
然后通过滤膜过滤,以获取纯净的样品溶液。
2. 色谱分离:将样品溶液注入色谱柱中,通过不同组分在色谱固定相和流动相之间的相互作用来实现分离。
可以调整流动相的组成和流速等条件来优化分离效果。
3. 定量检测:分离后的组分进入检测器,根据目标化合物的特性进行定量检测。
常用的方法是通过比较待测样品和已知浓度的标准溶液的峰面积或峰高来确定目标化合物的含量。
4. 数据处理:将检测到的信号转化为对应的色谱图,并通过计算机数据处理系统进行数据分析和结果计算。
四、常见问题及解决方法:1. 色谱柱选择:根据目标化合物的特性选择合适的色谱柱,如苯甲酸和山梨酸可以选择C18反相色谱柱,糖精钠可以选择离子交换色谱柱。
2. 流动相的选择:合理选择流动相的组成和流速,以实现目标化合物的高效分离。
这需要根据不同化合物的极性和溶解度等参数进行优化。
3. 检测器的选择:根据不同化合物的特性选择合适的检测器,如苯甲酸和山梨酸可以选择紫外检测器进行检测,糖精钠可以选择荧光检测器进行检测。
4. 样品的提取:提取过程要注意样品的充分溶解和提取溶剂的选择,以获得准确的分析结果。
实验 9.3 食品中防腐剂苯甲酸(钠和山梨酸(钾的测定
薄层色谱法
一、实验目的
掌握薄层色谱定性和斑点面积半定量测定法。
学会制备聚酰胺薄层板。
二、仪器
吹风机层析缸玻璃板 10×18cm 玻璃板 50×80 cm 微量注射器10μL
喷雾器
三、试剂与试样
聚酰胺粉 200目乙醚可溶淀粉
无水硫酸钠盐酸溶液6mol • L-1
4%氯化钠酸性溶液于 4%氯化风俗溶液中加入少量mol • L-1盐酸溶液
展开剂:(1正丁醇:氨水:无水乙醇 =7:1:2
(2异丙醇:氨水:无水乙醇 =7:1:2
显色剂:0.04%溴甲酚紫的 50%乙醇溶液用0.1mol • L-1氢氧化钠调至 PH=8
苯甲酸标准溶液:精密称取苯甲酸 0.2000g ,用少量乙醇溶解后移入 100mL 容量瓶中,并用乙醇稀释至刻度摇匀,此溶液每亳升相当于 2mg 苯甲酸。
山梨酸标准溶液:精密称取山梨酸 0.2000g ,用少量乙醇溶解后移入 100mL 容量瓶中,并用乙醇稀释至刻度摇匀,此溶液每亳升相当于 2mg 山梨酸。
试样酱油、水果汁、果酱等
四、实验步骤
1、试样提取—试样溶液的制备
称取 2.5g 混合均匀的试样,置于 25mL 带塞量筒中,加0.5mL , 6 mol• L-1盐酸酸化,用乙醚提取两次 (15mL 、 10mL 每次振摇 1min , 将上层乙醚提取液吸入另一25mL 带塞量筒中, 合并乙醚提取液。
用 3mL4%氯化钠酸性溶液洗涤两次,静置
15min ,乙醚层通过无水硫酸钠脱水后过滤于 25mL 容量瓶中。
加乙醚稀释至刻度,摇匀。
吸取 10.00mL 乙醚提取液分两次置于 10mL 离心管中, 在约 40℃水浴上除去乙醚, 加入 0.1mL 乙醇溶解残渣,制成试样测定液备用。
2、聚酰胺粉板的制备
称取 1.6g 聚酰胺粉,加 4g 可溶性淀粉,加 15mL 水,研磨 3~5min,使其均匀即可涂10×18cm 厚度 0.3mm 的薄层板两块。
涂好的薄层板置于水平大玻璃板上, 于室温干燥后, 于 80℃干燥 1h 取出,置于干燥器中保存。
3、点样
在薄层板下端 2cm 的基线处,用 10ul 微量注射器,分别点1μL 、2μL 试样溶液和1μL 、2μL 苯甲酸、山梨酸标准溶液。
4、展开与显色
层析缸内倒入适量展开剂,在层析缸周围贴上滤纸,待滤纸湿润后,展开剂液层厚约 0.5~0.7cm,让展开剂在层析缸内饱和 10min ,将点样后的薄层板放入层析缸内,使薄层下端浸入展开剂中约 0.5cm , 迅速盖紧缸盖, 进行展开, 如图 8— 12。
待展开剂前沿上展至 10cm 时 , 取出吹干,喷显色剂,斑点呈黄色,背景为蓝色。
5、定性和半定量测定
把试样斑点与标准斑点比较,以比移值(Rf 值定性,在此实验条件下苯甲酸和山梨酸的比移值分别为 0.73、 0.82。
比较试样斑点与标准斑点面积大小及颜色深浅进行含量计算。
根据测定结果按下式计算试样中苯甲酸、山梨酸含量。
计算:
式中:X ——试样中苯甲酸(山梨酸的含量, g • kg-1;
A ——测定用试样溶液中苯甲酸(山梨酸的质量, mg ;
m ——试样的质量, g ;
V1——溶解苯甲酸(山梨酸时,加乙醇体积, mL ;
V2——测定时点样的体积, mL ;
25——试样乙醚提取液的总体积, mL;
10——测定时吸取乙醚提取液的体积, mL 。
五、说明和注意事项
1、此方法用于酱油、水果汁、果酱中苯甲酸、山梨酸含量的测定。
苯甲酸及其钠盐、山梨酸及其钠盐是食品常用防腐剂, 主要用于酸性食品的防腐。
国家规定在不同食品中其最大使用量为0.2~1.0 g• kg-1。
如碳酸饮料中苯甲酸或山梨酸的最大使用量为0.2 g• kg-1。
酱油、食醋中苯甲酸钠或山梨酸钠最大使用量为1.0 g• kg-1。
因此,测定食品防腐剂的含量以控制其用量,对保证食品质量,保障人民健康具有十分重要的意义。
2、本方法测定原理为:试样经酸化,使苯甲酸钠、山梨酸钾转变为苯甲酸、山梨酸,再用乙醚提取, 乙醚提取液经氯化钠酸性溶液洗涤,并用无水硫酸钠脱水后,将乙醚蒸出, 残渣用乙醇溶解后,点样于聚酰胺薄层板上,经展开,显色后,根据比移值与标准比较定性,根据斑点面积和颜色深浅进行半定量测定。
3、试样中如含有二氧化碳、酒精时应加热除去,富含脂肪和蛋白质的试样应除去脂肪和蛋白质,以防用乙醚萃取时发生乳化。
4、本方法灵敏度高,但操作繁琐,重现性差,现今多用气相色谱法测定,试样经酸化后, 用乙醚提取苯甲酸、山梨酸后, 用附氢火焰离子化检测器的气相色谱仪进行分离和测定, 与标准系列比较定量。
也可采用高效液相色谱法测定, 利用被分离组分在固定相和移动相中分配系数的不同, 使被测组分分离,用紫外检测器在特定波长下测定被测组分的吸收度,与标准比较定性和定量。
思考题:
1、本实验分离测定苯甲酸和山梨酸为何要选用聚酰胺薄层板?
2、在本实验条件下山梨酸 Rf 值较苯甲酸 Rf 值大的原因?。