第二单元 元素性质的递变规律
- 格式:ppt
- 大小:1.88 MB
- 文档页数:38





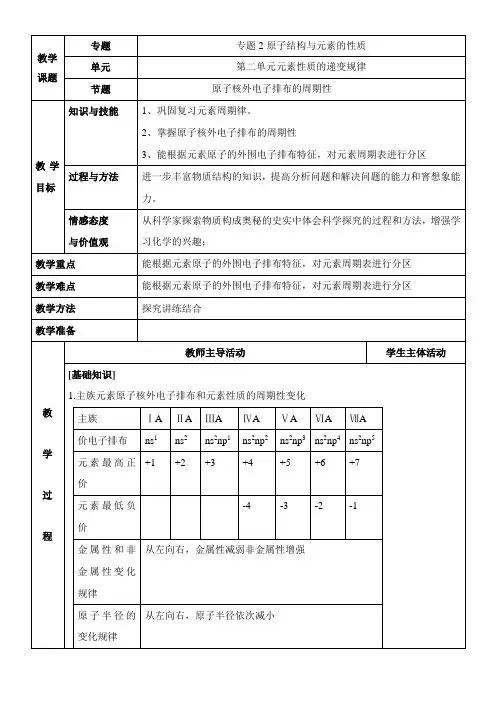
[讲解]对学过的知识进行巩固。
教学过程教师主导活动学生主体活动2、原子核外电子排布的周期性周期元素数目外围电子排布(ⅠA——0族)最多可容纳的外围电子数1 2 1s1——1s2 22 8 2s1——2s22p683 8 3s1——3s23p684 18 4s1——4s24p685 18 5s1——5s25p686 32 6s1——6s26p683、根据元素原子的外围电子排布的特征,对周期表进行分区。
分区族数外围电子排布S区ⅠA、ⅡA ns1-2p区ⅢA、ⅣA、ⅤA、ⅥA、ⅦA、0族ns2np1-6d区ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、Ⅷ(n-1)d1-10ns1-2ds区ⅠB、ⅡB (n-1)d10ns1-2f区[讲解](1)s区元素:外围电子只出现在s轨道上的元素。
价电子排布为ns1~2,主要包括ⅠA和ⅡA族元素,这些元素除氢以外都是活泼的金属元素,讨论后完成理解后完成[课堂练习]1、下面的能级表示中正确的是( )A、1pB、2dC、3fD、4s2、X原子的最外层电子的排布为ns2np4,则X的氢化物的化学式是( )A. HXB. H2XC. XH3D. XH43、一个电子排布为1s22s22p63s23p1的元素最可能的价态是( )A、+3B、+2C、+1D、-14、下列各原子或离子的电子排布式错误的是()A、Al 1s22s22p63s23p1B、O2-1s22s22p6C、Na+1s22s22p6D、Si 1s22s22p25、在元素周期表的第四周期的主族元素中,金属元素的种数是()A、4种B、5种C、6种D、7种6、A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A顺序依次减小,B和E同主族。
下列推断不正确的是()A、A、B、E一定在不同周期B、C的最高价氧化物的水化物可能显碱性C、A、D可能在同一主族D、C和D的单质可能化合形成离子化合物7、粒子的半径从小到大顺序排列的是( )、S、P 、O、F +、Mg2+、Na+、Na、Li8、下列各组元素性质递变情况错误的是( )A.Li、Be、B原子最外层电子数依次增多B.P、S、Cl元素最高正化合价依次升高C.N、O、F原子半径依次增大D.Na、K、Rb的金属性依次增强9、已知A原子只有一个不成对电子,M电子层又比N层多11个电子,试回答:(1)N电子层的s轨道和P轨道中只有一个未成对电子的元素有哪些?(2)写出A原子的电子排布式.略。

元素性质的递变性规律第⼆单元元素性质的递变规律【学海导航】元素的性质随着核电荷数的递增⽽呈现周期性的变化,这个规律叫做元素周期律。
⼀、原⼦核外电⼦排布的周期性元素按原⼦序数递增的顺序依次排列时,原⼦的最外层上的电⼦数,由1(s1)到8(s2p6),呈现出周期性变化。
相应于这种周期性变化,每周期以碱⾦属开始,以稀有⽓体结束。
元素的化学性质,主要取决于元素原⼦的电⼦结构,特别是最外层电⼦结构。
所以元素性质的周期性,来源于原⼦电⼦层结构的周期性。
根据元素原⼦的外围电⼦排布的特征,可将元素周期表分成五个区域:s区、p区、d区、ds区、f区。
⼆、元素第⼀电离能的周期性变化1、定义:从⽓态的基态原⼦中移去⼀个电⼦变成+1价⽓态阳离⼦所需的最低能量,称为第Ⅰ电离能。
常⽤符号I1表⽰。
M(g)→ M+(g)+ e-,+1价⽓态阳离⼦移去⼀个电⼦变成+2价⽓态阳离⼦所需的最低能量,称为第Ⅱ电离能。
依次类推。
元素的第⼀电离能越⼩,表⽰它越容易失去电⼦,即该元素的⾦属性越强。
2、影响电离能的因素电离能的⼤⼩主要取决于原⼦的核电荷、原⼦半径及原⼦的电⼦构型。
⼀般说来,核电荷数越⼤,原⼦半径越⼩,电离能越⼤。
另外,电⼦构型越稳定,电离能也越⼤。
3. 电离能的周期性变化同周期中, 从左向右,核电荷数增⼤,原⼦半径减⼩, 核对电⼦的吸引增强, 愈来愈不易失去电⼦, 所以 I 总的趋势是逐渐增⼤。
但有些元素(如Be、Mg、N、P等)的电离能⽐相邻元素的电离能⾼些,这主要是这些元素的最外层电⼦构型达到了全充满或半充满的稳定构型。
同主族元素⾃上⽽下电离能依次减⼩。
但在同⼀副族中,⾃上⽽下电离能变化幅度不⼤,且不甚规则。
4.电离能与价态之间的关系失去电⼦后, 半径减⼩, 核对电⼦引⼒⼤, 更不易失去电⼦, 所以有: I1 < I2< I3<I4…., 即电离能逐级加⼤.三、元素电负性的周期性变化1、定义:电负性: 表⽰⼀个元素的原⼦在分⼦中吸引电⼦的能⼒. 元素的电负性越⼤,表⽰原⼦吸引成键电⼦的能⼒越强,该元素的⾮⾦属性也就越强;电负性越⼩,该元素的⾦属性越强。
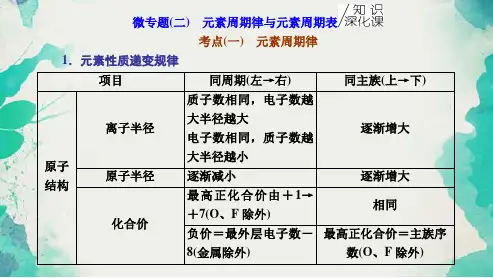
讨论[讲解] 3.周期表的右上角元素的第一电离能数值大,左下角元素的第一电离能的数值小(四)I1与洪特规则的关系同一周期元素的第一电离能存在一些反常,这与它们的原子外围电子排布的特征有关。
如镁的第一电离能比铝大,磷的第一电离能比硫大。
基本规律:当原子核外电子排布在能量相等的轨道上形成全空(p0、d0、[课堂练习]1、镭是元素周期表中第七周期的ⅡA族元素。
下面关于镭的性质的描述中不正确的是( )A.在化合物中呈+2价 B.单质使水分解放出氢气C.氢氧化物呈两性 D.碳酸盐难溶于水(解析)C、依据周期表性质的周期性2、在下面的电子结构中,第一电离能最小的原子可能是 ( )A.ns2np3 B.ns2np5 C.ns2np4 D.ns2np6(解析)C、原子核外电子排布在能量相同的轨道上形成全空(P0、d0、f0)、半满、全满结构时,原子的能量较低,该元素具有较大的第一电离能3、下列说法正确是A、第3周期所含元素中钠的第一电离能最小B、铝的第一电离能比镁的第一电离能大C、所有元素中氟的第一电离能最大D、钾的第一电离能比镁的第一电离能大(解析)AC、第一电离能大小由原子核外电子排布结构决定的。
4、A、B、C是短周期元素,核电荷数依次增大;A、C同族,B+ 离子核外有10个电子,回答下列问题(1)A、B、C三种元素分别是_________、_________、_________。
(2)A、B、C之间形成多种化合物,其中属于离子化合物的化学式分别为_________、__________、___________。
(3)分别写出A、B、C的电子排列式:A.________________B._____________C._____________(解析)氧、钠、硫。
[直击高考](03上海)下表是元素周期表的一部分。
表中所列的字母分别代表某一化学元素。
(1)下列(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、1 ④d、e、f(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。

