有机化合物波谱解析复习资料指导
- 格式:doc
- 大小:8.89 MB
- 文档页数:71


第一章紫外光谱一、名词解释1、助色团:有n电子的基团,吸收峰向长波方向移动,强度增强.2、发色团:分子中能吸收紫外或可见光的结构系统.3、红移:吸收峰向长波方向移动,强度增加,增色作用.4、蓝移:吸收峰向短波方向移动,减色作用.5、增色作用:使吸收强度增加的作用.6、减色作用:使吸收强度减低的作用.7、吸收带:跃迁类型相同的吸收峰.二、选择题1、不是助色团的是:DA、-OHB、-ClC、-SHD、 CH3CH2-2、所需电子能量最小的电子跃迁是:DA、σ→σ*B、 n →σ*C、π→π*D、 n →π*3、下列说法正确的是:AA、饱和烃类在远紫外区有吸收B、 UV吸收无加和性C、π→π*跃迁的吸收强度比n →σ*跃迁要强10-100倍D、共轭双键数目越多,吸收峰越向蓝移4、紫外光谱的峰强用εmax表示,当εmax=5000~10000时,表示峰带:B很强吸收B、强吸收 C、中强吸收 D、弱吸收5、近紫外区的波长为:CA、 4-200nmB、200-300nmC、200-400nmD、300-400nm6、紫外光谱中,苯通常有3个吸收带,其中λmax在230~270之间,中心为254nm的吸收带是:BA、R带B、B带C、K带D、E1带7、紫外-可见光谱的产生是由外层价电子能级跃迁所致,其能级差的大小决定了CA、吸收峰的强度B、吸收峰的数目C、吸收峰的位置D、吸收峰的形状8、紫外光谱是带状光谱的原因是由于:DA、紫外光能量大B、波长短C、电子能级差大D、电子能级跃迁的同时伴随有振动及转动能级跃迁的原因9、π→π*跃迁的吸收峰在下列哪种溶剂中测量,其最大吸收波长最大:AA、水B、乙醇C、甲醇D、正己烷10、下列化合物中,在近紫外区(200~400nm)无吸收的是:AA、 B、 C、 D、11、下列化合物,紫外吸收λmax值最大的是:A(b)A、 B、 C、 D、12、频率(MHz)为4.47×108的辐射,其波长数值为AA、σ→σ*B、π→π*C、n→σ*D、n→π*第二章红外光谱一、名词解释:1、中红外区2、fermi共振3、基频峰4、倍频峰5、合频峰6、振动自由度7、指纹区8、相关峰9、不饱和度10、共轭效应11、诱导效应12、差频二、选择题(只有一个正确答案)1、线性分子的自由度为:AA:3N-5 B: 3N-6 C: 3N+5 D: 3N+62、非线性分子的自由度为:BA:3N-5 B: 3N-6 C: 3N+5 D: 3N+63、下列化合物的νC=C的频率最大的是:( )A B C D答案:CH2CH2CH21651 1657 1678 1680O O1716 1745 1775 1810 OOCH24、下图为某化合物的IR图,其不应含有:DA:苯环 B:甲基 C:-NH2 D:-OH5、下列化合物的νC=C的频率最大的是:A B C D答案:1646 1611 1566 164116506、亚甲二氧基与苯环相连时(1,2亚甲二氧基苯:),其亚甲二氧基的δCH 特征强吸收峰为:AA:925~935cm-1B:800~825cm-1C:955~985cm-1D:1005~1035cm-17、某化合物在3000-2500cm-1有散而宽的峰,其可能为:AA:有机酸 B:醛 C:醇 D:醚8、下列羰基的伸缩振动波数最大的是:C9、中三键的IR区域在:BA ~3300cm-1B 2260~2240cm-1C 2100~2000cm-1D 1475~1300cm-110、偕三甲基(叔丁基)的弯曲振动的双峰的裂距为:DA 10~20 cm-1 B15~30 cm-1 C 20~30cm-1 D 30cm-1以上第三章核磁共振一、名词解释1、化学位移2、磁各向异性效应3、自旋-自旋驰豫和自旋-晶格驰豫4、屏蔽效应5、远程偶合6、自旋裂分7、自旋偶合8、核磁共振CRORACROHBCROFCROClC DC NR9、屏蔽常数10.m+1规律11、杨辉三角12、双共振13、NOE效应14、自旋去偶15、两面角16、磁旋比17、位移试剂二、填空题1、1HNMR化学位移δ值范围约为 0~14 。

有机波谱知识点总结波谱是化学分析中常用的一种手段,通过测定分子在电磁波中的吸收、散射或发射,可以了解分子的结构和性质。
有机波谱是指在有机化合物中应用的波谱分析方法,主要包括红外光谱、紫外-可见光谱、质谱和核磁共振谱等。
本文将针对有机波谱的各种知识点进行总结,包括波谱的基本原理、各种波谱的特点和应用、波谱分析中需要注意的问题等内容。
一、红外光谱1.基本原理红外光谱是利用物质对红外辐射的吸收和散射的规律来研究物质结构和性质的一种分析方法。
红外光谱的基本原理是在物质中分子或原子的振动和转动会产生特定的频率的红外光吸收,这样可以用红外光谱来检验物质的结构和成分。
2.特点和应用红外光谱对于分析有机化合物的结构和功能团具有非常重要的作用。
红外光谱具有分辨率高、灵敏度强、操作简便等特点,广泛应用于聚合物材料、药物分析、食品检测等领域。
3.需要注意的问题在进行红外光谱分析时,需要注意样品的处理、仪器的校准和数据的解释等问题。
此外,还需要对不同功能团的吸收峰进行了解,进行光谱图谱的解读。
二、紫外-可见光谱1.基本原理紫外-可见光谱是利用物质对紫外光和可见光的吸收的规律来研究物质结构和特性的一种分析方法。
紫外-可见光谱的基本原理是分子在吸收紫外-可见光时,电子跃迁至较高的能级,产生吸收峰,可以由此推测分子的结构和键合的性质。
2.特点和应用紫外-可见光谱对于分析有机化合物的共轭结构和电子转移能力有很大的作用。
紫外-可见光谱具有快速、敏感、定量等特点,广泛应用于有机合成、药物分析、环境监测等领域。
3.需要注意的问题在进行紫外-可见光谱分析时,需要注意样品的准备、仪器的校准和光谱图谱的解释。
此外,还需要了解分子在吸收紫外-可见光时的机理和特性,进行光谱图谱的解读。
三、质谱1.基本原理质谱是利用物质在电子轰击下的离子化和质子转移等规律来研究物质结构和成分的一种分析方法。
质谱的基本原理是将物质离子化后,通过质子转移和碎裂等反应产生一系列离子,再根据其质荷比来推测物质的结构和成分。

有机波谱分析要点例题和知识点总结一、有机波谱分析概述有机波谱分析是研究有机化合物结构的重要手段,它主要包括红外光谱(IR)、紫外可见光谱(UVVis)、核磁共振(NMR)和质谱(MS)等技术。
通过对这些波谱数据的解析,可以确定有机化合物的分子结构、官能团种类、化学键的性质等信息。
二、红外光谱(IR)(一)原理红外光谱是基于分子振动和转动能级的跃迁而产生的吸收光谱。
不同的官能团在特定的波数范围内会产生特征吸收峰。
(二)要点1、官能团的特征吸收峰例如,羰基(C=O)在 1700 1750 cm⁻¹有强吸收峰;羟基(OH)在 3200 3600 cm⁻¹有宽而强的吸收峰。
2、影响吸收峰位置的因素包括诱导效应、共轭效应、氢键等。
(三)例题例 1:某化合物的红外光谱在 1720 cm⁻¹有强吸收峰,可能含有什么官能团?答案:羰基(C=O)。
例 2:一个化合物在 3400 cm⁻¹有宽而强的吸收峰,在 1050 1100 cm⁻¹有吸收峰,推测其结构。
答案:可能含有羟基(OH)和醚键(COC)。
三、紫外可见光谱(UVVis)(一)原理基于分子中价电子的跃迁而产生的吸收光谱。
(二)要点1、生色团和助色团生色团如羰基、双键等能在紫外可见区域产生吸收;助色团如羟基、氨基等能增强生色团的吸收。
2、影响吸收波长的因素包括共轭体系的大小、取代基的性质等。
(三)例题例 1:某化合物在 250 nm 处有强吸收,可能的结构是什么?答案:可能含有共轭双键。
例 2:比较两个化合物的紫外吸收波长,一个有苯环,一个有苯环和一个羟基取代。
答案:含羟基取代的化合物吸收波长可能更长。
四、核磁共振(NMR)(一)原理利用原子核在磁场中的自旋能级跃迁产生的吸收信号。
(二)要点1、化学位移不同环境的氢原子或碳原子具有不同的化学位移值,可用于判断官能团的位置。
2、耦合常数相邻氢原子之间的相互作用导致峰的分裂,耦合常数可提供关于分子结构的信息。

一、名词解释:
1、生色基、助色基、红移现象、蓝移现象、增色效应、减色效应、官能团吸收峰、(n+1 规则)、偶合常数、基频峰、亚稳离子、自旋-自旋偶合?
二、问答题:
1、有机化合物结构测定的经典方法?
2、有机分子电子跃迁有哪几种类型?
4、紫外谱图提供的结构信息有哪些?
5、产生红外光谱的必要条件?
6、影响IR谱峰位置变化的因素有哪些?举例说明之。
7、IR谱图解析的基本步骤?
8、影响化学位移的因素有哪些?举例说明之。
9、NMR谱图可以向我们提供关于有机分子结构的哪些信息?
10、NMR谱图解析的基本步骤?
11、波谱综合分析方法的基本步骤?
12、紫外吸收光谱的基本原理是什么?
13、影响离子断裂的因素有哪些?
14、解析红外谱图应注意哪些事项?
15、化学位移是如何产生的?
三、波谱解析:
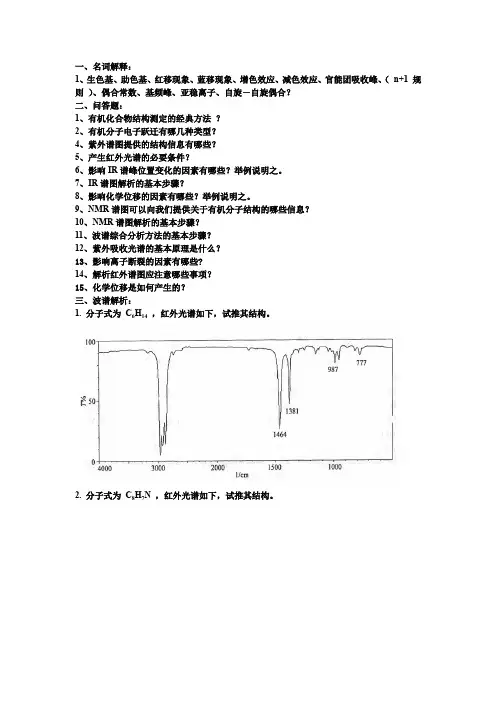
1. 分子式为C6H14,红外光谱如下,试推其结构。
2. 分子式为C8H7N ,红外光谱如下,试推其结构。
3. 分子式为C4H6 O2,红外光谱如下,试推其结构。
4. 分子式为C10H14S ,红外光谱如下,试推其结构。
5、C3H6O2IR 3000cm-1 1700cm-1
=1 NMR 11.3 (单峰1H) 2.3 (四重峰2H)
1.2 (三重峰3H)
6、C7H8O IR 3300,3010,1500,1600,730,690cm-1
=4 NMR 7.2 (多重峰5H) 4.5 (单峰2H)
3.7 (宽峰1H)
7、根据下列谱图决定化合物的结构,并解析谱图。

(一)常用解谱数据总结关于数据,是一定要记的···大家想怎么记爱怎么记就怎么记吧,建议自己总结,这样记的好一些。
下面是鄙人的,嘻嘻。
(老师PPT上有很多总结的)一、氢谱化学位移值δ(ppm)影响化学位移值的因素:只有空间效应和共轭效应是屏蔽效应增大,向高场位移,即σ↑,δ↓.(一)0.4~4.0为饱和C上的H① 0.4~1.8 连饱和C的饱和C上的H② 1.8~2.5 连不饱和C的饱和C上的HI. 1.8~2.1 连C=C、C≡C的饱和C上的HII. 2.1~2.5 连C=O、N、S、苯环的饱和C上的H③ 3.0~4.6 连-O-的饱和C上的H其中,4.1左右可能有酯基④例外的:2.3~3.0是叁键上的H(二)4.6~8.0为不饱和C上的H① 4.6~6.0 C=C上的H② 6.0~8.0 苯环上的H(三)4.0~5.5为脂肪醇-OH的H若有0.5~1.0,为稀溶液(四)3.5~7.7为酚的-OH的H若有10~16,为分子内氢键(五)9.0~10.0为H-C=0的H(六)10.5~13为-COOH的H(七)胺类①~1.0 脂肪胺②4~5(气泡峰)芳香胺③6~7(气泡峰)酰胺,仲胺类其它:J值:①任何情况下J顺<J反②总体情况:J苯环H<J邻(烯H)<J邻(烷H)<J偕H③苯环H:J对<J间<J邻(J对0 ~1Hz;J间1~3Hz;J邻6~12Hz)④烯烃H:J邻(顺)<J邻(反)(J邻(顺)6~14Hz;J邻(反)11~18Hz)⑤烷烃H:J邻6~8Hz⑥同碳上的H:J偕10~16Hz要求掌握给图能测量算得J值,再推化合物种类。
二、碳谱碳谱的DEPT值:季碳消失!θ=45°,季C消失;θ=90°,季C消失,只有CH向上;θ=135°,季C消失,只有CH2向下。
COM谱:峰全部为单峰。
OFR谱:裂分峰只有同一C上的,临近C不影响裂分。
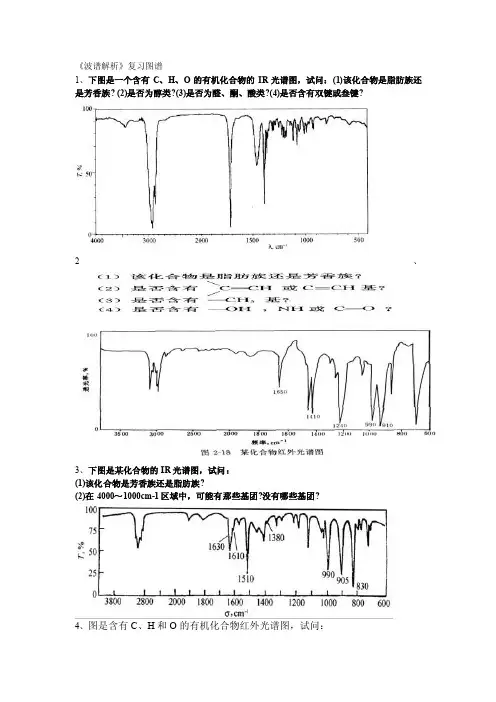
《波谱解析》复习图谱1、下图是一个含有C、H、O的有机化合物的IR光谱图,试问:(1)该化合物是脂肪族还是芳香族? (2)是否为醇类?(3)是否为醛、酮、酸类?(4)是否含有双键或叁键?2、3、下图是某化合物的IR光谱图,试问:(1)该化合物是芳香族还是脂肪族?(2)在4000~1000cm-1区域中,可能有那些基团?没有哪些基团?4、图是含有C、H和O的有机化合物红外光谱图,试问:(1)该化合物是脂肪族还是芳香族?(2)有哪些基团的存在?5、某化合物的化学式C7H9N,测得其红外光谱如下,推导其结构6、某一未知物分子式为C8H8O,红外光谱图如下,试推测其结构7、试推测化合物C8H8O的分子结构。
8、某检品通过TCL分析为纯物质,由质谱测得分子式为C9H10O2,测得红外图谱如下,试确定其结构,并给出峰归属。
9、C8H7N,确定结构、10、分子式为C14H14,测得红外图谱如下,试确定其结构,并给出峰归属。
11、化合物的分子式为C10H12O,测得其红外吸收光谱如图所示,试推导其化学结构。
12、核磁共振谱图见图.已知a峰高14.4,b峰高 2.4,c峰高12.0,已知1H的磁旋比 =267519000T¯¹S¯¹,而且该图使用的NMR仪器为60MHz的质子共振频率,试回答下列问题:1)求该化合物的不饱和度;2)a,b质子属一级偶合还是二级偶合?为什么?3)该化合物有哪几个偶合系统?4)该化合物中那些质子为磁等价质子?5)b峰有几个质子?6)试推出该化合物的结构。
7)C峰支子的化学位移为7.09,为什么?8)该仪器的磁场强度为多少?9) b 组质子裂分峰之间的距离是多少?10) 若使用100MHz 的仪器,则δa,δb,ν∆ab 各为多少?•13、以下为同一化合物的两种表达式:试解释为何J1,2=0~2Hz ,J2,3N=8~10Hz ,J3X,2=3~5Hz ,J7A,7S=9~11Hz?另外,试推测J2,7A ,J2,7S 何者数值较大,为什么?14、一个含溴化学物分子式为C4H7BrO2。



有机化学波谱分析知识要点一、红外光谱分析(IR Spectroscopy)红外光谱是利用物质对红外辐射的吸收、散射和透射特性进行分析的方法。
它可以提供关于有机化合物中的官能团、键的类型和官能团的有关信息。
IR光谱仪通常以波数(单位为cm-1)来表示光谱的X轴。
1. 标定标样:红外光谱的波数标定通常以空气中的CO2吸收峰为基准,波数为2349 cm-12.关键峰值:红外光谱中有一些常见的峰值对应着特定的官能团或基团,如OH伸缩振动、C=O伸缩振动等。
3. 官能团特征波数:红外光谱可以通过分析官能团的特征波数,如羧酸(1700-1720 cm-1)、酯(1735-1745 cm-1)等。
二、核磁共振波谱分析(NMR Spectroscopy)核磁共振波谱是通过分析核自旋在外加磁场中的共振吸收来获得有机化合物结构信息的方法。
常见的核磁共振波谱有质子核磁共振(1HNMR)和碳-13核磁共振(13CNMR)。
1.核磁共振吸收峰:核磁共振谱图中出现的各个峰对应着不同核成分的共振吸收。
2.位移:核磁共振谱图中每个峰的信号在横轴上的位置(化学位移)可以提供有关它们所对应原子的环境和化学环境的信息。
3.耦合:在核磁共振谱图中,出现在特定峰附近的小峰是由于核自旋耦合引起的。
耦合的模式和数量可以提供关于分子中不同核之间的相互关系。
三、质谱分析(Mass Spectrometry)质谱分析是通过将有机化合物中的分子离子化,并在电磁场作用下测量其质量/电荷比,从而确定分子的质谱图(mass spectrum)。
质谱技术可提供有机化合物的分子式和分子结构信息。
1.分子离子峰(M+):质谱图中最高峰对应分子的分子离子峰。
它的质荷比等于分子质量除以电子的质量。
2.碎片离子峰:质谱图中其他峰位来自分子断裂后的离子。
通过分析这些峰可推断出有机化合物的结构。
3.分子离子峰和碎片离子峰之间的相对丰度:通过分析质谱图中分子离子峰和碎片离子峰之间的相对丰度的比例,可以推断出有机化合物中不同官能团的相对含量。
有机化合物波谱解析复习指导广东药学院天然药物化学教研室200 5年 5 月目录第一章紫外光谱… … … … …… … … … … …… 2~4第二章红外光谱… … … … … … …… ………… 5~11第三章核磁共振… … … … … … … …… … ……… 12~34 第四章质谱… … … … …… … … … … … … …35~41 第五章综合解析… … … …… … … … … … … …… 42~70第一章紫外光谱一、名词解释1、助色团2、发色团3、红移4、蓝移5、增色作用6、减色作用7、吸收带二、选择题1、不是助色团的是:A、-OHB、-ClC、-SHD、CH3CH2-2、所需电子能量最小的电子跃迁是:A、σ→σ*B、n →σ*C、π→π*D、n →π*3、下列说法正确的是:A、饱和烃类在远紫外区有吸收B、UV吸收无加和性C、π→π*跃迁的吸收强度比n →σ*跃迁要强10-100倍D、共轭双键数目越多,吸收峰越向蓝移4、紫外光谱的峰强用εmax表示,当εmax=5000~10000时,表示峰带:A、很强吸收B、强吸收C、中强吸收D、弱吸收5、近紫外区的波长为:A、4-200nmB、200-300nmC、200-400nmD、300-400nm6、紫外光谱中,苯通常有3个吸收带,其中λmax在230~270之间,中心为254nm的吸收带是:A、R带B、B带C、K带D、E1带7、紫外-可见光谱的产生是由外层价电子能级跃迁所致,其能级差的大小决定了:A、吸收峰的强度B、吸收峰的数目C、吸收峰的位置D、吸收峰的形状8、紫外光谱是带状光谱的原因是由于:A、紫外光能量大B、波长短C、电子能级差大D、电子能级跃迁的同时伴随有振动及转动能级跃迁的原因9、π→π*跃迁的吸收峰在下列哪种溶剂中测量,其最大吸收波长最大:A、水B、乙醇C、甲醇D、正己烷10、下列化合物中,在近紫外区(200~400nm)无吸收的是:A、B、C、D、11、下列化合物,紫外吸收λmax值最大的是:A、B 、C 、D、12、频率(MHz)为4.47×108的辐射,其波长数值为A、670.7nmB、670.7μC、670.7cmD、670.7m13、化合物中,下面哪一种跃迁所需的能量最高A、σ→σ*B、π→π*C、n→σ*D、n→π*三、问答题1、根据Woodward计算规则,计算下列化合物的UVλmaxCH3 AcO CH3CHCH3CH3CHHOOCCHCH32、某化合物在乙醇中的UVλmax分别为236nm(ε=12000),245nm(ε=18000)请推断其分别为结构A还是B?CH3C H3A B3、一化合物初步推断其结构不是A就是B,经测定UVλmax EtOH=352nm,试问其结构为何?O OA B4、苯甲醛能发生几种类型电子跃迁?在近紫外区能出现几个吸收带?5、一环己烯酮衍生物,其UVλmax EtOH=235nm,假如共轭体系中连接有烷基(R),试问发色体系的可能结构是什么?指出烷基取代位置。
有机波谱分析复习纲要第一章 红外和拉曼光谱一.主要光谱信息1.峰的数目:与分子基团有关2.峰的位置:结构定性的主要依据3.峰的形状:宽窄,结构定性的辅助手段4.峰的强度:高低,结构定性的辅助手段,可作为定性的依据二.基本原理1.红外吸收:分子吸收特定频率的红外光,引起辐射光强的改变2.波长(μm)或波数(1/cm)为横坐标,百分透过率(T%)或吸光度(A)为纵坐标记录(A=lg1/T)3.吸收带分类1)很强吸收带(vs,T%<10)2)强吸收带(s,10<T%<40)3)中强吸收带(m,40<T%<90)4)弱吸收带(w,T%>90)5)宽吸收(b)4.红外光区分类5.产生条件:1)辐射光谱能量与振动跃迁所需能量相等2)辐射与物质之间必须有耦合作用在振动过程中,只有偶极矩发生改变的振动 (△μ≠ 0),才是红外活性振动6.振动自由度非线性分子振动自由度为(3n-6)线性分子振动自由度为(3n-5)7.分子的振动方式1)分类(变形振动亦称弯曲振动) 2)频率大小反对称伸缩振动>对称伸缩振动>>弯曲振动面内弯曲振动>面外弯曲振动8.红外光谱谱带1)基频带:基态向第一振动激发态的跃迁2)泛频带(跃迁几率小,强度弱,难检出)a.倍频带:基态向第二、三……振动激发态的跃迁b.和频带:分子吸收光子后同时发生频率为ν和ν'的跃迁,此时产生的跃迁为(ν+ν')的峰c.差频带:吸收峰和发射峰重叠时产生峰(ν-ν')3)振动耦合带:当分子中两个基团共用一个原子时,如果这两个基团的基频振动频率相同或相近,就会发生相互作用,使原来的两个基团的基频振动频率距离加大,形成两个独立的吸收峰4)费米共振带:当强度很弱的的倍频带或组频带与另一强的基频带接近时,发生耦合,相互作用而产生很强的吸收峰或发生裂分,产生费米共振三.影响振动频率的关键因素1.发生震动能级跃迁所需能量大小取决于键两端原子的折合质量(μ)和键力常数(k)(其中k为键力常数,μ为折合质量)1)键力常数:a.键长越短,键级越大,表示键越强,键力常数就越大b.k越大,表示原子振动离开平衡位置很小的距离时,就会受到很大的回复力,所以就相对不容易振动2)折合质量2.电子效应1)诱导效应a.机理:通过使分子中的电子云分布发生变化,引起k的变化,从而影响振动频率b.分类①推电子效应:导致羰基的成键电子云移向氧原子更加偏离几何中心,使羰基的双键性降低,羰基伸缩振动向低频位移动②拉电子效应:使羰基的成键电子云更加接近几何中心,导致羰基的双键性增强,羰基伸缩振动向高频位移动2)共轭效应共轭效应通过π-键电子传递,导致双键的极性增强,双键性降低,伸缩振动频率向低波数位移3)超共轭效应当C-Hσ键和π键(或p轨道)处于平行位置时,会产生离域现象,产生和共轭效应相似的效应3.场效应原子或基团间不是通过化学键,而是它们的静电场通过空间相互作用分子中带部分负电的溴原子和氧原子空间接近,电子云相互排斥,产生相反的诱导极化,使溴原子和氧原子的负电荷相应减小,羰基极性降低,双键性增强,伸缩振动频率增加4.空间效应1)定义:环张力和空间位阻2)环张力影响:随着环的缩小,环内键角缩小,成环σ键的p电子成分增加,键长变长,振动谱带向低波数位移3)空间位阻分子中存在某种或某些基团因空间位阻影响到分子中正常的共轭效应或杂化状态时,导致振动谱带位移5.跨环效应通过空间发生的电子效应(a) (b) (c)(b)中羰基极性增强,双键程度下降羰基频率向低波段移动,(c)中羰基峰消失,出现羟基峰极性基团的伸缩振动频率通常随溶剂极性增加而降低(红外光谱通常在非极性溶剂中测量)四.红外光谱的四大区1.第一峰区(3700~2500)X-H (X=O,N,C)1)O-H伸缩振动a.醇与酚①游离:~3600 中等强(m)②缔合:~3300 宽强 (s,b)(氢键存在向低波数移动)(区别伯仲叔醇:C-O伸缩振动峰位置的差异;区别酚醇:苯基特征吸收峰及高波数的的C-O峰)注意:样品中有水时,出现O-H伸缩及弯曲振动干扰判断b.羧酸①二聚体:~3000 宽散(波数降低,由于共振结构,氢键不断变化)(区别羧酸与醇酚:有羰基峰)2)N-H伸缩振动a.胺类①伯胺:~3500,~3400 尖弱(较低波数处可能出现第三条)②仲胺:~3400③叔胺无吸收b.酰胺类①游离态:~3450②伯酰胺:~3350,~3150③仲酰胺:~3200④叔酰胺无吸收(区别胺与酰胺:)c.铵盐3000~2250 强/中宽,多重 m/s.b.(与羧酸O-H类似,但波数更低)(区别胺与铵盐:铵盐谱带更宽,波数更低;区别铵盐与羧酸:铵盐谱带更宽,波数更低,且羧酸有羰基的特征吸收带) 3)C-H伸缩振动a.炔烃:~3300 尖强(与羰基共轭无影响)(区别炔烃与醇酚胺:比缔合态的O-H吸收弱,N-H吸收强,谱带尖锐)b.烯/芳烃: ~3050 m/w(羧酸,缔合羟基,酰胺等可能掩盖,环丙烷~3060干扰)c.饱和烃基①伯碳:~2960(s),~2870(m)②仲碳:~2926(s),~2850(s)③叔碳:~2890(被伯仲碳掩盖,无实际价值)d.醛基:~2850 m,~2720 we.巯基:~2550 尖2.第二峰区(2500~1900)1)C≡C伸缩振动炔烃:~22002)C≡N伸缩振动氰基:~22503)N≡N伸缩振动重氮基:~2260(s)4)累积双键(X=Y=Z)的伸缩振动a.O=C=O:~2349b.C=C=C:~2025(m),~1070(w)c.N=C=O:~2260(s),~1410(w)d.N=N=N:~2140(s),~1265(w)5)X-H(X=B,P,Se,Si)(s/m)a.有机硼化物:~2495b.有机膦化物:~2365c.有机硒化物:~2290d.有机硅化物:~22303.第三峰区(1900~1500)1)C=O伸缩振动(s)a.酮①R-CO-R: ~1715②R-CO-Ph:~1690①游离 ~1760②缔合 ~1720(在~3000出现s.b.,结合可以判断)d.酯① ~1740②不饱和酯 ~1760③不饱和酸酯 ~1715(在~1200出现2~3条s.b,结合可以判断)e.酰胺①酰胺Ⅰ带:~1665②酰胺Ⅱ带:~1550③酰胺III带:~1300f.酸酐①开链酸酐:~1850(s),~1780(s-,弱于前者)②环酸酐:~1830(s-),~1770(s,强于前者)2)C=C伸缩振动 (相比于C=C吸收频率较低,强度也弱得多) a.烯烃:~1630(结合~3050峰)b.苯环:~1600,~1500 2~3条3)硝基 ~1550,~1345 s.b.双峰4)亚硝基 ~15505)N-H弯曲振动a.伯胺 ~1600b.仲胺 ~15354.第四峰区(1500~650)(指纹区)1)C-H弯曲振动(烃类化合物)a.烷烃①伯碳:~1450(m),~1380(w)②仲碳:~1450(m)b.烯烃/芳香烃①RCH=CH2:~990(s),~910(s)②RR'C=CH2:~890(s)③RCH=CHR'(trans-):~970(s)④RCH=CHR'(cis-):~690(m)(不特征)c.芳香烃①环呼吸振动:~1600,~1500②面内弯曲振动:~1250(干扰大)③面外弯曲振动:PhCH3:~750,~700o-CH3PhCH3:~750m-CH3PhCH3:~780,~700p-CH3PhCH3:~8102)C-O伸缩振动a.醇①伯醇:~1050(s)②仲醇:~1100(s)③叔醇:~1150(s)(结合~3600/3300判断)b.酚 ~1200c.醚①对称:~1150②不对称:~1250,~1050d.酯~1200 2~3条(s)e.酸酐①开链酐:~1110②环酐:~12603)C-Cl:~7004)C-Br:~5505)C-S:~7006)C-N:~12307)Ar-N=:~13058)R-N=:~12309)-NH2:~78510)-NO2:~1350第二章 有机质谱一.基本原理1.质谱是化合物电离后按照质量数与所带电荷数之比被仪器分离并以离子质荷比与其相对强度记录下来的谱, 谱图与分子结构有关2.光谱信息:唯一可以给出分子量, 确定分子式的方法3.结构组成1)进样系统2)离子源离子化方法:a.电子轰击(EI)①电离效率高,产生较多碎片峰,可提供丰富的结构信息②分子离子峰较弱或不出现b.化学电离源(CI)①电离能小,质谱峰数少②准分子离子峰大c.场电离源(FI)电离温和,碎片少,主要产生分子离子峰d.场解析源(FD)①适于非挥发性且分子量上万的分子电离②产生分子离子峰和准分子离子峰e.快电子轰击(FAB)①适用于挥发性极低、极性很强的有机化合物、离子型化合物、热不稳定和分子量较大的化合物②会出现基质分子产生的相应的峰及基质分子与样品分子的结合峰f.电喷雾电离(ESI)①低分子量化合物产生单电荷离子(失去或得到1个质子)②高分子量生物大分子和聚合物产生多电荷离子③可能生成加合物和/或多聚体3)质量分析器4)检测器4.主要技术指标1)质量范围:指质谱计所检测的单电荷离子的质荷比范围2)分辨率(R)a.含义:质谱计分开相邻两离子质量的能力b.R=m/Δm(Δm为质谱计可分辨的相邻两峰的质量差,m为可分辨的相邻两峰的平均质量)5.质谱术语1)基峰2)质荷比3)低分辨率质量:组成离子的各元素同位素的原子核的质子和中子数目之和4)精确质量:基于精确原子量6.质谱中的离子:1)分子离子:z=1时, 其m/z等于天然丰度最大的同位素的原子量之和2)碎片离子:广义上指除分子离子以外的所有离子3)重排离子:经过重排,断裂一个以上化学键所生成的离子4)母/子离子:任何一个离子进一步裂解为质荷比较小 的离子,前者是后者的母离子或前体离 子,后者是前者的子离子5)奇/偶电子离子:带有未配对电子的离子为奇电子离子,无未配对电子的离子为偶电子离子6)多电荷离子:一个分子丢失一个以上(通常两个)电子所形成的离子7)准分子离子:比分子量多(或少)一的离子或准分子离子8)同位素离子:非单一同位素的元素在电离过程中产生同 位素离子,同位素离子构成同位素峰簇二.分子离子和分子式1.分子离子峰的识别1)假定分子离子峰2)判断是否合理:相邻碎片离子间的Δm/z=1,2,3,15,16,17,18,203)判断是否符合氮律:a.不含N或含偶数N的有机分子, 其分子离子峰的m/z为 偶数b.含奇数N的有机分子, 其分子离子峰的m/z为奇数2.分子离子峰的相对强度(RI)1)不稳定的分子,大分子,其分子离子的RI较弱2)稳定的分子, 大共轭分子, 其分子离子的RI较强3)脂肪族醇,胺,亚硝酸酯,硝酸酯,硝基化合物及多支链化合物分子离子峰通常很弱或不出现三.分子式判断1.分子式是否合理1)是否符合氮律2)不饱和度是否合理(UN>0)UN=(n+1)+a/2-b/2(其中,n为分子中4价原子数目,a为三价原子,b为一价原子)3)同位素峰簇的相对丰度a.S:32:33:34=100:0.8:4.4b.Si:28:29:30=100:5.1:3.4c.Cl:35:37≈3:1d.Br:79:81≈1:1三.有机质谱中的裂解反应1.分子中n电子比π电子易丢失,π电子比σ电子易丢失2.离子的正电荷愈分散,离子的稳定愈大3.分类1)自由基位置引发的裂解反应(α裂解)2)自由基位置引发的重排反应(γ氢重排)3)电荷位置引发的裂解反应(i裂解)OE+型(偶电子离子型),EE+型(奇电子离子型)4.一般的裂解规律1)偶电子规律a.偶电子离子裂解通常只能生成偶电子离子,质荷比较小的奇电子离子往往是由质荷比较大的奇电子离子裂解产生b.判断奇电子离子峰:①不含氮化合物质荷比为偶数值的峰为奇电子离子峰②含氮化合物,分子离子或碎片离子含奇数个氮,其质荷比为奇数时为奇电子离子③含氮化合物,分子离子或碎片离子含偶数个氮,其质荷比为偶数时为奇电子离子2)烃类化合物的裂解规律优先失去大的基团生成稳定的正碳离子3)含杂原子化合物的裂解规律α裂解和i裂解为主4)羰基化合物的裂解规律α裂解和i裂解为主5)逆D-A反应(RDA)6)氢的重排反应a.McLafferty重排(γ氢重排,六元环过渡态)b.自由基引发或正电荷诱导,经过四、五、六元环过渡态氢的重排c.长链酯基的双氢重排d.偶电子离子氢的重排经过四元环过渡态的β氢重排,使偶电子离子进一步裂解,生成质荷比较小的奇电子离子和稳定的小分子 e.芳环的邻位效应邻位取代芳环中,取代基通过六元环过渡态氢的重排,失去中性分子,生成奇电子离子的裂解过程四.各类有机化合物的质谱1.烃类1)直链烃a.弱分子离子峰可见b.M-29(C2H5),43+14n(CnH2n+1)峰(其中43,57往往是基峰)(伴随CnH2n-1,CnH2n峰群)2)支链烃a.分子离子峰弱或不见b.M-15峰(可能含有侧链甲基)c.侧链优先断裂,失去大基团,支链处峰强度增大3)环烷烃a.分子离子峰较强b.出现41,55,69峰4)烯烃a.α断裂 41峰(CH2=CH-CH2+) 基峰或强峰b.γ-氢重排 42峰(CH2=CH-CH3+·) 基峰或强峰c.41+14n峰(伴随CnH2n+1,CnH2n峰群)d.环己烯及其衍生物发生RDA反应或裂解生成稳定的环烯离子5)芳香烃a.分子离子峰强或中强b.α断裂,产生91的基峰或强峰c.γ-H的重排,产生m/z为92的奇电子离子峰d.进一步裂解产生78,52或66,40峰2.含氧化合物1)醇/酚a.分子离子峰弱或不出现b.α裂解:31+14n的含氧碎片离子峰c.M-18(H2O),M-18-28(C2H2)H2n-1,CnH2n+1峰群e.例①环己醇②苄醇③苯酚2)醚a.弱分子离子峰b.α断裂,碳-碳σ键断裂:31+14n峰c.i异裂,碳-氧σ键断裂:43+14n峰d.伴有CnH2n , CnH2n -1 峰e.区别醇:无M-18,M-18-28失水峰f.双取代芳香醚取代基位置对其质谱有较大影响(见四.1.5) 例.对二甲氧基苯邻二甲氧基苯3.含硫化合物1)硫醇a.分子离子峰强b.出现M-33(-SH),M-34(-SH2),33,34峰c.出现含硫碎片离子峰47+14n(CnH2n+1S)d.伴有CnH2n,CnH2n-1,CnH2n+1峰2)硫醚a.分子离子峰较强b.生成CnH2n+1S+系列含硫碎片离子峰4.含氮化合物1)脂肪胺a.分子离子峰弱b.30+14n的含氮特征碎片离子峰c.44(or 44+14n),58(or 58+14n)的峰为基峰或强峰2)环己胺a.分子离子峰相对较强b.出现56峰 (CH2=CH-CH=NH2+)c.类似于环己醇裂解3)苯胺5.卤代烃1)分子离子峰强度由氟向碘依次增大2)卤素存在特征:a.氟:M-19(-F),M-20(-HF)b.氯、溴:①M-35(-Cl),36(-HCl),M-79(-Br),79(Br+)6.羰基化合物1)醛a.α断裂:产生M-1(-H),M-29(-CHO),29(强,HCO+)峰b.有明显的分子离子峰c.43+14n特征碎片离子峰(脂肪醛)2)酮3)羧酸a.弱分子离子峰b.出现M-17(-OH),M-45(-COOH),45(-COOH)峰c.γ-H重排生成60峰4)酯类a.小分子酯有明显的分子离子峰b.甲酯,乙酯出现M-31(-OCH3),M-45(-OC2H5)峰c. γ-H的重排生成m/z为74+14n的峰d.乙酯以上的酯双氢重排生成61+14n的偶电子离子5)酰胺有明显的分子离子峰(β改为α)7.双取代芳环-邻位效应芳环的邻位取代基间容易形成六元环过渡态,发生氢的重排裂解8.非氢重排1)环化取代重排2)消去重排a.烷基迁移b.苯基迁移c.烷氧基迁移d.氨基迁移。
第一章质谱习题1、有机质谱图的表示方法有哪些?是否谱图中质量数最大的峰就是分子离子峰,为什么?2、以单聚焦质谱仪为例,说明质谱仪的组成,各主要部件的作用及原理。
3、有机质谱的分析原理及其能提供的信息是什么?4、有机化合物在离子源中有可能形成哪些类型的离子?从这些离子的质谱峰中可以得到一些什么信息?5、同位素峰的特点是什么?如何在谱图中识别同位素峰?6、谱图解析的一般原则是什么?7.初步推断某一酯类(M=116)的结构可能为A或B或C,质谱图上m/z 87、m/z 59、m/z 57、m/z29处均有离子峰,试问该化合物的结构为何?(A)(B)(C)8.下列化合物哪些能发生McLafferty重排?9.下列化合物哪些能发生RDA重排?10.某化合物的紫外光谱: 262nm(15);红外光谱:3330~2500cm-1间有强宽吸收,1715 cm-1处有强宽吸收;核磁共振氢谱:δ11.0处为单质子单峰,δ2.6处为四质子宽单峰,δ2.12处为三质子单峰,质谱如图所示。
参照同位素峰强比及元素分析结果,分子式为C5H8O3,试推测其结构式。
部分习题参考答案1、表示方法有质谱图和质谱表格。
质量分析器出来的离子流经过计算机处理,给出质谱图和质谱数据,纵坐标为离子流的相对强度(相对丰度),通常最强的峰称为基峰,其强度定为100%,其余的峰以基峰为基础确定其相对强度;横坐标为质荷比,一条直线代表一个峰。
也可以质谱表格的形式给出质谱数据。
最大的质荷比很可能是分子离子峰。
但是分子离子如果不稳定,在质谱上就不出现分子离子峰。
根据氮规则和分子离子峰与邻近峰的质量差是否合理来判断。
2、质谱仪的组成:进样系统,离子源,质量分析器,检测器,数据处理系统和真空系统。
进样系统:在不破坏真空度的情况下,使样品进入离子源。
气体可通过储气器进入离子源;易挥发的液体,在进样系统内汽化后进入离子源;难挥发的液体或固体样品,通过探针直接插入离子源。
第一章紫外光谱一、名词解释1、助色团:有n电子的基团,吸收峰向长波方向移动,强度增强.2、发色团:分子中能吸收紫外或可见光的结构系统.3、红移:吸收峰向长波方向移动,强度增加,增色作用.4、蓝移:吸收峰向短波方向移动,减色作用.5、增色作用:使吸收强度增加的作用.6、减色作用:使吸收强度减低的作用.7、吸收带:跃迁类型相同的吸收峰.二、选择题1、不是助色团的是:DA、-OHB、-ClC、-SHD、 CH3CH2-2、所需电子能量最小的电子跃迁是:DA、σ→σ*B、 n →σ*C、π→π*D、 n →π*3、下列说法正确的是:AA、饱和烃类在远紫外区有吸收B、 UV吸收无加和性C、π→π*跃迁的吸收强度比n →σ*跃迁要强10-100倍D、共轭双键数目越多,吸收峰越向蓝移4、紫外光谱的峰强用εmax表示,当εmax=5000~10000时,表示峰带:B很强吸收B、强吸收 C、中强吸收 D、弱吸收5、近紫外区的波长为:CA、 4-200nmB、200-300nmC、200-400nmD、300-400nm6、紫外光谱中,苯通常有3个吸收带,其中λmax在230~270之间,中心为254nm的吸收带是:BA、R带B、B带C、K带D、E1带7、紫外-可见光谱的产生是由外层价电子能级跃迁所致,其能级差的大小决定了CA、吸收峰的强度B、吸收峰的数目C、吸收峰的位置D、吸收峰的形状8、紫外光谱是带状光谱的原因是由于:DA、紫外光能量大B、波长短C、电子能级差大D、电子能级跃迁的同时伴随有振动及转动能级跃迁的原因9、π→π*跃迁的吸收峰在下列哪种溶剂中测量,其最大吸收波长最大:AA、水B、乙醇C、甲醇D、正己烷10、下列化合物中,在近紫外区(200~400nm)无吸收的是:AA、 B、 C、 D、11、下列化合物,紫外吸收λmax值最大的是:A(b)A、 B、 C、 D、12、频率(MHz)为4.47×108的辐射,其波长数值为AA、σ→σ*B、π→π*C、n→σ*D、n→π*第二章红外光谱一、名词解释:1、中红外区2、fermi共振3、基频峰4、倍频峰5、合频峰6、振动自由度7、指纹区8、相关峰9、不饱和度10、共轭效应11、诱导效应12、差频二、选择题(只有一个正确答案)1、线性分子的自由度为:AA:3N-5 B: 3N-6 C: 3N+5 D: 3N+62、非线性分子的自由度为:BA:3N-5 B: 3N-6 C: 3N+5 D: 3N+63、下列化合物的νC=C的频率最大的是:( )A B C D答案:CH2CH2CH21651 1657 1678 1680O O1716 1745 1775 1810 OOCH24、下图为某化合物的IR图,其不应含有:DA:苯环 B:甲基 C:-NH2 D:-OH5、下列化合物的νC=C的频率最大的是:A B C D答案:1646 1611 1566 164116506、亚甲二氧基与苯环相连时(1,2亚甲二氧基苯:),其亚甲二氧基的δCH 特征强吸收峰为:AA:925~935cm-1B:800~825cm-1C:955~985cm-1D:1005~1035cm-17、某化合物在3000-2500cm-1有散而宽的峰,其可能为:AA:有机酸 B:醛 C:醇 D:醚8、下列羰基的伸缩振动波数最大的是:C9、中三键的IR区域在:BA ~3300cm-1B 2260~2240cm-1C 2100~2000cm-1D 1475~1300cm-110、偕三甲基(叔丁基)的弯曲振动的双峰的裂距为:DA 10~20 cm-1 B15~30 cm-1 C 20~30cm-1 D 30cm-1以上第三章核磁共振一、名词解释1、化学位移2、磁各向异性效应3、自旋-自旋驰豫和自旋-晶格驰豫4、屏蔽效应5、远程偶合6、自旋裂分7、自旋偶合8、核磁共振CRORACROHBCROFCROClC DC NR9、屏蔽常数10.m+1规律11、杨辉三角12、双共振13、NOE效应14、自旋去偶15、两面角16、磁旋比17、位移试剂二、填空题1、1HNMR化学位移δ值范围约为 0~14 。
波谱分析第一章 紫外光谱1、为什么紫外光谱可以用于有机化合物的结构解析?紫外光谱可以提供:谱峰的位置(波长)、谱峰的强度、谱峰的形状。
反映了有机分子中发色团的特征,可以提供物质的结构信息。
2、紫外-可见区内(波长范围为100-800 nm )的吸收光谱。
3、Lamber-Beer 定律 适用于单色光• 吸光度: A = lg(I 0/I) = εlc • 透光度:-lg T = εbcA :吸光度;l :光在溶液中经过的距离;ε:摩尔吸光系数,为浓度在1mol/L 的溶液中在1 cm 的吸收池中,在一定波长下测得的吸光度;c :浓度。
4、有机物分子中含有π键的不饱和基团称为生色团;有一些含有n 电子的基团(如—OH 、—OR 、—NH 2、—NHR 、—X 等),它们本身没有生色功能(不能吸收λ>200 nm 的光),但当它们与生色团相连时,就会发生n —π共轭作用,增强生色团的生色能力(吸收波长向长波方向移动,且吸收强度增加),这样的基团称为助色团。
5、λmax 向长波方向移动称为红移,向短波方向移动称为蓝移(或紫移)。
吸收强度即摩尔吸光系数ε增大或减小的现象分别称为增色效应或减色效应。
6、电子跃迁的类型:1. σ→σ*跃迁:饱和烃(甲烷,乙烷);E 很高,λ<150 nm (远紫外区)。
2. n→σ*跃迁:含杂原子饱和基团(-OH ,-NH 2);E 较大,λ150~250 nm (真空紫外区)。
3. π→π*跃迁:不饱和基团(-C=C-,-C=O );E 较小,λ~ 200 nm ,体系共轭,E 更小,λ更大;该吸收带称为K 带。
4. n→π*跃迁:含杂原子不饱和基团(-C≡N ,C=O ):E 最小,λ 200~400 nm (近紫外区)该吸收带称为R 带。
7、λmax 的主要影响因素:1. 共轭体系的形成使吸收红移;2. pH 值对光谱的影响:碱性介质中,λ↑,吸收峰红移,ε↑ 3. 极性的影响:π→π*跃迁:极性↑,红移,λ↑;ε↓。
有机化合物波谱解析复习指导广东药学院天然药物化学教研室200 5年 5 月目录第一章紫外光谱… … … … …… … … … … …… 2~4第二章红外光谱… … … … … … …… ………… 5~11第三章核磁共振… … … … … … … …… … ……… 12~34 第四章质谱… … … … …… … … … … … … …35~41 第五章综合解析… … … …… … … … … … … …… 42~70第一章紫外光谱一、名词解释1、助色团2、发色团3、红移4、蓝移5、增色作用6、减色作用7、吸收带二、选择题1、不是助色团的是:A、-OHB、-ClC、-SHD、CH3CH2-2、所需电子能量最小的电子跃迁是:A、σ→σ*B、n →σ*C、π→π*D、n →π*3、下列说法正确的是:A、饱和烃类在远紫外区有吸收B、UV吸收无加和性C、π→π*跃迁的吸收强度比n →σ*跃迁要强10-100倍D、共轭双键数目越多,吸收峰越向蓝移4、紫外光谱的峰强用εmax表示,当εmax=5000~10000时,表示峰带:A、很强吸收B、强吸收C、中强吸收D、弱吸收5、近紫外区的波长为:A、4-200nmB、200-300nmC、200-400nmD、300-400nm6、紫外光谱中,苯通常有3个吸收带,其中λmax在230~270之间,中心为254nm的吸收带是:A、R带B、B带C、K带D、E1带7、紫外-可见光谱的产生是由外层价电子能级跃迁所致,其能级差的大小决定了:A、吸收峰的强度B、吸收峰的数目C、吸收峰的位置D、吸收峰的形状8、紫外光谱是带状光谱的原因是由于:A、紫外光能量大B、波长短C、电子能级差大D、电子能级跃迁的同时伴随有振动及转动能级跃迁的原因9、π→π*跃迁的吸收峰在下列哪种溶剂中测量,其最大吸收波长最大:A、水B、乙醇C、甲醇D、正己烷10、下列化合物中,在近紫外区(200~400nm)无吸收的是:11、下列化合物,紫外吸收λmax值最大的是:A、B 、C 、D、12、频率(MHz)为4.47×108的辐射,其波长数值为A、670.7nmB、670.7μC、670.7cmD、670.7m13、化合物中,下面哪一种跃迁所需的能量最高A、σ→σ*B、π→π*C、n→σ*D、n→π*三、问答题1、根据Woodward计算规则,计算下列化合物的UVλmaxCH3 AcO CH3CHCH3CH3CHHOOCCHCH32、某化合物在乙醇中的UVλmax分别为236nm(ε=12000),245nm(ε=18000)请推断其分别为结构A还是B?CH3C H3A B3、一化合物初步推断其结构不是A就是B,经测定UVλmax EtOH=352nm,试问其结构为何?O OA B5、一环己烯酮衍生物,其UVλmax EtOH=235nm,假如共轭体系中连接有烷基(R),试问发色体系的可能结构是什么?指出烷基取代位置。
6、某强心苷元的结构可能为(A)或(B),测得紫外光谱λmax EtOH=218nm,试问其结构为何者?OCH3CH3OH OOCH3CH3OHO(A)(B)7、下列二组化合物中,哪个吸收波长较长?(1)CH3-CH=CH2和CH2=CH-CH=CH=CH3(2)O CH3和O CH38、pH对某些化合物的吸收带有一定的影响,例如苯胺在酸性介质中它的K吸收带和B吸收带发生蓝移,而苯酚在碱性介质中其K吸收带和B吸收带发生红移,为什么?羟酸在碱性介质中它的吸收带和形状会发生什么变化?9、某化合物的紫外光谱有B吸收带,还有λ=240nm,ε=13×104及λ=319nm,ε=50两个吸收带,此化合物中含有什么基团?有何电子跃迁?10、将下列化合物按K吸收带波长大小次序排列起来,并证明排列的理由。
第二章红外光谱一、名词解释:1、中红外区2、fermi共振3、基频峰4、倍频峰5、合频峰6、振动自由度7、指纹区8、相关峰9、不饱和度10、共轭效应11、诱导效应12、差频二、选择题(只有一个正确答案)1、线性分子的自由度为:A:3N-5 B: 3N-6 C: 3N+5 D: 3N+62、非线性分子的自由度为:A:3N-5 B: 3N-6 C: 3N+5 D: 3N+63、下列化合物的νC=C的频率最大的是:A B C D4、下图为某化合物的IR图,其不应含有:A :苯环B :甲基C :-NH 2D :-OH5、下列化合物的νC=C 的频率最大的是:A B C D6、亚甲二氧基与苯环相连时,其亚甲二氧基的δCH 特征强吸收峰为: A : 925~935cm -1 B :800~825cm -1C : 955~985cm -1D :1005~1035cm -17、某化合物在3000-2500cm -1有散而宽的峰,其可能为: A : 有机酸 B :醛 C :醇 D :醚8、下列羰基的伸缩振动波数最大的是:9、 中三键的IR 区域在:A ~3300cm -1B 2260~2240cm -1C 2100~2000cm -1D 1475~1300cm -110、偕三甲基(特丁基)的弯曲振动的双峰的裂距为:A 10~20 cm -1 B15~30 cm -1 C 20~30cm -1 D 30cm -1以上三、问答题1、某化合物的分子式为C 3H 6O ,IR 如下,请推断其可能结构式。
C R OR A C R O H B C R O F C R O Cl C D C N R2、某化合物的IR 图谱如下,其分子式为C 8H 8O ,试推断其可能的结构式。
3、比较下列化合物的IR 的相同与不同处?4、某化合物的IR 如下,请问:C O C H 3OH A C O C H 3H B C O C H 3NH 2CC O CH 3CH 3D(3)是否有双键、三键等结构? (4)是否为有机胺类化合物? 说明有关理由。
5、比较下列化合物的IR 的相同与不同处?6、用红外光谱法区别下列各对化合物。
7、某化合物的IR 图谱如下,其分子式为C 7H 9N ,试推断其可能的结构式。
C O NH 2C O OHCO HA B C8、某化合物的IR 图谱如下,其分子式为C 10H 14O ,试推断其可能的结构式。
9、有一化合物的红外谱中2870cm -1及926 cm -1的强吸收,无2960 cm -1,试判断该化合物的正确结构,并说出理由?10、比较下列化合物的IR 的特征吸收的异同。
11、红外光谱产生的条件是什么?吸收峰的强度由那些因素决定?12、下列化合物的IR 光谱有何不同? (A )、CH 3-CH=CH-CH 3 (B )、CH 3-CH=CH 2O O C O A MeO MeO C O B CH 3CH 3CH 3CH 3CH 3CH 3A B COHOH和(2)CH 3COOHCOOCH 3和14、试将C=O 键的特征吸收峰按波数高低的顺序排列(1)(2)15、下列各组化合物在IR 光谱的什么区域有不同的特征吸收? (1)CH 3CH 2和CH3C OCH3C O OHCH3COCH3CH3C O NH2O CH 3CO CH 3CH 3COCH 3NH 2CO CH 3CH 3CH 3CH 3COCH 316、溴甲苯C7H7Br有一单峰在803cm-1处,它的正确结构是什么?17、下列两个化合物中,为什么A的νC=O频率低于B?OO O O(A)νC=O1731 cm-1 νC=O1731 cm-11760 cm-1 1776 cm-118、顺式环戊二醇-1,2的CCl4稀溶液,在3620 cm-1及3455 cm-1处显两个峰,为什么?19、下列三个化合物的IR光谱有何不同?(A)CH3(CH2)6COOH (B)(CH3)3CCHOHCH2CH3(C)(CH3)3CCH(CH2CH3)N(CH3)220、下列化合物在4000~1650 cm-1区域内有何吸收?ONH2CANHBCOOHCC OH3C3COH 和第三章核磁共振一、名词解释1、化学位移2、磁各向异性效应3、自旋-自旋驰豫和自旋-晶格驰豫4、屏蔽效应5、远程偶合6、自旋裂分7、自旋偶合8、核磁共振9、屏蔽常数10.m+1规律11、杨辉三角12、双共振13、NOE效应14、自旋去偶15、两面角16、磁旋比17、位移试剂二、填空题1、1HNMR化学位移δ值范围约为。
2、自旋量子数I=0的原子核的特点是。
三、选择题1、核磁共振的驰豫过程是A自旋核加热过程B自旋核由低能态向高能态跃迁的过程C自旋核由高能态返回低能态,多余能量以电磁辐射形式发射出去D高能态自旋核将多余能量以无辐射途径释放而返回低能态2、请按序排列下列化合物中划线部分的氢在NMR中化学位移的大小a HH b (CH3)3COH c CH3COO CH3 d CH3C CCH33、二氟甲烷质子峰的裂分数和强度比是A单峰,强度比1B双峰,强度比1:1C 三重峰,强度比1:2:1D 四重峰,强度比1:3:3:14、核磁共振波谱产生,是将试样在磁场作用下,用适宜频率的电磁辐射照射,使下列哪种粒子吸收能量,产生能级跃迁而引起的A 原子B 有磁性的原子核C 有磁性的原子核外电子D 有所原子核 5、磁等同核是指:A 、化学位移相同的核B 、化学位移不相同的核C 、化学位移相同,对组外其他核偶合作用不同的核D 、化学位移相同,对组外其他核偶合作用相同的核 6、具有自旋角动量,能产生核磁共振的原子核是:A 、13C 核B 、12C 核 C 、 32S 核D 、 16O 核7、在苯乙酮分子的氢谱中,处于最低场的质子信号为:A 、邻位质子B 、间位质子C 、对位质子D 、 甲基质子 8、下述化合物中的两氢原子间的4J 值为:H HA 、0-1HzB 、1-3HzC 、6-10HzD 、12-18Hz 9、NOE 效应是指:A 、屏蔽效应B 、各向异性效应C 、核的Overhauser 效应D 、电场效应10、没有自旋角动量,不能产生核磁共振的原子核是:A 、13C 核B 、2D 核C 、 15N 核D 、 16O 核11、在下述化合物的1HNMR 谱中应该有多少种不同的1H 核:A 、 1 种B 、2种C 、3种D 、4种12、下列各组化合物按1H 化学位移值从大到小排列的顺序为:CH 2=CH 2CHCHC H OHa b.. c. d.A 、a>b>c>dB 、d>c>b>aC 、 c>d>a>bD 、b>c>a>d13、当采用60MHz 频率照射时,发现某被测氢核共振峰与TMS 氢核间的频率差( )为420Hz ,试问该峰化学位移( )是多少ppm :A 、10B 、7C 、6D 、 4.214、下述化合物氢谱中的甲基质子化学位移范围为:C CH 3OA 、0-1ppmB 、2-3ppmC 、4-6ppmD 、 6-8ppm15、下述化合物中的两氢原子间的3J 值为:H HA 、0-1HzB 、1-3HzC 、6-10HzD 、12-18Hz 16、 没有自旋的核为A 、1HB 、2HC 、12CD 、13 C 17、当采用60MHz 频率照射时,某被测氢核的共振峰与TMS 间的频率差(△ν)为430Hz ,问该峰化学位移(δ)是多少ppm?A 、4.3B 、43C 、7.17D 、6.0 18、化合物的1H NMR 谱中应该有多少种化学环境不同的1H 核?A 、 8B 、 4C 、 2D 、1 19、化合物O的1H NMR 谱中,化学位移处在最低场的氢核为A 、甲基B 、邻位氢C 、间位氢D 、对位氢 20、判断CH 3CH 2CH 2CO 2H 分子中1H 核化学位移大小顺序 a b c dA 、 a>b>c>dB 、d>c>b>aC 、 c>b>a>dD 、 d>a>b>c21、当采用60MHz 频率照射时,对羟苯乙羟酸分子中苯环上的四个氢呈现两组峰,分别为6.84和7.88ppm ,偶合常数为8 Hz ,试问该两组氢核组成何种系统? A 、A 2 B 2 B 、A 2 X 2 C 、AA ` BB ` D 、AA ` XX ` 22、在刚性六元环中,相邻两个氢核的偶合常数J aa 值范围为 A 、8---10Hz B 、0----2Hz C 、2--3Hz D 、12--18Hz 23、在低级偶合的AX 系统中共有 条谱线。