有机化合物波谱综合解析
- 格式:ppt
- 大小:366.50 KB
- 文档页数:42

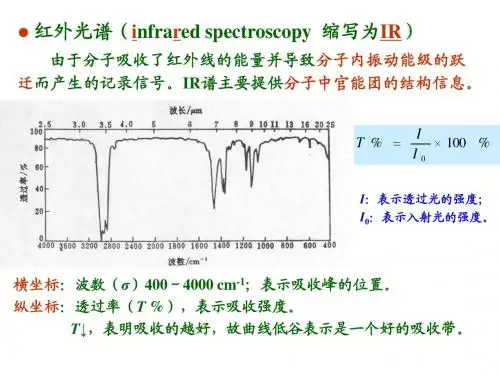
红外光谱(i nfra r ed spectroscopy 缩写为IR )由于分子吸收了红外线的能量并导致分子内振动能级的跃迁而产生的记录信号。
IR 谱主要提供分子中官能团的结构信息。
横坐标:波数(σ)400~4000cm -1;表示吸收峰的位臵。
纵坐标:透过率(T %),表示吸收强度。
T ↓,表明吸收的越好,故曲线低谷表示是一个好的吸收带。
%100%0⨯=I IT I :表示透过光的强度;I 0:表示入射光的强度。
红外光谱官能团区(4000-1500 cm -1)由分子的伸缩振动导致,用于鉴定各种不同官能团产生红外光谱的必要条件:1.红外辐射光的频率与分子振动的频率相当,才能满足分子振动能级跃迁所需的能量,而产生吸收光谱。
2.只有能引起分子偶极矩的变化的振动才能产生IR 光谱。
完全对称的分子H 2、O 2、N 2不会产生红外吸收光谱。
H―C≡C―H 、R―C ≡C―R ,其C≡C (三键)振动也不能引起红外吸收。
指纹区(1500-650 cm-1)分子弯曲及伸缩振动吸收峰,多用于鉴定基团的结合方式官能团区(高频区)1500-4000 cm-1Y -H 伸缩振动区2500~3700 cm-1,Y= O、N、C。
Y≡Z 三键和累积双键伸缩振动区2100~2400 cm-1,主要是:C≡C、C≡N 三键和C=C=C、C=N=O 等累积双键的伸缩振动吸收峰。
Y=Z双键伸缩振动区1600~1800 cm-1,主要是:C=O、C=N、C=C等双键。
指纹区(低频区)650-1500 cm-1主要是:C-C、C-N、C-O等单键和各种弯曲振动的吸收峰,其特点是谱带密集、难以辨认。
红外谱图各主要官能团红外光谱的特征吸收峰频率3600-3200NH, OH d, br, s3300C CHstrong3100-3010 =C-H middle2960-2850 -C-H strong2260-21002700-CHO doubleC Cvariable1850-1690 C=OAcids, esters Ketones Aldehydes very strong1680-1620 or 1600-1500 C=C variable 1470-1350 bend C-H1000-700 bend alkenes benzene substituted type4000cm-1650cm-11300-1030 bend C-O C-N几个明显的红外特征峰-OH(醇和酚):-OH吸收处于3200~3650cm-1,由于-OH可形成分子间或分子内氢键,而氢键所引起的缔合对红外吸收峰的位臵、形状和强度都有重要影响。


有机化合物波谱分析有机化合物波谱分析是一种重要的手段,可用于确定有机物的分子结构和功能基团。
其中,核磁共振波谱(NMR)和红外光谱(IR)是两种常用的波谱技术。
本文将重点介绍这两种波谱分析技术的基本原理、应用和解读方法。
核磁共振波谱(NMR)是一种基于核自旋的波谱分析方法。
它通过测量核自旋与外加磁场相互作用导致的能量变化来获得信息。
核磁共振波谱图通常由若干个特征峰组成,每个峰对应于一种不同类型的核。
峰的位置称为化学位移,可以通过参考物质(如四氯化硅)来标定。
峰的形状和强度可以提供有关分子结构和相互作用的信息。
核磁共振波谱提供了关于有机分子的碳氢骨架以及官能团、取代基等信息,因此在有机化学和药物化学领域有广泛应用。
红外光谱(IR)是一种基于分子振动的波谱分析方法。
它通过测量物质吸收红外辐射的能量来获得信息。
由于不同分子具有不同的振动模式和结构,它们吸收红外辐射的方式也不同。
红外光谱图通常由一系列特征峰组成,峰的位置称为波数,可以用来标识不同的官能团和化学键。
峰的强度和形状可以提供关于分子的结构和取向的信息。
红外光谱在有机化学、聚合物化学和无机化学等领域都有广泛的应用。
在进行有机化合物波谱分析时,需要先对样品进行样品制备。
核磁共振波谱通常需要溶解样品,然后将溶液转移到核磁共振管中进行测量。
红外光谱则可以对固体、液体和气体样品进行测量,通常需要将样品制备成固体片或涂在透明载体上。
波谱仪器通常会提供相应的样品制备方法和参数设置。
在分析核磁共振波谱和红外光谱时,需要注意以下几个方面。
首先,对于核磁共振波谱,要正确解读峰的化学位移。
化学位移受到许多因素的影响,如官能团、电子效应、取代基等。
因此,需要结合文献和经验来确定不同类型核的化学位移范围。
其次,对于红外光谱,要正确解读峰的波数。
不同的官能团和化学键都有特定的波数范围,可以用来确定它们的存在。
最后,对于波谱图的解读,需要综合考虑各种信息,如位置、形状、强度和相对强度等。


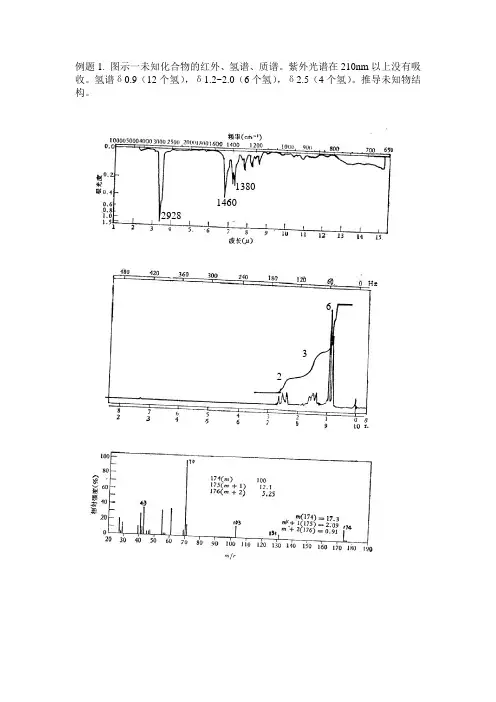
例题1. 图示一未知化合物的红外、氢谱、质谱。
紫外光谱在210nm以上没有吸收。
氢谱δ0.9(12个氢),δ1.2~2.0(6个氢),δ2.5(4个氢)。
推导未知物结构。
292814601380236例题2. 图示一未知化合物的氢谱、红外、紫外和质谱(M+为222)。
紫外光谱:浓度1.6mg/25ml的乙醇溶液,槽的厚度为5mm。
氢谱δ8.2~7.6多重峰(4个氢),δ4.5附近四重峰(4个氢),δ0.8附近三重峰(6个氢)。
根据这些光谱写出结构式。
446例题3.图示一未知化合物的氢谱、红外、紫外和质谱。
化合物由C、H、O、N 组成,高分辨质谱M+109.0527确定分子式C6H7NO。
紫外光谱:(a)浓度3.45mg/25ml,槽的厚度5mm.(b)加酸(c)加碱。
氢谱:δ7.8(1个氢),δ7~6.7(1个氢),δ6.3~6(3个氢),δ4.4(2个氢),推导结构式。
例题4. 未知物质谱确定分子量为137,其红外光谱图中3400~3200cm-1有一个宽而强的吸收峰,根据氢谱和碳谱推测未知物结构。
氢谱中从低场到高场各峰面积比为2:2:1:2:2:2。
例题5未知物元素分析结果为C:68.27%,H:7.63%,N:3.80%,O:20.30%。
图示未知物的红外、紫外、质谱、核磁共振谱(1H、13C、DEPT45、DEPT135、DEPT135、HMQC、HMBC),推测化合物结构。
例6.下面给出某一未知物的MS、IR、和氢谱,试推测其结构。
例7. 从伞形科植物防风中提取分离得到一个化合物,为无色针状结晶,UV max(MeOH)nm: 232,287,325, 在紫外灯下显天蓝色荧光,氢谱、碳谱、HMBC、MS谱如图所示,试解释其结构。



有机化合物波谱解析教案一、教学目标1. 让学生了解有机化合物波谱解析的基本概念和原理。
2. 使学生掌握红外光谱、核磁共振氢谱、质谱等常见波谱的分析方法和技巧。
3. 培养学生运用波谱解析技术解决实际问题的能力。
二、教学内容1. 有机化合物波谱解析概述1.1 波谱解析的概念1.2 波谱解析的方法和分类2. 红外光谱分析2.1 红外光谱的基本原理2.2 红外光谱图的解读2.3 红外光谱的应用实例3. 核磁共振氢谱分析3.1 核磁共振氢谱的基本原理3.2 核磁共振氢谱图的解读3.3 核磁共振氢谱的应用实例4. 质谱分析4.1 质谱的基本原理4.2 质谱图的解读4.3 质谱的应用实例5. 波谱解析的综合应用5.1 波谱解析在有机合成中的应用5.2 波谱解析在有机结构鉴定中的应用5.3 波谱解析在其他领域的应用三、教学方法1. 讲授法:讲解基本概念、原理和分析方法。
2. 案例分析法:分析具体实例,让学生学会运用波谱解析技术解决问题。
3. 互动讨论法:引导学生提问、思考和探讨,提高学生的学习兴趣和积极性。
四、教学准备1. 教材或教学资源:《有机化合物波谱解析》相关教材或教学课件。
2. 实验设备:红外光谱仪、核磁共振仪、质谱仪等。
3. 计算机和投影仪:用于展示波谱图和教学课件。
五、教学评价1. 课堂参与度:观察学生在课堂上的提问、思考和讨论情况,评价学生的学习积极性。
2. 课后作业:布置相关练习题,评价学生对知识点的掌握程度。
3. 实验报告:评价学生在实验中的操作技能和分析能力。
4. 期末考试:设置有关波谱解析的题目,全面评价学生的学习效果。
六、教学活动安排1. 第一课时:有机化合物波谱解析概述1.1 波谱解析的概念1.2 波谱解析的方法和分类2. 第二课时:红外光谱分析2.1 红外光谱的基本原理2.2 红外光谱图的解读2.3 红外光谱的应用实例3. 第三课时:核磁共振氢谱分析3.1 核磁共振氢谱的基本原理3.2 核磁共振氢谱图的解读3.3 核磁共振氢谱的应用实例4. 第四课时:质谱分析4.1 质谱的基本原理4.2 质谱图的解读4.3 质谱的应用实例5. 第五课时:波谱解析的综合应用5.1 波谱解析在有机合成中的应用5.2 波谱解析在有机结构鉴定中的应用5.3 波谱解析在其他领域的应用七、教学反思在教学过程中,教师应不断反思自己的教学方法和解题策略,针对学生的反馈情况进行调整,以确保教学效果的最大化。
