064-水产食品微生物检验原始记录
- 格式:doc
- 大小:57.00 KB
- 文档页数:1


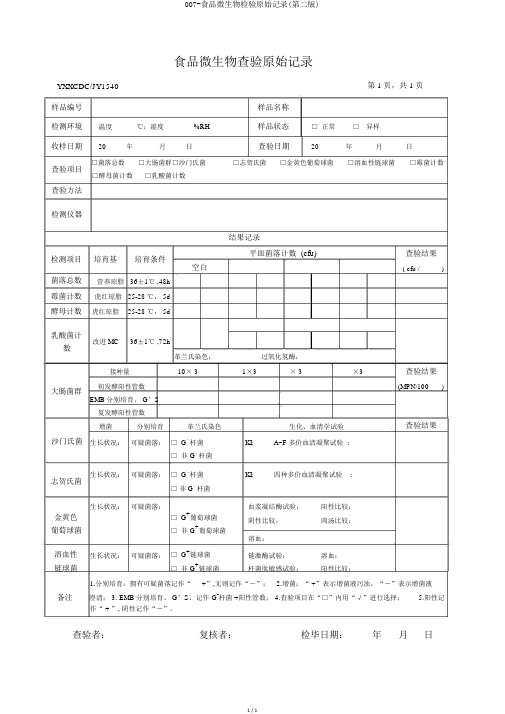
007-食品微生物检验原始记录(第二版)1 / 1食品微生物查验原始记录YXXCDC/JY1540 第1页,共 1页样品编号样品名称检测环境 温度℃;湿度%RH 样品状态 □ 正常 □ 异样收样日期 20年 月日查验日期20年月日查验项目□菌落总数 □大肠菌群□沙门氏菌 □志贺氏菌□金黄色葡萄球菌□溶血性链球菌□霉菌计数□酵母菌计数□乳酸菌计数查验方法检测仪器结果记录检测项目培育基 培育条件平皿菌落计数 (cfu)查验结果空白( cfu /)菌落总数 营养琼脂 36±1℃ ,48h 霉菌计数虎红琼脂 25-28 ℃, 5d酵母计数 虎红琼脂 25-28 ℃, 5d乳酸菌计改进 MC36±1℃ ,72h数革兰氏染色: 过氧化氢酶:接种量 10× 31×3× 3×3查验结果大肠菌群初发酵阳性管数(MPN/100)EMB 分别培育、 G ’S复发酵阳性管数增菌分别培育 革兰氏染色生化、血清学试验 查验结果沙门氏菌 生长状况: 可疑菌落: □ G -杆菌KI:A~F 多价血清凝聚试验 :□ 非 G -杆菌志贺氏菌 生长状况: 可疑菌落: □ G -杆菌KI:四种多价血清凝聚试验 :□ 非 G -杆菌生长状况: 可疑菌落: 血浆凝结酶试验: 阳性比较: 金黄色□ G +葡萄球菌 阴性比较:肉汤比较:葡萄球菌□ 非 G +葡萄球菌溶血:溶血性生长状况: 可疑菌落: □ G +链球菌链激酶试验: 溶血:链球菌□ 非 G +链球菌杆菌肽敏感试验:阳性比较:1.分别培育:拥有可疑菌落记作“ +”,无则记作“-”;2.增菌:“ +”表示增菌液污浊,“-”表示增菌液备注澄清; 3. EMB 分别培育、 G ’S :记作 G -杆菌 +阳性管数; 4.查验项目在“□”内用“√”进行选择; 5.阳性记作“ + ”, 阴性记作“-”。
查验者: 复核者: 检毕日期: 年 月 日。


检验原始记录(水产)
NO:
样品名称样品批号规格型号产品标准□GB/T23497
方法标准
项目及判定
GB/T4789.2 GB/T4789.3 GB /T5009.3 SC /T3011
1、菌落总数
cfu/g≤稀释度实测值结果备注100
10-1
10-2
2、大肠菌群MPN/1g(ml)
≤
0.1ml 0.01ml 0.001ml
3、感官
实测结果备注
4、净含量(g)含量1: g
含量2: g
含量3: g
= (g)
3
平均净含量:
g
5、水分(%)X—试样中水分的含量,(g/100g)
结果:
% M1--样品重量+称量瓶,g
M2--样品和称量瓶干燥后重量,g
M3--称量瓶重量,g
计算公式
M1-M2
X=×100%= %
M1-M3
6、盐分%/100g X—样品中盐分含量(以NaC1计),%;
V--滴定样品所用硝酸银标准液的体积,
mL;
V0--滴定空白所用硝酸银的体积,mL;
V1--滴定移取滤液的体积,mL;
V2—样品处理后的总体积,mL;
C--硝酸银标准液的浓度,mol/L;
m—称取样品质量,g;
0.05845—与1mL 1mol/L硝酸银标准液
相当的氯化纳质量,g;
计算公式
(V-V0)×C×0.05845
X=×100
m×(V1-V2)
计算结果
报出结果/标准要求 / 2-8
化验员:审核:。

微生物限度检查原始记录
品 名 规格 批 号 数量
检验依据
日期
年 月 日
检验人 复核人
菌落总数
培养基名称:营养琼脂培养基 培养温度:36±1℃ 培养时间:72h ±2h
稀释倍数 检验结果:
规定:
判定:
碟号1 碟号2 平均菌落数
霉菌数
培养基名称:孟加拉红培养基 培养温度:25~28℃ 培养时间:120h ±2h
稀释倍数 检验结果:
规定:
判定:
碟号1 碟号2 平均菌落数
酵母菌数
培养基名称:孟加拉红培养基 培养温度:25~28℃ 培养时间:120h ±2h
稀释倍数 检验结果:
规定:
判定:
碟号1 碟号2 平均菌落数
大肠菌群
乳糖发酵试验
培养基:乳糖胆盐发酵液 培养温度:36±1℃培养时间:48±2h
稀释倍数×取样量(ml )
检验结果:
规定:
判定:
大肠菌群阳性管数
伊红美蓝琼脂平板分离培养 时间 18~24小时(36±1℃)结果:
有可疑菌落( 管)
革兰氏染色结果:□G-无芽孢( 管) 乳糖发酵管试验(24±2h 、36±1℃)结果:
产气( 管)。
食品卫生微生物检验原始记录样品编号:检验开始时间:年月日样品名称:检验完成时间:年月日检测项目:检测依据:一、菌落总数/霉菌酵母菌落数测定:无菌操作称(量)取样品25g或ml加入225ml的无菌生理盐水中,均质2分钟,做成1∶10样品液。
取1∶10稀释液1ml加入到9ml生理盐水中,混匀,做成1∶100样品均液。
以上法制备10倍系列稀释样品均液。
选择2-3个适宜稀释度的样品均液,吸取1ml样品均液于无菌平皿内,每个稀释度做2个平皿。
同时,分别吸取1ml空白稀释液加入两个无菌平皿内作空白对照,及时将15-20ml冷至46℃的平板计数培养基倾注平皿,转动平皿使其混合均匀,凝固后翻转平板,置 36℃±1℃培养小时,计数平板上菌落数(CFU)。
霉菌和酵母菌计数采用孟加拉红培养基,正置,28℃±1℃培养天,计数平板上菌落数(CFU)。
计算及结果:菌落总数(CFU/g,ml):霉菌菌落数(CFU/g,ml):酵母菌落数(CFU/g,ml):二、大肠菌群测定(MPN计数法):按菌落总数测定方法制备lO0、10-1、10-2、10-3、10-4……稀释液。
选择3个适宜的连续稀释度的样品均液,每个稀释度接种3管乳糖胆盐发酵管内,每管接种1ml(接种量在1mL以上者,则用双料乳糖胆盐发酵管),36℃±1℃培养箱培养24h±2h,如所有乳糖胆盐发酵管都不产气,则可报告大肠菌群阴性;如有产气,将产气的发酵管分别转种在伊红美蓝琼脂平板上,置36℃±1℃培养箱培养18h~24h,然后取出,观察菌落形态,并做革兰氏染色和验证试验。
在上述平板上,挑去1~2个进行革兰氏颜色,同时接种乳糖发酵管,置36℃±1℃培养箱培养24h±2h,观察产气情况。
凡乳糖管产气、革兰氏染色为阴性的无芽孢杆菌,即可报告为大肠菌群阳性。
注:○+产酸产气;+产酸不产气或有可疑菌落;-不产酸不产气或无可疑菌落;G-b革兰氏阴性杆菌;G+b革兰氏阳性杆菌;G+c革兰氏阳性球菌。
微生物检测原始记录表
表码:22000—7.11-05
编号:
样品名称采样地点采样时间
样品批号采样人检验日期
检验项目:细菌总数、MPN、沙氏门菌、志贺氏菌、葡萄球菌、链球菌、霉菌计数、酵母菌计数、蜡样芽胞杆菌
样品处理:固体样品称取25g+225ml无菌水作成1︰10,稀释样,根据检样标准及要求依次作递减稀释,选择2—3个稀释度作应用液。
5、致病菌检验结果记录:
取上稀释1︰10的样液分别10ml作增菌处理(GN8h.37℃.SF37℃-24h..1%葡糖肉汤37℃-24h。
7.5%NaCl 肉汤37℃-24h。
GN.SF增菌后作沙门氏菌、志贺氏菌的分离,接种于SS平皿37℃24h,观察菌落形态:
1%葡糖肉汤,7.5%NaCl肉汤增菌后作链球菌,金黄色球菌的分离,分别接种于血琼脂平皿37℃24h培养。
观察菌落形态:
致病菌检验结论:
检验:审核:日期:
时间银行资知通鉴
电话:139****7125QQ号:1055966837。