无机化学 原子结构
- 格式:ppt
- 大小:2.08 MB
- 文档页数:71


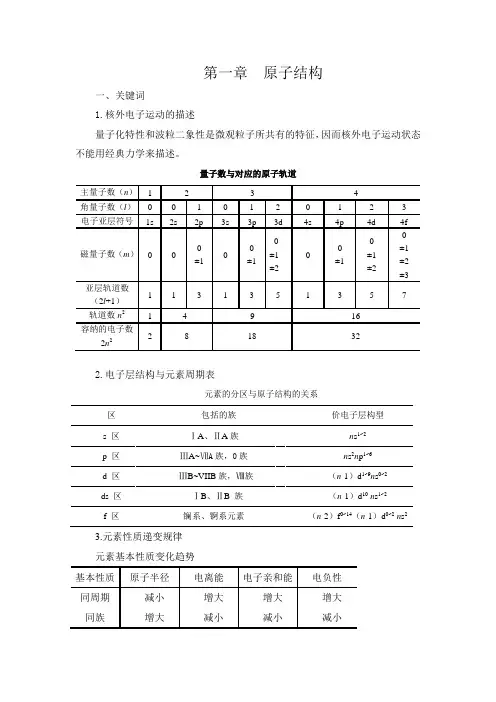
第一章原子结构一、关键词1.核外电子运动的描述量子化特性和波粒二象性是微观粒子所共有的特征,因而核外电子运动状态不能用经典力学来描述。
量子数与对应的原子轨道2.电子层结构与元素周期表元素的分区与原子结构的关系3.元素性质递变规律元素基本性质变化趋势二、学习感悟1.原子结构模型的演变历史给我们的启迪原子结构模型是科学家根据自己的认识,对原子结构的形象描摹。
一种模型代表了人类对原子结构认识的一个阶段。
人类认识原子的历史是漫长的、无尽的,随着科学技术的发展,人类对原子的认识过程还会不断深化。
①化学认识发展的规律和所有科学认识发展的规律一样是继承、积累和突破。
②实验方法是科学研究的一种重要方法,实验手段的不断改进促使化学理论向前发展。
人类对原子结构的认识体现了人类认识自然的历程,向我们提示了一个科学理论发展的模式:实践-认识-再实践-再认识。
2.研究原子结构涉及较深的数学知识和物理知识初学者往往觉得枯燥难懂,因此,学习时重点放在理解,接受相关的基本概念,加上一定的空间想像。
3.结构决定性质,性质体现结构元素的电离能、电子亲和能和电负性在衡量元素的金属性和非金属性强弱时,结果是大致相同的。
但由于元素的电负性的大小是表示分子中原子吸引电子的能力大小,所以它能方便地定性反映元素的某些性质,如:金属性与非金属性、氧化还原性;化合物中化学键的类型、键的极性等,故它在化学领域中被广泛地运用。
而元素的电子亲和能的数值一般较电离能小一个数量级,而且已知的元素的电子亲和能数据较少,测定的准确性也差,所以其重要性不如元素的电离能。
三、难点辅导1.微观粒子运动具有哪些特点?能量是量子化的。
量子化是相对于连续而言,也就是说变化过程是不连续的,是间隔的,是跳跃式的,一个一个的,不连续的。
与宏观物体的逐渐的、连续的运动有很大的区别。
打个比方说,光从微观角度讲就是不连续的,爱因斯坦的光子说中把每一个光子叫做光量子,是一个个不连续的能量包,虽然光没有静质量,但光有动质量,有质量就有能量。

第五章 原子结构和元素周期表本章总目标:1:了解核外电子运动的特殊性,会看波函数和电子云的图形2:能够运用轨道填充顺序图,按照核外电子排布原理,写出若干元素的电子构型。
3:掌握各类元素电子构型的特征4:了解电离势,电负性等概念的意义和它们与原子结构的关系。
各小节目标:第一节:近代原子结构理论的确立 学会讨论氢原子的玻尔行星模型213.6E eV n =。
第二节:微观粒子运动的特殊性1:掌握微观粒子具有波粒二象性(h h P mv λ==)。
2:学习运用不确定原理(2h x P mπ∆•∆≥)。
第三节:核外电子运动状态的描述1:初步理解量子力学对核外电子运动状态的描述方法——处于定态的核外电子在核外空间的概率密度分布(即电子云)。
2:掌握描述核外电子的运动状态——能层、能级、轨道和自旋以及4个量子数。
3:掌握核外电子可能状态数的推算。
第四节:核外电子的排布1:了解影响轨道能量的因素及多电子原子的能级图。
2;掌握核外电子排布的三个原则:○1能量最低原则——多电子原子在基态时,核外电子尽可能分布到能量最低的院子轨道。
○2Pauli 原则——在同一原子中没有四个量子数完全相同的电子,或者说是在同一个原子中没有运动状态完全相同的电子。
○3Hund原则——电子分布到能量简并的原子轨道时,优先以自旋相同的方式分别占据不同的轨道。
3:学会利用电子排布的三原则进行第五节:元素周期表认识元素的周期、元素的族和元素的分区,会看元素周期表。
第六节:元素基本性质的周期性掌握元素基本性质的四个概念及周期性变化1:原子半径——○1从左向右,随着核电荷的增加,原子核对外层电子的吸引力也增加,使原子半径逐渐减小;○2随着核外电子数的增加,电子间的相互斥力也增强,使得原子半径增加。
但是,由于增加的电子不足以完全屏蔽增加的核电荷,因此从左向右有效核电荷逐渐增加,原子半径逐渐减小。
2:电离能——从左向右随着核电荷数的增多和原子半径的减小,原子核对外层电子的引力增大,电离能呈递增趋势。

无机化学课程工程教学设计方案熊颖单位:江西省医药学校2014年 3 月5 日教学过程一、新课导入二、教学步骤2 §2.1 原子构造理论的开展概述一、含核的原子模型,古中国和古希腊的物质构造学说;,道尔顿的原子学说(1808 ):原子不行分;,卢瑟福的含核原子模型(1911 )。
二、玻尔的原子模型(一)氢原子光谱玻尔氢原子理论(1913 )(二)玻尔氢原子理论,原子构造理论的几点假设:原子构造理论的几点 3 1、在原子中,电子不是在随意轨道上绕核运动,而是在一些符合肯定条件(从量子论导出的条件)的轨道上运动。
稳定轨道(stable orbital)具有固定的能量,沿此轨道运动的电子,称为处在定态的电子,它不汲取能量,也不放射能量2、电子在不同轨道上运动时具有不同的能量,通常把这些具有不连续能量的状态称为能级(energy level)。
玻尔氢原子能级为:玻尔氢原子能级为: B E=, 2 n n称为量子数(quantum number n quantum number),其值可取1,2,3…等任何1 2 3… 正整数。
B为常数,其值等于2.18×10-18J。
3、当电子从某一轨道跃迁到另一轨道时,有能量的汲取或放出。
其频率ν 可由两个轨道的能量差,E确定:E2- E1 = ,E = hν h为普朗克常量,其数值为6.62618×1034J,s。
4 (三)对玻尔理论的评价优点:,优点:首先引入量子化的概念,说明了氢原子光谱为不连续光谱。
,缺乏:缺乏:(1)未能完全冲破经典力学连续概念,只是牵强加进了一些人为的量子化条件和假定。
(2)不能说明多电子原子(核外电子数大于1的原子)、分子或固体的光谱。
亦不能说明氢光谱的每条谱线事实上还可分裂为两条谱线的现象。
(3)未考虑其运动的波动性,采纳了宏观轨道的概念。
5 (四)几个根本概念,稳定轨道在原子中一些符合肯定条件(从量子论导出的条件)的轨道。





无机化学原子结构
无机化学是关于非有机物的研究,其原子结构由空间分子结构和核结构组成。
空间分子结构指物质的真实结构,而核结构是由原子核的结构组成,它由原子核和原子核外的电子构成。
首先,原子核结构包括核子和中子。
核子是原子核内的结构元素,它由原子核发射出的小点组成,可以由质量数和发射能量来描述。
原子核中的中子由原子核发射出的小点组成,可以由质量数和发射能量来描述。
其次,原子核外的电子结构可被分为电子层和电子层内的电子结构。
电子层由电子结构组成,它指电子组成原子的层次结构,如
1s,2s,2p,3s,3p,3d等加以形成,可以描述电子结构中各个电子能级的特征,比如它们的质量数和能量。
再次,原子核结构可以用空间分子结构来描述。
它是一种由原子核及其中的各原子组成的空间图案,根据质量数,其中原子核的形状可以描述为球形或长方体形,其中的原子由不同数量的电子组成,并且有多种层次结构,以便随着原子核电子束断裂的变化发生相应变化。
最后,空间分子结构还可以用于描述无机化学元素的分子性质,如分子式、分子量、熔点、沸点、折射率等。
无机化学基础知识归纳总结无机化学是研究无机物质的性质、结构、合成和应用的科学,是化学的重要分支之一。
在我们的日常生活中,无机化学无处不在,从药品和肥料到材料和电池都离不开无机化学的应用。
为了帮助大家更好地理解和掌握无机化学的基础知识,本文将对几个重要的概念和原理进行归纳总结。
一、原子结构与元素周期表1. 原子结构:原子由质子、中子和电子组成,质子和中子位于原子核中,电子环绕在核外的能级上。
2. 元素周期表:元素周期表是对元素进行分类和归纳的工具,按照原子的基本性质和化学行为,将元素有序地排列在周期表中。
二、化学键和化合物1. 化学键:化学键是原子之间的相互作用力,包括离子键、共价键和金属键等。
2. 化合物:化合物由两个或更多种元素通过化学键结合而成,具有特定的化学性质和结构特征。
三、离子反应和溶液化学1. 离子反应:离子反应是指溶液中的正离子与负离子之间发生的化学反应,包括酸碱中和反应和盐的生成等。
2. 溶液化学:溶液化学研究的是固体、液体或气体溶于溶液中的行为和性质,涉及到溶解度、溶液浓度和溶液的酸碱性等方面的内容。
四、配位化学1. 配位化学:配位化学研究的是过渡金属离子或中心金属离子与配体之间的相互作用和配合物的性质。
2. 配位反应:配位反应是指配体与金属离子形成配合物的过程,涉及到配位数、配合物的结构和性质等方面的内容。
五、无机反应和应用1. 氧化还原反应:氧化还原反应是指物质中电子的转移,涉及到氧化剂和还原剂的概念,包括电化学反应和电池等。
2. 无机化合物的应用:无机化合物在许多领域具有广泛的应用,如催化剂、药物、颜料和材料等。
六、无机分析1. 无机分析:无机分析是研究无机物质中化学成分和性质的方法和技术,包括定性分析和定量分析等。
2. 常用的分析方法:常用的无机分析方法包括滴定法、重量法、光谱法和电化学分析法等。
综上所述,无机化学基础知识涉及到原子结构、元素周期表、化学键和化合物、离子反应和溶液化学、配位化学、无机反应和应用,以及无机分析等多个方面。