§8.1 氢原子结构
1 1 例:n=1,l=0,m=0, ms , , 2 2
用四个量子数表示。
1 1 2 解: (1 , 0 , 0 , ) (1 , 0 , 0 , ) 1s 2 2
第八章
原子结构
§8.1 氢原子结构
例:填表。 原子轨道 2px 4f 6s n 2 l 1 m个数 容纳电子数 2
第八章 原子结构
(Atomic Structure) §8.1 氢原子结构
§8.2 多电子原子结构
§8.3 元素周期律
§8.1 氢原子结构
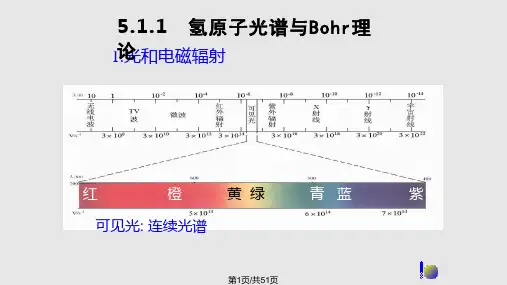
(Hydrogen Atomic Structure) 8.1.1 氢原子光谱与玻尔理论
8.1.2 电子的波粒二象性
8.1.3 薛定谔方程与波函数
8.1.4 量子数的物理意义
第八章
原子结构
§8.1 氢原子结构
2. 角量子数 (Azimuthal Quantum Number)
意义:决定原子轨道符号及形状,对应着同一主层 的电子亚层,和n共同决定电子能级。
取值:n个,从0 ~n-1(n个从零开始的正整 数)。 举例: l=0的原子轨道,在光谱中规定为 s轨道; l=0的原子轨道,说明角动量在各 方向无变化,原子轨道呈球形; l=0 的原子轨道,又称s亚层。
E2 E1 ν h
E:轨道能量(Orbital Energy)
ν :频率( Frequency )
h:Planck常数(Planck Constant)
普朗克
第八章
原子结构
§8.1 氢原子结构
(2)求出氢原子轨道的半径、能量、辐射能频率 18 1 2 r = 0.053n (nm) E - 2.179 10 2 J n 如 n=1,r = 0.053(nm), E= -2.17910-18J