(完整word)2013-2018年全国卷高考化学双向细目表(超全)
- 格式:doc
- 大小:1.14 MB
- 文档页数:12
![[VIP专享]高考化学双向细目表](https://uimg.taocdn.com/e5a1221fad02de80d5d8403e.webp)


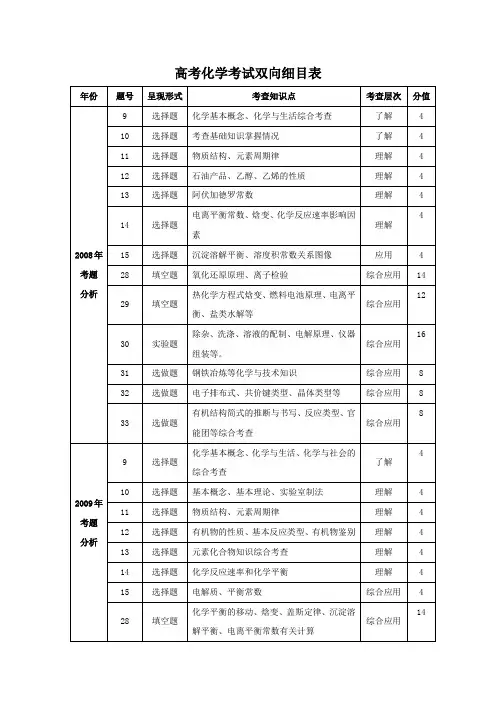
高考化学考试双向细目表2013年化学卷的知识点分布如下2014山东高考化学知识点高仿真试题一7.近来雾霾频现,“PM2.5”数据监测纳入公众视野.“PM2.5”是指大气中直径小于或等于2.5微米的细小颗粒物,也称为可入肺颗粒物.下列有关说法中,错误的是()A.雾霾有可能产生丁达尔现象B.近来雾霾的形成与工业排放的烟气有关系C.“PM2.5”没有必要纳入空气质量评价指标D.雾霾天气严重危害人体健康8.下列关于氮的说法正确的是()A.N2分子的结构较稳定,因而氮气不能支持任何物质燃烧B.23g NO2和N2O4混合气含有0.5N A个氮原子(N A表示阿伏加德罗常数)C.NO可用向上排空气法或者排水法收集D.浓硝酸保存在棕色瓶内是因为硝酸易挥发9.下列离子方程式正确的是()A.硫酸与氢氧化钡溶液反应:Ba2+ + SO42-=BaSO4↓B.铝和氢氧化钠溶液反应:Al+OH- + 3H2O=Al(OH)4-+ H2↑C.向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3-D.向沸水中逐滴加入FeCl3饱和溶液:Fe3+ +3 H2O Fe(OH)3(胶体) +3H+ 10.下列与有机物的结构、性质有关的叙述正确的是()A.乙烷和乙烯分别与C12反应均有二氯乙烷生成,反应类型相同B .纤维素−−→−水解葡萄糖−−→−氧化CO 2和H 2O (释放能量维持人体生命活动) C .乙醇、乙酸和乙酸乙酯能用饱和Na 2CO 3溶液鉴别D .汽油、水煤气、石蜡和纤维素的主要成分都是碳氢化合物11.臭氧是常见的强氧化剂,广泛用于水处理系统。
制取臭氧的方法很多。
其中高压放电法和电解纯水法原理如下图所示,下列有关说明不正确...的是 ( )A .高压放电法,反应的原理为:3O 2 2O 3B .高压放电出来的空气中,除含臭氧外还含有氮的氧化物C .电解法,电极b 周围发生的电极反应有:3H 2O-6e -=O 3+6H +;2H 2O-4e -=O 2+4H +D .电解时,H +由电极a 经聚合固体电解质膜流向电极b12.25℃,pH=3的醋酸溶液(I )和pH=l l 的氢氧化钠溶液(II ),下列说法正确的是( )A .I 和II 的物质的量浓度均为0.001mol•L﹣1B .将I 稀释l0倍,溶液中c (CH 3COOH )、c (OH ﹣)均减小 C .I 和II 溶液混合,若c (OH ﹣)>c (H +),则氢氧化钠过量D .I 和II 等体积混合后,溶液中离子浓度大小为c (CH 3COO ﹣)>c (Na +)>c (H +)>c (OH ﹣)13.如图,25℃时,在含有Pb 2+、Sn 2+的某溶液中,加入过量金属锡(Sn ),发生反应Sn (s )+Pb 2+(aq )Sn 2+(aq )+Pb (s )△H 体系中c (Pb 2+)和c (Sn 2+)变化关系下列判断正确的是( )A .往平衡体系中加入金属铅后,c (Pb 2+)增大B .往平衡体系中加入少量Sn (NO 3)2固体后,c (Pb 2+)不变 C .升高温度,平衡体系中c (Pb 2+)增大,说明该反应△H<0 D .c (Pb 2+)曲线表示正反应的快慢,c (Sn 2+)曲线表示逆反应的快慢28.(17分)工业上通常以铝土矿(主要成分为Al 2O 3,含有少量Fe 2O 3、SiO 2等杂质)为原料制备无水氯化铝:2Al 2O 3+6Cl 24AlCl 3+3O 2 ↑回答以下问题:(1)画出Al 的原子结构示意图 ;Cl 元素在元素周期表第 周期 族。
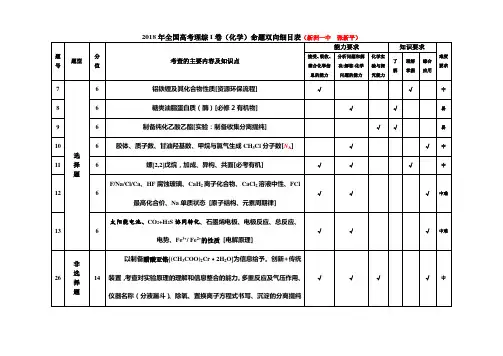


近三年高考理综考试化学双向细目表高考化学考试双向细目表年份题号呈现形式考查知识点考查层次分值 9 选择题化学基本概念、化学与生活综合考查了解 4 10 选择题考查基础知识掌握情况了解 4 11 选择题物质结构、元素周期律理解 4 12 选择题石油产品、乙醇、乙烯的性质理解4 13 选择题阿伏加德罗常数理解 4电离平衡常数、焓变、化学反应速率4 14 选择题理解影响因素15 选择题沉淀溶解平衡、溶度积常数关系图像应用 4 2008年 28 填空题氧化还原原理、离子检验综合应用 14 考题热化学方程式焓变、燃料电池原理、12 分析 29 填空题综合应用电离平衡、盐类水解等除杂、洗涤、溶液的配制、电解原理、16 30 实验题综合应用仪器组装等。
31 选做题钢铁冶炼等化学与技术知识综合应用 8电子排布式、共价键类型、晶体类型8 32 选做题综合应用等有机结构简式的推断与书写、反应类8 33 选做题综合应用型、官能团等综合考查化学基本概念、化学与生活、化学与4 9 选择题了解社会的综合考查10 选择题基本概念、基本理论、实验室制法理解 4物质结构、元素周期律 4 11 选择题理解有机物的性质、基本反应类型、有机4 12 选择题理解物鉴别 13 选择题元素化合物知识综合考查理解 4 14 选择题化学反应速率和化学平衡理解 4 2009年 15 选择题电解质、平衡常数综合应用 4 考题化学平衡的移动、焓变、盖斯定律、14 分析 28 填空题沉淀溶解平衡、电离平衡常数有关计综合应用算 29填空题原电池原理和电解原理综合应用 12 化学实验的基本操作、物质的提纯与16 30 实验题综合应用鉴别、尾气处理等31 选做题化学与技术模块、电解铝的有关问题综合应用 8物质结构与性质、原子结构、杂化方8 32 选做题综合应用式综合考查有机推断与合成、官能团、结构简式8 33 选做题综合应用综合考查同位素、同分异构体、阿伏加德罗常 4 数、物质的量基本计算、化学研究的9 选择题了解理解 2010年范畴考题化学反应的能量、盖斯定律、反应速4 10 选择题了解率化学键、元素周期律的实质、同周期4 11 选择题理解同主族的递变规律。
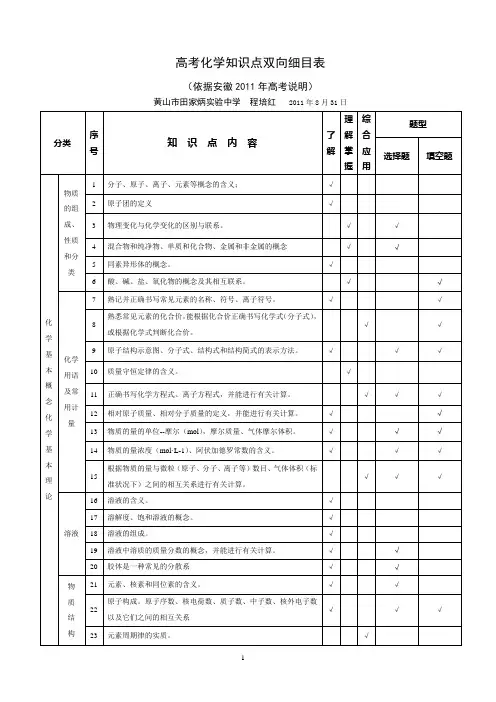

高中化学双向细目表高考化学双向细目表分类序号知识点内容1 物质的组成、性质和分类2 化学基本概念3 物质的分子、原子、离子、元素等概念的含义;初步了解原子团的定义4 物理变化与化学变化的区别与联系5 混合物、纯净物、单质和化合物、金属和非金属的概念6 同素异形体的概念7 酸、碱、盐、氧化物的概念及其相互联系8 熟记并正确书写常见元素的名称、符号、离子符号9 熟悉常见元素的化合价;能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价10 掌握电子式、原子结构示意图、分子式、结构式和结构简式的表示方法;理解质量守恒定律的含义;掌握热化学方程式的含义11 能正确书写化学方程式、离子方程式、电离方程式、电极反应式12 了解相对原子质量、相对分子质量的涵义13 掌握物质的量的单位--摩尔(mol),摩尔质量、气体摩尔体积(相应单位为g·mol-1、L·mol-1)的含义14 物质的量浓度(mol·L-1)、阿伏加德罗常数的含义15 掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系16 掌握化学反应的四种基本类型:化合、分解、置换、复分解17 理解氧化还原反应,了解氧化剂和还原剂等概念;掌握重要氧化剂、还原剂之间的常见反应18 能判断氧化还原反应中电子转移的方向和数目,并能配平反应方程式19 了解化学反应中的能量变化,吸热反应、放热反应、反应热、燃烧热和中和热及新能源的开发等概念20 了解溶液的涵义21 了解溶液的组成,理解溶质的质量分数的概念22 了解饱和溶液、不饱和溶液的概念;了解溶解度的概念;了解温度对溶解度的影响及溶解度曲线23 初步了解结晶、结晶水、结晶水合物、风化、潮解的概念24 了解胶体的概念及其重要性质和应用25 了解原子的组成及同位素的概念26 掌握原子序数、核电荷数、质子数、中子数、核外电子数,以及质量数与质子数、中子数之间的相互关系注:综合应用部分不在此表中列出。
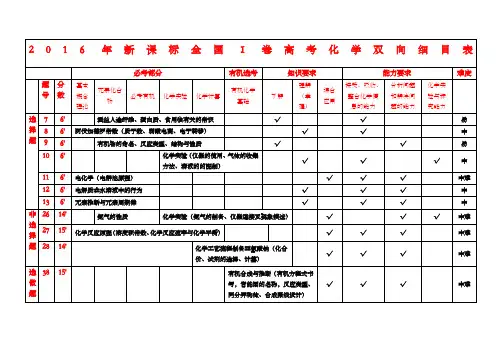

年普通高等学校招生全国统一考试理科综合能力测试化学部分全国甲卷细目表2023()题号7分值题型考查知识点666666选择题选择题选择题选择题选择题选择题化学与生活(食品防腐剂苯甲酸钠、丁达尔效应、S O2漂白原理、抗氧化剂维生素C)有机物的结构与性质(酯基的水解、原子共面、官能团的识别、与溴水反应)89化学实验基础(配制一定浓度的溶液需要使用的仪器)10 11 12阿伏加德罗常数(共价键数目、电子数目、溶液中离子数目、V m的适用范围)元素位构型推断(四种元素N、O、Mg、S、原子半径、简单氢化物沸点、化合物类型、最高价含氧酸的酸性)电解原理的应用——电化学还原C O2制多碳产物(电极反应的判断、电极反应式、离子移动方向、电化学的计算)沉淀溶解平衡p M-p H图像(难溶物K sp的计算、溶解度的计算、金属离子分步沉淀的原因、特定条件下金属离子沉淀的最大浓度的计算)13 26 27 28 35 366选择题以BaS O为原料制备粉状BaTiO(试剂的用途及试剂的选择与原因、化学方程式与离子方程式的书写、产物中物431414151515化学工艺流程题化学综合实验题化学反应原理综合题物质结构与性质有机化学基础质的物质的量比值的计算)无机物钴配合物[C o(N H)]C l的制备(仪器的选择、实验操作、实验操作的目的、不溶物成分的确定、试剂的作363用)甲烷选择性氧化制备甲醇(盖斯定律的应用、平衡常数的计算、曲线的分析、转化率的计算、反应进程-能量图的分析)酞菁、钴钛菁、三氯化铝、碳纳米管的相关考查(同素异形体、晶体类型、分子间作用力、化合价的判断、化学键类型、杂化轨道、配位数、晶体密度的计算)阿佐塞米(化合物L)的合成路线(有机物名称、有机化学方程式书写、条件的选择、含氧官能团的名称、反应类型的判断、结构简式的书写、同分异构体数目的判断及结构简式的书写)年普通高等学校招生全国统一考试理科综合能力测试化学部分全国乙卷细目表2023()题号7分值题型考查知识点6666666选择题选择题选择题选择题选择题选择题选择题生活中的氧化还原反应(明矾净水、撒盐融雪、暖贴原理、荧光指示牌发光原理)有机物的合成与性质(酯的合成方法、反应类型的判断、原子共面、有机物名称)实验装置的判断(制备C O、分离乙醇和乙酸、SO酸性验证、气体体积的测定)892210 11 12 13元素位构型推断(三种元素C、O、Mg、化合价、原子半径比较、化合物的性质、同素异形体)符号表征:用化学方程式解释化学变化(铁盐的性质、硫化钠的性质、溴水褪色的原因、胆矾的变化)二次电池钠-硫电池(离子移动方向判断、电子流动方向判断、正极反应式、特殊材料的作用)沉淀溶解平衡图像分析(图像的分析、特殊点的分析、反应的平衡常数的计算、离子沉淀的先后顺序)李比希元素分析法对有机化合物C H O进行C、H元素分析(实验操作的先后顺序、试剂的选择与作用、实验操4642614化学综合实验题化学工艺流程题作的补充、分子式的确定)以菱锰矿M n C O为原料制备L i M n O(化学方程式的书写、试剂的选择及原因、涉及K的计算、沉淀成分的确324sp27 28 35141515定、离子方程式的书写)化学反应原理综合题FeSO·7H O的脱水反应及分解反应(热重曲线的分析、盖斯定律的应用、分压及K的计算、K的影响)42p p橄榄石矿物Mg Fe SiO中元素的相关考查(价电子排布式、电负性比较、物质熔点的原因、物质的空间结构、x2x-4物质结构与性质有机化学基础杂化类型、物质化学式的确定、原子间的最近距离)奥培米芬(化合物J)的合成路线(含氧官能团的名称、结构简式的书写、有机物的化学名称、反应类型的判断、一定条件下同分异构体数目的判断及特定情况结构简式的书写)3615年普通高等学校招生全国统一考试理科综合能力测试化学部分新课标卷细目表2023()题号分值题型考查知识点7 8 9666选择题选择题选择题文物中的化学知识(竹简、龟甲的化学成分、修复古陶瓷的熟石膏、颜料中的铁红)有机化合物的合成与性质(有机材料的性质、手性碳原子的判断、产物结构的分析、反应类型的判断)物质结构与性质(氢键的判断、第一电离能大小比较、未成对电子数判断、杂化轨道类型)二次电池以V O和Zn为电极、Z n(C F SO)水溶液为电解质的电池(正负极的判断、离子的移动方向、充电时2533210 11 12666选择题选择题选择题总反应方程式、充电时阳极电极反应式)实验方案的评价(氧化性强弱比较、离子的检验、金属性强弱的比较、有机化学反应)N H O H与N H转化为肼的反应历程(极性分子的判断、化学键的断裂与形成、催化剂的变化历程、同位素产物23的分析)溶液中离子浓度的对数关系图(曲线的判断、溶度积的计算、反应的平衡常数的计算、溶液中离子浓度大小的比较)13 27 286选择题1414化学工艺流程题化学综合实验题以铬钒渣为原料分离提取铬和钒(物质化学式的确定、浸渣成分的确定、不同pH的影响、离子方程式的书写)以安息香为原料制备二苯乙二酮(仪器的识别、实验操作的目的分析、实验方案的评价、试剂的用途、产率的计算)以合成氨为载体考查化学反应原理(盖斯定律的应用、速控步的分析、晶胞中所含原子数目的计算、平衡曲线的分析、压强平衡常数K p的计算)29 301515化学反应原理综合题物质结构与性质莫西赛利(化合物K)的合成路线(有机物的化学名称、杂化轨道类型、官能团的名称、反应类型的判断、结构简式的书写、化学方程式的书写、同分异构体数目的判断与特定条件的结构简式的书写)年普通高等学校招生全国统一考试理科综合能力测试化学部分湖南卷细目表2023()题号分值题型考查知识点13选择题化学与传统文化(物理变化与化学变化、淀粉和纤维素、常见合金的组成、传统硅酸盐材料)化学用语(共价型分子结构式、电子式、原子中相关数值及其之间的相互关系、电子排布式、价层电子对互斥理论的应用)23选择题3 433选择题选择题化学实验基本操作(化学实验基础操作、蒸馏与分馏、过滤、中和滴定)物质结构和性质(分子的手性、配合物的应用、氢键对物质性质的影响、酰胺的性质与应用)离子方程式(离子方程式的正误判断、水解的离子方程式书写、电解池电极反应式及化学方程式的书写与判断、常见阳离子的检验)5 633选择题选择题物质结构和性质位构性推断(微粒半径大小的比较方法、根据原子结构进行元素种类推断、能级间能量大小比较、元素性质与电负性的关系)7 8 9333选择题选择题选择题化学实验基本操作(氨水的性质、氢氧化铝、铁盐的检验、常见的几种羧酸)有机化学基础(催化剂对化学反应速率的影响、电解原理的应用、羧酸酯化反应、多官能团有机物的结构与性质)化学工艺流程微题型(水解的离子方程式书写、溶度积常数相关计算)元素及其化合物(氧化还原反应方程式的配平、基于氧化还原反应守恒规律的计算、利用杂化轨道理论判断分子的空间构型)10 11 12333选择题选择题选择题物质结构和性质晶胞结构(根据晶胞结构确定晶体化学式、晶胞的有关计算)水溶液中的离子平衡曲线(影响水电离的因素、酸碱中和滴定原理的应用、盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理、盐溶液中离子浓度大小的比较)化学反应原理化学平衡图像(影响化学反应速率的因素、化学平衡图像分析、化学平衡状态的判断方法、化学平衡常数的影响因素及应用)13 14 1533选择题选择题化学反应机理图(氧化还原反应的规律、催化剂对化学反应速率的影响、共价键的形成及主要类型)雷尼N i的制备及其催化氢化性能探究(铝与强碱溶液反应、常用仪器及使用、物质制备的探究、综合实验设计与评价)中化学实验综合以聚苯乙烯为载体考查化学反应原理知识(盖斯定律及其有关计算、催化剂对化学反应速率的影响、化学平衡的有关计算、溶度积)16 17 18难难中化学反应原理化学工艺流程有机化学基础以粗镓为原料制备超纯G a(C H3)3(控温的原因、电极反应式书写、化学方程式书写、理由的分析、分子中键角大小的判断)含吡喃萘醌骨架有机化合物的制备(有机合成综合考查、多官能团有机物的结构与性质、有机酸酸性强弱比较、同分异构体数目判断、合成路线的设计)题号分值 题型 考查知识点 13 选择题 化学与 S T S E (吸热反应和放热反应、化学科学对人类文明发展的意义、新能源的开发) 化学反应基本规律(氧化还原反应的几组概念、难溶电解质溶解平衡定义及特征、原电池原理理解、同主族元素性质递 变规律理解及应用) 23 选择题 3453 3 3 选择题 选择题 选择题 元素及其化合物(硅的制备、熵判据、实验安全、常见共价晶体的结构) 有机化学基础(有机官能团的性质及结构、常见官能团名称、组成及结构、分子的手性、多官能团有机物的结构与性质) 物质结构与性质(化学用语综合判断、共价型分子结构式、电子式、缩聚反应机理及判断、共价键的实质与形成) 物质结构与性质位构性推断(电离能变化规律、键能、键长、键角及应用、价层电子对互斥理论、极性分子和非极性分 子) 63 选择题 化学与 STSE (淀粉和纤维素组成与结构、淀粉、纤维素的水解、氢键对物质性质的影响、化学科学对人类文明发展的 意义) 783 3 3 3 3 选择题 选择题 选择题 选择题 选择题 化学实验基础(乙酸的酯化反应、乙酸乙酯制备实验、常见有机物的制备) 分子结构与性质(键能、键长、键角及应用、价层电子对互斥理论、价层电子对互斥理论的应用、利用杂化轨道理论判 断分子的空间构型)。
高考化学知识点双向细目表
高考知识要求的三个层次(高层次包含低层次):
了解:对所学化学知识有初步认识,能够正确复述、再现、辨认或直接使用。
下表标为“A”。
理解(掌握):领会所学化学知识的含义及其适用条件,能够正确判断、解释和说明有关化学现象和问题,即不仅“知其然”,还能“知其所以然”。
下表标为“B”。
综合应用:在理解所学各部分化学知识的本质区别与内在联系的基础上,运用所掌握的知识进行必要的分析、类推或计算,解释、论证一些具体的化学问题。
下表标为“C”。