血清总胆汁酸循环酶法测定法-检验科生化室作业书
- 格式:doc
- 大小:34.50 KB
- 文档页数:5

血清总胆汁酸循环酶法测定法1. 实验原理胆汁酸会被3α-羟基类固醇脱氢酶(3α-HSD)以及β-硫代烟酰胺腺嘌呤二核苷酸氧化型(Thio-NAD)特异性地氧化,生成3-酮类固醇以及β-硫代烟酰胺腺嘌呤二核苷酸还原型(Thio-NADH)。
生成的3-酮类固醇在3α-羟基类固醇脱氢酶(3α-HSD)及β-硫代烟酰胺腺嘌呤二核苷酸还原型(Thio-NADH)存在下,生成胆汁酸及β-硫代烟酰胺腺嘌呤二核苷酸氧化型(Thio-NAD)。
如上所述,依据循环酶而放大微量的胆汁酸量,测定单位时间内生成的β-硫代烟酰胺脲嘌呤二核苷酸还原型(Thio-NADH)在405nm处的吸光度变化,以求得胆汁酸的浓度。
(胆汁酸会被3α-羟基类固醇脱氢酶及Thio-NAD 特异性地氧化,生成3-酮类固醇及Thio-NADH,此外,生成的3-酮类固醇在3α-羟基类固醇脱氢酶及NADH 存在下,和NAD。
如上所述,循环往复从而放大微量的胆汁酸量,测定生成的Thio-NADH的吸光度变化,以求得胆汁酸的浓度。
)2. 标本:2.1 病人准备:标本以空腹血清为宜,餐后胆汁酸会升高,应注意采血时间。
2.2类型:血清、肝素或EDTA处理的血浆。
应使用新鲜标本。
标本必须避光保存。
3. 标本存放4℃保存可稳定7天,-20℃保存可稳定3个月。
4. 标本运输常温条件下避光保存运输。
5. 标本拒收标准细菌污染的标本。
6. 实验材料6.1 试剂威特曼总胆汁酸测定试剂盒Good’s缓冲液120mmol/L3a-羟基类固醇脱氢酶(3a-HSD) 12.5 KU/L硫代辅酶(Thio-NAD) 6.1g/L6.1.2 试剂准备:试剂为即用式。
6.1.3 试剂稳定性与贮存:试剂避光保存于2~8℃,若无污染,可稳定至失效期。
试剂不可冰冻,试剂2必须避光保存。
6.1.4 变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。

总胆汁酸(TBA)试剂盒标准操作程序1.摘要本试剂盒供医疗机构用于体外定量测定人血清或血浆样本中总胆汁酸(TBA)的含量。
2.适用范围程序适用于日立7600自动生化分析仪检测血清或血浆样本中总胆汁酸(TBA)的含量。
3.职责使用日立7600自动生化分析仪进行测定直接胆红素浓度的工作人员要严格按照本SOP 程序进行,室负责人监督管理;本SOP的改动,可由任一使用本SOP的工作人员提出,并报经生化室负责人、科主任签字批准生效。
4.检测方法上海科华生物工程股份有限公司生产的总胆汁酸(TBA)试剂盒采用的是循环酶法。
5.原理血清中微量的胆汁酸(3α-羟甾醇)会被3α-羟甾醇脱氢酶(3α-HSD)及β-硫代烟酰胺腺嘌呤二核苷酸氧化型(Thio-NAD)特异性氧化生成3α-酮甾醇,同时Thio-NAD被还原成β-硫代烟酰胺腺嘌呤二核苷酸还原型(Thio-NADH)。
新生成的3α-酮甾醇在3α-HSD及β-烟酰胺腺嘌呤二核苷酸还化型(NADH)存在下,还原成胆汁酸,同时NADH氧化为β-烟酰胺腺嘌呤二核苷酸氧化型(NAD)。
这样,血清中微量的胆汁酸在多次酶循环的过程中被放大,同时可使生成的Thio-NADH扩增。
在405nm处测定Thio-NADH吸光度的变化值,可以求得血清中胆汁酸的含量。
胆汁酸THio−NAD3α−HSD→THio−NADHNAD←NADH3α−铜羟甾醇6.仪器日立7600自动生化分析仪7.试剂7.1试剂来源:上海科华生物工程股份有限公司提供7.2注册号:沪食药监械(准)字2011第2400009号7.3试剂瓶内主要成分:R1: -硫烟酰胺腺嘌呤二核苷酸氧化型(THio-NAD)、Good’s缓冲液;R2 :β-硫烟酰胺腺嘌呤二核苷酸还原型(NADH)、3α-羟甾醇脱氢酶(3α-HSD)、Good’s 缓冲液、叠氮钠7.4试剂稳定性:试剂于2℃-8℃避光保存,有效期为一年;开瓶后2-8℃避光保存,可稳定一个月8.标准品和质量控制8.1校准程序:使用某某公司的校准品对自动分析仪进行校准。

郾城微检综合门诊部生化检验作业指导书文件编号:YCWJZHMZB-2编制:刘桂菊审核:周风霞编辑日期:2017 年8月20日生效日期:2017 年8月30 日郾城微检综合门诊部检验科目录修订页8. 操作步骤8.1 项目基本参数:参见生化检验CS-6400生化分析仪项目测定参数.SOP文件8.2 仪器操作步骤:参见生化检验CS-6400生化分析仪操作规程.SOP文件检验结果的判断与分析10. 质量控制:在每一批标本中都应把非定值血清水平I与II质控做为未知标本进行分析,以2S为质控警告限,3S为失控限,绘制质控图,判断是否在控。
质控规则参见生化室室内质控操作规程.SOP文件。
11. 计算方法以TruCal U复合校准品校准仪器后,在病人结果可报告范围内,仪器直接报告可靠的检测结果无需手工计算,以μmol/L报告。
手工测定计算方法为:△Au直接胆红素(μmol/L) =--------×校准液浓度△As12. 参考值范围:≤6.8mol/L参考值因性别、年龄、饮食和地域的不同而有所差别。
根据好的实验室经验,每个实验室应建立自己的参考值。
13. 临床意义:胆红素是血红蛋白的降解产物。
游离胆红素非极性很强,几乎不溶解于水。
在血液中与白蛋白形成复合物由脾脏向肝脏运输。
在肝脏中,胆红素与葡萄糖醛酸结合,生成可溶性胆红素葡萄糖醛酸酯由胆管排入肠道。
溶血(肝前黄疸)、实质的肝损伤(肝性黄疸)和胆管堵塞(肝后黄疸)都会导致血液胆红素增高,形成高胆红素血症。
人群中常见先天性慢性高胆红素血症,称为Gilbert综合症。
由于胆红素降解酶的功能滞后以及出生后红细胞破碎增多,使60~70%的婴儿血液出现总胆红素增高。
常用的胆红素检测方法能检测总胆红素和直接胆红素。
直接胆红素的测定主要检测水溶性的结合胆红素,因此可以根据总胆红素和直接胆红素的差来估计游离胆红素的含量。
14. 操作性能14.1 线性范围:1.7~171mol/L14.2 精密度:精密度的评估是根据NCCLS推荐的标准方法5,AU1000批内精密度小于4%或SD≤0.04,总精密度小于5%或SD≤0.07。
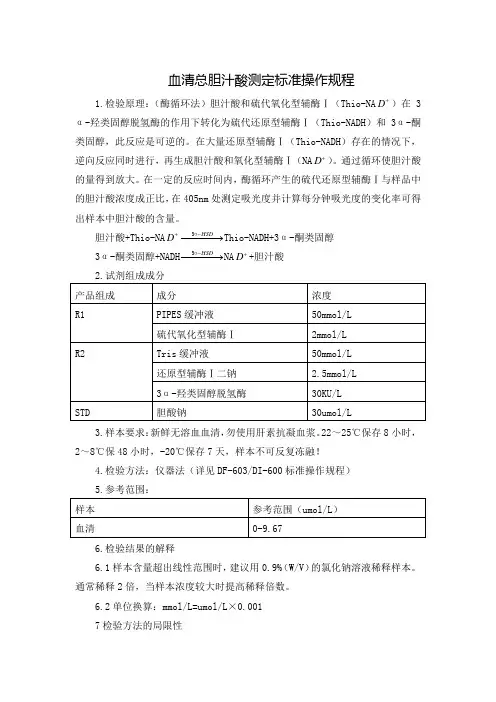
血清总胆汁酸测定标准操作规程1.检验原理:(酶循环法)胆汁酸和硫代氧化型辅酶Ⅰ(Thio-NA +D )在3α-羟类固醇脱氢酶的作用下转化为硫代还原型辅酶Ⅰ(Thio-NADH )和3α-酮类固醇,此反应是可逆的。
在大量还原型辅酶Ⅰ(Thio-NADH )存在的情况下,逆向反应同时进行,再生成胆汁酸和氧化型辅酶Ⅰ(NA +D )。
通过循环使胆汁酸的量得到放大。
在一定的反应时间内,酶循环产生的硫代还原型辅酶Ⅰ与样品中的胆汁酸浓度成正比,在405nm 处测定吸光度并计算每分钟吸光度的变化率可得出样本中胆汁酸的含量。
胆汁酸+Thio-NA +D −−−→−-HSDα3Thio-NADH+3α-酮类固醇 3α-酮类固醇+NADH −−−→−-HSD α3NA +D +胆汁酸 2.试剂组成成分3.样本要求:新鲜无溶血血清,勿使用肝素抗凝血浆。
22~25℃保存8小时,2~8℃保48小时,-20℃保存7天,样本不可反复冻融!4.检验方法:仪器法(详见DF-603/DI-600标准操作规程)5.参考范围:6.检验结果的解释6.1样本含量超出线性范围时,建议用0.9%(W/V )的氯化钠溶液稀释样本。
通常稀释2倍,当样本浓度较大时提高稀释倍数。
6.2单位换算:mmol/L=umol/L ×0.001 7检验方法的局限性7.1结果的准确性依赖于仪器的校正和测定温度、时间的控制。
7.2若试剂浑浊或以水空白在405nm处吸光度大于0.800时不能使用。
8.产品性能指标8.1线性范围:在给定的样本/试剂比例和条件下测定时,本试剂线性范围可达0-180umol/L。
8.2试剂空白吸光度:在405nm处,光径1cm时,空白吸光度A≤0.800,△A空白/分钟≤0.005.8.3准确度:相对偏差≤10%。
8.4精密度8.4.1批内精密度CV≤3%8.4.2批间精密度:R≤10%8.5分析灵敏度:在给定的样本/试剂比例和条件下测定时,1umol/L的总胆汁酸对应的△A不低于×4108.6干扰试验无明显干扰:添加干扰物后的测定值与初始测定值的相对偏差处于±10%以内。

血清总胆汁酸循环酶法测定法1. 实验原理胆汁酸会被3α-羟基类固醇脱氢酶(3α-HSD)以及β-硫代烟酰胺腺嘌呤二核苷酸氧化型(Thio-NAD)特异性地氧化,生成3-酮类固醇以及β-硫代烟酰胺腺嘌呤二核苷酸还原型(Thio-NADH)。
生成的3-酮类固醇在3α-羟基类固醇脱氢酶(3α-HSD)及β-硫代烟酰胺腺嘌呤二核苷酸还原型(Thio-NADH)存在下,生成胆汁酸及β-硫代烟酰胺腺嘌呤二核苷酸氧化型(Thio-NAD)。
如上所述,依据循环酶而放大微量的胆汁酸量,测定单位时间内生成的β-硫代烟酰胺脲嘌呤二核苷酸还原型(Thio-NADH)在405nm处的吸光度变化,以求得胆汁酸的浓度。
(胆汁酸会被3α-羟基类固醇脱氢酶及Thio-NAD 特异性地氧化,生成3-酮类固醇及Thio-NADH,此外,生成的3-酮类固醇在3α-羟基类固醇脱氢酶及NADH 存在下,和NAD。
如上所述,循环往复从而放大微量的胆汁酸量,测定生成的Thio-NADH的吸光度变化,以求得胆汁酸的浓度。
)2. 标本:2.1 病人准备:标本以空腹血清为宜,餐后胆汁酸会升高,应注意采血时间。
2.2类型:血清、肝素或EDTA处理的血浆。
应使用新鲜标本。
标本必须避光保存。
3. 标本存放4℃保存可稳定7天,-20℃保存可稳定3个月。
4. 标本运输常温条件下避光保存运输。
5. 标本拒收标准细菌污染的标本。
6. 实验材料6.1 试剂威特曼总胆汁酸测定试剂盒Good’s缓冲液120mmol/L3a-羟基类固醇脱氢酶(3a-HSD) 12.5 KU/L硫代辅酶(Thio-NAD) 6.1g/L6.1.2 试剂准备:试剂为即用式。
6.1.3 试剂稳定性与贮存:试剂避光保存于2~8℃,若无污染,可稳定至失效期。
试剂不可冰冻,试剂2必须避光保存。
6.1.4 变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。


胆汁酸测定试剂盒(循环酶法)标准化操作规程1 目的规范实验室操作,保证检验工作顺利有效进行特制定此规程。
2 授权操作人经培训且考核通过的实验室检验人员。
3 适用范围本试剂适用于体外定量检测人血清或血浆中胆汁酸的含量。
4 检验方法本试剂盒采用循环酶法测定胆汁酸的含量。
5 检验原理本试剂采用酶分析法测定血清总胆汁酸。
3α-羟基类固醇脱氢酶特异性作用于3α-羟甾族化合物,使之转化为相应的酮类固醇,反应中thio-NAD被还原为thio-NADH。
通过在405nm波长处测定单位时间内吸光度的变化值,可以计算出样品中总胆汁酸的含量。
6 标本要求6.1 样本为空腹患者血清。
样本应及时离心分离,不得使用溶血或被污染的样本。
6.2 样本应避免微生物污染,在2℃~8℃可稳定数月。
7 试剂及配套品7.1试剂来源长春迪瑞医疗科技股份有限公司胆汁酸试剂盒(循环酶法)7.27.3试剂的稳定性与贮存:7.3.1 试剂在2℃~8℃条件下,干燥、避光、密封贮存,有效期为12个月。
7.3.2 试剂开封后在2℃~8℃条件下可稳定30天。
8 实验仪器及性能指标8.1 实验仪器迪瑞CS系列全自动生化分析仪8.2试剂性能指标8.2.1 试剂空白:试剂空白吸光度:A≤0.800。
试剂空白吸光度变化率:△A/min≤0.040。
8.2.2 分析灵敏度:测试1μmol/L被测物时,吸光度变化率(△A/min)>0.0002。
8.2.3 线性范围:1μmol/L~180μmol/L;线性相关系数r≥0.9900;[1,36]μmol/L区间内,线性绝对偏差应不超过±7.2µmol/L;(36,180]μmol/L区间内,相对偏差不超过±15%。
8.2.4 准确度:比对试验:r≥0.9900;[1,36]μmol/L区间内,绝对偏差不超过±7.2μmol/L,(36,180]μmol/L区间内,相对偏差不超过±15%。

沭阳县仁慈医院检验科生化室作业指导书文件编号:SYXRCYYLAB-SH –SOP第A版编制:路珊珊钱丽萍审核:李萍批准:侯波生效日期:2012年10月01日沭阳县仁慈医院检验科修订页血清总胆红素(T-BIL)测定一、目的保证总胆红素测定的结果准确、可靠。
二、修改程序本标准操作程序的改动,可由任一使用本SOP的工作人员提出,并报经下述人员批准签字:质量主管、授权人(科主任)。
三、适用范围钒酸盐氧化法测定总胆红素。
四、试剂来源本标准操作程序适用于上海执诚生物科技股份有限公司生产的总胆红素测定试剂盒。
五、溯源全国临床检验操作规程(第二版)。
六、原理此方法基于样品中的总胆红素在pH3.0 环境中,在有机复合物氧化剂的作用下,可以被氧化成胆绿素,而胆红素特有的黄色也随即消失,在450nm 处测定吸光度的变化,即可计算出样品中总胆红素的浓度。
七、试剂R1:硫磺酸缓冲液(pH2.9) 0.1mol/L表面活性剂R2:磷酸缓冲液(pH7.0) 10mmol/L有机钒酸盐 4mmol/L 不同批号试剂盒中各组份不能互换。
本试剂对光敏感,2~8℃密闭避光保存可以稳定18个月(勿冷冻);首次开启试剂后,避光保存于2~8℃防污染环境中,可继续稳定至效期。
校准液: Randox 公司提供的系列校准品。
八、标本采血清总胆红素(T-BIL)测定血清、血浆。
样本2~8℃保存可以存放约3天,-20℃保存可以存放3个月,但只能冻融一次。
九、操作步骤1、标本编号,分离血清,依顺序置样品架上。
2、按标本编号在全自动化生化仪器上输入标本的基本信息和测定要求,进行测定。
3、仪器校准:将校准液置试管架上,输入校准液浓度,然后进行测定(测定参数与下同),其吸光度贮存在电脑中,浓度值测定符合要求即可应用。
一般每3~6个月校准一次,若更换不同批号的试剂、质控超标或仪器维修处理后应进行校准。
4、测定参数:血清量 7μl试剂Ⅰ 200μl试剂Ⅱ 50μl主波长 444nm次波长 548nm反应类型终点法;负反应测定时间 10分钟温度 37℃报告单位μmol/L5、结果计算:ΔA 样品样本中总胆红素的含量 = ------- ×标准液浓度ΔA 标准单位换算:mg/dl×17.1=μmol/L十、正常参考值5.1-20μmol/L血清总胆红素(T-BIL)测定十一、室内质控质控方法:每天测定样品前做一组质控,在标本中间插一组质控,最后再做一组质控品,共三组。

目录目录 (1)第1章目的和范围 (2)1.1 目的 (2)1.2 适用范围 (2)第2章操作规程 (2)2.1 测定原理 (2)2.2 试剂贮存与稳定性 (2)2.3 试剂与样本准备 (2)2.4 测定参数 (2)2.5 操作步骤 (3)2.6 校准和质控 (3)第3章结果计算 (3)3.1 吸光度变化率的计算 (3)3.2 活性的计算 (3)第4章方法学特性 (3)4.1 正常参考范围 (3)4.2 线性范围 (3)第5章临床意义 (4)第6章安全防护 (4)第1章目的和范围1.1目的为用户使用迈瑞公司TBA试剂时,提供正确的操作流程和操作规范。
1.2适用范围适用于各级医疗机构的用户。
第2章操作规程2.1测定原理γ-GT催化胆汁酸会被3α-羟甾醇脱氢(3α-HSD)以及β-硫代烟酰胺脲嘌呤二核苷酸氧化型(Thio-NAD)特异性地氧化,生成3-酮类固醇以及β-硫代烟酰胺脲嘌呤二核苷酸还原型(Thio-NADH)。
此外生成的3-酮类固醇在3α-羟甾醇脱氢(3α-HSD)及β-硫代烟酰胺脲嘌呤二核苷酸还原型(Thio-NADH)存在下,生成胆汁酸及β-硫代烟酰胺脲嘌呤二核苷酸氧化型(Thio-NAD)。
如上所述,依据循环酶而放大微量的胆汁酸量,测定单位时间内生成的β-硫代烟酰胺脲嘌呤二核苷酸还原型(Thio-NADH)在405nm处的吸光度变化,以求得胆汁酸的浓度。
2.2试剂贮存与稳定性试剂贮存在2~8℃环境时,在试剂盒上规定的有效期前可以保持稳定。
2.3试剂与样本准备本试剂为液体双试剂,取出后可以直接使用。
样本可以为血清、肝素或EDTA抗凝的血浆。
尽量使用新鲜标本。
2.4测定参数测定波长:405nm;分析类型:连续监测法,扣除试剂空白;孵育时间:3分钟;延迟时间:1分钟;读数时间:3分钟;第一试剂/样本/第二试剂比例:270/4/90。
2.5 操作步骤A/min· R1: 270 μl2.6 校准和质控请使用迈瑞公司推荐的校准品和质控品。

总胆汁酸(TBA)测定试剂盒(酶循环法)说明书【产品名称】总胆汁酸(TBA)测定试剂盒(酶循环法)【包装规格】a)试剂1:2×45mL 试剂2:2×15mL b)试剂1:4×60mL 试剂2:4×20mL c)试剂1:2×60mL试剂2:2×20mL【预期用途】用于体外定量测定人体血清中总胆汁酸的含量。
血清中TBA 水平升高见于急性病毒性肝炎、肝硬化、胆汁淤积性胆管炎、慢性活动性肝炎、酒精性肝炎、阻塞性黄疸、肝囊性纤维变性[1]。
【检验原理】胆汁酸被3α-HSD 及THIO-NAD 特异性的氧化,生成3-酮类固及还原型硫代辅酶Ⅰ(THIO -NADH )。
此外,生成的3-酮类固醇在3α羟基类固醇脱氢酶及还原型硫代辅酶Ⅰ(THIO -NADH )存在下,生成胆汁酸及氧化型硫代辅酶Ⅰ(THIO -NAD )。
如上述,据循环酶而放大微量的胆汁酸量,测定在单位时间内生成的还原型硫代辅酶Ⅰ在405nm 处的吸光度变化,可求得样本中总胆汁酸的含量。
【主要组成成分】试剂1主要组分磷酸氢二钠-柠檬酸缓冲液100mmol/L 氧化型硫代辅酶Ⅰ(THIO-NAD)950mg/L还原型辅酶(NADH)6g/L 聚氧乙烯油醇醚适量试剂2主要组分Tris 缓冲液100mmol/L 3α-羟基类固醇脱氢酶(3α-HSDH)12.5KU/L聚氧乙烯油醇醚适量注:不同批号试剂盒中各组分未经试验不可互换。
【储存条件及有效期】贮存于2~8℃,有效期为18个月,生产日期、有效期见标签。
【适用仪器】艾威德AS-420/AS-660/AS-1200;日立HITACHI 7020型/7060型/7180型/7600型/LABOSPECT 008AS 型;贝克曼AU400/AU480/AU640/AU680/AU2700/AU5400/AU5800/AU5811/AU5821;佳能TBA-FX8/TBA-120FR /TBA-2000FR ;罗氏cobas 8000c 702/cobas 8000c 701/cobas 8000c 502;西门子SIEMENS ADVIA 1800/ADVIA 2400;雅培ABBOTT ARCHITECT c8000/ARCHITECT c16000/ARCHITECT ci8200;西森美康SYSMEX BM6010/C ;科华KHB 卓越310/卓越330/卓越400/卓越450/ZY-1200/ZY-1280;迪瑞CS-240/CS-T300/CS-300B/CS-380/CS-400A/CS-400B/CS-600A/CS-600B/CS-800A/CS-800B/CS-1200/CS-1200ISE/CS-1300B/CS-1400;迈瑞MINDRAY BS-220/BS-330/BS-350E/BS-380/BS-390/BS-400/BS-430/BS-600/BS-800/BS-2000M ;颐兰贝ES-200/ES-380/ES-480;赛诺迈德SUNMATIK-9050型;雷杜Chemray 420;英诺华D280;特康TC6010L ;锦瑞GS400;普康6066。

ISO15189质量管理体系范本文件(第五册)生化室作业指导书文件编号:ABCD-3-SF-01~61第A版编制:审核:批准:生效日期:2006年8月8日ABCD人民医院检验科目录修订页血清总胆红素(T-BIL)测定1. 实验原理血清中的胆红素分为直接(结合)胆红素和间接(未结合)胆红素。
大多数方法是在1883年Ehrlich提出的重氮法胆红素测量法1,一些改良的方法已被用来增进反应。
这些改良的方法是使直接胆红素直接和重氮化合物进行反应,生成一种有颜色的化合物,而间接胆红素需要一种溶剂,如表面活性剂后才能进行反应。
申能总胆红素试剂是改良的重氮法。
使用一种稳定的重氮盐,2,4-二氯苯胺重氮盐(DCA),与胆红素反应,形成红色偶氮化合物,它在540nm吸光度最大。
在540/600nm时的吸光度与标本中总胆红素的浓度成正比。
胆红素+DCA 红色偶氮化合物表面活性剂2. 标本:2.1 病人准备:无特殊要求。
最好用禁食的标本以减少乳糜血的干扰。
2.2 类型:血清、肝素或EDTA血浆,应避光保存。
3. 标本存放:15~25℃保存可稳定2天;2~8℃保存可稳定7天;-20℃保存可稳定3个月,如冰冻保存,不可反复冻融!。
4. 标本运输:常温条件下避光保存运输。
5. 标本拒收标准:标本溶血、细菌污染、脂血、非避光保存运输的标本。
6. 实验材料6.1 试剂:申能总胆红素试剂盒(141 0817170 1 试剂1+试剂2)6.1.1 试剂组成试剂1:6×64 ml磷酸缓冲液40mmol/L氯化钠9g/L表面活性剂,稳定剂适量试剂2:6×16 ml2,4-二氯苯胺重氮盐1mmol/L盐酸30mmol/L表面活性剂适量6.1.2 试剂准备:试剂为即用式。
6.1.3 试剂稳定性与贮存试剂避光保存于2~8℃,若无污染,可稳定至失效期。
试剂有效期为18个月。
试剂2必需避光保存。
试剂不可冰冻。
6.1.4 变质指示:当试剂有浊度时,表明有细菌污染,不能继续使用。
总胆汁酸TBA循环酶速率法作业指导书1、前言试验名称:总胆汁酸测定,英文名称:TBA,方法:循环酶速率法。
本文件适用于安阳鼎城糖尿病医院检验科生化实验室,目的是指导工作人员正确的在科华KHB450全自动生化分析仪上测定血清、血浆样本中的TBA活力,以保证测定结果的准确可靠。
本试验用体外定量测定人血清或血浆样本中TBA的活力。
胆汁酸(bile acids)是胆汁中的主要成份,是消化吸收功能所需的物质,也是胆固醇通过胆汁排泄时的必要成份。
胆汁酸的代谢包括合成、排泌及肝肠循环三个主要环节,以肝脏为中心,涉及到胆道、肠道及门脉系统等途径。
故胆汁酸的代谢紊乱可诱致许多消化系统的疾病,反之许多消化系统的疾病,也能影响胆汁酸的代谢。
急性肝炎、慢性肝炎、肝硬化等肝实质性损伤时TBA的含量会明显升高。
临床上,本实验列入肝功能实验,常和转氨酶测定、胆红素测定、蛋白测定等实验同时用于肝脏疾病的诊断和功能检测。
2、测定原理本试验测定原理在生化类检验测定原理中较为特殊,其测定原理如下:TBA+Thio-NAD 3-α-HSD3-酮类固醇+Thio-NADH 3-酮类固醇+NADH3-α-HSD TBA+NAD+在上述反应中如不考虑反应过程反应式可改写为:Thio-NAD+NADH3-α-HSD TBA Thio-NADH+NAD+从上述反应式中可以看出,在3-α-HSD过量时,反应的速率仅与TBA的量有关,通过检测Thio-NADH在405nm处吸光度值的变化,即可得出TBA的含量。
NAD+ 氧化型β-烟酰胺脲嘌呤二核苷酸NADH还原型β-烟酰胺脲嘌呤二核苷酸Thio-NADH还原型β-硫代烟酰胺脲嘌呤二核苷酸Thio-NAD氧化型β-硫代烟酰胺脲嘌呤二核苷酸3-α-HSD3-α-羟甾醇脱氢酶3、试剂试剂生产商:上海科华公司。
剂型:液体双试剂。
包装量:R1:3*50ml R2:2*25ml注册号:沪食药监械(准)字2011第2400009号。
Thio-NADH酶法检测血清总胆汁酸的方法评价摘要】目的通过对方法学评价试验,选择一种检测血清总胆汁酸的方法。
方法 Thio-NADH黄色发光系统酶循环法检测血清总胆汁酸。
结果本法线性达150mol/L,精密度,批内CV0.98%,0.85%,批间CV4.58%,4.13%,本法与普通酶显示法比较Y=0.903x-1.45 r=0.9955,n=50,配对t检验P>0.05,胆红素<830umol/L,血红蛋白<50g/L,肝素钠<100mmol/L,枸橼酸钠<120mmol/L,乳酸<30mmol/L,抗坏血酸<280mmol/L,对测定结果无显著干扰。
结论本法线性好,精密度高,结果无明显干扰,对仪器管道、比色杯基本无色素沉着污染,是测定血清总胆汁酸的一种理想方法,值得推广应用。
【关键词】酶循环法血清总胆汁酸(TBA) Thio-NAD本文采用无色素污染的Thio-NADH黄色发光系统酶循环法测定血清总胆汁酸,现将方法评价报导如下。
1 测定原理血清中的胆汁酸(3α-羟类固醇)被3α-羟类固醇脱氢酶(3α-HSD)及β-硫代烟酰胺腺嘌呤二核苷酸氧化型(Thio-NAD)特异性地氧化,生成3-酮类固醇及β-硫代烟酰胺腺嘌呤二核苷酸还原型(Thio-NADH)。
而生成的3-酮类固醇在3α-HSD及β-烟酰胺腺嘌呤二核苷酸还原型(NADH)作用下,生成胆汁酸及β-烟酰胺腺嘌呤二核苷酸氧化型(NAD)。
如此,血清中微量的胆汁酸在多次酶循环过程中被放大,同时可使生成的Thio-NADH扩增。
在405nm测定Thio-NADH吸光度变化值,即得血清中胆汁酸的含量。
2 材料和方法2.1仪器日立7170-A全自动生化分析仪。
2.2试剂四川迈克生物科技总胆汁酸检测试剂盒。
2.3方法根据试验说明书编制测试参数,反应类型,速率法,反应温度37℃,波长405nm(主波)/660nm(次波)样品5ul,试剂Ⅰ215ul,试剂Ⅱ50ul,延迟时间1min,读数时间4min。
血清总胆汁酸操作程序1.目的规范血清总胆汁酸(TBA)检测试验,确保检测结果准确性和重复性。
2.范围本操作规程适用于生化室工作人员、实习人员、进修人员的操作前培训。
3.术语4.测定原理4.1 测定方法:循环酶法4.2 测定原理:胆汁酸会被3α-羟甾醇脱氢(3α-HSD)以及β-硫代烟酰胺腺嘌呤二核苷酸氧化型(Thio-NAD)特异性地氧化,生成3-酮类固醇以及β-硫代烟酰胺腺嘌呤二核苷酸还原型(Thio-NADH)。
此外生成的3-酮类固醇在3α-羟甾醇脱氢(3α-HSD)及β-硫代烟酰胺腺嘌呤二核苷酸还原型(Thio-NADH)存在下,生成胆汁酸及β-硫代烟酰胺腺嘌呤二核苷酸氧化型(Thio-NAD)。
如上所述,依据循环酶而放大微量的胆汁酸量,测定单位时间内生成的β-硫代烟酰胺腺嘌呤二核苷酸还原型(Thio-NADH)在405nm处的吸光度变化,以求的胆汁酸的浓度。
5. 标本采集与处理5.1标本种类:新鲜无溶血血清。
5.2标本采集:见生化标本采集程序。
5.3 标本稳定性:4℃保存可稳定1周,-20℃保存可稳定3个月。
6. 试剂6.1试剂:本科使用浙江伊利康生物工程有限公司试剂盒,为即用式液体双试剂。
试剂内各主要成分如下:试剂成分浓度试剂1 Good’缓冲液80mmol/LThio-NAD 0.95g/L试剂2 Good’缓冲液80mmol/L3α-羟甾醇脱氢13KU/LThio-NADH 6.10g/L防腐剂适量6.2 总胆汁酸校准血清:浙江伊利康生物工程有限公司浓度50μmol/L标准品。
6.3 试剂与校准血清的稳定性:未开瓶的试剂于2~8℃避光保存,可稳定至有效期(12个月)。
如试剂空白吸光度大于0.5即不能使用。
6.4 试剂不可入口!避免接触皮肤及粘膜。
7. 仪器参数设定AU2700参数设定:科华试剂仪器参数设置参见试剂厂家提供相应仪器设置参数。
8.校准:具体参见临床生化校准程序8.1 校准条件:8.1.1仪器光路系统经过光路保养或更换光源等重要部件后。
血清总胆汁酸循环酶法测定法
1.实验原理
胆汁酸会被3α-羟甾醇脱氢(3α-HSD)以及β-硫代烟酰胺脲嘌呤二核苷酸氧化型(Thio-NAD)特异性地氧化,生成3-酮类固醇以及β-硫代烟酰胺脲嘌呤二核苷酸还原型(Thio-NADH)。
此外生成的3-酮类固醇在3α-羟甾醇脱氢(3α-HSD)及β-硫代烟酰胺脲嘌呤二核苷酸还原型(Thio-NADH)存在下,生成胆汁酸及β-硫代烟酰胺脲嘌呤二核苷酸氧化型(Thio-NAD)。
如上所述,依据循环酶而放大微量的胆汁酸量,测定单位时间内生成的β-硫代烟酰胺脲嘌呤二核苷酸还原型(Thio-NADH)在405nm处的吸光度变化,以求得胆汁酸的浓度。
2.标本:
2.1病人准备:标本以空腹血清为宜,餐后胆汁酸会升高,应注意采血时间。
2.2类型:血清、肝素或EDTA处理的血浆。
应使用新鲜标本。
标本必须避光保存。
3.标本存放4℃保存可稳定7天,-20℃保存可稳定3个月。
4.标本运输常温条件下避光保存运输。
5.标本拒收标准细菌污染的标本。
6.实验材料
6.1试剂南京波因特总胆汁酸测定试剂盒(试剂1:2×60ml试剂2:2×20ml)
6.1.1试剂组成
试剂1(R1):
β-硫代烟酰胺脲嘌呤二核苷酸氧化型(Thio-NAD)2mmol/L
Tris缓冲液30mmol/L
试剂2(R2):
脲嘌呤二核苷酸氧化型(NAD)2mmol/L
3a-羟甾醇脱氢酶(3a-HSD)5U/L
6.1.2试剂准备:试剂为即用式。
6.1.3试剂稳定性与贮存:试剂避光保存于2~8℃,若无污染,可稳定至失效期。
试剂不可冰冻,试剂2必须避光保存。
6.1.4变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。
6.1.5注意事项:不可入口!避免接触皮肤及粘膜。
应采取必要的预防措施使用试剂
6.2校准品:使用南京波因特公司提供的TBA校准品对自动分析仪进行校准,具体参见生化检验校准品和质控品.SOP文件。
6.3质控品:具体参见生化检验校准品和质控品.SOP文件。
7.仪器:奥林巴斯AU1000生化分析仪
8.操作步骤:
8.1项目基本参数:参见AU1000生化分析仪项目测定参数.SOP文件
8.2仪器操作步骤:参见AU1000生化分析仪操作规程.SOP文件
9.检验结果的判断与分析
10.质量控制:在每一批标本中都应把非定值血清水平I与II质控做
为未知标本进行分析,以2S为质控警告限,3S为失控限,绘制质控图,判断是否在控。
质控规则参见室内质控操作规程.SOP文件。
11.计算方法:以南京波因特公司提供的TBA校准品校准仪器后,在病人结果可报告范围内,仪器直接报告可靠的检测结果,以μmol/L 报告。
12.参考值范围[2,3]:成年人:<10μmol/L
参考值因性别、年龄、饮食和地域的不同而有所差别。
根据好的实验室经验,每个实验室应建立自己的参考值。
13.临床意义
14.操作性能
14.1线性范围:1.06~90μmol/L。
14.3方法学比较:本公司的试剂盒(y)与某商品化试剂盒(x),同时对
79个样品进行TBA检测,将检测结果作方法学比较,其统计结果如下:y=0.999x+0.19μmol/L;r=0.999。
14.4灵敏度:本试剂的检测限为1.06μmol/L。
14.5病人结果可报告范围:1.06~90μmol/L。
15.超出范围结果处理本法的检测范围为1.06~90μmol/L。
当样品测定值超过上限时,应将样品用9g/L氯化钠溶液作1+1稀释,重新测定,结果乘以2。
16.病危报警值的处理
17.方法局限性
17.1本法的检测范围为1.06~90μmol/L。
当样品测定值超过上限时,应将样品用9g/L氯化钠溶液作1+1稀释,重新测定,结果乘以2。
17.2干扰物质:当样品中抗坏血酸浓度≤100mg/L,胆红素≤50mg/L,血红蛋白≤5g/L,乳糜度≤3000度时没有观察到干扰。
18.补救措施:当仪器发生故障时,迅速联系仪器厂家进行维修。
19.参考文献
1. JungK,BohmM.Enzyme,23:201(1978)
2. HafkenscheidJCM,DijitCCM.ClinChem,25(1):55(1979)
3.TietzNW.Fundamentalsofclinicalchemistry,W.B.SaundersCo.,p674(19 82)
4.TsunodaT,EtoT,FurukawaM,NakataT,KusanoT,LinY,TashiroK,WatabeS,T suchiyaR.Clearandcolorlessfluidobservedduringpercutaneoustranshepati cgallbladderdrainage.GastroenterolJpn1990;25:619-24.
5.Keller,h.:klinisch-chemischelabordiagnostikfurdiepraxis,2ndedition,g
eorgthiemeverlag,stuttgart,1991:246.
6.ScientificTablesGeigy,partialvolumebodyfluids.Basel:Ciba-Geigy1977; 8:136-43.
7.KruisW,PaumgartnerG.Bileaciddepletionsyndrome.DtArztebl1982;79 :33-6
20.其他:仪器测定后的废液及难降解的材料集中收集后按《检验科废物处置管理规定》执行。