8配位化合物
- 格式:ppt
- 大小:2.50 MB
- 文档页数:88







zn晶体的配位数
硅酸锆(Zirconia)是一种具有重要用途的复杂的无定形配位化合物,它的配位数为8。
它的化学式是ZrO2,其中硅酸根负责八个配位位置,而锆离子则负责四个配位位置。
硅酸锆的稳定性是由它配位数所决定的,配位数为8的硅酸锆具有较高的热稳定性,可以经受高温的腐蚀环境,而且具有良好的耐腐蚀性。
它也具有优异的抗磨损性,从而可以用来制作耐磨的工具、刀具和机械零件等。
此外,硅酸锆还具有优异的电绝缘性、导热性和导电性,可用于制作电子元件和电缆线等。
硅酸锆具有多种特性,可以满足不同应用领域的需求,其配位数为8也是它的重要特征之一。
硅酸锆的特性可以得到有效发挥,从而在制造各种电子元件和电气产品方面发挥着重要作用。
因此,硅酸锆的配位数是其重要性的体现,对于硅酸锆的研究、开发和应用具有重要意义。


八面体配位化合物一、介绍八面体配位化合物是一类具有特殊结构的化合物,其分子中心原子(通常是金属离子)被八个配体离子或分子所包围,形成一个八面体的结构。
八面体配位化合物在化学领域中具有重要的地位,并广泛应用于催化剂、光电材料、生物医药等领域。
二、八面体配位化合物的结构特点八面体配位化合物的结构特点主要体现在以下几个方面:1. 八面体结构八面体配位化合物的分子结构呈现八面体形状,中心原子被八个配体离子或分子所包围。
八面体结构的稳定性使得八面体配位化合物在化学反应中具有较高的活性和选择性。
2. 配体的配位方式配体以配位键的形式与中心原子结合,形成稳定的配位键。
常见的配位方式有顶点配位、棱配位和面配位等。
不同的配位方式会对化合物的性质和反应活性产生影响。
3. 配体的性质配体的性质对八面体配位化合物的性质起到重要的影响。
配体可以是阴离子、中性分子或阳离子,其电荷和电子云分布会影响配位键的稳定性和配位键的极性。
4. 配位数八面体配位化合物的配位数为八,即中心原子与八个配体形成八个配位键。
配位数的确定与中心原子的电子构型和配体的性质有关。
三、八面体配位化合物的应用八面体配位化合物在各个领域都有广泛的应用,主要体现在以下几个方面:1. 催化剂八面体配位化合物常用作催化剂,可以参与氧化、还原、催化裂解等反应。
其特殊的结构和配位键的活性使得催化剂具有高效率和高选择性。
2. 光电材料八面体配位化合物在光电材料领域有重要应用。
通过调控配位离子的能级和电子云分布,可以实现光电材料的吸收光谱范围的调节和能级结构的优化。
3. 生物医药八面体配位化合物在生物医药领域有广泛的应用。
通过配体的选择和配位方式的调控,可以设计出具有特定功能的药物分子,用于治疗疾病或探测生物分子。
4. 材料科学八面体配位化合物在材料科学领域有着重要的地位。
通过调控配位离子的性质和配位方式,可以实现材料的结构和性能的调控,用于制备具有特殊功能的材料。
四、八面体配位化合物的合成方法八面体配位化合物的合成方法多种多样,常见的合成方法包括:1.水热合成法:利用高温高压的水热条件,使得反应物在水溶液中发生反应,形成八面体配位化合物。
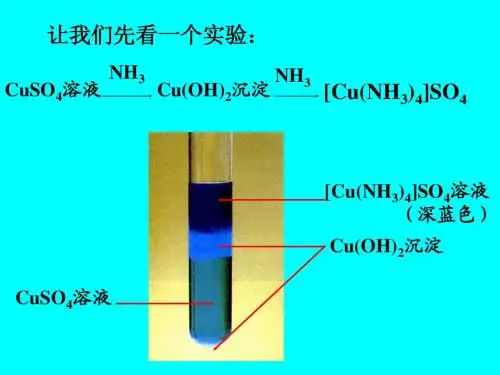
同步练习P265[Ni(CO)4]四羰基合镍K2[HgI4] 四碘合汞(Ⅱ)酸钾H[AuCl4]四氯合金(Ⅲ)酸K[Co(NO2)4(NH3)2] 四硝基⋅二氨合钴(Ⅲ)酸钾[Co(ONO)(NH3)5]SO4硫酸一(亚硝酸根)⋅五氨合钴(Ⅲ) 二氯化异硫氰酸根⋅五氨合钴(III) [Co(NCS)(NH3)5]Cl2亚硝酸氯⋅硫氰酸根⋅二(乙二胺)合钴(III)[CoCl(SCN)(en)2]NO2四氯⋅二氨合铂(IV)[PtCl4(NH3)2]P266名称或化学式配体配位原子中心离子氧化数[Pt(NH3)2Cl2] 二氯⋅二氨合铂(Ⅱ) NH3N +2[CoCl(NH3)5]Cl2二氯化一氯⋅五氨合钴(III) Cl–NH3ClN+3[Cu(NH3)4][PtCl4] 四氯合铂(Ⅳ)酸四氨合铜(Ⅱ) NH3Cl–NClCu +2、Pt+4六氟合硅(Ⅳ)酸铜Cu[SiF2] F– F +4二氯乙二胺合铂(Ⅱ) [Pt(en)]Cl2en N +2P271稳定性:[FeF6]3–<[Fe(CN)6]3–、[Ni(CN)4]2–>[Ni(NH3)4]2−配合物思考题与答案1.设计一些实验,证明粗盐酸的黄色是Fe3+与Cl-的络离子而不是铁的水合离子或者羟合离子的颜色。
(略)2.配位化学创始人维尔纳发现,将等物质的量的黄色CoCl3.6NH3﹑紫红色CoCl3.5NH3﹑绿色CoCl3.4NH3和紫色CoCl3.4NH3四种配合物溶于水,加入硝酸银,立即沉淀的氯化银分别为 3 ﹑2 ﹑1 ﹑1mol,请根据实验事实推断它们所含的配离子的组成。
答:配离子分别是[Co(NH3)6]3+, [Co(NH3)5Cl]2+ , [Co(NH3)4Cl2] +, [Co(NH3)4Cl2] +,颜色不同的原因是有同分异构体。
3.实验测得Fe(CN)64-和Co(NH3) 63+均为反磁性物质(磁矩等于零),问它们的杂化轨道类型。
co2(co)8钴的化合价Co2(CO)8钴是一种含有钴元素的化合物,它的化合价是8。
在本文中,我们将探讨Co2(CO)8钴的化学性质、用途以及对环境的影响。
Co2(CO)8钴是一种配位化合物,其中的钴原子被8个CO(一氧化碳)分子配位。
钴元素在这个化合物中的化合价为8,这意味着每个钴原子与8个CO分子形成了配位键。
这种化合价表示了钴原子与配位分子之间的电子转移和共享程度,以及化合物的稳定性和反应性。
Co2(CO)8钴的化学性质主要与配位键的强度和稳定性有关。
由于每个钴原子与8个CO分子配位,形成的配位键非常稳定。
这种稳定性使得Co2(CO)8钴在化学反应中能够作为催化剂或配体的载体。
它可以参与各种有机合成反应、催化剂的制备以及金属有机化学反应。
Co2(CO)8钴在有机合成中的应用非常广泛。
它可以用作氢化反应、氧化反应、羰基化反应、加成反应等的催化剂。
此外,它还可以用于合成复杂有机分子、有机金属化学反应以及有机合成新材料的研究。
由于Co2(CO)8钴具有较高的催化活性和选择性,因此在有机合成领域受到广泛关注和应用。
然而,需要注意的是,Co2(CO)8钴是一种有毒物质。
在使用和处理时,应注意遵循相关的安全操作规程,以防止对人体和环境造成伤害。
此外,Co2(CO)8钴的合成和应用过程也需要进行环境风险评估和控制,以减少对环境的污染和损害。
总结起来,Co2(CO)8钴是一种化合价为8的配位化合物,具有广泛的应用前景。
它在有机合成领域可以作为催化剂参与多种反应,有助于合成复杂有机分子和新材料。
然而,应注意其有毒性和环境风险,采取相应的安全措施和环境保护措施。
通过进一步的研究和开发,可以发掘更多Co2(CO)8钴的应用潜力,并为人类社会的发展做出更大的贡献。