高一化学开发海水中的卤素资源(20200806100059)
- 格式:pdf
- 大小:1.21 MB
- 文档页数:10






第二单元开发海水中的卤素资源一、教材分析本单元是在学习原子结构的基础上,通过研究开发海水中的化学资源,重点学习有关元素化合物的知识。
通过以食盐为原料的化工产品的学习,认识盐酸、烧碱、氯气、漂粉精等重要的氯碱工业产品;通过海水中提取镁、溴、碘和氯气性质的研究,探索氯、溴、碘的性质和递变规律;通过粗盐提纯、气体制取和卤素性质实验的研究,培养学生的实验动手和实验设计能力;通过氧化—还原反应、气体摩尔体积、电离方程式和离子方程式等化学基本概念和基本理论的学习,为以后的化学学习打下重要的基础。
二、本章内容的核心观念元素观、物质结构与性质、分类观、氧化—还原转价观、守恒观三、把核心观念转化成一些基本理解本单元涉及的卤素及其化合物、氧化—还原反应、离子反应、气体摩尔体积及实验操作和设计等有关知识是中学化学中的重点。
将元素及其化合物的知识与基本概念、基本理论、化学计算、实验操作技能联系起来,达到加深、巩固对元素及其化合物知识的理解。
四、基本理解可以采用“问题”驱动,通过实验设计来促进学生的基本理解1、海水晒盐的原理。
食盐的用途。
粗盐为什么易潮解?如何进行粗盐的提纯?2、探究电解饱和食盐水的原理:如何知道阴阳两级产生的是什么气体?怎么进行检验?得到的产品有什么用途?3、探究盐酸和氯化氢的性质。
实验室制备氯化氢气体,在发生气体过程中那些装置是必需的?4、氯气的物理性质和化学性质。
如何用实验来探究氯水的主要成分?5、决定物质体积大小的因素是什么?为什么相同质量的固体、液体体积会不同?为什么标准状况下相同物质的量的气体的体积几乎相同?6、“同温同压”与“标准状况”有什么联系和区别?阿伏加德罗定律的运用7、在学习海水晒盐的基础上如何进行海水提溴和海水提碘?氯溴碘在结构上有什么相似性?性质上有什么相似性及递变规律?如何进行卤离子的检验?8、得氧失氧的氧化还原反应与无氧参与的氧化还原反应的共同特征是什么?9、氧化还原反应的实质是什么?如何分析卤素单质以及化合物的氧化性和还原性的判断。

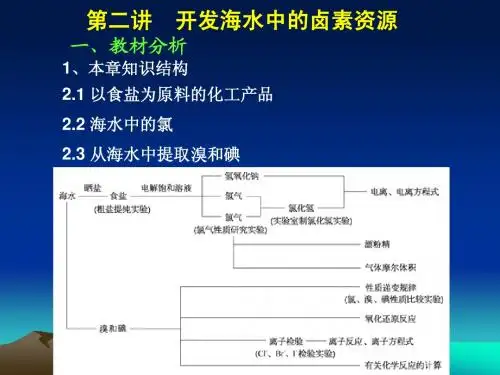
高一化学第一学期2.开发海水中的卤素资源教学设计(五)本章知识结构二、本节教材分析(一)教学目标知识与技能:1.理解实际生产中应适当控制卤水密度的原因。
2.理解粗盐提纯中除去其中难溶性杂质和可溶性杂质的原理,学会溶解、过滤、洗涤、蒸发的操作,提高动手实验的能力。
3.知道氯碱工业的基本反应和主要产品,认识电解在化学工业中的作用和氯碱工业的重要性,掌握氯化氢(盐酸)和氢氧化钠的性质。
4.学会实验室制氯化氢气体的方法及其实验装置的装配和操作。
5.理解电离方程式及书写。
过程与方法:通过卤水密度的控制,学习分析数据解决简单化学问题的方法。
对实验室气体制取和收集的方法有进一步了解。
通过实验活动,提高实验设计能力和创新精神。
(2)电解饱和食盐水化学方程式:2NaCl+2H2O−−−→通电2NaOH+H2↑+C12↑现象:两极产生气体的体积相同,在溶液中滴入酚酞试剂,阴极附近溶液变红,说明阴极生成了NaOH。
阳极:电极材料炭棒,产生黄绿色的C12,用淀粉碘化钾试纸检验,试纸变蓝,原理C12+2KI→2KCl+I2,碘单质遇淀粉显蓝色。
阴极:电极材料铁棒,产生无色的氢气,点燃发出淡蓝色火焰,验纯方法:搜集一试管的气体,管口向下移至火焰处,听到轻微的爆鸣声。
【教学建议】只要求学生掌握电解饱和食盐水的化学方程式,不涉及有关电解质和电解的概念和原理等。
电解饱和食盐水及产物检验的实验可由教师播放视频帮助学生回顾。
要求学生观察现象并进行描述、填空,教师可以提问并进行归纳。
主要观察阳极和阴极产生气体的颜色和量的多少,以及在哪个区域使酚酞试液变红。
同时要求掌握检验氯气和氢气的方法。
3.盐酸(1)工业制法工业上常用氯气在氢气中燃烧的方法来制取氯化氢气体如右图,氯气在氢气中燃烧时,有毒的氯气被过量的氢气所包围,使氯气充分反应。
注意:在生产上,往往采取使用一种过量的原料而使有害的或价格较昂贵的原料充分反应。
(2)性质盐酸:纯净的盐酸是无色液体,工业上用的盐酸常因含有杂质(主要是铁的化合物)而显黄色。



第二章开发海水中的卤素资源教课方案教材剖析地位:本章是整个高中阶段较为详尽、全面地学习和研究一族元素的性质及其变化规律的一章,是一个典型的非金属元素族,本章为元素族观点的形成,同族元生性质递变规律,元素周期律的形成累积感性资料,是学习元素周期律、周期表知识的重要基础。
内容:本章教课内容分为(1)以食盐为原料的化工产品:介绍食盐的提取,工业上电解饱和食盐水,盐酸、氢氧化钠的性质,氯化氢的溶解性及制法。
(2)氯气的性质及重要用途(3)从海水中提取重要元素:学习镁、溴、碘的提取及溴、碘的溶解性、特征。
卤族元素的物理性质及化学性质的相像形和递变性。
(4)进一步学习氧化复原反响,电离方程式,离子方程式,为此后各章节的学习打下重要基础。
教课中可增添氯气的实验室制法,将研究气体体积的规律内容放在物质的量的计算中学习。
教法与学法:重视基础知识的落实和科学方法的培育。
经过对氯气的性质、用途及实验室制法的学习,将其余卤素的性质与氯气的性质进行比较,从个别到一般逐渐地、客观地显现这一族元素的性质及变化规律,也为后边学习同族元素的性质供给了方法和研究思路。
教师一定以学生为主体,精心设计问题、创建实验指引学生踊跃思虑,让学生在学习的过程中感觉、体验学习的方法,领悟知识的内涵及实质。
所以在本章的内容的教课中知识的掌物和方法的形成同样重要。
重视化学实验的教课功能。
俗语说“百闻不如一见,百见不如一练”。
只需能让学生着手的实验,就应当踊跃地创建条件让学生着手做,不可以让学生着手做的实验,教师应当尽量演示。
让学生在实验中察看思虑,议论剖析,推理判断,自己去发现问题,解决问题和得出结论。
使学生生动、开朗、主动地发展。
重视联系生产、生活实质。
含卤化合物的介绍,海水资源的开发利用,氯碱工业等应密切联系生产、生活实质,反应现代科技发展状况,是培育学生学习兴趣,加强学生学习动机的素材。
教师应依据实质状况,有针对性地指导阅读,也可环绕有关问题指导学生采集一些资料,研究一些问题,展开议论或撰写小论文。