尿微量白蛋白(MALB)测定试剂盒(胶乳免疫比浊法)产品技术要求shangjing
- 格式:docx
- 大小:14.10 KB
- 文档页数:2

微量白蛋白测定试剂盒(免疫比浊法)
适用范围:该产品用于体外定量测定人尿液中微量白蛋白的含量。
1.1 包装规格
试剂1(R1):1×40ml 试剂2(R2):1×10ml;
试剂1(R1):2×40ml 试剂2(R2):2×10ml;
试剂1(R1):2×60ml 试剂2(R2):2×15ml ;
2.1外观
试剂盒文字符号清晰;试剂1、试剂2试剂均应澄清、无异物。
2.2净含量
试剂净含量不低于标示值。
2.3试剂空白
用蒸馏水作为样品进行检测,其空白吸光度≤0.5。
2.4分析灵敏度
测定微量白蛋白为100mg/L样本时,测定吸光度差值应>0.005△A。
2.5线性范围
本试剂盒线性(10,240)mg/L区间内,其相关系数r≥0.9900;在线性(10,40]mg/L 区间内,绝对偏差不超过±4mg/L,在线性(40,240)mg/L区间内,相对偏差不超过±10%。
2.6重复性
2.6.1测量精密度
用高低两个浓度的质控物或样本测试同一批号试剂盒,其变异系数(CV)应≤10%。
2.6.2批间差
用高低两个浓度的质控物或样本测试三个不同批号试剂盒,其批间差应≤10%。
2.7准确度
检测国际标准参考物质ERM470,相对偏差不超过±15%。
2.8稳定性
试剂盒在2~8℃条件可保存12个月,取效期末的试剂盒,检测其试剂空白吸光度,试剂空白吸光度变化率,分析灵敏度,准确度,线性和重复性等,其质量指标应符合2.1,2.2,2.3,2.4,2.5,2.6.1,2.7的要求。

尿微量白蛋白测定卡(胶体金免疫层析法)适用范围:本产品用于体外定量检测人体尿液中的白蛋白水平。
1.1 产品型号1.2 产品规格1支/袋×1袋/盒;1支/袋×2袋/盒;1支/袋×5袋/盒;1支/袋×10袋/盒;1支/袋×20袋/盒。
1.3 产品组成每盒含有测定卡、1支校准卡、尿杯(选配)、滴管(选配)。
每个铝箔袋中包括1支尿微量白蛋白测定卡和1包干燥剂。
尿微量白蛋白测定卡由样品垫(玻璃纤维素膜)、金标垫(氯金酸约14μg、鼠抗人白蛋白单克隆抗体约0.6μg、无机盐约60%)、硝酸纤维素膜(T线包被有人血清白蛋白;C线包被有羊抗鼠IgG)、吸水纸、背板(PVC板)。
2.1 外观2.1.1 外观平整,材料附着牢固,内容齐全。
2.1.2 包装完整,标签清晰。
2.2 物理检查2.2.1 膜条宽度应不低于3.0mm。
2.2.2 液体移行速度应不低于10mm/min。
2.3 准确度应在85%~115%范围内。
2.4 重复性重复测试低、中、高浓度后样本,测试结果的变异系数CV≤20%。
2.5 线性在[10,30]mg/L的范围内,线性相关系数(r)应不小于0.990。
样品中白蛋白浓度为[10,20)mg/L时,测量平均值与理论值的绝对偏差不超过±3.0mg/L;样品中白蛋白浓度[20,30]mg/L时,测量平均值与理论值的相对偏差不超过±15%。
2.6 空白限空白限应不超过3mg/L。
2.7 批间差批间相对极差R≤15%。
2.8 特异性用下列浓度的干扰物加入后测定结果的相对偏差应不超过±15%。
2.9 稳定性4℃~30℃保存,有效期(15个月)到期后三个月内的留样,应符合2.3、2.4、2.5、2.6的要求。
2.10 校准信息溯源性校准卡中的校准曲线,按照GB/T 21415-2008 《体外诊断医疗器械生物样品中量的测量标准品和控制物质赋值的计量学溯源性》的要求溯源,溯源到怡成公司企业校准品,选用罗氏尿微量白蛋白测试系统对校准品进行比对赋值。


医疗器械产品技术要求编号:尿微量白蛋白(mALB)测定试剂盒(化学发光-免疫分析法)2性能指标2.1试剂盒2.1.1外观和性状(1)试剂盒各个组分应齐全、完整、液体无渗漏。
(2)中文包装标签应清晰,准确、牢固。
(3)试剂R1 为澄清透明液体,无沉淀、颗粒或絮状物。
(4)试剂R2 为略带乳白色均一性液体,无明显沉淀、颗粒或絮状物。
(5)试剂R3 为澄清透明液体,无沉淀、颗粒或絮状物。
2.1.2装量液体装量应不少于标示值。
2.1.3准确度相对偏差应不超过±10 .0%。
2.1.4空白限应不大于 2.0mg/L。
2.1.5线性(a)在 4.0mg/L~200.0mg/L 范围内,其相关系数r 应不小于0.9900。
(b)[4.0,20.0] mg/L 范围内,线性绝对偏差应不超过±2.0 mg/L;在(20.0,200.0] mg/L 范围内,线性相对偏差应不超过±10 %。
2.1.6批内精密度批内变异系数(CV)应≤10.0%。
2.1.7批间精密度批间变异系数(CV)应≤10.0%。
2.2校准品2.2.1外观和性状澄清透明液体,不得有沉淀、颗粒或絮状物。
2.2.2装量液体装量应不小于标示值。
2.2.3校准品测量准确度(S0 除外)用工作校准品校准测量系统后,以试剂盒配套的校准品作为样本进行检测,其测定结果与标示值的相对偏差应在±10.0%范围内。
2.2.4校准品均一性(S0 除外)瓶内CV 应不大于10.0%;瓶间CV 应不大于10.0%。
2.3质控品2.3.1外观和性状澄清透明液体,不得有沉淀、颗粒或絮状物。
2.3.2装量液体装量应不小于标示值。
2.3.3质控品测定值用试剂盒配套的校准品校准测量系统后,以试剂盒配套的质控品作为样本进行检测,其测定结果应在标示范围内。
2.3.4质控品均一性瓶内CV 应不大于10.0%;瓶间CV 应不大于10.0%。

尿微量白蛋白(MAU)测定试剂盒(胶体金免疫层析法)适用范围:于体外定量测定人尿液中的尿微量白蛋白(MAU)含量。
1.1包装规格20人份/盒1.2 主要组成成分本试剂盒由MAU检测卡、干燥剂和滴管组成。
MAU检测卡由试纸条外壳与试纸条构成。
试纸条由样品垫、胶体金垫(喷有由胶体金标记的MAU单克隆抗体)、层析膜(T线包被有MAU单克隆抗体,C线包被有羊抗鼠IgG抗体)、吸水纸、衬垫构成。
检测卡为20人份/盒,干燥剂为1个/袋,滴管为20个/盒。
2.1 物理性状2.1.1 外观试剂盒各组分齐全、完整;包装袋应密封性好无破损;标签清晰;材料附着牢固,条宽应适应于卡壳且装配紧密。
2.1.2 膜条宽度膜条宽度应不低于4.0mm。
2.1.3 液体移行速度液体移行速度应不低于10mm/min。
2.2 空白检测限应小于5.0mg/L。
2.3 重复性用10mg/L尿微量白蛋白(MAU)参考品和100mg/L尿微量白蛋白(MAU)参考品各重复检测10次,其变异系数(CV)应不大于15%。
2.4 准确度将200.0mg/L尿微量白蛋白(MAU)参考品加入到尿微量白蛋白(MAU)含量5.0mg/L 正常人尿液参考品中,按照体积比1:9混合,对混合后样本进行检测,回收率应在85%~115%范围内。
2.5 线性线性范围为[5.0,200]mg/L,试剂盒的相关系数r应≥0.99。
2.6 批间差用3个批号试剂盒分别对10.0mg/L尿微量白蛋白(MAU)参考品和100.0mg/L 尿微量白蛋白(MAU)参考品各重复检测10次,则3个批号试剂盒之间的批间相对偏差(R)应不大于15%。
2.7 稳定性效期稳定性:2~30℃条件下放置有效期12个月后一个月内,检测物理性状、空白检测限、重复性、准确度、线性应符合2.1~2.6项的要求。

尿微量白蛋白(胶体金法)技术要求哎呀,说起尿微量白蛋白(胶体金法)技术要求,这可真是个技术活儿,得慢慢道来。
首先,咱们得聊聊这个尿微量白蛋白是个啥。
简单来说,它就是尿液里的一种蛋白质,正常情况下,尿液里是不应该有这种蛋白质的。
但是,如果肾脏出了点小问题,比如糖尿病肾病啊,高血压肾病啊,这种蛋白质就会偷偷溜进尿液里。
所以,检测这个尿微量白蛋白,对于早期发现肾脏问题还是挺重要的。
接下来,咱们得说说这个胶体金法。
这是一种检测方法,用一种叫做胶体金的东西来标记抗体,然后通过化学反应来检测尿液中的微量白蛋白。
这个方法的好处是灵敏度高,操作简便,结果也快。
那么,这个技术要求具体是啥呢?首先,你得有个干净的尿样。
这个尿样得是新鲜的,最好是早上第一次尿,因为这时候尿液浓度最高,检测结果最准确。
然后,你得有个靠谱的检测试剂盒,这个试剂盒里包含了胶体金标记的抗体和一些其他必要的化学试剂。
操作的时候,你得按照说明书来,一步步来。
首先,把尿样滴到试剂盒的测试区,然后等个几分钟,让尿液和试剂充分反应。
这个过程中,你可能会看到一些颜色变化,这就是胶体金抗体和尿微量白蛋白结合的结果。
最后,你得对照试剂盒上的对照线,看看测试区的颜色变化,以此来判断尿微量白蛋白的浓度。
这个过程中,你得注意几个细节。
首先,操作的时候手要干净,别让脏东西污染了尿样或者试剂。
其次,等待时间要准确,太短了反应不充分,太长了结果可能会受影响。
最后,读结果的时候要仔细,别因为颜色变化不明显就忽略了。
总的来说,尿微量白蛋白(胶体金法)技术要求就是:干净的尿样,靠谱的试剂盒,准确的操作,仔细的结果解读。
虽然听起来有点复杂,但只要按照步骤来,还是挺简单的。
这个技术对于早期发现和监测肾脏问题还是挺有帮助的,希望我说的这些对你有所帮助。
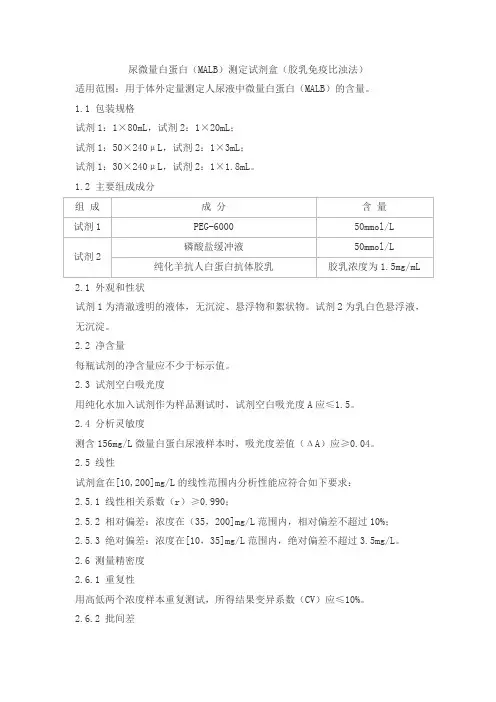
尿微量白蛋白(MALB)测定试剂盒(胶乳免疫比浊法)适用范围:用于体外定量测定人尿液中微量白蛋白(MALB)的含量。
1.1 包装规格试剂1:1×80mL,试剂2:1×20mL;试剂1:50×240μL,试剂2:1×3mL;试剂1:30×240μL,试剂2:1×1.8mL。
1.2 主要组成成分2.1 外观和性状试剂1为清澈透明的液体,无沉淀、悬浮物和絮状物。
试剂2为乳白色悬浮液,无沉淀。
2.2 净含量每瓶试剂的净含量应不少于标示值。
2.3 试剂空白吸光度用纯化水加入试剂作为样品测试时,试剂空白吸光度A应≤1.5。
2.4 分析灵敏度测含156mg/L微量白蛋白尿液样本时,吸光度差值(ΔA)应≥0.04。
2.5 线性试剂盒在[10,200]mg/L的线性范围内分析性能应符合如下要求:2.5.1 线性相关系数(r)≥0.990;2.5.2 相对偏差:浓度在(35,200]mg/L范围内,相对偏差不超过10%;2.5.3 绝对偏差:浓度在[10,35]mg/L范围内,绝对偏差不超过3.5mg/L。
2.6 测量精密度2.6.1 重复性用高低两个浓度样本重复测试,所得结果变异系数(CV)应≤10%。
2.6.2 批间差试剂盒的批间相对极差(R)应≤15.0%。
2.7 准确度在样品中加入一定量的纯品,计算回收率,应在85%~115%范围内。
2.8 稳定性2℃~8℃避光贮存,有效期为12个月,取过有效期后一个月内的试剂盒进行检测,试剂盒应仍能符合2.1、2.3、2.4、2.5、2.6.1、2.7要求。
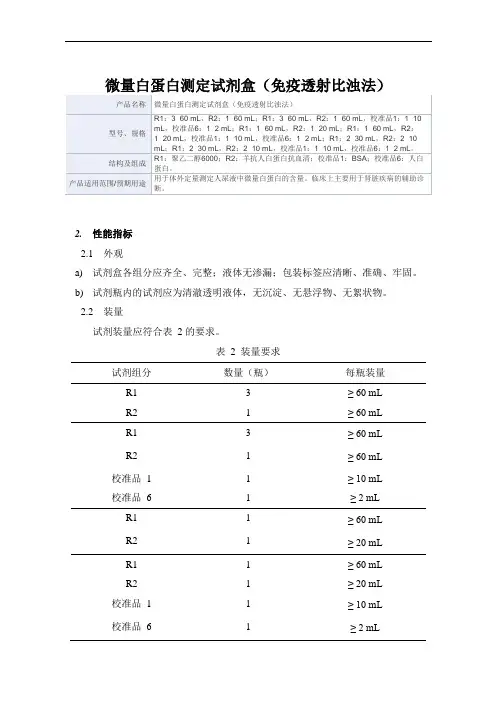
微量白蛋白测定试剂盒(免疫透射比浊法)2.性能指标2.1外观a)试剂盒各组分应齐全、完整;液体无渗漏;包装标签应清晰、准确、牢固。
b)试剂瓶内的试剂应为清澈透明液体,无沉淀、无悬浮物、无絮状物。
2.2装量试剂装量应符合表 2 的要求。
表 2 装量要求试剂组分数量(瓶)每瓶装量R1 3 ≥ 60 mLR2 1 ≥ 60 mLR1 3 ≥ 60 mLR2 1 ≥ 60 mL 校准品 1 1 ≥ 10 mL校准品 6 1 ≥ 2 mLR1 1 ≥ 60 mLR2 1 ≥ 20 mLR1 1 ≥ 60 mLR2 1 ≥ 20 mL 校准品 1 1 ≥ 10 mL校准品 6 1 ≥ 2 mLR1 2 ≥ 30 mL R2 2 ≥ 10 mL R1 2 ≥ 30 mL R2 2 ≥ 10 mL试剂组分数量(瓶)每瓶装量校准品1 1 ≥ 10 mL校准品6 1 ≥ 2 mL2.3空白限不大于0.6 mg/L。
2.4分析灵敏度试剂盒测试30 mg/L 的被测物时,其吸光度差值≥0.040 Abs。
2.5线性区间试剂盒线性在[7,1000] mg/L 区间内,应符合如下要求:a)线性相关系数(r)≥0.990;b) [7,100] mg/L 区间内,线性绝对偏差在±10 mg/L 范围内;(100,1000] mg/L 区间内,线性相对偏差在±10%范围内。
2.6精密度2.6.1重复性试剂盒测试浓度在(25±5)mg/L 和(200±40)mg/L 范围内的样本时,变异系数(CV)≤5.0%。
2.6.2批间差试剂盒测试浓度在(25±5)mg/L 和(200±40)mg/L 范围内的样本时,相对极差(R)≤10.0%。
2.7准确度测试有证参考物质或可溯源至有证参考物质的企业校准品,测定值与理论值的相对偏差应在±10.0%范围内。
2.8校准品外观a)校准品的外观应整洁,标识应清晰、准确、牢固;b)瓶内液体清澈透明,无沉淀、无悬浮物、无絮状物。

尿微量白蛋白(MAU)测定试剂盒(荧光免疫层析法)
适用范围:本试剂盒用于体外定量测定人尿液中尿微量白蛋白(MAU)的含量。
1.1规格
10人份/盒、20人份/盒、50人份/盒。
1.2主要组成成分
注:1.质控品质控范围批特异,具体浓度详见标签。
2.1物理性能
2.1.1外观
检测卡应整洁完整、无毛刺、无破损、无污染;材料附着牢固。
2.1.2膜条宽度
膜条的宽度应不小于3mm。
2.1.3移行速度
液体移行速度应不低于10mm/min。
2.2溯源性
根据GB/T21415-2008的有关规定,提供所用校准品的来源、赋值过程及测量不确定度等内容,溯源至企业工作校准品,并与已上市产品比对赋值。
2.3空白限
空白限应不高于5μg/mL。
2.4准确度
回收率应在85%~115%之间。
2.5线性
在线性范围[10,200]μg/mL内,相关系数(r)应不低于0.99。
2.6重复性
分别检测高值和低值两个样本,重复性(CV%)应不高于15.0%。
2.7批间差
在三个批次产品之间,样本测定结果的变异系数(CV%)应不高于20.0%。
2.8特异性
2.9质控品赋值有效性
测定高值、低值浓度质控品,其结果均应在质控范围内。
2.10稳定性
10℃~30℃储存(质控品2℃~8℃),有效期12个月,效期后2个月内分别检测2.3~2.6,2.8,2.9项,其结果应符合各项要求。

尿微量白蛋白测定试剂盒(免疫比浊法)适用范围:用于体外定量测定人尿液中微量白蛋白的浓度。
1.1包装规格a) 试剂1:1×40ml,试剂2:1×10ml;b) 试剂1:2×40ml,试剂2:2×10ml;c) 试剂1:4×40ml,试剂2:4×10ml;d) 试剂1:1×32ml,试剂2:1×8ml;e)试剂1:2×200ml,试剂2:2×50ml;f)试剂1:2×16ml,试剂2:2×4ml。
1.2 主要组成成分试剂1主要组成成分:Tris缓冲液(PH 6.0-9.0) 0.1mol/L 聚乙二醇6000 1.1mol/L试剂2主要组成成分:羊抗人MALB抗体适量防腐剂适量表面活性剂适量2.1 外观和性状2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;外包装完好、无破损,标签完好、字迹清晰。
2.1.2 试剂1应为无色透明溶液;试剂2应为无色或乳白色溶液。
2.2 净含量应不低于试剂瓶标示装量。
2.3 试剂空白测定试剂空白吸光度,应<0.5。
2.4 分析灵敏度测试200mg/L的被测物时,吸光度变化(ΔA)应不低于0.05。
2.5 准确性测试可用于评价常规方法的国家标准参考物质,相对偏差<15%。
2.6 重复性变异系数(CV)应不超过5%。
2.7 线性2.7.1在(1,240)mg/L范围内,线性回归的确定系数应不低于0.990;2.7.2[30,240) mg/L范围内,相对偏差≤15%;(1,30)mg/L范围内,绝对偏差≤5mg/L。
2.8 批间差对同一份样品进行重复测定,相对偏差<10%2.9 稳定性该产品在2℃~8℃条件下贮存有效期为18个月,取效期末的产品进行检测,应符合2.1、2.2、2.3、2.4、2.5、2.6、2.7之规定。
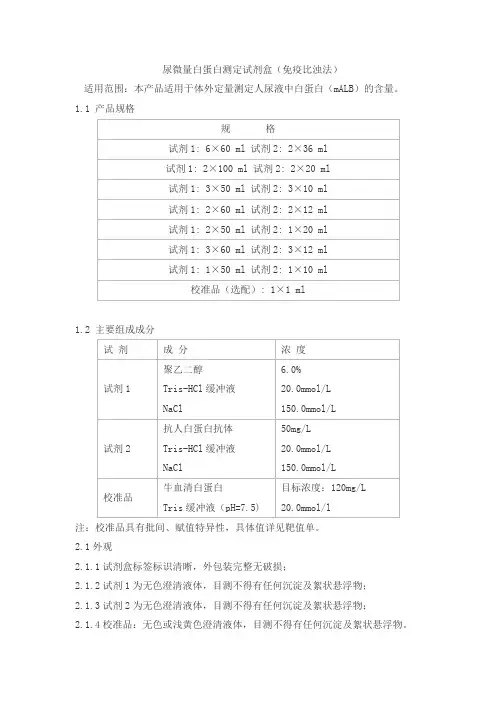
尿微量白蛋白测定试剂盒(免疫比浊法)适用范围:本产品适用于体外定量测定人尿液中白蛋白(mALB)的含量。
1.1 产品规格1.2 主要组成成分注:校准品具有批间、赋值特异性,具体值详见靶值单。
2.1外观2.1.1试剂盒标签标识清晰,外包装完整无破损;2.1.2试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;2.1.3试剂2为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;2.1.4校准品:无色或浅黄色澄清液体,目测不得有任何沉淀及絮状悬浮物。
2.2净含量净含量不低于标示值。
2.3空白吸光度测定待检试剂在主波长340nm、副波长700nm、37℃条件下:A≤0.2。
2.4线性范围(5,280)mg/L范围内,相关系数r≥0.990;(5,30]mg/L范围内,绝对偏差不超过±3mg/L;(30,280)mg/L范围内,相对偏差不超过±10.0%。
2.5分析灵敏度在说明书规定参数设定条件下,测定浓度50mg/L的样本,△A≥0.05。
2.6 精密度2.6.1批内重复性CV≤10.0%。
2.6.2 批间差相对极差R≤10.0%。
2.7 准确度与已上市产品比对:(5,280)mg/L范围内,相关系数r≥0.990;(5,30]mg/L 范围内,绝对偏差不超过±3mg/L;(30,280)mg/L范围内,相对偏差不超过±10.0%。
2.8 校准品2.8.1 均一性:CV≤5.0%;2.8.2 开瓶稳定性:开瓶后3天,相对偏差不超过±10.0%。
2.9 稳定性未开封试剂2℃~8℃储存,可稳定12个月。
取到效期后2个月内产品进行检测, 检测结果应满足2.3、2.4、2.5、2.6.1和2.7的要求。
2.10溯源性依据GB/T 21415—2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,校准品溯源至工作校准品,工作校准品经与Audit Diagnostics尿微量白蛋白测定试剂盒比对测量赋值。
尿微量白蛋白MALB检测1检验目的指导本室工作人员规范操作本检测项目,确保检测结果的准确。
2 实验原理将未稀释的样品加入含有抗人血清白蛋白特异性抗体的缓冲液变浊溶液吸光度值(340nm)与尿液样品中白蛋白浓度成正相关。
3 标本:3.1 病人准备:留取24h尿液标本(加苯防腐)混匀后记录尿液总量取少量尿液离心;清晨中段尿。
3.2 类型:尿液3.3 标本存放尿液的稳定性:20~25℃保存可稳定1天,2~8℃保存至少可稳定2天; -20℃保存可稳定6个。
3.4 标本运输常温条件下运输。
3.5 标本拒收标准细菌污染的标本。
4 实验材料4.1 试剂:上海倍特生物科技有限公司Malb试剂盒4.1.1 试剂组成R1:TRIS /HCL缓冲液:20 mmol/l,pH 7.4;氯化钠:150 mmol/L;聚乙二醇6%R2:抗人白蛋白TRIS /HCL缓冲液:20 mmol/l,pH 7.4氯化钠:150 mmol/l4.1.2 试剂准备:试剂为即用式。
4.1.3 试剂稳定性与贮存:2-8°C下保存期限:见试剂标签上的有效期。
机上稳定期:90天。
4.1.4变质指示:当试剂有浊度时,表明有细菌污染则试剂不能使用。
4.2 校准品:使用试剂盒里校准品自动分析仪进行校准。
5 仪器AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪6 操作步骤6.1 样品的准备:将标好号的样品离心后放到仪器规定的位置。
6.2 试剂的检测:仪器开机后,检查各种试剂的位置,体积等确认无误后方可进行测定。
6.3 项目基本参数:参见生化检验AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪项目测定参数。
6.4仪器操作步骤:参见生化检验AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪操作规程。
2性能指标
2.1外观和性状
2.1.1颜色性状
质控品应为液体,无沉淀、悬浮物和絮状物。
2.1.2包装
分装瓶应为白色硬质塑料瓶,盖有塑料外盖;盒贴、瓶贴、标签标识应完整、清晰。
塑料外盖应无明显划痕、崩缺。
2.2装量
液体质控品的含量应不少于标示值。
2.3均一性
2.3.1瓶内均一性
质控品瓶内均一性应不大于表 2 的要求(SD 和CV 值满足其一即可)。
表 2 质控品瓶内均一性要求
2.3.2瓶间均一性
质控品瓶间均一性应不大于表3 的要求(SD 和CV 值满足其一即可)。
表3 质控品瓶间均一性要求
1
2.4参考值及参考范围
每批质控品均应提供本批产品的参考值表。
经迈瑞校准品校准的BS 系列生化分析仪及配套试剂对质控品进行测定,测定结果应在给定的参考范围内。
2。
1.1规格规格1:(试剂1:20mL;试剂2:5mL);规格2:(试剂1:40mL;试剂2:10mL);.规格3:(试剂1:80mL;试剂2:20mL);校准品(冻干品):为选配:规格1(0.3mL×1;1水平);规格2(0.5mL×1;1水平);规格3(1.0mL×1;1水平);质控品(冻干品):为选配规格1(0.5mL×2;2水平);规格2(1.0mL×2;2水平)。
1.2组成试剂盒组成见表1定试表1微量白蛋白测定试剂盒组成2.1试剂2.1.1外观试剂盒外观应整洁,文字符号标识清晰;试剂1、试剂2均为无色透明液体,不得有沉淀和絮状物。
2.1.2装量每瓶不少于标示值。
2.1.3试剂空白吸光度用指定的空白样品测试试剂(盒),在光径1cm下,在A340nm处测定试剂空白吸光度A≤0.2。
2.1.4分析灵敏度测定30mg/L的样品,吸光度差值△A≥0.01。
2.1.5线性范围2.1.5.1在[2,400]mg/L内,相关系数R≥0.990。
2.1.5.2在[2,30]mg/L内,线性绝对偏差不超过±3.0mg/L;(30,400]mg/L内,线性相对偏差不超过±10%。
2.1.6重复性重复测试(45±9)mg/L和(90±18)mg/L样本,所得结果的变异系数(CV%)应不大于5%。
2.1.7批间差测定(45±9)mg/L和(90±18)mg/L样本,所得结果的批间相对极差(R)应不大于10%。
2.1.8准确度)中加入一定体积高于400mg/L的白蛋在正常浓度范围的临床样本(C白纯品(C)或由纯品配制的标准溶液,回收率应在90%-110%范围内。
s2.2校准品2.2.1外观校准品为冻干品。
2.2.2瓶间差瓶间差CV≤10%2.2.3准确度与配套试剂组成测试系统,指标要求同2.1.8。
2.2.4溯源性根据GB/T21415-2008的要求,本产品校准品溯源至企业工作校准品,与已取得医疗器械产品注册证的企业产品对比赋值(德赛生物技术有限公司)。
尿微量白蛋白(mALB)测定试剂盒(免疫比浊法)性能指标1.性能指标1.1外观外观应符合以下要求:a)试剂盒各组分应齐全、完整,液体无渗漏;包装标签文字符号清晰。
b)R1:无色澄清液体。
c)R2:无色至淡黄色透明液体,目测均不得有任何沉淀及絮状悬浮物。
d)校准品、质控品:无色至淡黄色透明液体。
1.2装量液体试剂装量要求不低于标示量。
1.3空白限空白限不高于5 mg/L。
1.4分析灵敏度测定30 mg/L样本时,吸光度差值(△A)应≥0.02。
1.5线性范围1.5.1在[5,400]mg/L范围内,线性相关系数|r|≥0.990;1.5.2在[5,30]mg/L范围内,线性绝对偏差应不超过±3mg/L;在(30,400]mg/L范围内,线性相对偏差应不超过±10%。
1.6重复性变异系数(CV)应≤5%。
1.7批间差批间相对极差R≤10%。
1.8准确度回收率应在90%~110%。
1.9分析特异性当抗坏血酸≤100mg/dL,胆红素≤40mg/dL,肌酐≤100mg/dL,葡萄糖≤800mg/dL,尿素≤400mg/dL时,对试剂检测结果的偏差影响在±10%以内。
1.10量值溯源应明确分析物的量值溯源。
1.11校准品赋值结果及其不确定度的表示方式应使用规范的表示方式,主要表示方式可选择:a)赋值结果±扩展不确定度;b)赋值结果,扩展不确定度。
1.12校准品正确度量值传递的正确度应符合E≤1。
n1.13质控品赋值准确度在用校准品校准后的生化分析仪上测试定值质控品,结果应在制造商指定的赋值范围内。
1.14校准品均匀性应不大于10%。
1.14.1瓶内均匀性:CV瓶内应不大于10%。
1.14.2瓶间均匀性:CV瓶间1.15质控品均匀性应不大于10%。
1.15.1瓶内均匀性:CV瓶内1.15.2瓶间均匀性:CV应不大于10%。
瓶间。
水平1:1mL×1;1mL×10;5mL×1;5mL×10;
水平2:1mL×1;1mL×10;5mL×1;5mL×10;
水平1:1mL×1,水平2:1mL×1;
水平1:5mL×1,水平2:5mL×1。
1.2主要组成成分
2水平,牛血清基质冻干质控品
注:质控品质控范围批特异,详见瓶签。
2.1性状
质控品为白色至淡黄色冻干粉末。
2.2可接受区间
质控品测定值应在靶值范围内。
2.3瓶间均匀性
赋值结果的瓶间均匀性变异系数(CV)≤5%。
2.4稳定性
2.4.1效期稳定性
质控品原包装在2℃~8℃避光保存,有效期为18个月,在稳定期内赋值结果的变化趋势不显著。
2.4.2复溶稳定性
质控品复溶后,在2℃~8℃下避光密封保存,可保存24小时,在-20℃下避光密封保存,避免反复冻融,可保存30天,在稳定期内赋值结果的变化趋势不显著。
尿微量白蛋白(MALB)测定试剂盒(胶乳免疫比浊法)
适用范围:用于体外定量测定人尿液中微量白蛋白(MALB)的含量。
1.1 包装规格
试剂1:1×80mL,试剂2:1×20mL;
试剂1:50×240μL,试剂2:1×3mL;
试剂1:30×240μL,试剂2:1×1.8mL。
1.2 主要组成成分
2.1 外观和性状
试剂1为清澈透明的液体,无沉淀、悬浮物和絮状物。
试剂2为乳白色悬浮液,无沉淀。
2.2 净含量
每瓶试剂的净含量应不少于标示值。
2.3 试剂空白吸光度
用纯化水加入试剂作为样品测试时,试剂空白吸光度A应≤1.5。
2.4 分析灵敏度
测含156mg/L微量白蛋白尿液样本时,吸光度差值(ΔA)应≥0.04。
2.5 线性
试剂盒在[10,200]mg/L的线性范围内分析性能应符合如下要求:
2.5.1 线性相关系数(r)≥0.990;
2.5.2 相对偏差:浓度在(35,200]mg/L范围内,相对偏差不超过10%;
2.5.3 绝对偏差:浓度在[10,35]mg/L范围内,绝对偏差不超过
3.5mg/L。
2.6 测量精密度
2.6.1 重复性
用高低两个浓度样本重复测试,所得结果变异系数(CV)应≤10%。
2.6.2 批间差
试剂盒的批间相对极差(R)应≤15.0%。
2.7 准确度
在样品中加入一定量的纯品,计算回收率,应在85%~115%范围内。
2.8 稳定性
2℃~8℃避光贮存,有效期为12个月,取过有效期后一个月内的试剂盒进行检测,试剂盒应仍能符合2.1、2.3、2.4、2.5、2.6.1、2.7要求。