气体的制备与除杂-5气体的净化与除杂
- 格式:pptx
- 大小:293.30 KB
- 文档页数:15
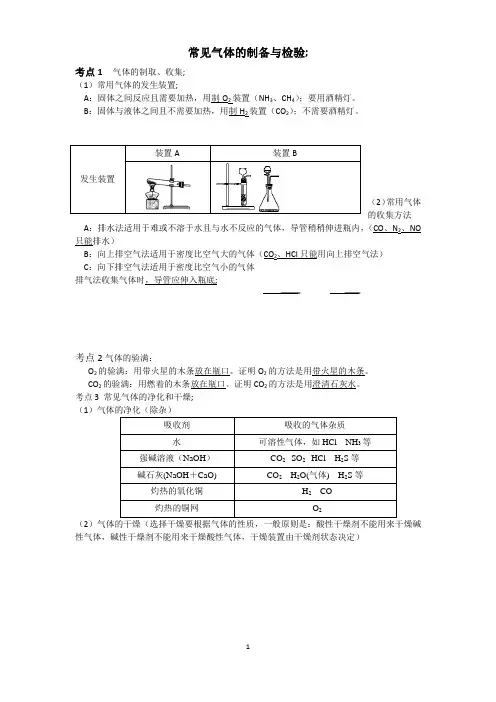
常见气体的制备与检验;考点1 气体的制取、收集;(1)常用气体的发生装置;A:固体之间反应且需要加热,用制O2装置(NH3、CH4);要用酒精灯。
B:固体与液体之间且不需要加热,用制H2装置(CO2);不需要酒精灯。
(2)常用气体的收集方法A:排水法适用于难或不溶于水且与水不反应的气体,导管稍稍伸进瓶内,(CO、N2、NO 只能排水)B:向上排空气法适用于密度比空气大的气体(CO2、HCl只能用向上排空气法)C:向下排空气法适用于密度比空气小的气体排气法收集气体时,导管应伸入瓶底;考点2气体的验满:O2的验满:用带火星的木条放在瓶口。
证明O2的方法是用带火星的木条。
CO2的验满:用燃着的木条放在瓶口。
证明CO2的方法是用澄清石灰水。
考点3 常见气体的净化和干燥;(1(2)气体的干燥(选择干燥要根据气体的性质,一般原则是:酸性干燥剂不能用来干燥碱性气体,碱性干燥剂不能用来干燥酸性气体,干燥装置由干燥剂状态决定)考点4常见气体的制取(二氧化碳、氧气与氢气制取的比较) 氧气(O 2)氢气(H 2)2KMnO 4K 2MnO 4+MnO 2+O 2↑(或2H 2O 22H 2O+O 2↑)Zn+H 2SO 4ZnSO 4+H 2↑CaCO 或稀石灰石或大理石(CaCO 3)和稀盐酸(HCl)①检查装置的气密性②试管口要略向下倾斜(防止凝结在试管口的小水珠倒流流入试管底部使试管破裂)来源学科网③加热时应先使试管均匀受热,再集中在药品部位加热④排水法收集完氧气后,先撤导管后撤酒精灯(防止水槽中的水倒流,使试管破裂)①检查装置的气密性②长颈漏斗的管口要插入液面下③点燃氢气前,一定要检验氢气的纯度(空气中,氢气的体积达到总体积的4%~74.2%点燃会爆炸)①检查装置的气密性②长颈漏斗的管口要插入液面下③不能用排水法收集考点5 气体的净化与干燥1.原则:不能引入新的气体杂质;不能减少被净化的气体的量。
2.顺序:气体的发生装置——除杂——干燥——主体实验——尾气处理。

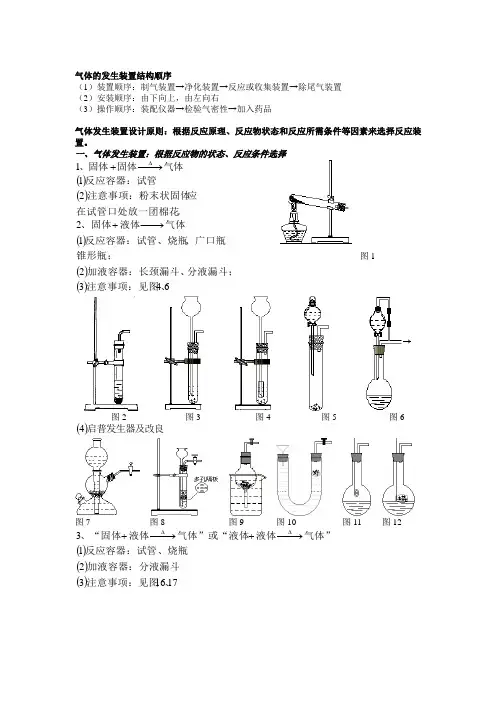
气体的发生装置结构顺序(1)装置顺序:制气装置→净化装置→反应或收集装置→除尾气装置 (2)安装顺序:由下向上,由左向右(3)操作顺序:装配仪器→检验气密性→加入药品气体发生装置设计原则:根据反应原理、反应物状态和反应所需条件等因素来选择反应装置。
一、气体发生装置:根据反应物的状态、反应条件选择气体固体、固体−→−+∆1 ()()。
在试管口处放一团棉花应注意事项:粉末状固体反应容器:试管21()()()643212、注意事项:见图分液漏斗;加液容器:长颈漏斗、锥形瓶;、广口瓶反应容器:试管、烧瓶气体液体、固体−→−+图1图2图3图4 图5图6()启普发生器及改良4图7图8图9图10图11图12()()()17163213、注意事项:见图加液容器:分液漏斗反应容器:试管、烧瓶气体”液体气体”或“液体液体、“固体−→−+−→−+∆∆图13 图14 图15 图16 图17 二、气体收集装置:根据气体的密度和溶解性选择、排空气法1图18 图19 图20 图21 图22 图23、排水法23、储气法三、尾气处理装置:根据多余气体的性质选择气体、在水中溶解性不大的1(图27)、燃烧或袋装法2(图28、图29)图27 图28 图29气体:防倒吸。
、在水中溶解性很大的.3图26图24 图25图30图31图32图33图34图35图36图37图38四、气体净化装置:根据净化剂的状态和条件选择图39图40图41图42五、气体性质实验装置:根据反应物的状态及反应的条件选择、常温反应装置1 、加热反应装置2、冷却反应装置3六、排水量气装置:测量气体的体积相平。
中左短水位与右端水位中水相平,图中量器内的水位与水槽注意事项:图5250图45图46图47图43图44图48图49图50图51图52图53常见气体的制取原理、除杂、检验、收集和尾气处理 ⑴氧气↑+===22332KC 2O KCl lO MnO ↑++===∆224242O M n O M n O K K M n O ↑+=====∆2222222O O H O H MnO 、 ↑+=+2222422O N a O HO H O Na 装置: 除杂: 检验: 收集:⑵氢气Zn+H ₂SO ₄ ==== ZnSO ₄+H ₂↑ 装置: 除杂: 检验: 收集: 尾气处理: ⑶氯气O H Cl MnCl HCl MnO 22222(4+↑+===+∆浓) O H Cl KCl HCl KClO 22333(6+↑+==+浓)装置: 除杂: 检验: 收集: 尾气处理: ⑷硫化氢制取原理:强酸与强碱的复分解反应 制取方程式:FeS+2HCl====FeCl ₂+H ₂S↑ 装置:启普发生器检验:能使湿润的醋酸铅试纸变黑除杂:先通入饱和NaHS 溶液(除HCl),再通入固体CaCl ₂ (或P ₂O5)(除水蒸气) 收集:向上排气法尾气回收:H ₂S+2NaOH==== Na ₂S+H ₂O 或H ₂S+NaOH==== NaHS+H ₂O ⑸二氧化硫Na ₂SO ₃+H ₂SO ₄==== Na ₂SO ₄+SO ₂↑+H ₂OO H SO CuSO SO H u 224422(2C +↑+==+∆浓)装置: 检验: 除杂: 收集: 尾气回收: ⑹二氧化碳CaCO ₃+2HCl====CaCl ₂+CO ₂↑+H ₂OO H CO NaCl HCl CO a 223222N +↑+=+⑺氨气O H NH CaCl Cl NH OH Ca 23242222)(+↑+==+∆↑+=+⋅3223)(C O H NH NH OH Ca aO装置: 检验: 除杂: 收集: 尾气回收: ⑻氯化氢↑+==+∆HCl SO Na SO H NaCl 2(24242浓)↑+=+H C l N a H S O SO H NaCl 442(浓)浓盐酸滴入浓硫酸中装置: 检验: 除杂: 收集: 尾气回收: ⑼二氧化氮O H NO NO Cu HNO Cu 2223322)((4+↑+===+∆浓)装置: 检验: 除杂: 收集: 尾气回收: ⑽一氧化氮O H NO NO Cu HNO Cu 223342)(3(83+↓+==+∆稀)装置: 检验: 除杂: 收集: 尾气回收:注:1.只能用排水集气法的气体:①与空气密度相差不大有________________ ②与空气中的某种气体反应有___________________________________ 2. 只能用排空气集气法的气体:①与水反应反应有_______________________ ②易溶于水有_______________________________________________________一、选择题1.实验室用下列方法制取气体:①过氧化氢中加少量二氧化锰 ②浓硝酸中加入铜片 ③氯化铵与消石灰混合加热 ④稀硝酸中加入铜片共热。
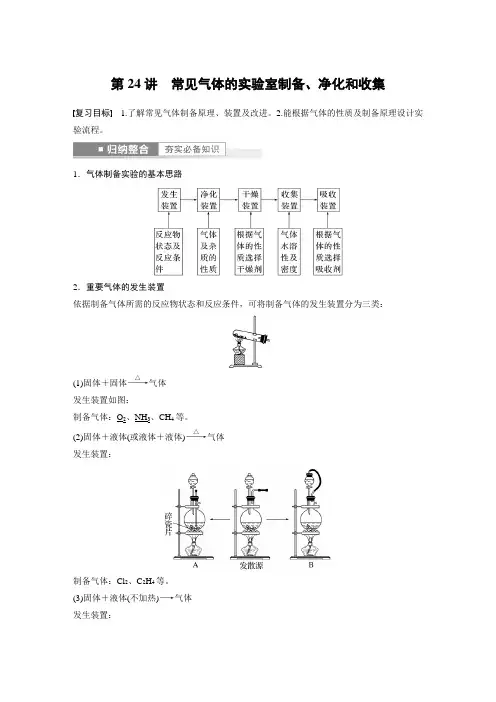
第24讲 常见气体的实验室制备、净化和收集复习目标 1.了解常见气体制备原理、装置及改进。
2.能根据气体的性质及制备原理设计实验流程。
1.气体制备实验的基本思路2.重要气体的发生装置依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为三类:(1)固体+固体――→△气体 发生装置如图:制备气体:O 2、NH 3、CH 4等。
(2)固体+液体(或液体+液体)――→△气体 发生装置:制备气体:Cl 2、C 2H 4等。
(3)固体+液体(不加热)―→气体 发生装置:制备气体:选择合适的药品和装置能制取中学化学中常见的气体。
3.常见气体典型制备系统举例(1)Cl2的实验室制备(2)SO2的实验室制备(3)NH3的实验室制备4.气体的除杂方法(1)除杂试剂选择的依据:主体气体和杂质气体性质上的差异,如溶解性、酸碱性、氧化性、还原性。
除杂原则:①不损失主体气体;②不引入新的杂质气体;③在密闭装置内进行;④先除易除的杂质气体。
(2)气体干燥净化装置类型液态干燥剂固态干燥剂固体,加热装置图ⅠⅡⅢⅣ常见干燥剂浓H2SO4(酸性、强氧化性)无水氯化钙(中性)、碱石灰(碱性)除杂试剂Cu、CuO、Mg等当CO2中混有O2杂质时,应选用上述Ⅰ~Ⅳ中的Ⅳ装置除O2,除杂试剂是Cu粉。
5.气体的收集方法收集方法收集气体的类型收集装置可收集的气体(举例)排水法难溶于水或微溶于水,且不与水反应的气体O2、H2、NO、CO等排空气法向上排空气法密度大于空气且不与空气中的成分反应Cl2、SO2、NO2、CO2向下排空气法密度小于空气且不与空气中的成分反应H2、NH36.集气装置的创新——排液集气装置装置(Ⅰ)从a管进气b管出水可收集难溶于水的气体,如H2、O2等。
若将广口瓶中的液体更换,还可以收集以下气体。
①饱和食盐水——收集Cl2。
②饱和NaHCO3溶液——收集CO2。
③饱和NaHS溶液——收集H2S。
④四氯化碳——收集HCl或NH3。

初中化学综合实验——气体的制取、净化和除杂!一、气体制取的仪器组合顺序制备纯净干燥气体的步骤是:1、实验仪器组装公式:气体发生装置—除杂质装置—干燥装置—气体收集装置→尾气处理⑴制气装置的选择:A 所需药品的状态;B 反应条件⑵集气装置的选择:A 气体的溶解性;B 气体的密度⑶除杂质的试剂和干燥剂的选择:实验室制取的气体常常有酸雾或水份。
(4) 酸雾可用水、氢氧化钠溶液、澄清的石灰水或饱和碳酸钠(碳酸氢钠)溶液除去,水份可用干燥剂如:浓硫酸(酸性)、碱石灰(碱性)、固体氢氧化钠(碱性)、氧化钙(碱性)、五氧化二磷(酸性)、无水氯化钙(中性)、无水硫酸铜(中性)等除去.(5)酸性干燥剂(浓硫酸)不能干燥碱性气体如氨气;(6)碱性干燥剂(NaOH )不能干燥酸性气体如二氧化硫、二氧化碳、氯化氢等2、气体除杂的方法:A 水吸收法:易溶于水的气体杂质用水吸收。
(如HCl)B 酸碱吸收法:酸性气体杂质用碱性试剂吸收。
(如氢氧化钠溶液吸收CO2、HCl。
)C 沉淀法:将杂质气体转变为沉淀除去。
(如用澄清石灰水除CO2)D 固化法:将杂质气体与固体试剂反应生成固体而除去。
(如除去O2用灼热的氧化铜)E 转纯法:将杂质转化为所需气体。
(如除去CO中的CO2,可将气体通过炽热的炭粉)3、气体除杂的原则:不减少被净化气体的质量,不引进新的杂质。
4、气体除杂的注意事项:A 选择除杂试剂:一般只能跟杂质起反应,而不能与被净化的气体反应。
B 除杂务尽:选择除杂试剂要注意反应进行的程度。
(如除去CO2时用氢氧化钠溶液比用澄清石灰水要好。
因为氢氧化钠的溶解度比氢氧化钙要大很多,因此其溶质质量分数较大。
)C 有许多杂质要除去时,要注意除杂的顺序。
一般来说,杂质中有许多酸性杂质时,先除酸性较强的杂质;而水蒸气要放在最后除去。
除去杂质和干燥的装置一般用洗气瓶或干燥管。
在洗气瓶中导气管一般是长进短出,在干燥管中一般是大进小出。
除杂和干燥一般是先除杂后干燥。

第21讲 常见气体的制备、净化和收集[复习目标] 1.掌握常见气体的制备、净化、收集及尾气处理的方法。
2.能对整套气体制备及性质实验装置进行分析,并能处理相关问题。
考点一 常见气体的制备、净化、收集及尾气处理必备知识夯实1.常见气体的发生装置 (1)固体+固体――→△气体发生装置如图:制备气体:□1O 2、□2NH 3等 (2)固体(液体)+液体――→△气体发生装置如图:制备气体:□3Cl 2、CH 2===CH 2(需加温度计)等 (3)固体+液体(不加热)→气体发生装置如图:制备气体:选择合适的试剂和装置能制取中学化学中常见的气体,如NH 3(□4生石灰、□5浓氨水)、O 2(MnO 2、□6H 2O 2溶液)、Cl 2(KMnO 4、□7浓盐酸)、SO 2(□8Na 2SO 3、较浓硫酸)等2.常见气体的除杂装置4.(1)实验室制取Cl2时,尾气的处理可采用□1b装置。
(2)制取CO时,尾气的处理可采用□2a、c装置。
(3)实验室制取NH3时,尾气的处理可采用□3d装置。
名师课堂点拨实验室中制取气体时实验装置的设计关键能力提升一、常见气体的制备和收集1.(2023·北京石景山区模拟)实验室制备下列气体所选试剂、制备装置及收集方法均正确的是()【解析】制取NO2可选用Cu和浓硝酸反应,不能选用稀硝酸,A错误;NH4Cl受热分解生成NH3和HCl,遇冷时NH3和HCl重新化合生成NH4Cl,不能用于制取NH3,B错误;H2O2在MnO2催化下分解生成H2O和O2,可用排水法收集O2,C正确;KMnO4和浓盐酸在常温下反应生成Cl2,Cl2的密度大于空气的密度,采用向上排空气法收集,选择装置c,D错误。
【答案】C2.实验室制取下列气体,所选反应试剂、制备装置与收集方法均合理的是()【解析】铜与稀硝酸生成NO且反应不需加热,NO与空气中的氧气反应生成NO2,不能用排空气法收集NO,A错误;乙醇在浓硫酸作用下迅速升高温度到170 ℃,乙醇生成乙烯气体,乙烯难溶于水,可以用排水法收集,B正确;氨的密度小于空气,应该使用向下排空气法收集,C错误;Na2SO3和硫酸反应不需要加热,且SO2能与水反应,不能用排水法收集,D错误。


气体的制取、净化和除杂初中化学中的实验组合题一般以氧气、氢气和二氧化碳三大气体的制取和性质实验或迁移应用其原理和性质的实验为主线,将许多仪器连接起来形成完整的实验装置图,再根据要求进行实验。
1.气体制取的仪器组合顺序制备纯净干燥气体的步骤是:实验仪器组装公式:气体发生装置—除杂质装置—干燥装置—气体收集装置→尾气处理⑴制气装置的选择:A 所需药品的状态;B 反应条件⑵集气装置的选择:A 气体的溶解性;B 气体的密度⑶除杂质的试剂和干燥剂的选择:实验室制取的气体常常有酸雾或水份。
酸雾可用水、氢氧化钠溶液、澄清的石灰水或饱和碳酸钠(碳酸氢钠)溶液除去,水份可用干燥剂如:浓硫酸(酸性)、碱石灰(碱性)、固体氢氧化钠(碱性)、氧化钙(碱性)、五氧化二磷(酸性)、无水氯化钙(中性)、无水硫酸铜(中性)等除去(1)酸性干燥剂(浓硫酸)不能干燥碱性气体如氨气;(2)碱性干燥剂(NaOH )不能干燥酸性气体如二氧化硫、二氧化碳、、氯化氢等气体除杂的方法:A 水吸收法:易溶于水的气体杂质用水吸收。
(如HCl) B 酸碱吸收法:酸性气体杂质用碱性试剂吸收。
(如氢氧化钠溶液吸收CO、HCl。
)2C 沉淀法:将杂质气体转变为沉淀除去。
(如用澄清)石灰水除CO2D 固化法:将杂质气体与固体试剂反应生成固体而除用灼热的氧化铜)去。
(如除去O2E 转纯法:将杂质转化为所需气体。
(如除去CO中的,可将气体通过炽热的炭粉)CO2气体除杂的原则:不减少被净化气体的质量,不引进新的杂质。
气体除杂的注意事项:A 选择除杂试剂:一般只能跟杂质起反应,而不能与被净化的气体反应。
时 B 除杂务尽:选择除杂试剂要注意反应进行的程度。
(如除去CO2用氢氧化钠溶液比用澄清石灰水要好。
因为氢氧化钠的溶解度比氢氧化钙要大很多,因此其溶质质量分数较大。
)C 有许多杂质要除去时,要注意除杂的顺序。
一般来说,杂质中有许多酸性杂质时,先除酸性较强的杂质;而水蒸气要放在最后除去除去杂质和干燥的装置一般用洗气瓶或干燥管。


气体除杂九年级化学知识点气体除杂是化学中的一个重要知识点,它涉及到气体的纯化和净化过程。
在化学实验和工业生产中,常常需要处理含有杂质的气体,为了确保实验结果的准确性和产品质量的稳定性,必须对气体进行除去杂质的处理。
本文将为大家介绍气体除杂的相关知识点。
一、气体的纯化方法气体的纯化方法主要包括物理方法和化学方法。
1. 物理方法物理方法主要利用了气体杂质的不同性质,通过物理性质的差异将气体中的杂质除去。
(1)冷凝法:根据气体的沸点差异,利用低温将混合气体冷凝,使其中的杂质凝固而得到纯净气体。
(2)吸附法:利用活性炭等材料对气体杂质的吸附性,将气体通入含有活性炭的吸附设备,通过吸附剂的作用将气体中的杂质吸附剔除。
(3)扩散法:利用气体分子速度分布不均匀的特性,将气体通过多个孔隙,使得分子速度快的气体分子相对集中在一起,达到纯化的目的。
2. 化学方法化学方法主要通过化学反应将气体中的杂质转化为其他物质,以达到纯化的目的。
(1)氧化还原法:通过氧化还原反应,将气体中的杂质氧化或还原为其他物质,再通过其他方法将其除去。
(2)吸收法:利用溶液中某些物质与气体杂质发生化学反应,将其吸收并与溶液中的其他物质结合,从而将杂质除去。
二、常见的气体除杂设备气体除杂的设备种类繁多,下面将介绍几种常见的设备。
1. 分子筛装置分子筛主要是一种多孔的固体物质,具有特定的吸附性能。
它可将分子直径较大的杂质截留在表面,从而达到除杂的效果。
分子筛广泛应用于石油、化工、医药等行业。
2. 活性炭过滤器活性炭是一种多孔的吸附剂,能有效去除气体中的有机杂质、异味物质和一些有毒有害气体。
活性炭过滤器广泛应用于空气净化、防毒面具等领域。
3. 冷凝器冷凝器是一种将气体冷凝成液体的装置。
它通过降低气体的温度,使气体中的水蒸气等杂质冷凝成液体,从而实现除湿和除杂的功能。
4. 吸附塔吸附塔是用于气体吸附除杂的设备,它采用吸附剂将气体中的杂质吸附下来,从而实现气体的纯化。
中学化学专题讲座气体的试验室制备、净化和收集1.气体制备试验的基本过程(1)气体制备试验装置一般包含以下几部分发生装置―→净扮装置―→干燥装置―→尾气处理装置 (2)气体制备的一般试验操作步骤①组装(从下到上,从左到右);②检验装置的气密性;③加入药品;④排尽装置内的空气;⑤验纯;⑥反应;⑦拆除装置。
2.气体发生装置依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为三类: (1)固体+固体――→△气体 发生装置:制备气体:O 2、NH 3、CH 4等留意事项:①试管口应稍向下倾斜,以防止产生的水蒸气在试管口冷凝后倒流,而使试管炸裂。
②铁夹应夹在距试管口1/3处。
③固体药品应平铺在试管底部。
④胶塞上的导管伸入试管内不能过长,否则会影响气体导出。
⑤如用排水集气法收集气体,当停止制气时,应先从水槽中把导管撤出,然后再撤走酒精灯,防止水倒吸。
(2)固体+液体或液体+液体――→△气体 发生装置:(a) (b) (c) 制备气体:Cl 2、C 2H 4等留意事项:①烧瓶应固定在铁架台上。
②先把固体药品放入烧瓶中,再缓缓加入液体。
③分液漏斗应盖上盖,留意盖上的凹槽对准分液漏斗颈部的小孔。
④对烧瓶加热时要垫上石棉网。
⑤液体+液体――→△气体时要加沸石,防止暴沸,如用(b)装置制取乙烯时需加碎瓷片。
⑥(c)装置中导管的作用是平衡气压,便于分液漏斗中的液体顺当滴下。
(3)固体+液体(不加热)―→气体发生装置:制备气体:H2、CO2、NO2、SO2、NO等留意事项:①块状固体及液体的混合物在常温下反应制备气体,可用启普发生器制备,当制取气体的量不多时,也可采纳简易装置。
②简易装置中长颈漏斗的下口应伸入液面以下,否则起不到液封作用而无法运用。
③加入块状固体药品的大小要相宜。
④加入液体的量要适当。
⑤最初运用时应待容器内原有的空气排净后,再收集气体。
⑥在导管口点燃氢气或其他可燃性气体时,必需先检验纯度。
中考常见气体的制备,净化,干燥和收集在中考化学中,实验室常见气体的制备,净化,干燥,收集以及性质的相关知识点是必考的内容,考察知识点比较综合,会涉及相关装置的选择问题,常见气体实验室制备的化学反应方程式,反应现象的书写,误差判断以及简单的计算。
在这里我们来总结一下实验室常见气体的制备过程中的相关实验装置的选择方法。
综合性气体制备实验装置的设计包括哪些方面?1、发生装置和收集装置的选择:(1)根据制取气体的反应原理,即制取气体时反应物的状态和反应条件,常用的气体发生装置有两种,分别是“固体加热型”和“固液常温型”,如图中的A、B。
(2)常用的气体收集装置有三种,分别是“排水法”、“向上排空气法”和“向下排空气法”,如图中的C、D、E。
常用气体的收集装置的选取的依据是气体的溶解性、密度及其是否与水或者空气的成分发生反应等:①如果气体是不易溶于水或难溶于水的,并且不与水发生反应,那么该气体可选取“排水法”的装置来收集。
②如果气体的密度比空气的大,并且不与空气的成分发生反应,那么该气体可选取“向上排空气法”的装置来收集。
③如果气体的密度比空气的小,并且不与空气的成分发生反应,那么该气体可选取“向下排空气法”的装置来收集。
2、净化装置的选择气体的净化(除杂),就是指将气体中的杂质除去,使其得到净化。
其理论依据是利用杂质所具有的与所需气体不同的物理性质或化学性质,选用适当的试剂,科学地设计实验方案,或者按照给出的实验设计方案,进行分析探究,逐步将气体中的杂质除去,使其得到净化。
常用的气体的净化(除杂)方法主要有两种:一是吸收法:即选用适当的试剂,通过物理变化或化学反应,将杂质直接吸收,转变为液体或固体等而除去。
例如,除去CO中混有的少量的CO2时,可先将混合气通过盛有浓NaOH溶液的洗气瓶中,吸收掉其中的CO2,然后再通过盛有浓硫酸的洗气瓶中,吸收掉其中的水蒸气。
而常见气体的吸收剂如下表:乐冲刺:做的更少,学的更好二是转化法:即将杂质通过化学反应转化为被所需气体而除去。