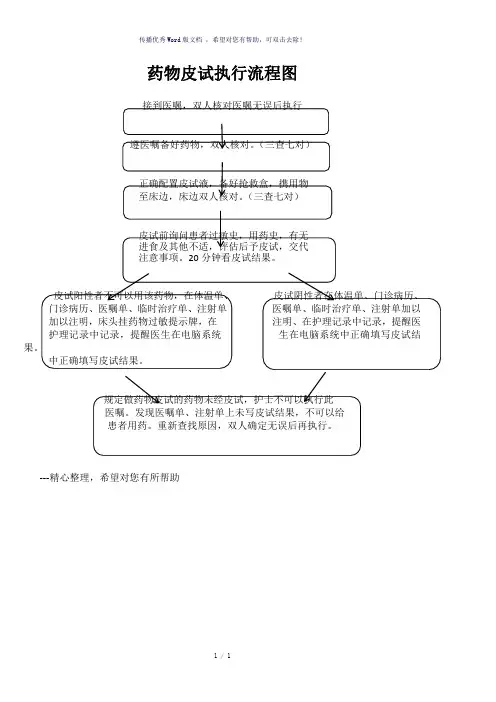
药物临床试验运行管理流程图
- 格式:docx
- 大小:10.60 KB
- 文档页数:1

药物临床试验运行管理制度和流程I目的:遵照中国GCP及ICH-GCP要求,参照国内、外开展药物临床试验的经验,结合本机构临床试验的特点,制定本制度与流程。
II适用范围:适用于本机构药物临床试验。
III内容:1.立项准备1.1申办者/CRO若有意在我院开展药物临床试验,需首先与本机构就研究科室、主要研究者等相关问题进行商洽。
1.2申办者/CRO与临床科室和机构共同商定主要研究者(PI),承担药物临床试验项目负责人应具有高级职称,参加过3个以上临床试验,并取得院外GCP培训证书。
1.3P1提出研究小组成员(必须有相关GCP培训证书)。
1.4若本单位为该项目的组长单位,P1主持召开研究者会议;若为参加单位,P1机构代表应参加研究者会议。
1.5申办者或CRO负责派出合格的、研究者所接受的监查员。
1.6申办者或CRo按照附件1准备申请临床试验的相关材料,递交机构办公室秘书。
2,立项审核机构对送审材料及研究小组成员资质进行形式审核,由科主任、机构主任审批后立项,正式立项后通知P1及申办者或CROo3,伦理委员会审核3.1申办者/CRO按照伦理委员会要求准备材料,并递交至伦理委员会秘书(电话:XXXX)进行伦理审评。
3.2申办者/CRO将最终的审评意见交机构办公室秘书存档。
4.合同和第三方CRC协议审核4.1项目取得本中心伦理批件后,申办者/CRO与研究者初步拟定合同和经费预算,和第三方CRC 协议(如有)提交医院0A,由药物临床试验机构、科技处、审计室、财务科、医院主管领导、中心主任对合同进行审核。
4.2经审核通过的合同和第三方CRC协议,申办者/CRO法人(或其授权人)与项目负责人共同签署后,交医院法人(或其授权人)审批签字并加盖公章后生效。
4.3合同和第三方CRC协议正式签署后,方能开始临床试验。
5.人类遗传资源管理1.1凡涉及人类遗产资源采集、收藏、利用、对外提供,项目启动前需按照《中华人民共和国人类遗传资源管理条例》和我中心人类遗传资源管理相关规定办理相关手续。


药物临床试验运行管理制度与工作流程Ⅰ.概念:药物临床试验是指任何在人体(病人或健康受试者)进行的药物的系统性研究,以证实或发现试验药物的临床、药理和/或其他药效学方面的作用、不良反应和/或吸收、分布、代谢及排泄,目的是确定试验药物的安全性和有效性。
Ⅱ.管理部门:药物临床试验机构(以下简称“机构”)对我院药物临床试验实行管理。
Ⅲ.工作程序:1.立项准备1.1.申办者/CRO(合同研究者组织)联系机构办、意向科室共同确定主要研究者。
CRA提交“药物临床试验立项申请表”(附件1),并按照“药物临床试验报送资料目录”(附件2)准备临床试验相关完整材料一份,交机构办公室。
1.2.PI提出研究小组成员,填写“主要研究者履历”(附件3)“项目研究团队成员表”(附件4),由CRA连同试验资料一起递交机构办公室。
研究小组人员的资质必须符合以下要求:研究团队成员必须经GCP培训并获取证书;主要研究者组建研究团队,包括:①临床医师;②病区护士;③研究护士;④药物管理人员;⑤药物代谢研究人员(如需要);⑥其他相关科室人员(如需要)1.3.一页均为文件目录,每项文件中间用带数字标识的隔页纸分隔。
请按文件目录所列文件顺序排列各项文件,文件夹中不包括的文件无需列入目录。
文件多的项目请准备多个“机构文件夹”,编号“①,②,③……”。
2.受理立项机构对送审材料及研究小组成员资质进行审核,决定是否同意立项。
若同意,则向伦理委员会发出“临床试验审批受理通知”(附件5)。
3.伦理审核3.1.申请者持“临床试验审批受理通知”(附件5)按照伦理委员会要求准备材料,将申报材料交伦理委员会进行伦理评审。
3.2.评审结束后,将“伦理委员会接受临床试验回执”(附件5)和“伦理委员会审批件”原件交回机构办公室。
若按伦理委员会要求所提交项目资料有所修订,要将已修订的项目资料补交到机构办公室备案。
4.签订协议4.1.临床试验协议样本先由研究团队审核确认后再交机构办公室复审,协议终版以主要研究者、机构办公室及申办者三方达成一致为准。
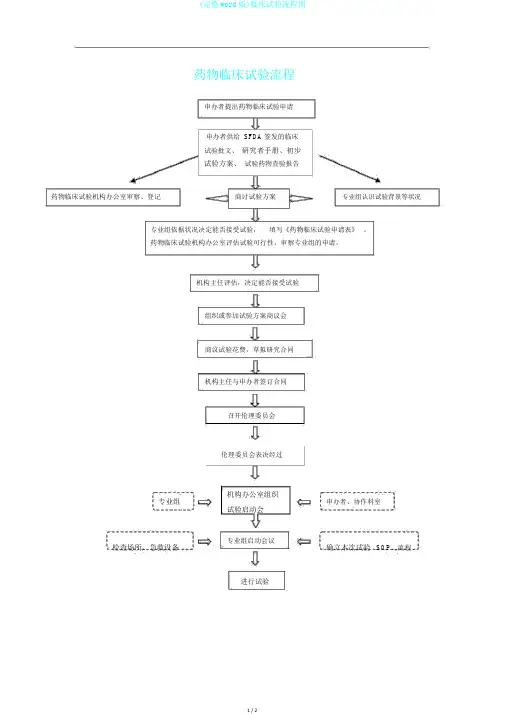
药物临床试验流程
申办者提出药物临床试验申请
申办者供给SFDA 签发的临床
试验批文、研究者手册、初步
试验方案、试验药物查验报告
药物临床试验机构办公室审察、登记商讨试验方案专业组认识试验背景等状况
专业组依据状况决定能否接受试验,填写《药物临床试验申请表》。
药物临床试验机构办公室评估试验可行性,审察专业组的申请。
机构主任评估,决定能否接受试验
组织或参加试验方案商议会
商议试验花费,草拟研究合同
机构主任与申办者签订合同
召开伦理委员会
伦理委员会表决经过
机构办公室组织
专业组申办者、协作科室
试验启动会
检查场所、急救设备专业组启动会议
确立本次试验SOP、流程进行试验
进行试验
受试者挑选药品管理
知情赞同过程、签知情赞同书中期试验文件采集、归档
协作会
试验数据记录项目负责人监察试验质量
监查员、机构办公室的监查不良事件监查、办理、记录
试验结束
向机构和有
严重不
良事件关单位报告
专业组整理、自查、审察CRF,移交
CRF及其余文件资料,退回试验用药
解盲
机构办公室审察CRF,整理、归档文件资料
机构办公室向申办者提交CRF 第一联,退回试验用药物
项目负责人依据统计结果撰写小结
报告,组长单位撰写总结报告
机构办公室审察小结报告,最
后交申办者,小结报告归档
组长单位与申办者组织召开临床试验总结会
总结报告归档,与申办者办理有关手续
机构办公室提交财务报告,机构主任
审批,财务科发放劳务费或一致划帐。
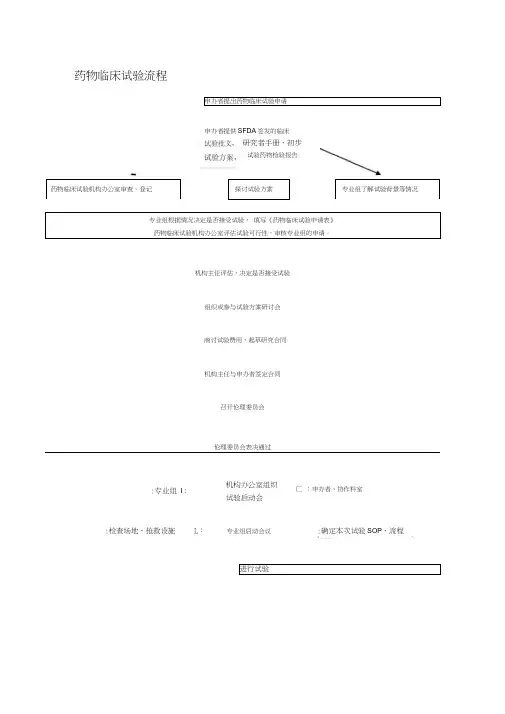
申办者提岀药物临床试验申请
申办者提供SFDA 签发的临床
药物临床试验机构办公室审查、登记
探讨试验方案
专业组了解试验背景等情况
专业组根据情况决定是否接受试验, 填写《药物临床试验申请表》 药物临床试验机构办公室评估试验可行性,审核专业组的申请。
机构主任评估,决定是否接受试验
组织或参与试验方案研讨会
商讨试验费用,起草研究合同
机构主任与申办者签定合同
召开伦理委员会
伦理委员会表决通过
进行试验
药物临床试验流程
:专业组 I :
机构办公室组织 试验启动会 匚 :申办者、协作科室
:检查场地、抢救设施
L : 专业组启动会议 :确定本次试验SOP 、流程 J _ _ _ _ _ _ -1
研究者手册、初步
试验药物检验报告
进行试验
机构办公室向申办者提交 CRF 第一联,退回试验用药物 项目负责人根据统计结果撰写小结 报告,组长单位撰写总结报告
机构办公室审核小结报告,最
后交申办者,小结报告归档
E
组长单位与申办者组织召开临床试验总结会
总结报告归档,与申办者办理相关手续
机构办公室提交财务报告,机构主任
审批,财务科发放劳务费或统一划帐 知情同意过程、签知情同意书 中期试验 协作会 <—[文件收集、归档 ' F 及进程责人监督试验质量 试验数据记录 监查员、机构办公室的监查 <=1不良事件监查、处理、记录。
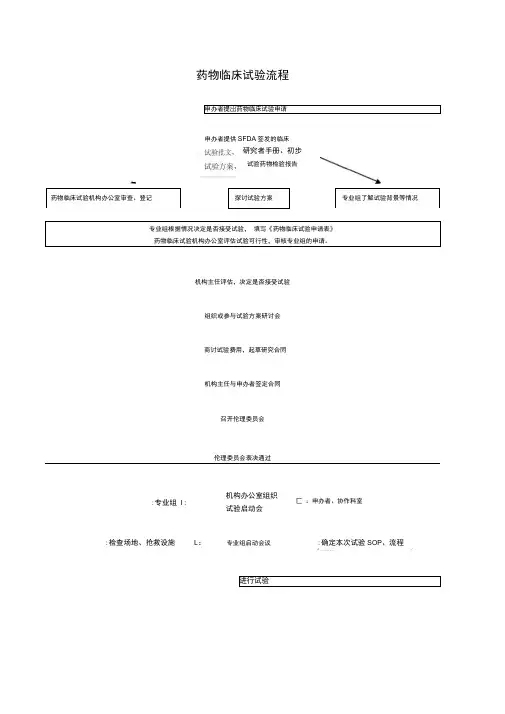
药物临床试验流程 申办者提岀药物临床试验申请
申办者提供SFDA 签发的临床
药物临床试验机构办公室审查、登记
探讨试验方案
专业组了解试验背景等情况
专业组根据情况决定是否接受试验, 填写《药物临床试验申请表》 药物临床试验机构办公室评估试验可行性,审核专业组的申请。
机构主任评估,决定是否接受试验
组织或参与试验方案研讨会
商讨试验费用,起草研究合同
机构主任与申办者签定合同
召开伦理委员会
伦理委员会表决通过
进行试验
:专业组 I :
机构办公室组织 试验启动会 匚 :申办者、协作科室
:检查场地、抢救设施
L : 专业组启动会议 :确定本次试验SOP 、流程 J _ _ _ _ _ _ -1
研究者手册、初步
试验药物检验报告
进行试验
机构办公室向申办者提交 CRF 第一联,退回试验用药物 项目负责人根据统计结果撰写小结 报告,组长单位撰写总结报告
机构办公室审核小结报告,最
后交申办者,小结报告归档
E
组长单位与申办者组织召开临床试验总结会
总结报告归档,与申办者办理相关手续
机构办公室提交财务报告,机构主任
审批,财务科发放劳务费或统一划帐 知情同意过程、签知情同意书 中期试验 协作会 试验数据记录 监查员、机构办公室的监查 <—[文件收集、归档 [ * "1 <3- 1项目负责人监督试验质量 <= 不良事件监查、处理、记录。

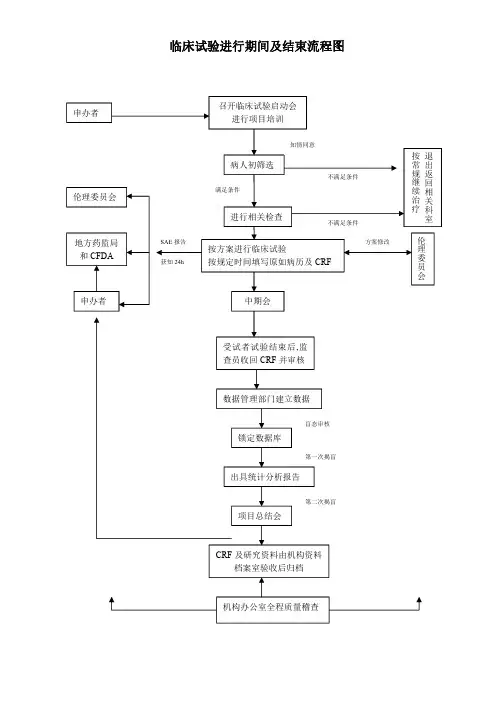
临床试验进行期间及结束流程图
申办者
召开临床试验启动会
进行项目培训
病人初筛选
进行相关检查
按方案进行临床试验
按规定时间填写原如病历及CRF
中期会
受试者试验结束后,监
查员收回CRF并审核
数据管理部门建立数据
盲态审核
锁定数据库
第一次揭盲出具统计分析报告
第二次揭盲项目总结会
知情同意满足条件
CRF及研究资料由机构资料
档案室验收后归档
机构办公室全程质量稽查
伦理委员会
地方药监局和CFDA
申办者SAE报告
获知24h
退
出
返
回
相
关
科
室
按
常
规
继
续
治
疗
方案修改
不满足条件
不满足条件
伦
理
委
员
会。