烷烯炔的化学性质宋
- 格式:doc
- 大小:77.50 KB
- 文档页数:3

烷烯炔的结构与性质烷烯炔是有机化合物中常见的一类化合物,它们在化学反应和应用中具有重要的地位。
本文将对烷烯炔的结构与性质进行探讨。
一、烷烯炔的结构烷烯炔由碳、氢原子组成,其中碳原子形成链状结构,并与氢原子通过共价键相连。
烷烯炔分为烷烃、烯烃和炔烃三类。
烷烃中的碳原子之间通过单键相连,无不饱和键;烯烃中有一个或多个双键,其中一个碳原子与另一个碳原子之间通过一个双键相连;炔烃中有一个或多个三键,其中一个碳原子与另一个碳原子之间通过一个三键相连。
二、烷烯炔的性质1. 物理性质烷烯炔的物理性质与其分子结构有关。
一般来说,烷烯炔在常温常压下为无色气体或液体,呈无色透明状。
烷烯炔的沸点较低,挥发性强。
2. 化学性质烷烯炔的化学性质较为活泼,容易发生反应。
以下是烷烯炔常见的化学反应及其性质。
(1)加成反应:烷烯炔与其他化合物中较活泼的原子或原团发生加成反应,生成新的有机化合物。
这类反应常见的有氢化、卤化等。
例如,炔烃可以与氯气反应生成取代的炔烃。
(2)氧化反应:烷烯炔在强氧化剂的作用下可以发生氧化反应,生成醛、酮、羧酸等有机化合物。
例如,丙炔经过氧化反应可以生成丙酮。
(3)聚合反应:烯烃和炔烃可以发生聚合反应,生成高分子化合物。
例如,乙烯可以聚合成聚乙烯等。
三、烷烯炔的应用烷烯炔在化学工业中具有广泛的应用。
以下是烷烯炔的几个应用领域。
1. 燃料和能源烷烯炔在燃料领域有重要的作用。
例如,烯烃被用作高效燃料,如乙烯可以用于制造乙烯燃料。
2. 合成材料烷烯炔可以用于合成各种高分子材料,如聚乙烯、聚丙烯、聚丁烯等。
这些材料在塑料、纤维和橡胶等领域中具有广泛的应用。
3. 医药领域烷烯炔在医药领域中也有重要的应用。
一些炔烃化合物被用作医药中间体,如乙炔酸可以用于合成某些药物。
4. 农药和化肥烷烯炔可以用于制造农药和化肥,如丙炔可以用于制造杀菌剂。
5. 光电材料烯烃和炔烃可以用于合成光电材料,如聚苯乙烯可以用于制造光纤。
综上所述,烷烯炔是一类重要的有机化合物,具有丰富的结构和多样的化学性质。

烷烃烯烃和炔烃的结构和性质有哪些基本特征烷烃烯烃和炔烃是有机化合物中的三种基本类别。
它们在化学结构和性质上都具有一些基本特征。
下面将分别介绍烷烃烯烃和炔烃的结构和性质。
烷烃是由碳和氢原子组成的碳氢化合物,其分子式为CnH2n+2。
烷烃分子中的碳原子通过共价键连接在一起,形成直链或支链结构。
烷烃的碳原子通过单键连接,每个碳原子还与四个氢原子形成单键。
这种结构使烷烃分子具有饱和的化学环境,因此烷烃通常比较稳定。
烷烃根据碳原子数目的不同可以分为甲烷、乙烷、丙烷等。
烯烃是具有碳碳双键的烃类化合物,其分子式为CnH2n。
烯烃分子中含有至少一个碳碳双键,这使得烯烃分子具有较为活泼的化学性质。
由于双键的存在,烯烃分子可以进行加成反应、烯烃的碳碳双键可以被氢气直接加成,生成相应的饱和烃。
烯烃根据碳原子数目的不同可以分为乙烯、丙烯、丁烯等。
炔烃是具有碳碳三键的烃类化合物,其分子式为CnH2n-2。
炔烃分子中含有至少一个碳碳三键,这使得炔烃分子具有极高的反应活性。
由于三键的存在,炔烃分子可以进行加成反应、炔烃的碳碳三键可以被氢气加成形成烯烃;炔烃还可以进行消除反应,使一个炔烃分子中的两个氢原子脱去,形成芳烃分子。
炔烃根据碳原子数目的不同可以分为乙炔、丙炔、丁炔等。
烷烃烯烃和炔烃具有某些共同特征。
首先,它们的化学结构都以碳原子链为基础,通过共价键连接。
其次,它们中的碳原子都处于sp3杂化状态(烷烃)或sp2杂化状态(烯烃和炔烃),这种杂化状态影响了它们的结构和化学性质。
此外,烷烃烯烃和炔烃都是无色、无味的气体或液体,在常温下主要以分子形式存在。
然而,烷烃烯烃和炔烃也存在一些区别。
最显著的区别是它们的饱和度和反应性。
烷烃是饱和化合物,其所有碳原子均以单键连接,并且由于没有不饱和键的存在,烷烃的反应性较低。
烯烃和炔烃都是不饱和化合物,它们中至少存在一个碳碳双键或三键,这使得它们具有较高的反应活性。
除此之外,由于不同的碳碳键类型,烯烃和炔烃具有不同的化学性质。

烷烯炔知识点总结烷烯炔的命名和结构烷烯炔的命名符合有机化学的一般命名规则,烷烯的命名以根据含有双键的个数来决定,烷烯中双键的位置通过编号来表示。
比如,乙烯是一种两碳的烯烃,丙烯则是一种三碳的烯烃。
炔的命名也是类似的,炔的命名以含有三键的个数来决定,炔中三键的位置通过编号来表示。
比如,丙炔是一种三碳的炔,戊炔则是一种四碳的炔。
烷烯炔的结构也符合共价键的结构,烷烯中的双键是通过sp2杂化的碳原子构成的,炔中的三键是通过sp杂化的碳原子构成的。
这些结构决定了烷烯炔的一些化学特性,比如稳定性和反应性等。
烷烯的化学性质烷烯是含有双键的碳氢化合物,在化学性质上有着一些特点。
在工业上,很多烷烯的制备都是通过烷烃的脱氢来实现的。
烷烯可以参与一系列的加成反应,比如加氢反应、卤素化反应、水化反应等。
烷烯还可以进行脱氢反应,生成烷烯或芳烃。
除此之外,烷烯还可以通过重排反应和氧化反应来合成其他化合物。
炔的化学性质炔是含有三键的碳氢化合物,在化学性质上也有着一些特点。
炔的三键是可以被氢化的,生成烯烃或烃。
在工业上,炔可以参与一系列的加成反应,比如加氢反应、卤素化反应、水化反应等。
炔还可以与金属形成金属炔配合物,这些金属炔配合物在有机合成中有着重要的应用。
烷烯炔的化学反应烷烯和炔在化学反应中都可以参与一系列的加成反应。
双键和三键的位置和数量会决定其反应性,比如双键或三键的位置对于反应的位置选择性和立体选择性有着重要的影响。
比如烯烃可以进行选择性的氢化反应,生成烷烃或烯烃,而炔可以进行选择性的水化反应,生成醛或酮。
烷烯炔的制备烷烯和炔可以通过多种方法进行制备。
对于烷烯来说,很多烷烃可以通过脱氢反应来得到,比如乙烷可以通过蒸汽裂化或热裂化得到乙烯。
而对于炔来说,也可以通过脱氢反应或氢化反应来得到,比如氯乙炔可以通过钠和乙烯的氢化反应来得到。
烷烯炔的应用烷烯和炔在工业上有着广泛的应用。
烷烯可以用来合成高级燃料,比如乙烯可以用来合成乙烯聚合物,还可以用来生产乙醛、乙醇和醋酸等化工产品。

烃和卤代烃知识点总结在上课的时候,总是会有些知识点是需要我们记住的,记不住怎么办呢?下面,小编为大家分享烃和卤代烃知识点总结,希望对大家有所帮助!烷烃、烯烃和炔烃1.概念及通式(1)烷烃:分子中碳原子之间以单键结合成链状,碳原子剩余的价键全部跟氢原子结合的饱和烃,其通式为:cnh2n+2(n≥l)。
(2)烯烃:分子里含有碳碳双键的不饱和链烃,分子通式为:cnh2n(n≥2)。
(3)炔烃:分子里含有碳碳三键的一类脂肪烃,分子通式为:cnh2n-2(n≥2)。
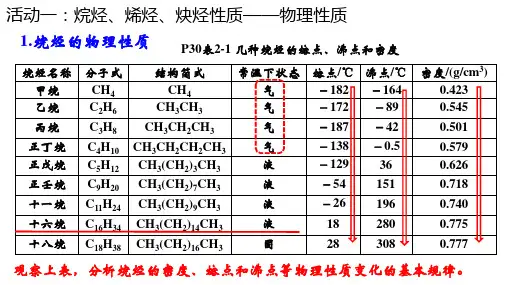
2.物理性质(1)状态:常温下含有1~4个碳原子的烃为气态烃,随碳原子数的增多,逐渐过渡到液态、固态。
(2)沸点:①随着碳原子数的增多,沸点逐渐升高。
②同分异构体之间,支链越多,沸点越低。
(3)相对密度:随着碳原子数的增多,相对密度逐渐增大,密度均比水的小。
(4)在水中的溶解性:均难溶于水。
3.化学性质(1)均易燃烧,燃烧的化学反应通式为:化学(2)烷烃难被酸性kmno4溶液等氧化剂氧化,在光照条件下易和卤素单质发生取代反应。
(3)烯烃和炔烃易被酸性kmno4溶液等氧化剂氧化,易发生加成反应和加聚反应。
几类重要烃的代表物比较1.结构特点2、化学性质(1)甲烷化学性质相当稳定,跟强酸、强碱或强氧化剂(如kmno4)等一般不起反应。
①氧化反应甲烷在空气中安静的燃烧,火焰的颜色为淡蓝色。
其燃烧热为890kj/mol,则燃烧的热化学方程式为:ch4(g)+2o2(g)化学co2(g)+2h2o(l);△h=-890kj/mol②取代反应:有机物物分子里的某些原子或原子团被其他原子或原子团所替代的反应。
甲烷与氯气的取代反应分四步进行:第一步:ch4+cl2化学ch3cl+hcl第二步:ch3cl+cl2化学ch2cl2+hcl第三步:ch2cl2+cl2化学chcl3+hcl第四步:chcl3+cl2化学ccl4+hcl甲烷的四种氯代物均难溶于水,常温下,只有ch3cl是气态,其余均为液态,chcl3俗称氯仿,ccl4又叫四氯化碳,是重要的有机溶剂,密度比水大。



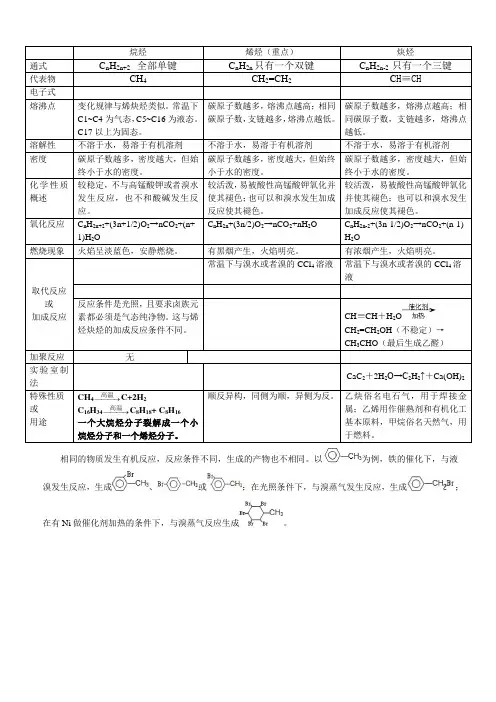
烷烃、烯烃、炔烃的结构与性质1.烷烃、烯烃、炔烃的组成、结构特点和通式2.脂肪烃的物理性质性质变化规律状态常温下含有1~4个碳原子的烃都是气态,随着碳原子数的增多,逐渐过渡到液态、固态沸点随着碳原子数的增多,沸点逐渐升高;同分异构体之间,支链越多,沸点越低相对密度随着碳原子数的增多,相对密度逐渐增大,密度均比水小水溶性均难溶于水3.脂肪烃的化学性质(1)烷烃的取代反应①取代反应:有机物分子中某些原子(或原子团)被其他原子(或原子团)所替代的反应。
②烷烃的卤代反应a.反应条件:气态烷烃与气态卤素单质在光照下反应。
b.产物成分:多种卤代烃混合物(非纯净物)+HX。
c.定量关系:~X2~HX,即取代1 mol氢原子,消耗1_mol卤素单质生成1 mol HX。
(2)烯烃、炔烃的加成反应①加成反应:有机物分子中的不饱和碳原子与其他原子(或原子团)直接结合生成新的化合物的反应。
②烯烃、炔烃的加成反应(写出有关反应的化学方程式)(3)加聚反应①丙烯加聚反应的化学方程式为n CH 2==CH —CH 3―――→催化剂。
②乙炔加聚反应的化学方程式为 n CH ≡CH ――→催化剂CH==CH 。
(4)二烯烃的加成反应和加聚反应 ①加成反应②加聚反应:n CH 2==CH —CH==CH 2――→催化剂CH 2—CH==CH —CH 2。
(5)脂肪烃的氧化反应烷烃 烯烃 炔烃 燃烧现象 燃烧火焰较明亮 燃烧火焰明亮,带黑烟 燃烧火焰很明亮,带浓黑烟通入酸性KMnO 4溶液不褪色褪色褪色[拓展延伸]烯烃、炔烃被酸性KMnO 4溶液氧化产物规律[应用举例]某烃的分子式为C11H20,1 mol该烃在催化剂作用下可以吸收2 mol H2;用热的酸性KMnO4溶液氧化,得到丁酮()、琥珀酸()和丙酮()三者的混合物。
该烃的结构简式:______________________________________________________。

烷烃烯烃炔烃列表总结烷烃、烯烃、炔烃是有机化合物中的三类常见烃类化合物。
它们在化学结构和性质上有很大的差异。
本文将对烷烃、烯烃、炔烃进行总结和分类,以便更好地理解它们的特性和应用。
烷烃烷烃是由碳和氢原子组成的无环烷烃化合物。
它们的分子结构是直链、支链或环状的。
烷烃通常具有以下特点:•烷烃分子中的碳原子与四个不同的氢原子相连,形成一个完全饱和的碳骨架。
•烷烃中的碳原子通过单键连接(σ键)。
•烷烃的命名规则是根据碳原子数目和其排列方式来命名的。
•烷烃具有较低的反应活性,不易与其他物质发生化学反应。
•烷烃在石油和天然气中广泛存在,是燃料和石化工业的重要原料。
常见的烷烃包括甲烷、乙烷、丙烷等,它们的分子结构和命名规则如下:分子式分子结构常用名称CH4 H—C—H 甲烷C2H6 H—C—C—H 乙烷C3H8 H—C—C—C—H 丙烷………烯烃烯烃是含有碳-碳双键(C=C)的烃类化合物。
它们的分子结构是直链或环状的。
烯烃通常具有以下特点:•烯烃分子中至少有一个碳原子与其他碳原子通过双键连接(π键)。
•烯烃的碳原子仍然与两个氢原子相连,形成一个不饱和的碳骨架。
•烯烃的命名规则是根据碳原子数目、双键位置和其排列方式来命名的。
•烯烃比烷烃具有更高的反应活性,容易进行加成反应、聚合反应等。
常见的烯烃包括乙烯、丙烯、戊烯等,它们的分子结构和命名规则如下:分子式分子结构常用名称C2H4 H2C=C=CH2 乙烯C3H6 CH2=CH—CH3 丙烯C5H10 CH2=CH—CH2—CH2—CH3 戊烯………炔烃炔烃是含有碳-碳三键(C≡C)的烃类化合物。
它们的分子结构是直链或环状的。
炔烃通常具有以下特点:•炔烃分子中至少有一个碳原子与其他碳原子通过三键连接(π键)。
•炔烃的碳原子仍然与一个氢原子相连,形成一个不饱和的碳骨架。
•炔烃的命名规则是根据碳原子数目、三键位置和其排列方式来命名的。
•炔烃比烷烃和烯烃具有更高的反应活性,容易进行加成反应、聚合反应等。
烷烃、烯烃、炔烃的结构与性质.docx烷烃、烯烃、炔烃的结构与性质1.烷烃、烯烃、炔烃的组成、结构特点和通式2.脂肪烃的物理性质性质变化规律常温下含有1~ 4 个碳原子的烃都是气态,随着碳原子数的增多,逐渐过渡到液状态态、固态沸点相对密度水溶性随着碳原子数的增多,沸点逐渐升高;同分异构体之间,支链越多,沸点越低随着碳原子数的增多,相对密度逐渐增大,密度均比水小均难溶于水3.脂肪烃的化学性质(1)烷烃的取代反应①取代反应:有机物分子中某些原子或原子团被其他原子或原子团所替代的反应。
②烷烃的卤代反应a.反应条件:气态烷烃与气态卤素单质在光照下反应。
b.产物成分:多种卤代烃混合物(非纯净物 )+ HX 。
c.定量关系:~Cl2~HCl即取代 1 mol氢原子,消耗1_mol卤素单质生成1 mol HCl 。
(2)烯烃、炔烃的加成反应①加成反应:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。
②烯烃、炔烃的加成反应(写出有关反应的化学方程式)(3)加聚反应①丙烯加聚反应的化学方程式为催化剂nCH2==CH—CH 3――→。
催化剂②乙炔加聚反应的化学方程式为nCH≡ CH――→CH===CH。
(4)二烯烃的加成反应和加聚反应①加成反应催化剂②加聚反应:nCH 2 ==CH—CH==CH 2――→CH 2— CH==CH — CH 2。
(5)脂肪烃的氧化反应烷烃烯烃炔烃燃烧现象燃烧火焰较明亮燃烧火焰明亮,带黑烟燃烧火焰很明亮,带浓黑烟通入酸性不褪色褪色褪色KMnO 4溶液(1)符合通式C n H 2n+2的烃一定是烷烃(√ )(2)丙烷分子中的碳原子在同一条直线上(× )(3)乙烯和乙炔可用酸性KMnO 4溶液鉴别(× )(4)聚丙烯可发生加成反应(× )(5)烷烃同分异构体之间,支链越多,沸点越高(× )(6)顺 -2-丁烯和反 -2-丁烯均能使溴水褪色(√ )(7)CH 2==CHCH==CH 2与 Br 2发生加成反应可生成Br — CH 2CH==CHCH 2— Br 和2种物质(× )1.烃反应类型判断(1)CH 3CH==CH 2+________―→,反应类型:____________。
高三有机烷烯炔知识点总结有机化学是高中化学中的重要分支,而有机烷烯炔是其中的一类有机化合物。
本文将对高三有机烷烯炔知识点进行总结,以帮助同学们更好地理解和掌握这一部分知识。
一、有机烷烯炔的基本概念有机烷烯炔是由碳和氢构成的有机化合物,分为烷、烯和炔三类。
其中,烷是碳原子通过单键连接而形成的链状结构;烯是碳原子通过双键连接而形成的链状结构;炔是碳原子通过三键连接而形成的链状结构。
二、烷的命名和性质烷的命名按照碳原子数目进行命名,以及碳原子间的连接方式。
烷的性质主要取决于其分子量和分子结构。
一般来说,烷是饱和的,不容易发生化学反应,且在常温下大部分为气体或液体。
三、烯的命名和性质烯的命名按照碳原子数目进行命名,以及双键的位置。
烯的性质与烷相比更为活泼,容易发生加成反应、与酸性物质反应等。
烯多为液态或固态,其中较低碳数的烯可以是气体。
四、炔的命名和性质炔的命名按照碳原子数目进行命名,以及三键的位置。
炔的性质较为活泼,容易发生加成反应、与酸性物质反应等。
大部分炔为气体,少数碳数较高的炔为液态或固态。
五、有机合成反应有机烷烯炔能够通过多种合成反应得到。
常见的有机合成反应包括取代反应、加成反应和消除反应等。
其中,取代反应是指原有的官能团被其他官能团取代的反应;加成反应是指不同物质通过共有键形成新的化学键的反应;消除反应是指分子内某个官能团与另一个官能团失去原子(通常是氢)形成化学键的反应。
六、有机烷烯炔的应用有机烷烯炔在化学工业、医药领域等具有广泛的应用。
烷类化合物可用作溶剂、燃料等;烯类化合物可用作合成橡胶、塑料、染料等;炔类化合物可用于合成橡胶、润滑剂等。
七、有机烷烯炔的环境影响和安全注意事项有机化合物的排放和应用对环境有一定的影响,其中有机烷烯炔尤其需要注意。
排放燃烧产物中含有大量的氧化物和碳氢化合物,对空气质量和人体健康有潜在危害。
在使用和储存有机烷烯炔化合物时,需要注意安全操作,避免接触皮肤、吸入有害气体等。
学案编号:有机选修3 组编:宋立坤 审核:张力 2011-4-15第一节 烃 第二课时 烷烃 烯烃 炔烃的化学性质【温故知新区】回顾必修中甲烷、乙烯的性质,类比乙烯推测乙炔的性质。
并写出有关方程式。
【课前预习区】1. (p32上)甲烷是有机物中含H 质量百分数最 的,单位质量甲烷放热量最,所以是理想的有机燃料。
、的主要成分是甲烷。
液化石油气的主要成分是。
水煤气的主要成分是。
2. 同系物具有相同的官能团,结构相似,则性质相似,所以我们根据甲烷的性质,可以预测出其他烷烃的化学性质……本节我们学习的同系物有烷烃、烯烃、炔烃。
请写出他们的通式,填写p27表格。
3. p30烷烃的通式: ,常温下烷烃很不活泼,与 、 、 和还原剂等都不反应,只有在特殊条件(例如 、 )下在能反应。
其主要化学性质有,其特征反应是。
4. p32烯烃的通式:。
最简单的烯烃为 ,比烷烃活泼,其主要化学性质有。
其特征反应是5. 炔烃的通式:。
最简单的炔烃为,比烷烃活泼,其主要化学性质有。
其特征反应是【课堂互动区】 一、 复习取代反应、加成反应、加聚反应类型1. 取代反应:取代反应(卤代)是烷烃共同具有的一个性质。
有关该反应应注意:○1纯卤素(不能是卤素的任何溶液)②光照条件③逐步取代④1mol 卤素只取代1molH 原子。
书写氯气与甲烷的反应方程式2. 加成反应1) 乙烯加成:学生书写反应方程式CH 2=CH 2 ⎩⎪⎨⎪⎧—→HClCH 3CH 2Cl —→Br 2CH 2BrCH 2Br —→H 2O CH 3CH 2OH2) 乙炔加成特点:逐步加成。
由于C ≡C 比C=C 键能大,因此使溴水褪色速率CH ≡CH 比CH 2=CH 2慢。
注意:CH ≡CH+H 2O ———→催化剂加成CH 2=CHOH (不稳定)—————→立即转化为CH 3CHO思考:如何制取CH 2Br ―CHCl Br?3) 拓展:二烯烃的加成(二烯烃,通式为C n H 2n -2与同数碳原子炔烃互为同分异构,化学性质与烯烃相似,主要是在加成反应时有多种情况)CH 2=CH-CH=CH 2+Br 2 ⎩⎪⎨⎪⎧1.2-加成(低温)1.4-加成(高温)完全加成(Br 2足量)3. 加聚反应: 学生书写反应方程式 ,指出单体、链节、聚合度。
学案编号:有机选修3 组编:宋立坤 审核:张力 2011-4-15
第一节 烃 第二课时 烷烃 烯烃 炔烃的化学性质
【温故知新区】
回顾必修中甲烷、乙烯的性质,类比乙烯推测乙炔的性质。
并写出有关方程式。
【课前预习区】
1. (p32上)甲烷是有机物中含H 质量百分数最 的,单位质量甲烷放热量最
,所以是理想的有机燃料。
、
的主要成分是甲烷。
液化石油气的主要成分是。
水煤气的主要成分是。
2. 同系物具有相同的官能团,结构相似,则性质相似,所以我们根据甲烷的性质,可以预测出
其他烷烃的化学性质……本节我们学习的同系物有烷烃、烯烃、炔烃。
请写出他们的通式,填写p27表格。
3. p30烷烃的通式: ,常温下烷烃很不活泼,与 、 、 和还
原剂等都不反应,只有在特殊条件(例如 、 )下在能反应。
其主要化学性质有
,其特征反应是。
4. p32烯烃的通式:。
最简单的烯烃为 ,比烷烃活泼,其主要化学性质有。
其特征反应是
5. 炔烃的通式:。
最简单的炔烃为
,比烷烃活泼,其主要化学性质有。
其特征反应是
【课堂互动区】 一、 复习取代反应、加成反应、加聚反应类型
1. 取代反应:取代反应(卤代)是烷烃共同具有的一个性质。
有关该反应应注意:
○1纯卤素(不能是卤素的任何溶液)②光照条件③逐步取代④1mol 卤素只取代1molH 原子。
书写氯气与甲烷的反应方程式
2. 加成反应
1) 乙烯加成:
学生书写反应方程式
CH 2=CH 2 ⎩
⎪⎨⎪⎧—→HCl
CH 3CH 2Cl —→Br 2
CH 2BrCH 2Br —→H 2O CH 3CH 2OH
2) 乙炔加成
特点:逐步加成。
由于C ≡C 比C=C 键能大,因此使溴水褪色速率CH ≡CH 比CH 2=CH 2慢。
注意:CH ≡CH+H 2O ———→催化剂加成
CH 2=CHOH (不稳定)—————→立即转化为
CH 3CHO
思考:如何制取CH 2Br ―CHCl Br?
3) 拓展:二烯烃的加成(二烯烃,通式为C n H 2n -2与同数碳原子炔烃互为同分异构,化学性
质与烯烃相似,主要是在加成反应时有多种情况)
CH 2=CH-CH=CH 2+Br 2 ⎩⎪⎨⎪⎧1.2-加成(低温)
1.4-加成(高温)完全加成(Br 2足量)
3. 加聚反应: 学生书写反应方程式 ,指出单体、链节、聚合度。
nCH 2=CH 2 ———→引发剂[— CH 2―CH 2]—n nCH 3CH=CHCl ———→引发剂
nCH 3CH=CH 2 ———→引发剂 n CH ≡CH ———→引发剂
nCH 2=CH —CH=CH 2———→引发剂 nCH 2=C —| CH 3CH=CH 2———→引发剂
乙烯和丙烯按物质的量比1:1聚合时,可生成聚合物乙丙树脂,写出该聚合物的可能的结构简式
【学生总结】请总结加聚反应的特点,并与同学交流你的想法。
试卷编号:有机选修3 主任签字:
【课后练习区】
1.请写出下列反应的化学方程式
a)乙炔与氢气用镍做催化剂在加热条件下发生加成反应生成乙烷。
b)乙烯与水用硫酸做催化剂在加热条件下发生加成反应
c)1-丁烯与氢气用镍做催化剂在加热条件下发生加成反应。
2.关于烷烃性质的叙述,错误的是( )
A. 都能使酸性高锰酸钾溶液褪色B.都能燃烧
C.通常情况下跟酸、碱和氧化剂都不反应D.都能发生取代反应
3.2—甲基丁烷和氯气发生取代反应,得到的一氯代物共有()
A.3种B.4种C.5种D.6种
4.制取氯乙烷最合理的方法是()
A.乙烷与Cl2取代B.乙烯与Cl2加成
C.乙烯与HCl加成D.把乙烯通入盐酸中
5.既可用来除去甲烷中的丙烯,又可用来鉴别乙烷与丁烯的方法是()
A.把气体通入足量液溴中B.在导管口处点燃
C.一定条件下与H2发生加成反应D.把气体通入足量溴水中
6.下列关于聚氯乙烯的有关说法,正确的是()
A.聚氯乙烯为纯净物B.聚氯乙烯可使溴水褪色
C.聚氯乙烯的单体可作果实催化剂D.聚氯乙烯的单体,可使KMnO4溶液褪色
7.某气态烃0.5mol能和1molHCl完全加成,加成后产物分子上的氢原子又可被3molCl2取代,
则此气态烃可能是()
A.CH≡CCH3B.CH2=CH2C.CH≡CH D.CH2=C(CH3)2
8.将20mL含某烷烃与炔烃的混合气体在催化剂作用下与H2加成,最多需要同温同压下
H210mL,则混合气体中烷炔与炔烃物质的量之比是
A.1∶1
B.1∶2
C.1∶3
D.3∶1
9.两种气态烃组成的混合气0.1mol,完全燃烧后,得到3.36L(标准状况下)CO2和3.6g H2O。
下列说法中正确的是()
A.一定有乙烯B.一定有甲烷C.一定没有CH4D、一定没有乙烷
10.有A、B、C、D四种烃,在常温下A、C是气体,B、D是液体。
A完全燃烧后生成二氧化
碳与水物质的量之比是2:1;B的分子量是A的三倍;C既不能使酸性高锰酸钾溶液褪色也不能使溴水褪色,但在光照条件下最多可与六倍体积氯气发生反应;燃烧相同物质的量C与D,生成二氧化碳的体积比为1:4,D不能使溴水褪色但能使酸性高锰酸钾溶液褪色,在催化剂作用下1摩尔D能与3摩尔氢气完全反应;在铁粉存在下与溴反应生成一溴代物只有一种。
试推断有机物A、B、C、D,分别写出结构简式:
A:B:C:D:
11.根据实验室蒸馏石油实验,回答问题:
①指出各主要仪器的名称
②石油的分馏属于物理变化还是化学变化?
③烧瓶中加入几片碎瓷片,其作用是
④温度计水银球的位置
⑤冷凝管中口进水,口出水。
⑥该实验是利用原油中各成分不同,分馏出各
种产品。
向锥形瓶里得到的各馏分中加入溴水,现象
是。
⑦。