烷烯炔性质小结
- 格式:ppt
- 大小:796.00 KB
- 文档页数:40

烷烯炔的结构与性质烷烯炔是有机化合物中常见的一类化合物,它们在化学反应和应用中具有重要的地位。
本文将对烷烯炔的结构与性质进行探讨。
一、烷烯炔的结构烷烯炔由碳、氢原子组成,其中碳原子形成链状结构,并与氢原子通过共价键相连。
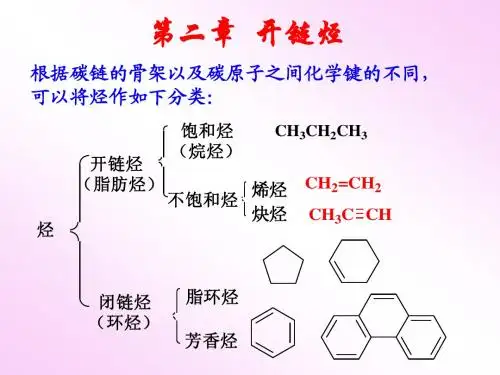
烷烯炔分为烷烃、烯烃和炔烃三类。
烷烃中的碳原子之间通过单键相连,无不饱和键;烯烃中有一个或多个双键,其中一个碳原子与另一个碳原子之间通过一个双键相连;炔烃中有一个或多个三键,其中一个碳原子与另一个碳原子之间通过一个三键相连。
二、烷烯炔的性质1. 物理性质烷烯炔的物理性质与其分子结构有关。
一般来说,烷烯炔在常温常压下为无色气体或液体,呈无色透明状。
烷烯炔的沸点较低,挥发性强。
2. 化学性质烷烯炔的化学性质较为活泼,容易发生反应。
以下是烷烯炔常见的化学反应及其性质。
(1)加成反应:烷烯炔与其他化合物中较活泼的原子或原团发生加成反应,生成新的有机化合物。
这类反应常见的有氢化、卤化等。
例如,炔烃可以与氯气反应生成取代的炔烃。
(2)氧化反应:烷烯炔在强氧化剂的作用下可以发生氧化反应,生成醛、酮、羧酸等有机化合物。
例如,丙炔经过氧化反应可以生成丙酮。
(3)聚合反应:烯烃和炔烃可以发生聚合反应,生成高分子化合物。
例如,乙烯可以聚合成聚乙烯等。
三、烷烯炔的应用烷烯炔在化学工业中具有广泛的应用。
以下是烷烯炔的几个应用领域。
1. 燃料和能源烷烯炔在燃料领域有重要的作用。
例如,烯烃被用作高效燃料,如乙烯可以用于制造乙烯燃料。
2. 合成材料烷烯炔可以用于合成各种高分子材料,如聚乙烯、聚丙烯、聚丁烯等。
这些材料在塑料、纤维和橡胶等领域中具有广泛的应用。
3. 医药领域烷烯炔在医药领域中也有重要的应用。
一些炔烃化合物被用作医药中间体,如乙炔酸可以用于合成某些药物。
4. 农药和化肥烷烯炔可以用于制造农药和化肥,如丙炔可以用于制造杀菌剂。
5. 光电材料烯烃和炔烃可以用于合成光电材料,如聚苯乙烯可以用于制造光纤。
综上所述,烷烯炔是一类重要的有机化合物,具有丰富的结构和多样的化学性质。
![烷烃烯烃炔烃知识点总结[汇编]](https://uimg.taocdn.com/c9abe9b86aec0975f46527d3240c844768eaa046.webp)
烷烃烯烃炔烃知识点总结[汇编]
烷烃是一类无色透明的液体,具有比油脂低的沸点和闪点,在通常情况下容易挥发、燃烧和溶于水。
它具有较高的稳定性和抗氧化能力,可以被广泛应用于日常用品及化工工业等领域。
由于烷烃具有良好的抗氧化性,它们能够稳定金属和金属材料,可起到防腐作用。
此外,烷烃还可用于油类加分子量的改变,从而改变油的特性;或者将烷烃作为油的添加剂用于改善油的品质,例如可以增加油的抗氧化能力和抗老化性能。
此外,烷烃还可用于生产石油冷浸油、乳化油、乳液和乳剂等制品。
烷烃还可以被用作催化剂,促进化学反应,从而产生大量的中间体用于化学制品的生产。
它也可用于生产合成橡胶、橡塑树脂和合成染料等,并可用作溶剂或半溶剂。
烯烃是一类分子结构相对简单的化合物,通常具有低沸点和低闪点,具有良好的抗污染性、抗氧化性和抗老化性,非常适合作为有机溶剂。
烯烃可以作为汽油、石油化学及农业作业的基础溶剂或添加剂,常被作为合成染料的原料,可用于制备汽车、航空油和机油等,甚至作为煤炭液化剂。
此外,烯烃还可用来生产涂料、油漆和日用化学品,可增加涂料的硬度和耐候性。
综上所述,烷烃和烯烃都是重要的有机化合物,同时也都具有较好的抗氧化性和耐腐蚀性。
烷烃和烯烃的特点决定着它们有许多应用,包括工业、农业、消费者品等。
在高温情况下,烷烃和烯烃的分子结构也会发生一些变化,从而影响最终的产品性能。
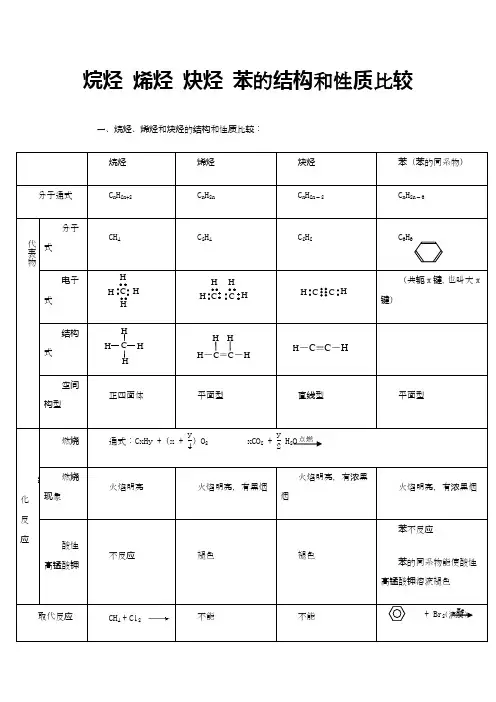

烷烯炔知识点总结烷烯炔的命名和结构烷烯炔的命名符合有机化学的一般命名规则,烷烯的命名以根据含有双键的个数来决定,烷烯中双键的位置通过编号来表示。
比如,乙烯是一种两碳的烯烃,丙烯则是一种三碳的烯烃。
炔的命名也是类似的,炔的命名以含有三键的个数来决定,炔中三键的位置通过编号来表示。
比如,丙炔是一种三碳的炔,戊炔则是一种四碳的炔。
烷烯炔的结构也符合共价键的结构,烷烯中的双键是通过sp2杂化的碳原子构成的,炔中的三键是通过sp杂化的碳原子构成的。
这些结构决定了烷烯炔的一些化学特性,比如稳定性和反应性等。
烷烯的化学性质烷烯是含有双键的碳氢化合物,在化学性质上有着一些特点。
在工业上,很多烷烯的制备都是通过烷烃的脱氢来实现的。
烷烯可以参与一系列的加成反应,比如加氢反应、卤素化反应、水化反应等。
烷烯还可以进行脱氢反应,生成烷烯或芳烃。
除此之外,烷烯还可以通过重排反应和氧化反应来合成其他化合物。
炔的化学性质炔是含有三键的碳氢化合物,在化学性质上也有着一些特点。
炔的三键是可以被氢化的,生成烯烃或烃。
在工业上,炔可以参与一系列的加成反应,比如加氢反应、卤素化反应、水化反应等。
炔还可以与金属形成金属炔配合物,这些金属炔配合物在有机合成中有着重要的应用。
烷烯炔的化学反应烷烯和炔在化学反应中都可以参与一系列的加成反应。
双键和三键的位置和数量会决定其反应性,比如双键或三键的位置对于反应的位置选择性和立体选择性有着重要的影响。
比如烯烃可以进行选择性的氢化反应,生成烷烃或烯烃,而炔可以进行选择性的水化反应,生成醛或酮。
烷烯炔的制备烷烯和炔可以通过多种方法进行制备。
对于烷烯来说,很多烷烃可以通过脱氢反应来得到,比如乙烷可以通过蒸汽裂化或热裂化得到乙烯。
而对于炔来说,也可以通过脱氢反应或氢化反应来得到,比如氯乙炔可以通过钠和乙烯的氢化反应来得到。
烷烯炔的应用烷烯和炔在工业上有着广泛的应用。
烷烯可以用来合成高级燃料,比如乙烯可以用来合成乙烯聚合物,还可以用来生产乙醛、乙醇和醋酸等化工产品。

烃和卤代烃知识点总结在上课的时候,总是会有些知识点是需要我们记住的,记不住怎么办呢?下面,小编为大家分享烃和卤代烃知识点总结,希望对大家有所帮助!烷烃、烯烃和炔烃1.概念及通式(1)烷烃:分子中碳原子之间以单键结合成链状,碳原子剩余的价键全部跟氢原子结合的饱和烃,其通式为:cnh2n+2(n≥l)。
(2)烯烃:分子里含有碳碳双键的不饱和链烃,分子通式为:cnh2n(n≥2)。
(3)炔烃:分子里含有碳碳三键的一类脂肪烃,分子通式为:cnh2n-2(n≥2)。
2.物理性质(1)状态:常温下含有1~4个碳原子的烃为气态烃,随碳原子数的增多,逐渐过渡到液态、固态。
(2)沸点:①随着碳原子数的增多,沸点逐渐升高。
②同分异构体之间,支链越多,沸点越低。
(3)相对密度:随着碳原子数的增多,相对密度逐渐增大,密度均比水的小。
(4)在水中的溶解性:均难溶于水。
3.化学性质(1)均易燃烧,燃烧的化学反应通式为:化学(2)烷烃难被酸性kmno4溶液等氧化剂氧化,在光照条件下易和卤素单质发生取代反应。
(3)烯烃和炔烃易被酸性kmno4溶液等氧化剂氧化,易发生加成反应和加聚反应。
几类重要烃的代表物比较1.结构特点2、化学性质(1)甲烷化学性质相当稳定,跟强酸、强碱或强氧化剂(如kmno4)等一般不起反应。
①氧化反应甲烷在空气中安静的燃烧,火焰的颜色为淡蓝色。
其燃烧热为890kj/mol,则燃烧的热化学方程式为:ch4(g)+2o2(g)化学co2(g)+2h2o(l);△h=-890kj/mol②取代反应:有机物物分子里的某些原子或原子团被其他原子或原子团所替代的反应。
甲烷与氯气的取代反应分四步进行:第一步:ch4+cl2化学ch3cl+hcl第二步:ch3cl+cl2化学ch2cl2+hcl第三步:ch2cl2+cl2化学chcl3+hcl第四步:chcl3+cl2化学ccl4+hcl甲烷的四种氯代物均难溶于水,常温下,只有ch3cl是气态,其余均为液态,chcl3俗称氯仿,ccl4又叫四氯化碳,是重要的有机溶剂,密度比水大。




烷烃烯烃炔烃列表总结烷烃、烯烃、炔烃是有机化合物中的三类常见烃类化合物。
它们在化学结构和性质上有很大的差异。
本文将对烷烃、烯烃、炔烃进行总结和分类,以便更好地理解它们的特性和应用。
烷烃烷烃是由碳和氢原子组成的无环烷烃化合物。
它们的分子结构是直链、支链或环状的。
烷烃通常具有以下特点:•烷烃分子中的碳原子与四个不同的氢原子相连,形成一个完全饱和的碳骨架。
•烷烃中的碳原子通过单键连接(σ键)。
•烷烃的命名规则是根据碳原子数目和其排列方式来命名的。
•烷烃具有较低的反应活性,不易与其他物质发生化学反应。
•烷烃在石油和天然气中广泛存在,是燃料和石化工业的重要原料。
常见的烷烃包括甲烷、乙烷、丙烷等,它们的分子结构和命名规则如下:分子式分子结构常用名称CH4 H—C—H 甲烷C2H6 H—C—C—H 乙烷C3H8 H—C—C—C—H 丙烷………烯烃烯烃是含有碳-碳双键(C=C)的烃类化合物。
它们的分子结构是直链或环状的。
烯烃通常具有以下特点:•烯烃分子中至少有一个碳原子与其他碳原子通过双键连接(π键)。
•烯烃的碳原子仍然与两个氢原子相连,形成一个不饱和的碳骨架。
•烯烃的命名规则是根据碳原子数目、双键位置和其排列方式来命名的。
•烯烃比烷烃具有更高的反应活性,容易进行加成反应、聚合反应等。
常见的烯烃包括乙烯、丙烯、戊烯等,它们的分子结构和命名规则如下:分子式分子结构常用名称C2H4 H2C=C=CH2 乙烯C3H6 CH2=CH—CH3 丙烯C5H10 CH2=CH—CH2—CH2—CH3 戊烯………炔烃炔烃是含有碳-碳三键(C≡C)的烃类化合物。
它们的分子结构是直链或环状的。
炔烃通常具有以下特点:•炔烃分子中至少有一个碳原子与其他碳原子通过三键连接(π键)。
•炔烃的碳原子仍然与一个氢原子相连,形成一个不饱和的碳骨架。
•炔烃的命名规则是根据碳原子数目、三键位置和其排列方式来命名的。
•炔烃比烷烃和烯烃具有更高的反应活性,容易进行加成反应、聚合反应等。

烷烃、烯烃、炔烃的结构与性质.docx烷烃、烯烃、炔烃的结构与性质1.烷烃、烯烃、炔烃的组成、结构特点和通式2.脂肪烃的物理性质性质变化规律常温下含有1~ 4 个碳原子的烃都是气态,随着碳原子数的增多,逐渐过渡到液状态态、固态沸点相对密度水溶性随着碳原子数的增多,沸点逐渐升高;同分异构体之间,支链越多,沸点越低随着碳原子数的增多,相对密度逐渐增大,密度均比水小均难溶于水3.脂肪烃的化学性质(1)烷烃的取代反应①取代反应:有机物分子中某些原子或原子团被其他原子或原子团所替代的反应。
②烷烃的卤代反应a.反应条件:气态烷烃与气态卤素单质在光照下反应。
b.产物成分:多种卤代烃混合物(非纯净物 )+ HX 。
c.定量关系:~Cl2~HCl即取代 1 mol氢原子,消耗1_mol卤素单质生成1 mol HCl 。
(2)烯烃、炔烃的加成反应①加成反应:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。
②烯烃、炔烃的加成反应(写出有关反应的化学方程式)(3)加聚反应①丙烯加聚反应的化学方程式为催化剂nCH2==CH—CH 3――→。
催化剂②乙炔加聚反应的化学方程式为nCH≡ CH――→CH===CH。
(4)二烯烃的加成反应和加聚反应①加成反应催化剂②加聚反应:nCH 2 ==CH—CH==CH 2――→CH 2— CH==CH — CH 2。
(5)脂肪烃的氧化反应烷烃烯烃炔烃燃烧现象燃烧火焰较明亮燃烧火焰明亮,带黑烟燃烧火焰很明亮,带浓黑烟通入酸性不褪色褪色褪色KMnO 4溶液(1)符合通式C n H 2n+2的烃一定是烷烃(√ )(2)丙烷分子中的碳原子在同一条直线上(× )(3)乙烯和乙炔可用酸性KMnO 4溶液鉴别(× )(4)聚丙烯可发生加成反应(× )(5)烷烃同分异构体之间,支链越多,沸点越高(× )(6)顺 -2-丁烯和反 -2-丁烯均能使溴水褪色(√ )(7)CH 2==CHCH==CH 2与 Br 2发生加成反应可生成Br — CH 2CH==CHCH 2— Br 和2种物质(× )1.烃反应类型判断(1)CH 3CH==CH 2+________―→,反应类型:____________。
炔烃的性质总结炔烃是一类具有炔基(C≡C)的有机化合物。
由于炔基的存在,炔烃表现出一系列独特的性质。
本文将就炔烃的物理性质、化学性质以及一些重要的反应进行总结。
一、物理性质1.密度:炔烃的密度一般较小,且随碳链长度的增加而增大。
2.沸点和熔点:炔烃的沸点和熔点通常较低,随着碳链长度的增加,沸点和熔点逐渐升高。
3.溶解性:炔烃在水中极不溶解,但可溶于一些有机溶剂,比如乙醇、丙酮等。
二、化学性质炔烃具有较强的活性,容易参与各种化学反应。
1. 氧化反应炔烃可参与氧化反应,例如与氧气反应生成二氧化碳和水,反应通常是放热的。
C2H2 + 2.5O2 → 2CO2 + H2O ΔH = -1299.5 kJ/mol2. 加成反应炔烃的碳碳三键可以发生加成反应。
典型的例子是炔烃与氢气的加成反应,生成烯烃。
C2H2 + H2 → C2H4此外,炔烃还可以与卤素(如氯、溴)、氢卤酸(如盐酸、氢溴酸)等发生加成反应。
3. 氢化反应炔烃可以与氢气发生氢化反应,生成饱和烃。
C2H2 + 2H2 → C2H64. 炔烃的重要反应4.1 叠氮化反应炔烃可以与叠氮化物(如次氯酸钠)反应,生成底物中炔基上的氢被叠氮基取代的产物。
C2H2 + NaNO2 + HCl → C2H2N2Cl + NaCl + H2O4.2 重排反应炔烃在一定条件下可以发生重排反应,生成不同构的同分异构体。
4.3 氯化反应炔烃可以与氯气发生氯化反应,生成相应的氯代烃。
C2H2 + Cl2 → C2H2Cl24.4 烷化反应炔烃与醇或醛反应,可以发生烷化反应,生成相应的饱和化合物。
C2H2 + CH3OH → C2H2H4O5. 炔烃聚合反应炔烃可以发生聚合反应,生成具有碳碳双键的高分子化合物。
2C2H2 → (C2H2)n (n表示聚合度)三、结语炔烃的性质主要由其炔基决定,具有一系列特殊的物理性质和化学性质。
通过了解炔烃的性质,有助于我们更好地理解和应用这类重要的有机化合物。
烷烃烯烃炔烃知识点总结烷烃、烯烃和炔烃都是有机化合物中的一类,它们的分子结构不同,因而具有不同的性质和用途。
以下是对这三类化合物的详细总结。
一、烷烃1.定义烷烃是由碳和氢组成的有机化合物,其分子中只含有单键,没有双键或三键。
2.分类根据碳原子数目不同,可以将烷烃分为甲烷、乙烷、丙烷等。
根据分子结构不同,可以将其分为链式、支链式、环式等。
3.性质(1)无色无味,易挥发。
(2)不溶于水,在非极性溶剂中可溶。
(3)稳定性高,在常温下不易发生反应。
4.应用(1)作为化学反应中的溶剂和催化剂。
(2)作为能源来源,如天然气和液化气。
二、烯烃1.定义烯烃是由碳和氢组成的有机化合物,其分子中含有一个或多个双键。
2.分类根据双键位置不同,可以将其分为顺式异构体和反式异构体。
根据链状结构不同,可以将其分为直链烯烃和支链烯烃。
3.性质(1)易发生加成反应,如与氢气加成生成烷基化合物。
(2)容易被氧化,如与空气中的氧气接触会发生自由基反应。
4.应用(1)作为溶剂、催化剂和原料。
(2)制备聚合物,如聚乙烯、聚丙烯等。
三、炔烃1.定义炔烃是由碳和氢组成的有机化合物,其分子中含有一个或多个三键。
2.分类根据三键位置不同,可以将其分为内炔和外炔。
根据链式结构不同,可以将其分为直链炔和支链炔。
3.性质(1)容易发生加成反应,如与卤素加成生成卤代化合物。
(2)容易被氧化,并在高温下易爆。
4.应用(1)作为溶剂、催化剂和原料。
(2)制备聚合物,如聚乙炔等。
总结:以上是对于有机化合物中的三类化合物——烷烃、烯烃和炔烃的详细总结。
它们在分子结构、性质和应用等方面都有所不同,但都具有广泛的应用价值。
对于有机化学的学习和实践,这些知识点是必须掌握的。
高三有机烷烯炔知识点总结有机化学是高中化学中的重要分支,而有机烷烯炔是其中的一类有机化合物。
本文将对高三有机烷烯炔知识点进行总结,以帮助同学们更好地理解和掌握这一部分知识。
一、有机烷烯炔的基本概念有机烷烯炔是由碳和氢构成的有机化合物,分为烷、烯和炔三类。
其中,烷是碳原子通过单键连接而形成的链状结构;烯是碳原子通过双键连接而形成的链状结构;炔是碳原子通过三键连接而形成的链状结构。
二、烷的命名和性质烷的命名按照碳原子数目进行命名,以及碳原子间的连接方式。
烷的性质主要取决于其分子量和分子结构。
一般来说,烷是饱和的,不容易发生化学反应,且在常温下大部分为气体或液体。
三、烯的命名和性质烯的命名按照碳原子数目进行命名,以及双键的位置。
烯的性质与烷相比更为活泼,容易发生加成反应、与酸性物质反应等。
烯多为液态或固态,其中较低碳数的烯可以是气体。
四、炔的命名和性质炔的命名按照碳原子数目进行命名,以及三键的位置。
炔的性质较为活泼,容易发生加成反应、与酸性物质反应等。
大部分炔为气体,少数碳数较高的炔为液态或固态。
五、有机合成反应有机烷烯炔能够通过多种合成反应得到。
常见的有机合成反应包括取代反应、加成反应和消除反应等。
其中,取代反应是指原有的官能团被其他官能团取代的反应;加成反应是指不同物质通过共有键形成新的化学键的反应;消除反应是指分子内某个官能团与另一个官能团失去原子(通常是氢)形成化学键的反应。
六、有机烷烯炔的应用有机烷烯炔在化学工业、医药领域等具有广泛的应用。
烷类化合物可用作溶剂、燃料等;烯类化合物可用作合成橡胶、塑料、染料等;炔类化合物可用于合成橡胶、润滑剂等。
七、有机烷烯炔的环境影响和安全注意事项有机化合物的排放和应用对环境有一定的影响,其中有机烷烯炔尤其需要注意。
排放燃烧产物中含有大量的氧化物和碳氢化合物,对空气质量和人体健康有潜在危害。
在使用和储存有机烷烯炔化合物时,需要注意安全操作,避免接触皮肤、吸入有害气体等。
口诀法记有机知识在新课程理念下,如何让学生学好有机化学知识?让学生在题海战术、死记硬背中解放出来。
有机知识是中学化学的重点之一,也是考试热点之一,但由于种类繁多、概念杂、各类物质性质的差异,以及前面学习无机化学对学生思维的影响;要快速而准确的掌握有机知识也不是一件容易的事,为了让学生尽快掌握有机化学,喜欢有机化学。
本文将烃类相关知识编成顺口溜,供广大师生参阅:一:烃类性质归纳:有机化学中心碳,必须形成四个键,单双三键均可连,形成长链或碳环,同分异构性质变,种类多达几千万;学好有机也不难,结构基团是关键,只有碳氢叫做烃,有氧可能是酸醇,醛酮苯酚要分清,醚类酯类记在心;烃类包括烷烯炔,单双三键是区别,另外还有芳香烃,好似单双相间行(1)。
甲烷性质就三招,分解取代和燃烧,取代条件是光照,二一取代最为妙(2);分解高温需加热,产物氢气和碳黑,高锰酸钾不褪色,一氯取代是气体,三四取代作溶剂,四种取代皆不溶,三四取代比水重(3)。
烷中甲烷是代表,其它烷烃性质套,化学性质多不变,物理性质需细看,状态熔沸和密度,主要取决碳个数,状态气体要记全,甲乙丙丁新戊烷;丙烷熔点为最低,甲乙位置要更替,沸点密度渐攀高(4),特殊丙烷需记好,烷烃密度比水轻,与水混合要分层;式子相同结构异(5),互为同分异构体;同分异构要写全:最长碳链做主链,找出中心对称线,主链由长渐变短,支链先整后分散,位置由心再到边,支链排布邻对间;同碳烷烃支链多,熔沸密度走下坡(6),结构写完看命名,系统命名记在心;最长碳链做主链,甲乙丙丁称某烷,编写号码定支链,简单基团写在前,位置基团连短线,相同基团用二三。
加成多为烯和炔,氧化燃烧少不得(7),高锰酸钾和溴液,烯炔使其变颜色;多加氢卤卤化氢(8),产物烷或卤代烃,乙烯加水加催化,所得产物叫酒精;简单芳烃当是苯,物理性质需记清;无色有味也有毒,沸点低且水上浮,五点五度下凝固,合成纤维和胶塑,农药医药香染料,工业农业皆需要,卤素用它来萃取,必是一种有机剂,苯的结构最美观,碳键介与单双间,化学性质要记牢,加成取代和燃烧,相关反应较为难,高锰酸钾色不变;反应多需催化剂,条件产物要仔细,液溴取代铁催化,产物溴苯密度大;硝化硝酸不能少,硫酸作用要记牢,硫酸吸水催化剂,药品添加有顺序,反应温度要求高(9),水浴加热为最好,无色油状硝基苯,与水混合水上层(10),性质有毒味也苦(11),制取苯胺是用途;硫酸磺化苯磺酸,催化加氢环己烷;苯环若和甲基连,相互影响性质变,高锰酸钾要褪色,甲基氧化成羧酸,苯环取代更容易,二四六位硝基替;烈性炸药梯恩梯,国防开矿和水利。
烃甲烷:烃:分子中仅由的化合物,也称作。
1、甲烷分子结构:电子式、结构式、甲烷分子为构型。
2、甲烷的物理性质:甲烷是一种色, 气味气体,密度比空气 , 溶于水,故收集甲烷的方法为或3、甲烷的化学性质:(1)氧化反应:甲烷的燃烧方程式:,火焰呈色。
甲烷与强酸、强碱、强氧化剂均不反应,甲烷通入酸性高锰酸钾溶液后的现象为。
(2)甲烷的取代反应:在量筒中将CH4与Cl2混合,倒置于水槽中,光照,现象为,发生的二元取代反应方程式为:,生成的有机产物中常温下为气体的是,可作为灭火剂的是。
取代反应定义:。
(3)高温分解:。
(制炭黑)【巩固练习】1、下列物质在一定条件下可与CH4发生化学反应的是()A.氯气B.溴水C.氧气D.KMnO4溶液2、“西气东输”工程,即从新疆开发天然气,贯穿东西多省市一直引至上海。
关于天然气的下列叙述中,不正确...的是()A.天然气和沼气主要成分都是甲烷B.天然气和空气混合点燃时不会发生爆炸C.在天然气燃烧的废气中,SO2等污染物的含量少D.液化石油气含碳量高于天然气的含碳量烷烃:1、烷烃(饱和链烃):;同系物:;同系物特点:⑴结构,⑵组成。
2、烷烃的通式。
3、烷烃的物理性质随着分子中碳原子数的递增呈现规律性的变化。
通常状况下,~个碳的烃为液态;烷烃的沸点随着碳原子数的增多逐渐,相对密度逐渐。
4、烷烃的通性:(1)、烷烃的化学性质与CH4相似。
一般情况很稳定,与酸、碱及氧化剂(如酸性高锰酸钾)都不起反应。
但在一定条件下也能发生下列反应:反应、反应、反应。
(2)烷烃燃烧的通式:。
5、同分异构现:;同分异构体:。
比较熔、沸点:正戊烷异戊烷新戊烷正丁烷6、烃基:。
书写甲基结构简式,电子式;乙基结构简式,电子式;CH3- 的电子式; CH3+ 的电子式;7、烷烃的命名:(1)习惯法(俗称):碳原子数1—10分别用:甲、乙、丙、丁、戊、己、、、、表示,10个碳原子以上用中文小写数字表示。
(2)系统命名法:{要义:①“最长”;②“最近”;③“最小”;④“最简”}例如: 命名为: 。