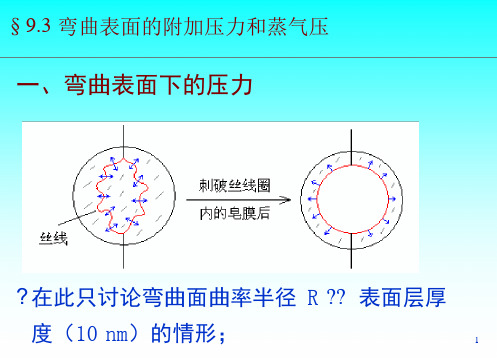
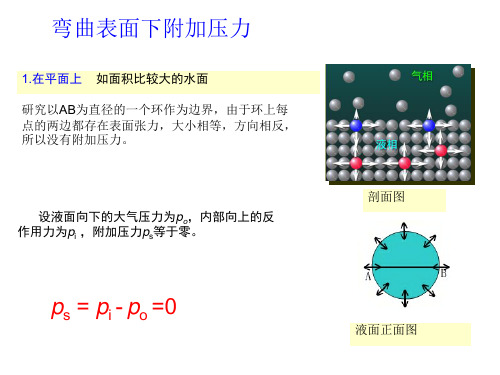
(1) 过饱和蒸气: 按相平衡条件应当凝 p 结而未凝结的蒸气. 原因是蒸气不能 变成化学势更高的微小液滴.
过饱和蒸气的压力超过了相应温 度下通常体积液体的饱和蒸气压, 但 仍小于该液体微小液滴的饱和蒸气压 (见图示). 引入凝结中心可使液滴核心易于生 成, 减轻过饱和程度(如人工降雨).
过饱和蒸气的产生 4 g
在过冷液体中投入小 晶体作为新相的种子, 能使 液体迅速凝固.
气相区
T′ f Tf
T
6
过冷液体的产生
亚稳状态及新相的生成
(4) 过饱和溶液: 在一定温度下, 浓度超过饱和浓度, 而仍未析 出晶体的溶液. 原因是微小晶粒具有高表面吉布斯函数(高的 饱和蒸气压)而不能在正常饱和浓度下析出.
与微小液滴一样, 微小晶体的 饱和蒸气压大于普通晶体. 蒸气压 与溶解度有密切的关系, 微小晶粒 具有比普通晶体更大的溶解度. 晶 体的颗粒愈小, 溶解度愈大. (见图) 可知, 当溶液浓度达到普通晶 体的饱和浓度时, 相对于微小晶粒 还未饱和, 微小晶粒就不能从中析 出.
p2 (g ) Vm (l ){ p2 (l ) p1 (l )} ln = p1 (g ) RT (Vm = M / ρ )
用 p 和 pr 分别表示平面液体和微小液滴的蒸气压, 结合 拉普拉斯方程, 得 小液滴 3
Pr / p
pr 2γ M 开尔文公式: RT ln = p ρr
2 1 平面液体
式中液面曲率半径 r1 与毛细管半径 r 及接 触角 θ 间的关系为:
r1 r
θ
θ
h
cosθ = r / r1
2 γ cos θ h= rρ g
γ : 液体表面张力; ρ: 液体密度;
g : 重力加速度.