铝三角专题
- 格式:ppt
- 大小:387.00 KB
- 文档页数:111


专题12突破铝三角的图像和计算提升练习高考化学一轮复习微专题一、单选题,共13小题1.(2022·浙江·金华市曙光学校模拟预测)下列反应的方程式不正确...的是 A .石灰石与醋酸反应:CO 23-+2CH 3COOH=2CH 3COO - +CO 2↑+H 2OB .铜片上电镀银的总反应(银作阳极,硝酸银溶液作电镀液):Ag(阳极)通电Ag(阴极)C .铜与稀硝酸反应:3Cu+2NO 3-+8H +=3Cu 2+ +2NO↑+4H 2OD .明矾溶液中加入少量氢氧化钡溶液:2Al 3+ +3SO 24-+ 3Ba 2++6OH -=2Al(OH)3↓+ 3BaSO 4↓2.(模拟)下列物质之间通过一步反应不能实现如图所示转化的是(部分反应中的2H O 已略去)选项 WX Y Z A2OCCO2COB 2CONaOH23Na CO3Na HCOCNaOH 3AlCl()3Al OH2NaAlOD 2Cl Fe2FeCl3FeClA .AB .BC .CD .D3.(2022·陕西·汉中市龙岗学校高三阶段练习)下列实验对应的离子方程式正确的是A .氢氧化钠溶液中滴入少量硫酸铝溶液:333OH Al Al(OH)-++=↓B .硫化钠溶液中通入过量2222SO :2S SO 2H O 3S 4OH --++=↓+C .次氯酸钙溶液中通入少量的2223CO :ClO H O CO HCO HClO --++=+D .水杨酸溶液中加入足量的碳酸氢钠溶液:+ HCO -3−−→+CO 2↑+H 2O4.(模拟)能正确表示下列变化的离子方程式是A .向次氯酸钙中通入过量的二氧化碳气体:Ca 2++2ClO -+CO 2+H 2O=2HClO+CaCO 3↓B .向硝酸铝溶液中滴加足量氢氧化钡溶液:Al 3+ +4OH -=AlO 2-+2H 2OC .向氯化铜溶液中通入硫化氢气体:S 2- +Cu 2+= CuS↓D .碳酸镁与稀硫酸反应:CO 23-+2H +=CO 2↑+H 2O5.(模拟)为探究Al 2(SO 4)3溶液与Ba(OH)2溶液的反应,取0.1mol·L -1的溶液进行如下实验:下列分析错误的是A .试管1中,当硫酸根离子恰好完全沉淀时,沉淀的质量最大B .试管2中,当钡离子恰好完全沉淀时,铝元素也完全转变为沉淀C .试管l 、2中,沉淀均会先增多后减少D .试管l 、2中,沉淀均含BaSO 46.(模拟)铵明矾()4422NH Al SO 12H O ⎡⎤⋅⎣⎦常用于发酵粉加工、油炸食品、粉条加工等食品工业,其实验室制备流程如图所示,已知:铵明矾的溶解度随温度升高明显增大。

重难点九 铝的化合物之间的相互转化----“铝三角”【要点解读】 1.Al 3+―→Al(OH)3(1)可溶性铝盐与少量NaOH 溶液反应: (2)可溶性铝盐与氨水反应:2.Al(OH)3―→Al 3+:Al(OH)3溶于强酸溶液: 3.Al 3+―→AlO 2-:可溶性铝盐与过量的强碱反应: 4.AlO 2-―→Al 3+:偏铝酸盐溶液与足量的盐酸反应: 5.AlO 2-―→Al(OH)3:偏铝酸钠溶液中加入少量盐酸: 6.Al(OH)3―→ AlO 2- :Al(OH)3溶于强碱溶液: 【温馨提示】三种物质相互转化注意反应条件,特别是Al(OH)3既能溶于强酸,又能溶于强碱。
【特别提醒】 1.两性化合物的概念指既能与酸反应,又能与碱反应的化合物。
与酸或碱反应生成的产物是盐和水的化合物才是两性化合物。
弱酸的铵盐、弱酸的酸式盐不属于两性化合物。
2.Al(OH)3的三种制备方法(1)用铝盐和氨水制备Al(OH)3,不选用强碱(如NaOH)溶液,是由于Al(OH)3溶于强碱溶液,而不溶于弱碱(如氨水)溶液。
(2)溶液中AlO 2-→Al(OH)3最好通入CO 2,而不是选用强酸,因为氢氧化铝溶于强酸,而不溶于较弱的酸。
3.常见的既能与酸反应又能与碱反应的物质 (1)金属单质:Al 等; (2)两性氧化物:Al 2O 3等; (3)两性氢氧化物:Al(OH)3 等;(4)弱酸的铵盐:(NH 4)2CO 3、CH 3COONH 4、(NH 4)2S 等; (5)弱酸的酸式盐:NaHCO 3、KHS 、NaHSO 3等。
【重难点指数】★★★★【重难点考向一】氢氧化铝的制取和性质探究【例1】实验室制取氢氧化铝的最佳方案是( )A.Al+H2O B.Al2O3+H2O C.AlCl3+NaOH D.Al2(SO4)3+NH3•H2O【重难点考向二】铝及其化合物性质探究【例2】某同学通过系统实验探究铝及其化合物的性质,操作正确且能达到目的是( ) A.向氯化铝溶液中滴加过氨水,最终得到澄清溶液B.等质量的铝分别与足量的盐酸和氢氧化钠溶液反应制得等质量的氢气C.常温下铝与浓硝酸反应制得大量的NO2D.AlCl3溶液加热蒸干得到无水氯化铝晶体【重难点考向三】铝三角之间的转化【例3】A、B、C、D、E五种化合物均含有同一种短周期常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E易溶于水.若取A溶液灼烧,焰色反应为紫色(透过蓝色钴玻璃片)(1)写出化学式:A______,B________,C________,D________,E________;(2)写出下列反应的离子方程式:A→B:___________________________________________________;A→D:___________________________________________________。

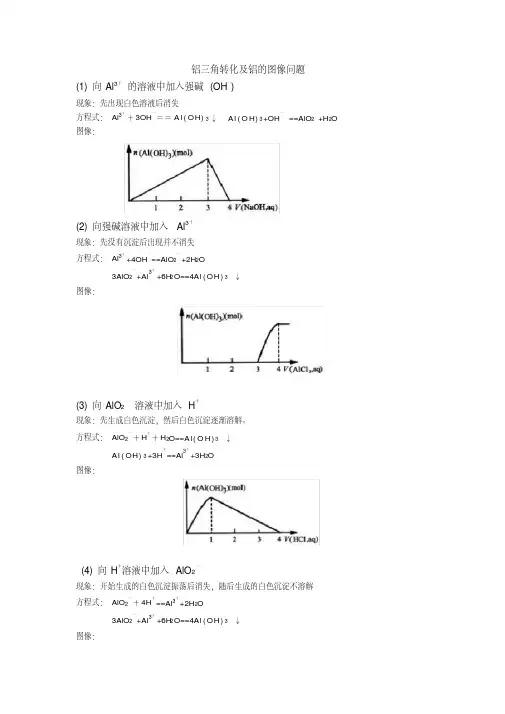
铝三角转化及铝的图像问题(1) 向Al3+的溶液中加入强碱(OH―)现象:先出现白色溶液后消失方程式:Al3++3OH―==A l(OH)3↓A l(O H)3+OH―==AlO2―+H2O 图像:(2) 向强碱溶液中加入Al3+现象:先没有沉淀后出现并不消失方程式:Al3++4OH―==AlO2―+2H2O3AlO2―+Al3++6H2O==4Al(OH)3↓图像:(3) 向AlO2―溶液中加入H+现象:先生成白色沉淀,然后白色沉淀逐渐溶解。
方程式:AlO2―+H++H2O==A l(O H)3↓A l(OH)3+3H+==Al3++3H2O图像:(4) 向H+溶液中加入AlO2―现象:开始生成的白色沉淀振荡后消失,随后生成的白色沉淀不溶解方程式:AlO2―+4H+==Al3++2H2O3AlO2―+Al3++6H2O==4Al(OH)3↓图像:具体应用:例1、有一定质量的Mg、Al 合金投入100 mL一定物质的量浓度的盐酸溶液中,合金全部溶液,向所得溶液中滴加 5 mol/L NaOH溶液到过量,生成沉淀的质量与加入NaOH溶液的体积关系如图所示,求(1) 原合金中Mg、Al的质量各是多少?(2) HCl的浓度是多少?解:(1) 设原合金中Mg的质量为X,Al的质量为yMg -----M g(O H)2Al-----A l(O H)324 58 27 78x 11.6 y 19.4-11.6==7.8x=4.8 g y == 2.7 g(2) 当沉淀达到最大值时,则n(HCl)==n(NaOH)则c(HCl)== 5*160/100= 8 mol/L[点击试题]1、0.1molAl2(SO4)3跟2mol/L NaOH溶液350mL混合,所得沉淀的质量为( )A.78gB.15.6gC.7.8gD.3.9g2.向10mL 0.2mol/L的AlCl3溶液中,逐滴加入未知浓度的Ba(OH)2溶液,测得滴加15mL 和45mL时,所得沉淀同样多,求Ba(OH)2溶液的物质的量浓度。
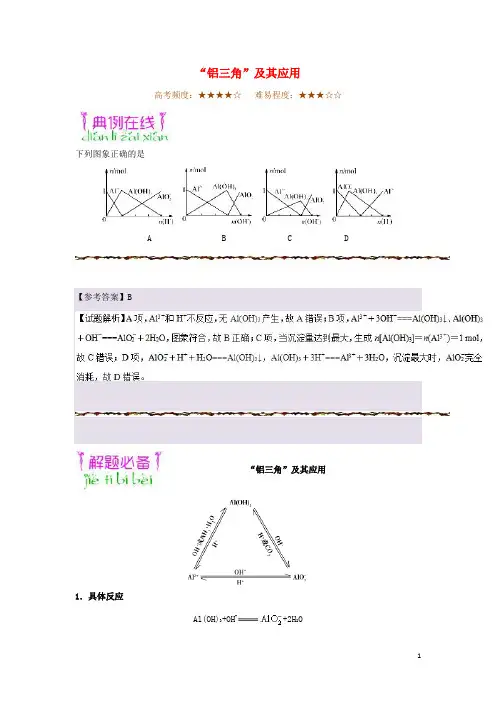
“铝三角”及其应用高考频度:★★★★☆难易程度:★★★☆☆下列图象正确的是A B C D 【参考答案】B“铝三角”及其应用1.具体反应Al(OH)3+OH−+2H2OAl(OH)3+3H+Al3++3H2OAl3++3OH−Al(OH)3↓+H++H 2O Al(OH)3↓+4H+Al3++2H 2OAl3++4OH−+2H 2OAl3++3+6H 2O4Al(OH)3↓2.应用(1)判断离子共存问题Al3+与OH−及、、S2−等弱酸根阴离子或与H+、以及弱碱阳离子Al3+、Fe3+等因生成沉淀或发生水解相互促进反应而不能大量共存。
(2)鉴别(利用滴加顺序不同,现象不同)①向AlCl3溶液中滴加NaOH溶液,先产生白色沉淀,后沉淀溶解。
②向NaOH溶液中滴加AlCl3溶液,开始无明显现象,后产生白色沉淀,沉淀不溶解。
(3)分离提纯①利用Al能溶于强碱溶液,分离Al与其他金属的混合物。
②利用Al2O3,能与强碱溶液反应,分离Al2O3与其他金属氧化物。
③利用Al(OH)3能与强碱溶液反应,分离Al3+与其他金属阳离子。
1.下列除杂质的方法不正确的是A.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥B.FeCl3溶液中混有少量AlCl3:加入过量的氨水,过滤洗涤沉淀,将沉淀再用适量盐酸溶解C.Fe2O3中混有少量Al2O3:加入过量NaOH溶液充分反应,过滤、洗涤、干燥D.Al(OH)3中混有少量Mg(OH)2:加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO2后过滤2.甲、乙、丙三种物质均含有铝元素,在溶液中的转化关系如图所示。
下列说法正确的是A.若甲是Al,丙是Al(NO3)3,则乙一定是NaAlO2B.若甲是Al2O3,丙是NaAlO2,则乙一定是Al(NO3)3C.若甲是Al(NO3)3,丙是NaAlO2,则乙一定是Al(OH)3D.若甲是Al(OH)3,丙是Al(NO3)3,则乙一定是NaAlO23.用下列两种方案制备氢氧化铝:Ⅰ.2.7 g Al X溶液氢氧化铝Ⅱ.2.7 g Al Y溶液氢氧化铝已知所用的稀盐酸与氢氧化钠溶液的浓度均为3 mol·L−1。



实用文档铝及其化合物、铝三角图像问题1、铝(1)物理性质:密度小熔点较低,硬度较小银白色金属。
(3)化学性质:①跟O 2及其它非金属反应:常温下,在空气中因生成氧化膜,具有抗腐蚀能力。
4Al+3O 2−−−→点燃2Al 2O 3 2Al+3S −−−→点燃Al 2S 3 ②跟某些氧化物:2Al+Fe 2O 3−→−∆2Fe+Al 2O 3 (铝热反应) ③跟水反应:2Al+6H 2O → 2Al(OH)3+3H 2↑ (一般不反应,只有氧化膜被破坏后反应)④跟酸的反应:2Al+6H +→ 3Al 3+ + 3H 2↑(常温下,在浓H 2SO 4、浓HNO 3中钝化)⑤跟强碱溶液反应:2Al+2NaOH+2H 2O → 2NaAlO 2+3H 2↑2、Al 2O 3(两性氧化物):白色固体、熔点高(1)跟酸反应:Al 2O 3+6H + →2Al 3++3H 2O (2)跟碱反应:Al 2O 3+2OH -→AlO 2—+2H 2O3、Al(OH)3 (两性氢氧化物)Al(OH)3的两性:Al(OH)3 + 3H + → Al 3+ + 3H 2O Al(OH)3 + OH - → AlO 2- + 2H 2OAl(OH)3显两性的在本质是:H 2O + H + + AlO 2-垐?噲?Al(OH)3垐?噲?Al 3+ + 3OH -(1)物理性质:白色胶状物质,难溶于水(2)受热分解:2Al(OH)3−→−∆ Al 2O 3+3H 2O (3)Al(OH)3实验室制法:①可溶性铝盐加氨水:Al 3++3NH 3·H 2O →Al(OH)3↓+3NH 4+②可溶性偏铝酸盐与弱酸:AlO 2—+ H 2CO 3 +H 2O → Al(OH)3↓+ HCO 3—③ 3AlO 2- +Al 3++6H 2O →4Al(OH)3↓4、铝盐(1)Al 3+与碱溶液反应:Al 3++3OH -→Al(OH)3↓(碱不足)Al 3++4OH -→AlO 2-↓+2H 2O (碱过量)(2)Al 3+水解:Al 3++3H 2O 垐?噲?Al(OH)3+3H +(3)明矾:Kal(SO 4)2•12H 2O 是一种复盐。
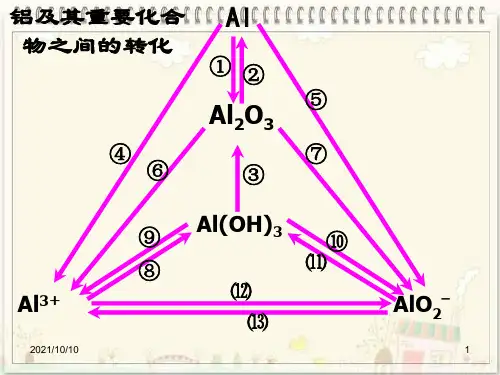
微专题12 铝三角及其转化关系1.Al3+、Al(OH)3、AlO-2之间的转化关系实现上述各步转化的离子方程式:(1)①Al3++3NH3·H2O===Al(OH)3↓+3NH+4②Al3++3AlO-2+6H2O===4Al(OH)3↓③Al3++3OH-===Al(OH)3↓(2)Al(OH)3+3H+===Al3++3H2O(3)Al3++4OH-===AlO-2+2H2O(4)AlO-2+4H+===Al3++2H2O(5)①AlO-2+CO2+2H2O===Al(OH)3↓+HCO-3②AlO-2+H++H2O===Al(OH)3↓(6)Al(OH)3+OH-===AlO-2+2H2O2.与Al(OH)3沉淀生成有关的图象分析(1)可溶性铝盐溶液与NaOH溶液反应的图象(从上述转化关系中选择符合图象变化的离子方程式,下同)。
操作可溶性铝盐溶液中逐滴加入NaOH溶液至过量NaOH溶液中逐滴加入可溶性铝盐溶液至过量现象立即产生白色沉淀→渐多→最多→渐少→消失无沉淀(有但即溶)→出现沉淀→渐多→最多→沉淀不消失图象方程式序号AB:(1)③BD:(6) AB:(3)BC:(1)②(2)偏铝酸盐溶液与盐酸反应的图象。
操作偏铝酸盐溶液中逐滴加入稀盐酸至过量稀盐酸中逐滴加入偏铝酸盐溶液至过量现象立即产生白色沉淀→渐多→最多→渐少→消失无沉淀→出现沉淀→渐多→最多→沉淀不消失图象方程式序号AB:(5)②BC:(2)AB:(4)BC:(1)②3.可溶性铝盐与强碱反应的计算规律(1)求产物Al(OH)3的量①当n (OH -)≤3n (Al 3+)时,n [Al(OH)3]=13n (OH -);②当3n (Al 3+)<n (OH -)<4n (Al 3+)时,n [Al(OH)3]= 4n (Al 3+)-n (OH -);③当n (OH -)≥4n (Al 3+)时,n [Al(OH)3]=0,无沉淀。
高考过关知识点4“铝三角”的转化关系及图像分析命题点1“铝三角”转化与应用1.Al3+、Al(OH)3、[Al(OH)4]-之间的转化关系2.“铝三角”转化的应用(1)判断离子共存问题:Al3+与OH-及[Al(OH)4]-、CO2-3、S2-等弱酸根阴离子;[Al(OH)4]-与H+、HCO-3以及弱碱阳离子Al3+、Fe3+等因生成沉淀或发生水解相互促进反应而不能大量共存。
(2)鉴别(利用滴加顺序不同,现象不同)。
①向AlCl3溶液中滴加NaOH溶液,先产生白色沉淀,后沉淀溶解。
②向NaOH溶液中滴加AlCl3溶液,开始无明显现象,后产生白色沉淀,沉淀不溶解。
[对点训练1](2017·青岛模拟)下列说法不正确的是()A.铝箔插入稀硝酸中,无现象,说明铝箔表面被HNO3氧化,形成致密的氧化膜B. 如右图所示,①中为AlCl3溶液,②中为浓氨水,①中有白色沉淀生成C.Al2O3――→NaOH(aq)△Na[Al(OH)4](aq)――→CO2Al(OH)3D.AlCl3溶液中滴加NaOH溶液后铝的存在形式:A[铝与稀HNO3发生反应有NO生成,不能形成氧化膜,A不正确;浓氨水挥发出的NH3被AlCl3溶液吸收生成白色沉淀Al(OH)3,B正确;Al2O3为两性氧化物与NaOH反应生成Na[Al(OH)4],Na[Al(OH)4]溶液遇CO2生成Al(OH)3,C正确;当n(NaOH)∶n(AlCl3)=3时,恰好生成Al(OH)3,当n(NaOH)∶n(AlCl3)=4时,恰好生成Na[Al(OH)4],D正确。
][对点训练2](2017·西安名校三检)某无色透明溶液与铝反应放出氢气,该溶液中可能含有Mg2+、Cu2+、Ba2+、H+、Ag+、SO2-4、SO2-3、HCO-3、OH-、NO-3十种离子中的若干种,下列推断正确的是()A.当溶液中有Al3+生成时,溶液中可能存在:SO2-4、NO-3、H+、Mg2+B.当溶液中有Al3+生成时,溶液中一定存在:H+、SO2-4;可能存在Mg2+C.当溶液中有[Al(OH)4]-生成时,溶液中一定存在:OH-、Ba2+、NO-3D.当溶液中有[Al(OH)4]-生成时,溶液中可能存在:OH-、Ba2+、NO-3、SO2-3B[据题意,一定不含有Cu2+、HCO-3。
铝是高中化学重要的金属,主要有铝、氧化铝、氢氧化铝。
高考化学中铝的考点主要集中的铝及其化合物的两性,即既可以与酸反应,也可以与碱反应。
铝三角主要体现了铝及其化合物的两性一、单质铝(Al)铝是一种活泼金属,具有金属的共性,能够与非金属、酸、某些盐反应,同时具有自己特有的性质,可以与碱反应。
铝极易失去最外层3个电子形成铝离子:Al -3e -=Al 3+。
1.铝与非金属反应铝可以与大多数非金属单质反应,如氧气、氯气、硫、溴等,生成相应的氧化物或盐。
4Al +3O 2 Δ → 2Al 2O 3;2Al +3S Δ → Al 2S 3;2Al +3Cl 2 点燃→ 2AlCl 3;2.铝与酸反应这里所说的酸,主要指稀硫酸和稀盐酸,常温常压下,铝遇浓硫酸或浓硝酸会发生钝化,所以可用铝制容器盛装浓硫酸或浓硝酸。
注意钝化也属于化学变化。
2Al +6HCl → 2AlCl 3+3H 2↑;2Al +3H 2SO 4 → Al 2(SO 4)3+3H 2↑;3.铝与强碱反应大多数金属不与碱反应,与强碱反应,是铝特有的性质,(锌也可以发生类似的反应,了解即可)2Al +2NaOH +2H 2O → 2NaAlO 2+3H 2↑;该反应的本质是铝首先与水反应,生成氢氧化铝与氢气,2Al+6H2O=2Al(OH)3+3H2↑;然后,氢氧化铝与氢氧化钠反应,2Al(OH)3+2NaOH=2NaAlO2+4H2O。
在整个过程中,水是氧化剂,而氢氧化钠不是氧化剂。
在解答电子转移和电线桥双线桥法的题目中要注意。
4.铝热反应铝热反应是指铝在高温条件下还原金属氧化物,置换金属单质的一种反应,不是特指与铝与氧化铁的反应。
2Al+Fe2O3高温→ 2Fe+Al2O3,铝具有较强的还原性,可以还原一些金属氧化物,如氧化钨,二氧化锰等等。
二、氧化铝(Al2O3)氧化铝熔点较高,硬度较大,可以与酸碱反应。
1.氧化铝与酸反应Al2O3+6HCl→2AlCl3+3H2O;对应离子方程式:Al2O3+6H+→2Al3++3H2O;2.氧化铝与碱反应Al2 O 3+2 N a O H 3.电解氧化铝生成金属铝2Al2O34Al+3O2↑;加入冰晶石可以降低电解温度。