选修四化学反应与能量综合练习题
- 格式:doc
- 大小:254.50 KB
- 文档页数:6

选修4作业(三)第一章化学反应与能量单元测试一、选择题(本题共10小题,每小题只有一个正确选项)1.下列叙述正确的是A.反应的活化能越小,单位时间内有效碰撞越多。
B.反应的活化能越大,单位时间内有效碰撞越多。
C.反应的活化能越小,单位时间内有效碰撞越少。
D.反应的活化能太小,单位时间内几乎无有效碰撞。
2.已知反应X+Y==M+N为放热反应,对该反应的下列说法中正确的是A.X的能量一定高于MB.Y的能量一定高于NC.X和Y的总能量一定高于M和N的总能量D.因该反应为放热反应,故不必加热就可发生3.下列说法错误的是A.热化学方程式各物质前的化学计量数不表示分子个数只代表物质的量B.热化学方程式未注明温度和压强,△H表示标准状况下的数据C.同一化学反应,化学计量数不同,△H值不同,化学计量数相同而状态不同,△H 值也不相同D.化学反应过程所吸收或放出的热量与参加反应的物质的物质的量成正比4.强酸和强碱的稀溶液的中和热可表示为:H+(aq)+OH-(aq)=H2O(1) △H =—57.3kJ/mol 已知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(1) △H =—Q1kJ/mol 1/2 H2SO4(浓) + NaOH(aq) == 1/2Na2SO4(aq) +H2O(1) △H =—Q2kJ/molHNO3(aq)+KOH(aq)=KNO3(aq)+H2O(1) △H =—Q3kJ/mol 上述反应均为溶液中的反应,则Q1、Q2、Q3的大小关系为A.Q1=Q2=Q3B.Q2>Q1>Q3C.Q2>Q3>Q1D.Q2=Q3>Q15.在相同的温度和压强下,将32g硫分别于纯氧中和空气中完全燃烧,令前者的反应热为△H1,后者的反应热为△H2,则关于△H1和△H2的相对大小,正确的判断是A.△H1=△H2B.△H1>△H2C.△H1<△H2D.无法判断6.工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3,已知该反应为一放热反应。

2020-2021学年高二化学人教版选修四第一章化学反应与能量——化学能与热能的应用一.选择题(共15小题)1.下列变化中,一定不存在化学能与热能相互转化的是()A.铝热反应B.金属钝化C.干冰气化D.燃放爆竹2.据研究,若把太阳光变成激光用于分解海水制氢,反应可表示为:2H2OH2↑+O2↑.有下列几种说法:①水分解反应是放热反应;②氢气是可再生能源;③使用氢气作燃料有助于控制温室效应;④若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件。
其中叙述正确的是()A.①②B.③④C.②③④D.①②③④3.伦敦奥运火炬彩用的是环保型燃料﹣﹣丙烷,其燃烧时发生反应的化学方程式为C3H8+5O23CO2+4H2O.下列说法中不正确的是()A.火炬燃烧时化学能只转化为热能B.所有的燃烧反应都会释放热量C.1 mol C3H8和5 mol O2所具有的总能量大于3 mol CO2和4 mol H2O所具有的总能量D.丙烷完全燃烧的产物对环境无污染,故丙烷为环保型燃料4.关于能源的叙述正确的是()A.植物通过光合作用将CO2转化为葡萄糖是太阳能转变为热能的过程B.氢气属于理想的二次能源,可以寻找催化剂使水分解,同时释放能量C.化石燃料属于一次能源,属于不可再生能源,属于来自太阳的能源D.大力开发丰富的煤炭资源,将煤进行气化处理提高煤的利用率,可减少对石油的依赖5.下列措施,能使煤炭燃烧更充分,提高热能利用率的是()A.多加煤以使炉火更旺B.把煤炭做成大煤球C.把煤中掺合一些黄泥做成蜂窝煤D.把煤粉碎,在煤粉燃烧器中燃烧6.下列变化过程中,一定不存在化学能与热能相互转化的是()A.原电池反应B.干冰升华C.粮食酿酒D.节日放鞭炮焰火7.下列措施能使煤炭燃烧最充分,提高热能利用率的是()A.向燃烧正旺的炉火上洒一些水B.把煤炭做成大煤球C.把煤中掺一些黄泥做成蜂窝煤D.把煤粉碎,在煤粉燃烧器中燃烧8.下列说法正确的是()A.分子式为C2H6O的有机化合物性质相同B.相同条件下,等质量的碳按a、b两种途径完全转化,途径a比途径b放出更多热能途径a:CCO+H2CO2+H2O途径b:CCO2C.在氧化还原反应中,还原剂失去电子总数等于氧化剂得到电子的总数D.通过化学变化可以直接将水转变为汽油9.下面是四位同学在学习化学能与热能后产生了一些认识,其中一定正确的是()A.B.C.D.10.化学已经渗透到人类生活的各个方面,下列说法不正确的是()A.户外钢架桥生锈主要是电化学腐蚀所致B.葡萄中的花青素在碱性环境下显蓝色,故可用苏打粉检验假葡萄酒C.导电塑料是应用于电子工业的一种新型有机高分子化合物D.青岛世园会喷雾风扇依据化学能与热能转化原理,会自动喷出清凉水雾11.已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列叙述正确的是()A.每生成2分子AB吸收bkJ热量B.该反应热△H=(b﹣a)kJ•mol﹣1C.反应物的总能量低于生成物的总能量D.断裂1molA﹣A和1molB﹣B键,放出akJ能量12.各种能量可以相互转化.下述能量未必由化学能转化而来的是()A.电解铝所需的电能B.人的体能C.化学电池的电能D.燃油汽车的动能13.下列有关化学变化中的能量关系的说法中,错误的是()A.任何一个化学变化的过程中都包含着能量的变化B.化学变化过程中能量变化的实质就是旧键断裂要吸收能量,新键生成会放出能量C.如果生成物的能量比反应物的能量高,则该反应为放热反应D.如不特别注明,化学反应的反应热就是就是该反应的焓变14.下列变化中,一定不存在化学能与热能相互转化的是()A.酸碱中和B.干冰汽化C.淀粉发酵D.金属钝化15.化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列叙述正确的是()A.每生成2个AB分子放出bkJ热量B.AB(g)A2(g)B2(g)△H(a﹣b)kJ•mol﹣1C.该反应中生成物的总能量低于反应物的总能量D.断裂1mol A2和1mol B2中的化学键,放出akJ能量二.填空题(共1小题)16.(1)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ.则表示甲烷燃烧热的热化学方程式为。

第一章化学反应与能量一、选择题(每小题有1个或2个选项符合题意)1.炽热的炉膛内有反应:C(s)+O2(g)=CO2(g);ΔH=-392 kJ·mol-1,往炉膛内通入水蒸气时,有如下反应:C(s)+H2O(g)=CO(g)+H2(g);ΔH=+131 kJ·mol-1,2CO(g)+O2(g)=2CO2(g);ΔH=-564 kJ·mol-1,2H2(g)+O2(g)=2H2O(g);ΔH=-482 kJ·mol-1,由以上反应推断往炽热的炉膛内通入水蒸气时,() A.不能节约燃料,但能使炉膛火更旺B.虽不能使炉膛火更旺,但可节约燃料C.既可使炉膛火更旺,又能节约燃料D.即不能使炉膛火更旺,又不能节约燃料【解析】将炉膛内通入水蒸气时,对应的第一个方程式中C(s)+H2O(g)=CO(g)+H2(g),ΔH=+131 kJ·mol-1乘以2与第二个、第三个方程式叠加,可得炉膛内C与O2反应的化学方程式:C(s)+O2(g)=CO2(g),ΔH=-392 kJ·mol-1,即能量守恒,不能节约燃料;但将固体燃料转变为气体燃料(CO,H2)显然增大了与O2的接触面积,使炉膛火更旺。
【答案】 A2.A、B、C、D均是短周期元素,当A、B两元素的原子分别得到两个电子形成稳定结构时,A放出的能量大于B放出的能量;当C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量。
若A、B、C、D四种元素间分别形成化合物时,属于离子化合物可能性最大的是() A.C2A B.C2BC.D2A D.D2B【解析】设初始的原子能量趋于相等,由能量守恒关系可得:A、B两元素的原子分别得到两个电子形成稳定的结构时,A放出的能量大于B放出的能量,可知A2-比B2-能量低,即A原子比B原子较易得电子形成稳定的A2-,即A的非金属性比B强;C、D两元素的原子分别失去一个电子形成稳定的结构时,D吸收的能量大于C吸收的能量,即C+的能量比D+低,即C原子更易失去电子显示更强的金属性,则最可能形成离子化合物的是活泼金属C与活泼非金属A形成的化合物C2A。


2020—2021人教化学选修四第1章:化学反应与能量含答案第1章化学反应与能量1、一定条件下,在水溶液中1 mol Cl-、ClO x-(x=1,2,3,4)的能量(kJ)相对大小如图所示。
下列有关说法正确的是()A.a、b、c、d、e中,c最稳定B.b→a+c反应的活化能为反应物能量减生成物能量C.b→a+d反应的热化学方程式为:3ClO-(aq)===ClO3-(aq)+2Cl-(aq)ΔH=+116 kJ·mol-1D.一定温度下,Cl2与NaOH溶液反应生成的产物有a、b、d,溶液中a、b、d的浓度之比可能为11∶1∶22、由N2O和NO反应生成N2和NO2的能量变化如图所示。
下列说法正确的是()A.断键吸收能量之和大于成键释放能量之和B.反应物总能量小于生成物总能量C.N2O(g)+NO(g)===N2(g)+NO2(g)ΔH=-139 kJ·mol-1D.反应生成1 mol N2时转移4 mol电子3、下列说法正确的是()A.风力、化石燃料、天然铀矿都是一次能源B.需要加热才能发生的反应都是吸热反应C.断开1 mol C—H键要放出415 kJ的能量D.燃煤发电是将化学能直接转化为电能4、向Na2CO3溶液中滴加盐酸,反应过程中能量变化如下图所示,下列说法正确的是()A.反应HCO-3(aq)+H+(aq)===CO2(g)+H2O(l)为放热反应B.ΔH1>ΔH2ΔH2<ΔH3C.CO2-3(aq)+2H+(aq)===CO2(g)+H2O(l)ΔH=ΔH1+ΔH2+ΔH3D.H2CO3(aq)===CO2(g)+H2O(l),若使用催化剂,则ΔH3变小5、下列有关热化学方程式正确的是()N2(g)+3H2(g)2NH3(g)ΔH=-2a kJ·mol-16、行为中有悖于这一保证的是()A.开发太阳能、生物质能、风能等新能源,减少使用煤、石油等化石燃料B.研究采煤、采油新技术,提高产量以满足工业生产的快速发展C.在农村推广使用沼气D.减少资源消耗、增加资源的重复使用和资源的循环再生7、化学反应的本质是旧化学键的断裂和新化学键的形成。

《化学反应与能量变化》小练1、已知反应:下列结论正确的是①101kPa时,2C(s)+O2(g)=2CO(g);ΔH=-221kJ/mol②稀溶液中,H+(aq)+OH-(aq)=H2O(l);ΔH=-57.3kJ/molA.碳的燃烧热大于110.5kJ/molB.①的反应热为221kJ/molC.稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/molD.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量2.银锌钮扣电池的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为 Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-;总反应为:Ag2O+Zn=2Ag+ZnO,下列判断正确的是()A、锌为正极,Ag2O为负极;B、锌为阳极,Ag2O为阴极;C、原电池工作时,负极区PH减小;D、原电池工作时,负极区PH增大;3.在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,最好选用()A.NaOH B.HC1 C.NaCl D.CuSO44.已知H—H键能为436 KJ/mol,H—N键能为391KJ/mol,根据化学方程式:N2 + 3H2 = 2NH3ΔH=—92.4 KJ/mol,则N≡N键的键能是 ( )A.431 KJ/mol B.946 KJ/mol C.649 KJ/mol D.869 KJ/mol 5.已知:CH3CH2CH2CH3(g)+6.5O2(g)4CO2(g)+5H2O(l);∆H =-2878 kJ(CH3)2CHCH3(g)+6.5O2(g)4CO2(g)+5H2O(l);∆H =-2869 kJ下列说法正确的是( )(A)正丁烷分子储存的能量大于异丁烷分子 (B)正丁烷的稳定性大于异丁烷(C)异丁烷转化为正丁烷的过程是一个放热过程 (D)异丁烷分子中的碳氢键比正丁烷的多6.灰锡(以粉末状存在)和白锡是锡的两种同素异形体。
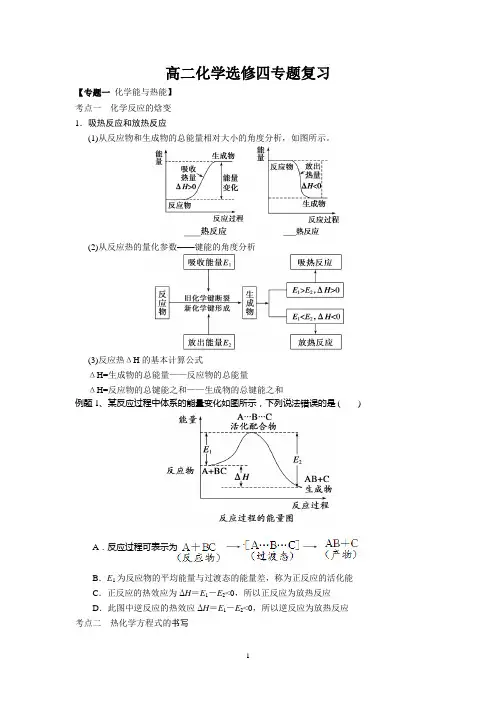
高二化学选修四专题复习【专题一化学能与热能】考点一化学反应的焓变1.吸热反应和放热反应(1)从反应物和生成物的总能量相对大小的角度分析,如图所示。
(2)从反应热的量化参数——键能的角度分析(3)反应热ΔH的基本计算公式ΔH=生成物的总能量——反应物的总能量ΔH=反应物的总键能之和——生成物的总键能之和例题1、某反应过程中体系的能量变化如图所示,下列说法错误的是 ()A.反应过程可表示为―→―→B.E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能C.正反应的热效应为ΔH=E1-E2<0,所以正反应为放热反应D.此图中逆反应的热效应ΔH=E1-E2<0,所以逆反应为放热反应考点二热化学方程式的书写(1)注明反应条件:反应热与测定条件(温度、压强等)有关。
绝大多数反应是在25 ℃、101 kPa 下进行的,可不注明。
(2)注明物质状态:常用______、______、______、______分别表示固体、液体、气体、溶液。
(3)注意符号单位:ΔH 应包括“+”或“-”、数字和单位(kJ·mol -1)。
(4)注意守恒关系:①原子守恒和得失电子守恒;②能量守恒。
(ΔH 与化学计量数相对应) (5)区别于普通方程式:一般不注“↑”、“↓”以及“点燃”、“加热”等。
(6)注意热化学方程式的化学计量数热化学方程式中各物质化学式前面的化学计量数仅表示该物质的物质的量,可以是整数,也可以是分数。
且化学计量数必须与ΔH 相对应,如果化学计量数加倍,则ΔH 也要加倍。
例题2.已知在1×105Pa 、298 K 条件下,2 mol 氢气燃烧生成水蒸气,放出484 kJ 热量,下列热化学方程式正确的是 ( )A .H 2O(g)===H 2(g)+12O 2(g) ΔH =-242 kJ·mol -1B .2H 2(g)+O 2(g)===2H 2O(l) ΔH =-484 kJ·mol -1C .H 2(g)+12O 2(g)===H 2O(g) ΔH =-242 kJD .2H 2(g)+O 2(g)===2H 2O(g) ΔH =-484 kJ·mol -1考点三 中和热和燃烧热比较项目燃烧热中和热相同点能量变化 ____反应ΔH ΔH __0,单位:________不同点反应物的量 ____ mol (O 2的量不限)可能是1 mol ,也可能是0.5 mol生成物的量不限量H 2O 是 ____ mol 反应热的含义__________时,____ mol 纯物质完全燃烧生成稳定的氧化物时所放出的热量;不同反应物,燃烧热不同________中强酸跟强碱发生中和反应生成 ____ mol H 2O 时所释放的热量;不同反应物的中和热大致相同,均约为______ kJ·mol -1例题3.下列关于热化学反应的描述中正确的是( )A .HCl 和NaOH 反应的中和热ΔH =-57.3 kJ·mol -1,则H 2SO 4和Ca(OH)2反应的中和热ΔH =2×(-57.3) kJ·mol -1B .CO(g)的燃烧热是283.0kJ·mol -1,则2CO 2(g)===2CO(g)+O 2(g)反应的ΔH =+(2×283.0)kJ·mol -1C .1 mol 甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热D .稀醋酸与稀NaOH 溶液反应生成1 mol 水,放出57.3 kJ 热量【规律与方法】 一、反应热大小的比较1.比较ΔH 的大小时需带正负号吗?2.怎样比较两个反应的ΔH 大小?(1)、同一反应,生成物状态不同时,同一反应,反应物状态不同时。

选修4 化学反应原理全套同步练习--第一章第一章化学反应与能量 第一节 化学反应与能量的变化基础知识1.人们把能够发生 叫做活化分子,同时把 称做活化能;2.我们用ΔH 表示 ,其单位常用 ;放热反应的ΔH 为 填正或负值;3.能表示 的关系的化学方程式,叫做 ;巩固练习1.下列说法正确的是 A .需要加热才能发生的反应一定是吸热反应B .任何放热反应在常温条件下一定能发生反应C .反应物和生成物所具有的总能量决定了放热还是吸热D .吸热反应只能在加热的条件下才能进行 2.下列说法正确的是A .热化学方程式的计量数只表示分子的个数B .热化学方程式中只需标明生成物的状态C .反应热指的是反应过程中放出或吸收的热量D .有能量变化的不一定是化学变化 3. 根据热化学方程式:S l +O 2 g = SO 2 g ΔH =-mol 分析下列说法中正确的是A .Ss+O 2 g = SO 2 g ,反应放出的热量大于molB .S g +O 2 g = SO 2 g ,反应放出的热量小于molC .1mol SO 2的键能的总和小于1mol 硫和1mol 氧气的键能之和D .1mol SO 2的键能的总和大于1mol 硫和1mol 氧气的键能之和4.下列说法正确的是 A .焓变是指1mol 物质参加反应时的能量变化 B .当反应放热时ΔH >0,反应吸热时ΔH <0C .加热条件下发生的反应均为吸热反应D .一个化学反应中,当反应物质能量大于生成物能量时,反应放热,ΔH 为“—”5.同温同压下,已知下列各反应为放热反应,下列各热化学方程式中放热最少的是 A .2A l + B l = 2C g ΔH 1 B .2A g + B g = 2C g ΔH 2 C .2A g + B g = 2C l ΔH 3 D .2A l + B l = 2C l ΔH 46.热化学方程式中化学式前的化学计量数表示 A .分子个数 B .原子个数 C .物质的质量 D .物质的量 7.在相同温度和压强下,将32g 硫分别在纯氧中和空气中完全燃烧,令前者热效应为ΔH 1,后者热效应为ΔH 2, 则关于ΔH 1和ΔH 2的相对大小正确的是 A .ΔH 1=ΔH 2 B .ΔH 1>ΔH 2 C .ΔH 1<ΔH 2 D .无法判断9.已知在1×105Pa,298 K 条件下,2 mol 氢气燃烧生成水蒸气放出484 kJ 热量,下列热化学方程式正确的是 A .H 2O g = H 2 g +21O 2 g ΔH = +242 kJ/mol B .2H 2 g + O 2 g = 2H 2O l ΔH =-484 kJ/molC .H 2 g + 21O 2 g = H 2O g ΔH =-242 kJ/mol D .2H 2 g + O 2 g = 2H 2O g ΔH =+484 kJ/mol 10.有如下三个反应方程式 H 2g +21O 2g =H 2Og ΔH =a kJ/molH 2g +21O 2g =H 2O l ΔH =b kJ/mol2H 2g +O 2g =2H 2O l ΔH =c kJ/mol 关于它们的下列叙述正确的是 A .它们都是吸热反应 B .a 、b 、c 均为正值 C .a =b D .2b =c11.含NaOH 的稀溶液与足量的稀盐酸反应,放出的热量,表示该反应的热化学方程式是A .NaOHaq +HClaq =NaClaq +H 2Ol ;ΔH =+molB .NaOHaq +HClaq =NaClaq +H 2Ol ;ΔH =-molC .NaOHaq +HClaq =NaClaq +H 2Ol ;ΔH =+molD .NaOHaq +HClaq =NaClaq +H 2Ol ;ΔH =-mol 12.已知方程式2H 2g +O 2g =2H 2Ol ΔH 1=-mol,则关于方程式2H 2Ol =2H 2g +O 2g ; ΔH 2=的说法正确的是 A .方程式中化学计量数表示分子数 B .该反应的ΔH 2大于零C .该反应ΔH 2=-molD .该反应与上述反应属于可逆反应13.断裂以下的物质需要能量最多的是 A .HCl B .HBr C .HI D .HAt 14.下列叙述中正确的是 A .实现H 2→H+H 的变化,要放出能量 B .液态水变成气态水要吸收能量 C .金刚石在一定条件变成石墨要吸收能量 D .CaO 和水反应过程中焓变大于015.表示正反应是吸热反应的图像是;;23 molNO 2气体溶于水生成HNO 3和NO 气体,放出138kJ 热量 ;17.火箭推进器中盛有强还原剂液态肼N 2H 4和强氧化剂液态双氧水;当把液态肼和 H 2O 2混合反应,生成氮气和水蒸气,放出的热量相当于25℃、101 kPa 下测得的热量; 1反应的热化学方程式为 ;2又已知H 2Ol =H 2Og ΔH =+44kJ/mol;则16g 液态肼与液态双氧水反应生成液态水时放出的热量是 kJ;BCD A3此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 ; 18.用L 盐酸与LNaOH 溶液在如图所示的装置中进行中和反应;通过测定反应过程中 所放出的热量可计算中和热;回答下列问题:1从实验装置上看,图中尚缺少的一种玻璃用品 是 ;2烧杯间填满碎纸条的作用是 ; 3大烧杯上如不盖硬纸板,求得的中和热数值 填“偏大、偏小、无影响”4如果用L 盐酸与LNaOH 溶液进行反应,与上述实验相比,所放出的热量 填“相等、不相等”,所求中和热 填“相等、不相等”,简述理由 ; 5用相同浓度和体积的氨水NH 3·H 2O 代替NaOH 溶液进行上述实验,测得的中和热的数值会 ;填“偏大”、“偏小”、“无影响”; 19.已知:H 2 g + 21O 2 g = H 2O g ,反应过程中能量变化如图所示,请回答下列问题;1a 、b 、c 分别代表什么意义a : ;b : ; c : ; 2该反应是 填“放热”或“吸热”, ΔH 0填“>”“<”或“=”;能力提升20.由金红石TiO 2制取单质Ti,涉及到的步骤为:TiO 2→TiCl 4 Ti 已知①Cs+O 2g =CO 2g ΔH =― kJ/mol ②2COg+O 2g =2CO 2gΔH =―566 kJ/mol ③TiO 2s+2Cl 2g =TiCl 4g+O 2g ΔH =+141kJ/mol 则TiO 2s+2Cl 2g + Cs =TiCl 4g+ 2COg 的ΔH = ;反应TiCl 4+2Mg =2MgCl 2+Ti在Ar气氛中进行的理由cb 反应过程2H 2g+O 2gH 2g+1/2 O 2g能量H 2O gaMg−−−→−︒Al,C 800温度计硬纸板碎纸条是 ;第二节 燃烧热 能源基础知识1.反应热可分为多种,如: 、 、 等;,叫做该物质的燃烧热,单位为 ,通常可利用 由实验测得;2.能源就是 ,它包括化石燃料 、 、 、 、 、 等;能源是 和 的重要物质基础,它的开发和利用,可以用来衡量一个国家或地区的 和 ;巩固练习1.下列说法中正确的是 A .1molH 2SO 4和1mol BaOH 2完全中和所放出的热量为中和热 B .在25℃、101 kPa,1mol S 和2mol S 的燃烧热相等C .CO 是不稳定的化合物,它能继续和O 2反应生成稳定的CO 2,所以CO 的燃烧反应一定是吸热反应D .101kPa 时,1mol 碳燃烧所放出的热量为碳的燃烧热 2.下列热化学方程式中的反应热下划线处表示燃烧热的是 A .C 6H 12O 6s+6O 2g = 6CO 2g+6H 2Ol ΔH =―a kJ /molB .CH 3CH 2OHl+21O 2g = CH 3CHOl+H 2Ol ΔH =―b kJ /mol C .2COg+ O 2g =CO 2g ΔH =―c kJ /molD .NH 3g+45O 2g = NOg+46H 2Og ΔH =―d kJ /mol3.下列各组物质的燃烧热相等的是 A .碳和二氧化碳B .1mol 碳和3mol 碳C .3mol 乙炔和1mol 苯D .淀粉和纤维素4.下列热化学方程式中的ΔH 能表示物质燃烧热的是A .2CO g + O 2 g = 2CO 2 g ΔH = ―556 kJ/molB .CH 4 g + 2O 2 g = CO 2 g + 2H 2O l ΔH = —890kJ/molC .2H 2 g +O 2 g = 2H 2Ol ΔH =― kJ/molD .H 2 g + Cl 2 g = 2HCl g ΔH =― kJ/mol5.燃烧热与反应热的关系是 A .燃烧热是反应热的一种类型 B .当一个反应是燃烧反应时,该燃烧反应的反应热就是燃烧热C .燃烧热不属与反应热,反应热是在25℃、101 kPa 下测定的,而燃烧反应的温度要高D .反应热有正负之分,燃烧热全部是正值6.已知在一定条件下,CO 的燃烧热为283 kJ/mol,CH 4的燃烧热为890 kJ/mol,由1 mol CO 和3 mol CH 4组成的混合气体充分燃烧,释放的热量为 A .2912 kJ B .2953 kJ C.3236kJD .3867 kJ7.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生;下列属于未来新能源标准的是 ①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能 A .①②③④ B .⑤⑥⑦⑧ C .③⑤⑥⑦⑧ D .③④⑤⑥⑦⑧ 8.25℃、101 kPa 下,碳、氢气、甲烷和葡萄糖的燃烧热依次是 kJ/mol 、 kJ/molkJ/mol 、2800 kJ/mol,则下列热化学方程式正确的是 A .Cs+错误!O 2g =COg ΔH =― kJ/mol B .2H 2g+O 2g =2H 2Ol ΔH = + kJ/mol C .CH 4g+2O 2g =CO 2g+2H 2Og ΔH = ― kJ/mol D .C 6H 12O 6s +6O 2g =6CO 2g+6H 2Ol ΔH =―2800 kJ/mol9. g 火箭燃料二甲基肼CH 3-NH —NH -CH 3完全燃烧,放出50 kJ 热量,二甲基肼的燃烧热为 A .1000 kJ/mol B .1500 kJ/molC .2000 kJ/molD .3000 kJ/mol10.25℃、101 kPa 下,2g 氢气燃烧生成液态水,放出 kJ 热量,表示该反应的热化学方程式正确的是A .2H 2g+O 2g = 2H 2O1 ΔH =― kJ/molB .2H 2g+ O 2g = 2H 2O1 ΔH =+ kJ /molC .2H 2g+O 2g = 2H 2Og ΔH =― kJ/molD .H 2g+错误!O 2g = H 2O1 ΔH =― kJ/mol 11.下列能源通过化学反应产生的是 A .太阳能 B .潮汐能 C .电池产生的电能D .风能12.已知下列热化学方程式:① H 2g+21O 2g =H 2Ol ΔH =―285kJ/mol ② H 2g+21O 2g =H 2Og ΔH =―mol ③ Cs+21O 2g =COg ΔH =― kJ/mol ④ Cs+ O 2g =CO 2g ΔH =― kJ/mol回答下列各问:1上述反应中属于放热反应的是 ; 2C 的燃烧热为 ;3燃烧10g H 2生成液态水,放出的热量为 ;4CO 燃烧的热化学方程式为 ;13.由氢气和氧气反应生成 1 mol 水蒸气,放出 kJ 热量;写出该反应的热化学方程式: ;若1g 水蒸气转化为液态水放热,则反应H 2g +21O 2g =H 2O l 的ΔH = kJ/mol;氢气的燃烧热为 kJ/mol;14.硝化甘油C 3H 5N 3O 9,无色液体分解时产物为N 2、CO 2、O 2和液态水,它的分解反应的化学方程式是 ;已知20℃时,硝化甘油分解放出的热量为154kJ,则每生成1mol 气体伴随放出的热量为 kJ; 能力提升15.CO 、CH 4、均为常见的可燃气体;1等体积的CO 和CH 4在相同条件下分别完全燃烧,转移的电子数之比为 ;2已知在101 kPa 时,CO 的燃烧热为283 kJ/mol;相同条件下,若2 molCH 4完全燃烧生成液态水,所放出的热量为1mol CO 完全燃烧放出热量的倍,CH 4完全燃烧的热化学方程式是 ; 3120℃、101 kPa 下,a mL 由CO 和CH 4组成的混合气体在b mLO 2中完全燃烧后,恢复到原温度和压强; ①若混合气体与O 2恰好完全反应,产生b mLCO 2,则混合气体中CH 4的体积分数为 保留2位小数; ②若燃烧后气体体积缩小了4a mL,则a 与b 关系的数学表示是 ;第三节 化学反应热的计算基础知识1840年,瑞士化学家盖斯通过大量实验证明, ,其反应热是 的;换句话说,化学反应的反应热只与 有关,而与反应的 无关;这就是盖斯定律;巩固练习1.已知H 2Og =H 2O l ΔH 1=―Q 1 kJ/mol C 2H 5OHg =C 2H 5OH l ΔH 2=―Q 2 kJ/mol C 2H 5OHg + 3O 2g =2CO 2g + 3H 2Og ΔH 3=―Q 3 kJ/mol若使23g 酒精液体完全燃烧,最后恢复到室温,则放出的热量为 A .Q 1+Q 2+Q 3kJ B .Q 1+Q 2+Q 3kJ C .+Q 2+Q 3kJ D .-Q 2+Q 3kJ 2.已知下列热化学方程式:Zns +21O 2g =ZnOs ΔH 2=― kJ/mol Hgl +21O 2g =HgOs ΔH 2=― kJ/mol 由此可知Zns + HgOs =ZnOs +Hgl ΔH 3 ,其中ΔH 3的值是 A .― kJ/molB .―molC .― kJ/molD .― kJ/mol3.已知CH 4g+2O 2g =CO 2g+2H 2Ol ΔH =―Q 11,2H 2g+O 2g = 2H 2Og ΔH =―Q 222H 2g+O 2g = 2H 2Ol ΔH =―Q 33;常温下,取体积比为4 : 1的甲烷和氢气的混合物气体112L 标况,经完全燃烧后恢复到常温,则放出的热量为A .4 Q 1+ Q 3B .4 Q 1+ Q 2C .4 Q 1+ Q 3D .4 Q 1+2 Q 24.在一定条件下,CO 和CH 4燃烧的热化学方程式分别为:2COg + O 2 g = 2CO 2 g ; ΔH =―566 kJ/mol CH 4 g + 2O 2 g = CO 2 g + 2H 2Ol ; ΔH =―890 kJ/mol 由1molCO 和3molCH 4组成的混和气在上述条件下完全燃烧时,释放的热量为 你 A .2912kJ B .2953kJ C .3236kJ D .3867kJ 5.已知热化学方程式:SO 2g+ 1/2O 2g SO 3g ΔH =―/mol,在容器中充入2molSO 2和1molO 2充分反应,最终放出的热量为 A . B .小于 C .小于 D .大于6.已知葡萄糖的燃烧热是2840 kJ/mol,当它氧化生成1g 水时放出的热量是A .B .C .D .7.已知两个热化学方程式: Cs +O 2g =CO 2g ΔH =―mol2H 2g +O 2g =2H 2Og ΔH =―mol现有炭粉和H 2组成的悬浮气共,使其在O 2中完全燃烧,共放出的热量,则炭粉与H 2的物质的量之比是 A .1︰1 B .1︰2 C .2︰3 D .3︰28.已知在发射卫星时可用肼N 2H 4为燃料、二氧化氮作氧化剂,这两者反应生成氮气和水蒸气;又知:N 2g +2O 2g =2NO 2g ΔH =+molN 2H 4g +O 2g =N 2g +2H 2Og ΔH =-534kJ/mol 则肼与NO 2反应的热化学方程式为 A .N 2H 4g +NO 2g =23N 2g +2H 2Og ΔH =+mol B .N 2H 4g +NO 2g =23N 2g +2H 2Og ΔH =-mol C .N 2H 4g +NO 2g =23N 2g +2H 2Ol ΔH =+molD .N 2H 4g +NO 2g =23N 2g +2H 2Ol ΔH =-mol9.已知热化学方程式:2KNO 3s = 2KNO 2s +O 2g ΔH =+58kJ/mol Cs +O 2g = CO 2g ΔH =-94kJ/mol为提供分解1molKNO 3所需的能量,理论上需完全燃烧碳 A .58/94molB .58/94×2 mol C.58×2/94molD .94×2/58mol10.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是 ①CH 3OHg +H 2Og =CO 2g +3H 2g ΔH =+ kJ/mol②CH 3OHg +21O 2g =CO 2g +2H 2g ΔH =- kJ/mol下列说法正确的是A .CH 3OH 的燃烧热为 kJ/molB .反应①中的能量变化如右图所示C .CH 3OH 转变成H 2的过程一定要吸收能量D .根据②推知反应CH 3OHl +1/2O 2g =CO 2g +2H 2g 的ΔH >- kJ/mol11.盖斯定律在生产和科学研究中有很重要的意义;有些反应的反应热虽然无法直接测得但可通过间接的方法测定;现根据下列3个热化学反应方程式: Fe 2O 3s+3COg =2Fes+3CO 2g ΔH =―/mol 3Fe 2O 3s+ COg =2Fe 3O 4s+ CO 2g ΔH =―/molFe 3O 4s+COg =3FeOs+CO 2g ΔH = +/mol写出CO 气体还原FeO 固体得到Fe 固体和CO 2气体的热化学反应方程式:; 12.由氢气和氧气反应生成1mol 水蒸气放热,写出该反应的热化学方程式:;若1g 水蒸气转化为液态水放热,则反应H 2g +21O 2g = H 2Ol CO 2g+3H 2g能量 反应过程CH 3OHg +H 2Og 反应物的 总能量生成物的总能量ΔH的ΔH = kJ/mol ;氢气的燃烧热为 kJ/mol ;13.实验中不能直接测出石墨和氢气生成甲烷反应的反应热,但可测出甲烷,石墨,氢气燃烧的反应热:CH 4g+2O 2g=CO 2g+2H 2Ol ΔH 1=-molC 石墨+ O 2g= CO 2g ΔH 2=―393.5kJ/mol H 2g+21O 2g=H 2Ol ΔH 3=― kJ/mol ,则由石墨生成甲烷的反应热: C 石墨+ 2H 2g= CH 4g ΔH 4= ;能力提升14.已知H 2g 、C 2H 4g 和C 2H 5OH1的燃烧热分别是― kJ/mol、― kJ/mol 和― kJ/mol,则由C 2H 4g 和H 2Ol 反应生成C 2H 5OHl 的ΔH 为 A .― kJ/mol B .+ kJ/mol C .―330 kJ/molD .+330 kJ/mol15.灰锡以粉末状存在和白锡是锡的两种同素异形体;已知: ①Sns、白+2HClaq =SnCl 2aq +H 2g ΔH 1②Sns、灰+2HClaq =SnCl 2aq +H 2g ΔH 2 ③Sns、灰Sns 、白 ΔH 3=+mol 下列说法正确的是 A .ΔH 1>ΔH 2 B .锡在常温下以灰锡状态存在 C .灰锡转化为白锡的反应是放热反应 D .锡制器皿长期处于低于℃的环境中,会自行毁坏16.白磷与氧可发生如下反应:P 4+5O 2=P 4O 10;已知断裂下列化学键需要吸收的能量分 别为:P —P a kJ/mol 、P —O b kJ/mol 、P=O c kJ/mol 、O=O d kJ/mol; 根据图示的分子结构和有关数据估算该反应的ΔH ,其中正确的是 A .6a +5d -4c -12b kJ/mol B .4c +12b -6a -5d kJ/mol C .4c +12b -4a -5d kJ/molD .4a +5d -4c -12b kJ/mol17.为了提高煤热效率,同时减少煤燃烧时的环境污染,一般先将煤转化为洁净的燃料;将煤转化为水煤气是通过化学方法将煤转为洁净燃料的方法之一,主要化学反应为:C+H 2O =CO+H 2,Cs 、COg 、H 2g 燃烧的热化学方程式分别为: Cs+ O 2g= CO 2g ΔH 1=―393.5 kJ/mol H 2g+21O 2g=H 2Og ΔH 2=― kJ/mol COg +21O 2 g = CO 2 g ΔH 3=-mol 根据盖斯定律可得下列循环图 试回答:1根据以上数据,请你写出Cs 与水蒸气反应的热化学方程 ; 2比较反应热数据可知,1molCOg 和1molH 2g 完全燃烧放出的热量之和比1molCg 完全燃烧放出的热量 填“多”或“少”; 3请你判断ΔH 1、ΔH 2、ΔH 3、ΔH 4之间的关系式 ; 4甲同学据此认为:“煤炭燃烧时加少量水,可以是煤炭燃烧放出更多的热量”;乙同学据此认为:“将煤转化为水煤气再燃烧放出的热量,与直接燃烧煤放出的热量一样多;”仅从能量观点看,甲、乙两同学观点正确的是 ,出现错误观点的原因是 ;参考答案第一章 化学反应与能量第一节 化学反应与能量的变化1.C 2.D 3.D 4.D 5.A 6.D 7.B 8.B 9.AC 10.D 11.D 12.B 13.A 14.B 15.A 16.C 石墨,s+ 2H 2Og = CO 2g + 2H 2 g ΔH =+ kJ 3NO 2g + 2H 2Og = 2HNO 3aq + NOg ΔH =-138kJ17.1N 2H 4l+2H 2O 2l = N 2g +4H 2Og ΔH =- KJ/mol 2 3产物不会造成环境污染;18.1环形玻璃搅拌棒 2减少实验过程中的热量损失 3偏小 4不相等;相等;因为中和热是指酸跟碱发生中和反应生成1mol H 2O 所放出的热量,与酸碱的用量无关 5偏小19.1代表旧化学键断裂吸收的能量 代表生成新键放出的能量 代表反应热2放热 < 20.—80 kJ/mol 防止高温下MgTi 与空气中的O 2或CO 2、N 2作用第二节 燃烧热 能源1.B 2.A 3.B 4.B 5.A 6.B 7.B 8.D 9.C 10.D 11.C12.1 ①②③④;2 kJ /mol ;31425 kJ ;4COg+21O 2g =CO 2g ΔH =―mol; 13.H 2 g +21O 2 g =H 2O g ΔH =― kJ/mol 或2H 2 g + O 2 g =2 H 2O g ΔH =―mol ― ―Cs+H 2Og + O 2g−−→−∆1H COg + H 2Og ΔHCOg + O 2g +H 2g −−→−∆2H COg + H 2Og 21O 2gΔHP 4 P 4O 1014.4C3H5N3O9= 6N2↑+12CO2↑+ O2↑+ 10H2O .11 : 4 2CH4g+2O2g=CO2g+2H2Ol ΔH=― kJ/mol 3① ② b ≥45a第三节化学反应热的计算1.D 2.D 3.A 4.B 5.C 6.A 7.A 8.B 9.B 10.D11.COg+FeOs=Fes+CO2g ΔH=―/mol 12.H2g + 1/2O2g=H2Og;ΔH=-mol –13.– kJ/mol 14.A 15.D 16.A17.1Cs+H2Og=COg+H2g ΔH=/mol 2多3ΔH 1=ΔH 2+ΔH 3+ΔH 4 4乙甲同学忽略了煤与水蒸气反应是一个吸热反应选修4 化学反应原理全套同步练习----第二章第二章化学反应速率与化学平衡第一节化学反应速率基础知识1.在容积不变的反应器中,化学反应速率通常用来表示,即: ,浓度的单位一般为 ,时间可以根据反应的快慢用、或表示;2.化学反应速率是通过测定的,包括能够直接观察的某些性质,如和 ,也包括必须依靠科学仪器才能测量的性质,如、、、等;在溶液中,当反应物或产物本身有较明显的颜色时,人们常利用来跟踪反应的过程和测量反应的速度;巩固练习1.现有反应4NH3+5O2=4NO+6H2O,反应速率分别用v NH3、v O2、v NO、v H2O、表示,其关系正确的是A.4v NH3=5O2B.4 v NH3=5 v H2O C.4O2=5 v NO D.4 v NH3=5 v NO2.在一定条件下,在体积为V L的密闭容器中发生反应:m A + n B p C;t秒末,A减少了1 mol,B减少了 mol,C 增加了 mol;则m∶ n∶ p应为 A.4∶5∶2B.2∶5∶4 C.1∶3∶2 D.3∶2∶13.在一密闭容器内发生氨分解反应:2NH3N2+3H2;已知NH3起始浓度是mol/L,4s末为mol/L,若用NH3的浓度变化来表示此反应的速率,则v NH3应为A.0. 04 mol/L·s B.0. 4 mol/L·s C.1. 6 mol/L·s D.0.8 mol/L·s4.下列关于反应速率的说法正确的是 A.化学反应速率是指单位时间内反应物浓度的减小或生成物浓度的增加B.化学反应速率为mol/L·s指1s时某物质的浓度为 mol/LC.根据化学反应速率的大小可以知道化学反应进行的快慢 D.对任何化学反应来说,反应速率越快,反应越明显5.反应m A+n B p C,若v A=a mol/L·s 则用单位时间内C的浓度变化表示的反应速率是A.m/pa mol/L·s B.pa/m mol/L·s C.ma/p mol/L·s D.mp/a mol/L·s 6.在10L 密闭容器里发生反应4NH3g+5O2g 4NOg+6H2Og,反应半分钟后,水蒸气的物质的量增加了,则此反应的速率v X可表示为 A.v NH3=mol/L·s B.v O2=mol/L·sC.v NO=mol/L·s D.v H2O=mol/L·s7.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如下图所示:下列描述正确的是A.反应开始到10s,用Z表示的反应速率为L·sB.反应开始到10s,X的物质的量浓度为减少了LC.反应开始到10s时,Y的转化率为%D.反应的化学方程式为:Xg + Yg Zg8.把气体和气体混合于容积为2L的容器中,使其发生如下反应:时间/s10物质的量/molXYZ3Xg+Yg n Zg+2Wg;5min 末生成,若测知以Z 浓度变化表示的平均反应速率为 L· min,则n 的值为A.4B .3C .2D .19.将物质的量均为物质A 、B 混合于5L 容器中,发生如下反应:3A+B2C,在反应过程中C 的物质的量分数随温度变化如右图所示:1T 0对应的反应速率v 正 v 逆用“=”、“>”或“<”表示,下同; 2此反应的正反应为 热;填“放”或“吸”3X 、Y 两点A 物质正反应速率的大小关系是Y X ;4温度T <T 0时,C%逐渐增大的原因是: ; 5若Y 点的C 的物质的量分数为25%,则参加反应的A 物质的量为 mol ;若Y 点时所消耗时间为2min,则B 物质的反应速率为 ;第二节 影响化学反应速率的因素基础知识1.决定化学反应速率的内因是 ;2.其他条件相同时,增大反应物的浓度化学反应速率 ,减小反应物的浓度化学反应速率 ; 3.对于气体反应,其他条件不变时,增大压强减小容器容积相当于 ,反应速率 ,减小压强增大容器容积相当于 ,反应速率 ;4.其他条件相同时,升高温度反应速率 ,降低温度反应速率 ;5.升高温度,一方面通过提高温度使分子获得更高能量, 的百分数提高;另一个是因为含较高能量的分子间的 也随之提高;这两方面都使分子间的 的几率提高,反应速率因此也增大;6.催化剂能使发生反应所需的 降低,使反应体系中含有的 提高,从而使提高,反应速率增大;巩固练习1.下列方法能增加活化分子百分数的是 A .增加某一组分的浓度 B .增体系的大压强C .升高体系的温度D .使用合适的催化剂2.设反应C +CO 2 2CO 正反应吸热反应速率为v 1,N 2+3H 2 2NH 3正反应放热,反应速率为v 2;对于上述反应,当温度升高时,v 1、v 2的变化情况为 A .同时增大 B .同时减小 C .v 1增大,v 2减小 D . v 1减小,v 2增大 3.在一可变容积的密闭容器中进行反应:Cs + H 2Og= COg + H 2g,下列条件的改变对反应速率几乎无影响的是 A .增加C 的量 B .将容器的体积缩小一半 C .保持体积不变,充入N 2,使体系的压强增大 D .保持压强不变,充入N 2,使容器的体积变大4.能提高单位体积内活化分子数,但不改变活化分子百分数的是A .增大反应物的浓度B .增大气体压强C .升温D .使用催化剂5.Na 2S 2O 3溶液跟稀H 2SO 4反应的化学方程式为:O H S SO SO Na SO H O S Na 224242322+↓++=+;下列各组实验中,溶液中最先变浑浊的是 6.下列条件一定能使反应速率加快的是:①增加反应物的物质的量②升高温度③缩小反应容器的体积 ④加入生成物 ⑤加入MnO 2A .全部B .①②⑤C .②D .②③反应反 应 物H 2O温度 Na 2S 2O 3 H 2SO 4 V℃v mLc molL -1v mLc molL -1mLA 10 5 10 5B 10 5 5 10C 30 5 5 10 D305510Y X C%T/℃T 07.100 mL 6 mol/L H 2SO 4跟过量的锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量;可向反应物中加入适量的 A .硫酸钠固体 B .水 C .硫酸钾溶液D .硫酸铵固体8.NO 和CO 都是汽车排放尾气中的有害物质,它们能缓慢反应生成N 2和CO 2,对此反应下列叙述正确的A .使用催化剂并不能改变反应速率B .使用催化剂可以加快反应速率C .降低压强能加快反应速率D .降温可以加快反应速率9.下列体系加压后,对化学反应速率没有影响的是A .2SO 2+O 22SO 3B .CO+H 2OgCO 2+H 2C .CO 2+H 2OH 2CD .H ++OH-H 2O10.下列说法正确的是 A .活化分子碰撞即发生化学反应 B .升高温度会加快反应速率,原因是增加了活化分子碰撞次数C .某一反应的活化分子的百分数是个定值D .活化分子间的碰撞不一定是有效碰撞 11.用铁片与稀硫酸反应制氢气时,下列措施不能使氢气生成速率加快的是 A .对该反应体系加热B .不用稀硫酸,改用98%浓硫酸C .滴加少量的CuSO 4溶液D .不用铁片,改用铁粉12.反应3Fes+4H 2O====Fe 3O 4s+4H 2g,在一可变容积的密闭容器中进行,试回答:1增加Fe 的量,其正反应速率 填变快、不变、变慢,以下相同; 2将容器的体积缩小一半,其正反应速率 ,逆反应速率 ;3保持体积不变,充入N 2使体系压强增大,其正反应速率 ,逆反应速率 ; 4保持压强不变,充入N 2使容器的体积增大,其正反应速率 ,逆反应速率 ; 13.1将等质量的Zn 粉分别投入a :10 ml /L HCl 和b :10 ml /L 醋酸中;①若Zn 不足量,则反应速率a b 填>=或<= ②若Zn 过量,产生H 2的量a b 填>=或<= 2将等质量Zn 粉分别投入pH =1体积均为10 mL 的a :盐酸 b :醋酸中 ①若Zn 不足量,则反应速率a b 填>=或<= ②若Zn 过量,产生H 2的量a b 填>=或<=14.把除去氧化膜的镁条放入盛有一定浓度稀盐酸的试管中,发现H 2的生成速率v 随时间t 的变化关系如图所示;其中t 1~t 2段速率变化的原因是 ,t 2~t 3是 ;能力提升15.“碘钟”实验中,3I -+S 2O -28=I -3+2SO -24的反应速率可以用I -3与加入的淀粉溶液显蓝色的时间t 来度量,t 越小,反应速率越大;某探究性学习小组在20℃进行实验,得到的数据如下表:实验编号① ② ③ ④ ⑤ c I -/mol·L -c S 2O -28/mol·L -t /st 2回答下列问题:1该实验的目的是 ;2显色时间t 2= ;3温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t 2的范围为 填字母A . < B . ~ C . > D . 数据不足,无法判断 4通过分析比较上表数据,得到的结论是 ; 16.下表是稀硫酸与某金属反应的实验数据: 实验序号 金属 质量/g 金属状态c H 2SO 4/mol·L -1V H 2SO 4/mL 溶液温度/℃ 金属消失的时间/s 反应前 反应后 1 丝 50 20 34 500 2粉末50203550t 132v3 丝 50 20 36 2504 丝 50 20 35 200 5 粉末 50 20 36 25 6 丝 50 20 35 1257 丝 50 35 50 508 丝 50 20 34 100 9丝50204440分析上述数据,回答下列问题:1实验4和5表明, 对反应速率有影响, 反应速率越快,能表明同一规律的实验还有 填实验序号;2仅表明反应物浓度对反应速率产生影响的实验有 填实验序号;3本实验中影响反应速率的其他因素还有 ,其实验序号是 ;4实验中的所有反应,反应前后溶液的温度变化值约15℃相近,推测其原因: ;17.硼氢化钠NaBH 4不能与水共存,也不能与酸共存;1将NaBH 4投入水中,可生成偏硼酸钠NaBO 2和氢气,写出该反应的化学方程式 ;这一反应的实质是 ; 2将NaBH 4放入强酸溶液中,其反应速率比跟水反应 ,其理由是 ;18.氯酸钾和亚硫酸氢钠发生氧化还原反应:ClO -3+3HSO -3=3SO -4+3H ++ Cl —,该反应的反应速率受H +浓度的影响,如图是用ClO -3在单位时间内物质的量浓度的变化来表示反应速率的图像;1反应开始时速率增大的原因是 ; 2纵坐标为v Cl —的vt 曲线与上图中曲线 填“能”或“不能”完全重合;第三节 化学平衡基础知识1.在一定条件下,当正、逆两个方向的反应速率相等时,,这时的状态也就是在给定条件下,反应达到了“限度”;对于可逆反应体系,我们称之为 状态; 2.如果 ,平衡就向着方向移动,这就是着名的勒夏特列原理;3.催化剂能够 ,因此它对化学平衡的移动没有影响; 4.对于一般的可逆反应,m Ag+n Bgp Cg+q Dg,当在一定温度下达到平衡时,K = ;K 只受影响,与 无关;巩固练习1.下列说法正确的是 A .可逆反应的特征是正反应速率和逆反应速率相等B .在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态C .在其他条件不变时,升高温度可以使平衡向放热反应方向移动D .在其他条件不变时,增大压强一定会破坏气体反应的平衡状态2.一定条件下的反应:PCl 5g PCl 3g +Cl 2g ΔH > 0,达到平衡后,下列情况使PCl 5分解率降低的是 A .温度、体积不变,充入氩气 B .体积不变,对体系加热C .温度、体积不变,充入氯气 D .温度不变,增大容器体积3.在一定条件下,发生COg +NO 2g CO 2g +NOgΔH <0的反应,达到平衡后,保持体积不变,降低温度,混合气体的颜色A .变深B .变浅C .不变D .无法判断12tv ClO -34.在一不可变容器中发生如下反应:2NO22NO + O2ΔH 0达到平衡后,升温,混合气体的不变A.密度B.颜色C.压强 D. 总物质的量5.在一密闭容器中进行如下反应:2SO2气+O2气2SO3气,已知反应过程中某一时刻SO2、O2、SO3的浓度分别为L、L、L,当反应达平衡时,可能存在的数据是 A.SO2为L、O2为LB.SO2为L C.SO2、SO3均为L D.SO3为L6.氙气和氟气在一定条件下可反应达到平衡:Xeg+2F2g XeF 4g ΔH=-218kJ/mol;下列变化既能加快反应速率又能使平衡向正反应方向移动的是 A.升高温度B.减压C.加压D.适当降温7.下列事实,不能用勒夏特列原理解释的是 A.氯水中有下列平衡Cl2+H2O HCl + HClO,当加入AgNO3溶液后,溶液颜色变浅 B.对2HIg H2g+I2g,平衡体系增大压强可使颜色变深 C.反应CO+NO2CO2+NO ΔH <0,升高温度可使平衡向逆反应方向移动 D.合成NH3反应,为提高NH3的产率,理论上应采取降低温度的措施8.有一处于平衡状态的反应:Xs+3Yg 2Zg,ΔH<0;为了使平衡向生成Z的方向移动,应选择的条件是①高温②低温③高压④低压⑤加催化剂⑥分离出ZA.①③⑤B.②③⑤C.②③⑥D.②④⑥9.现有反应Xg+Yg 2Zg,ΔH<0;右图表示从反应开始到t1s时达到平衡,在t2s时由于条件变化使平衡破坏,到t3 s时又达平衡;则在图中t2 s时改变的条件可能是 A.增大了X或Y的浓度 B.增大压强C.增大Z的浓度D.升高温度10.接触法制硫酸通常在400~500℃、常压和催化剂的作用下,用SO2与过量的O2反应生成SO3;2SO2g+O2g 2SO3g ;ΔH < 0;在上述条件下,SO2的转化率约为90%;但是部分发达国家采用高压条件生成SO3,采取加压措施的目的是A.发达国家电能过量,以此消耗大量能源 B.高压将使平衡向正反应方向移动,有利于进一步提高SO2的转化率C.加压可使SO2全部转化为SO3,消除SO2对空气的污染D.高压有利于加快反应速率,可以提高生产效率11.在一定条件下,固定容积的密闭容器中反应:2NO2g 2NOg + O2gΔH>0,达到平衡;当改变其中一个条件X,Y随X的变化符合图中曲线的是A.当X表示温度时,Y表示NO2的物质的量B.当X表示压强时,Y表示NO2的转化率C.当X表示反应时间时,Y表示混合气体的密度D.当X表示NO2的物质的量时,Y表示O2的物质的量12.右图曲线a表示放热反应 Xg+Yg Zg+Mg+Ns进行过程中X的转化率随时间变化的关系;若要改变起始条件,使反应过程按b曲线进行,可采取的措施是A.升高温度 B.加大X的投入量 C.加催化剂 D.增大容器的体积13.可逆反应A+Bs C达到平衡后,无论加压或降温,B的转化率都增大,则下列结论正确的是A.A固体,C为气体,正反应为放热反应 B.A为气体,C为固体,正反应为放热反应C.A为气体,C为固体,正反应为吸热反应 D.A、C均为气体,正反应为吸热反应14.一定温度下,将4molPCl3和2molCl2充入容积不变的密闭容器中,在一定条件下反应:PCl3+Cl2 PCl5 ,各物质均为气态;达平衡后,PCl5为;若此时再移走2molPCl3和1molCl2 ,相同温度下达到平衡,PCl5的物质的量为A.B. C.<x<D.<15.某温度下,将2mo1A和3mo1B充入一密闭容器中,发生反应:a Ag+Bg Cg+Dg,5min 后达到平衡;已知该温度下其平衡常数K=1 ,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化,则 A.a=1 B.a =2 C.B的转化率为40 % D.B的转化率为60 %16.X、Y、Z三种气体,取X和Y按1∶1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y2Z ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于ZX或Y0 t1t2t3tZyx。

第一章从实验中学化学测试题3第一卷选择题(48分)一、选择题(共16小题,每题3分,共48分)1、下列说法不正确的是( C)A.利用盖斯定律可计算某些难以直接测量的反应焓变B.在指定状态下各物质的焓值都是确定且是唯一的C.当同一个化学反应以不同的过程完成时,反应的焓变是不同的D.如果一个化学方程式通过其他几个化学方程式相加减而得到,则该反应的焓变可由相关化学方程式的焓变相加减而得到2、已知298 K时,合成氨反应N2(g)+3H2(g)2NH3(g)ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。
测得反应放出的热量为(假定测量过程中没有能量损失)( A)A.一定小于92.0 kJB.一定大于92.0 kJC.一定等于92.0 kJD.无法确定3、下列反应可能属于吸热反应的是(B)A. 甲烷与氧气反应B. 碳酸钙分解反应C. KOH与稀硫酸反应D. 铁丝与氯气反应4、下列说法中正确的是( C)A.在化学反应过程中,发生物质变化的同时不一定发生能反量变化B.破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量时,该反应为吸热反应C.生成物的总焓大于反应物的总焓时,反应吸热,ΔH>0D.ΔH的大小与热化学方程式的化学计量数无关5、“嫦娥奔月”是一个充满浪漫主义的中国神话故事.2007年10月24日我国“嫦娥一号”探月卫星由长三甲火箭送入预定的轨道.长三甲火箭第三级推进剂采用低温液氧/液氢.已知在298K时,2g氢气与氧气完全反应生成液态水放热285.8kJ,则此反应的热化学方程式为(A. )A. 2H2(g)+O2(g)==═2H2O(l)△H =﹣571.6KJ•mol﹣1B. 2H2(g)+O2(g)==═2H2O(l)△H=﹣285.8KJ•mol﹣1C. 2H2(g)+O2(g)═==2H2O(l)△H=+285.8KJ•mol﹣1D. 2H2(g)+O2(g)═==2H2O(l)△H =+571.6KJ•mol﹣16、根据如下图所示的反应判断下列说法中错误的是( D )A.CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量B.该反应的焓变大于零C.该反应中有离子键断裂也有共价键断裂,化学键断裂吸收能量,化学键生成放出能量D.由该反应可推出凡是需要加热才能发生的反应均为吸热反应7、天然气燃烧过程中的能量转化方式为(C)A. 热能转化为化学能B. 化学能转化为电能C. 化学能转化为热能D. 化学能转化为机械能8、已知:(l)H2(g)+1/2O2(g)=H2O(g)△H1=a kJ•mol﹣1(2)2H2(g)+O2(g)=2H2O(g)△H2=b kJ•mol﹣1(3)H2(g)+1/2O2(g)=H2O(l)△H3=c kJ•mol﹣1(4)2H2(g)+ O2(g)=2H2O(l)△H4=d kJ•mol﹣1下列关系式中正确的是(C)A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>09、下列关于热化学反应方程式的描述中正确的是( B)10、25℃、101kPa下:①2Na(s)+12O2(g)=Na2O(s) △H= -414kJ mol-1②2Na(s)+O2(g)=Na2O2(s) △H= -511kJ mol-1下列说法正确的是(D)A.①和②产物的阴阳离子个数比不相等B.①和②生成等物质的量的产物,转移电子数不同C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快D. 25℃、101kPa 下:Na 2O 2(s)+2Na(s)=2Na 2O(s) △H= -317kJ mol -111、已知1 mol 白磷(s)转化为红磷(s)时放出18.39 kJ 的热量,又知:P 4(白,s)+5O 2(g)===2P 2O 5(s) ΔH 14P(红,s)+5O 2(g)===2P 2O 5(s) ΔH 2则ΔH 1和ΔH 2的关系正确的是( C )A .ΔH 1=ΔH 2B .ΔH 1>ΔH 2C .ΔH 2>ΔH 1D .无法确定12、已知:①CO(g)+12O 2(g)===CO 2(g) ΔH =-283.0 kJ·mol -1②H 2(g)+12O 2(g)===H 2O(g) ΔH =-241.8 kJ·mol -1 下列说法正确的是( B )A.通常状况下,氢气的燃烧热为241.8 kJ·mol -1 B.由①可知,1 mol CO(g)和 12mol O 2(g)反应生成 1 mol CO 2(g),放出283.0 kJ 的热量 C.可用下图表示2CO 2(g)===2CO(g)+O 2(g)反应过程中的能量变化关系D.分解1 mol H 2O(g),其反应热为-241.8 kJ13、用CH 4催化还原NO x ,可以消除氮氧化物的污染。

化学反应与能量的变化专题练习题带答案⾼⼆年级化学选修四同步⼩题狂练第⼀章第⼀节化学反应与能量的变化⼀、单选题1.下列对能量转化的认识中,不正确的是()A. 电解⽔⽣成氢⽓和氧⽓时,电能主要转化为化学能B. ⽩炽灯⼯作时,电能全部转化为光能C. 煤燃烧时,化学能主要转化为热能D. 风⼒发电时,风能主要转化为电能2.在⼀定条件下,1mol⽩磷转化为红磷放出29.2KJ热能.在该条件下,下列说法正确的是()A. ⽩磷⽐红磷的能量低B. ⽩磷⽐红磷稳定C. 该变化为物理变化D. 该变化的本质是旧化学键断裂,新化学键形成3.下列说法不正确的是()A. 放热反应不需加热即可发⽣B. 化学反应过程中的能量变化除了热能外,也可以是光能、电能等C. 需要加热才能进⾏的化学反应不⼀定是吸热反应D. 化学反应热效应数值与参加反应的物质多少有关4.从如图所⽰的某⽓体反应的能量变化分析,以下判断错误的是()A. 这是⼀个放热反应B. 该反应可能需要加热C. ⽣成物的总能量低于反应物的总能量D. 反应物⽐⽣成物更稳定5.已知:常温下,0.01mol?L?1MOH溶液的pH为10,MOH(aq)与H2SO4(aq)反应⽣成1mol正盐的△H=24.2kJmol1,强酸与强酸稀溶液反应的中和热为△H=?57.3kJ?mol?1,则MOH的⽔溶液中电离的△H为()A. ?69.4kJ?mol?1B. ?45.2kJ?mol?1C. +69.4kJ?mol?1D. +45.2kJ?mol?16.已知中和热的数值是57.3KJ/mol.下列反应物混合时,产⽣的热量等于57.3KJ的是()A. 500mL1 mol/LHCl(aq)和500mL 1mol/LNaOH(aq)B. 500mL 1mol/LH2SO4(aq)和500mL 1mol/LBa(OH)2(aq)C. 1000mL1.0mol/L的CH3COOH(aq)和1000mL1.0mol/L的NaOH(aq)D. 1000mL1.0mol/L的HCl(aq)和1000mL1.0mol/L的NaOH(aq)7.肼(N2H4)是⽕箭发动机的⼀种燃料,反应时N2O4为氧化剂,⽣成N2和⽔蒸⽓.已知:N2(g)+2O2(g)=N2O4(g)△H=+8.7kJ?mol?1N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=?534.0kJ?mol?1下列表⽰肼跟N2O4反应的热化学⽅程式,正确的是…()A. 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=?542.7kJ?mol?1B. 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=?1059.3kJ?mol?1C. N2H4(g)+12N2O4(g)=32N2(g)+2H2O(g)△H=?1076.7kJ?mol?1D. 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=?1076.7kJ?mol?18.已知:(1)H2(g)+12O2(g)=H2O(g);△H=a kJ/mol(2)2H2(g)+O2(g)=2H2O(g);△H=b kJ/mol(3)H2(g)+12O2(g)=H2O(l);△H=c kJ/mol(4)2H2(g)+O2(g)=2H2O(l);△H=d kJ/mol下列关系式中正确的是()A. aB. b>d>0C. 2a=b<0D. 2c=d>09.常温下,1mol化学键分解成⽓态原⼦所需要的能量⽤E表⽰.、结合表中信息判断下列说法不正确的是()共价键H?H F?F H?F H?Cl H?IE(kJ?mol?1)436157568432298A. 432kJ?mol?1>E(H?Br)>298kJ?mol?1B. 表中最稳定的共价键是H?F键C. H2(g)→2H(g)△H=+436kJ?mol?1D. H2(g)+F2(g)=2HF(g)△H=?25kJ?mol?110.下列有关叙述正确的是()A. 如图所⽰,测定中和热时,⼤⼩两烧杯间填满碎纸条或泡沫塑料的⽬的是固定⼩烧杯B. 若⽤50 mL 0.55mol?L?1的氢氧化钠溶液,分别与50 mL 0.50mol?L?1的盐酸和50 mL 0.50mol?L?1的硫酸充分反应,两反应测定的中和热不相等C. 中和热测定实验也可以⽤稀硫酸与氢氧化钠溶液反应D. 为了简化装置,中和热测定实验中的环形玻璃搅拌棒可以由温度计代替⼆、填空题11.(1)肼(N2H4)是发射航天飞船常⽤的⾼能燃料.将NH3和NaClO按⼀定物质的量⽐混合反应,⽣成肼、NaCl和⽔,该反应的化学⽅程式是______ .(2)在⽕箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产⽣⼤量⽓体,并放出⼤量热.已知:H2O(l)H2O(g)△H=+44kJ/mol.12.8g液态肼与⾜量过氧化氢反应⽣成氮⽓和⽔蒸⽓,放出256.65kJ的热量.①请写出液态肼与过氧化氢反应⽣成液态⽔的热化学⽅程式______ .②则16g 液态肼与⾜量过氧化氢反应⽣成液态⽔时放出的热量是______ .12.依据事实写出下列反应的热化学⽅程式.(1)1g碳与适量⽔蒸⽓反应⽣成CO和H2,需要吸收10.94KJ热量,此反应的热化学⽅程式为______(2)已知2.0g燃料肼(N2H4)⽓体完全燃烧⽣成N2和⽔蒸⽓时,放出33.4KJ的热量,则肼燃烧的热化学⽅程式为______(3)2molAl(s)与适量O2(g)反应⽣成Al2O3(s),放出1669.8KJ的热量.此反应的热化学⽅程式为______(4)2.3g某液态有机物和⼀定量的氧⽓混合点燃,恰好完全燃烧,⽣成2.7g液态⽔和2.24LCO2(标准状况)并放出68.35KJ的热量.写出此反应的热化学⽅程式______ .13.某实验⼩组⽤0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进⾏中和热的测定.Ⅰ.配制0.50mol/L NaOH溶液(1)若实验中⼤约要使⽤245mL NaOH溶液,⾄少需要称量NaOH固体______ g.(2)配制过程中需要⽤到的玻璃仪器除烧杯、玻璃棒外还需要有______ 、______ .Ⅱ.测定中和热的实验装置如图所⽰.(3)⼤⼩烧杯之间填满碎泡沫塑料的作⽤是______ ,从实验装置上看,图中缺少的⼀种玻璃仪器______ .(4)使⽤补全仪器后的装置进⾏实验,取50mL 0.25mol/L H2SO4溶液与50mL0.55mol/L NaOH溶液在⼩烧杯中进⾏中和反应,实验数据如表.实验次数起始温度t1/℃终⽌温度t2/℃温度差平均值(t2?t1)/℃H2SO4NaOH平均值①请填写下表中的空⽩:②通过计算可得中和热△H=______ (精确到⼩数点后⼀位)③上述实验数值结果与57.3kJ/mol有偏差,产⽣偏差的原因可能是______ .(填字母)a.实验装置保温、隔热效果差b.量取NaOH溶液的体积时仰视读数c.分多次把NaOH溶液倒⼊盛有硫酸的⼩烧杯中d.⽤温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度(5)实验中若⽤60mL0.25mol?L?1H2SO4溶液跟50mL0.55mol?L?1NaOH溶液进⾏反应,与上述实验相⽐,所放出的热量______ (填“相等”、“不相等”),所求中和热______ (填“相等”、“不相等”);,若⽤50mL0.50mol?L?1醋酸代替H2SO4溶液进⾏上述实验,测得反应前后温度的变化值会______ (填“偏⼤”、“偏⼩”、“不受影响”).答案和解析【答案】1. B2. D3. A4. D5. D6. D7. D8. C9. D10. C11. 2NH3+NaClO=N2H4+NaCl+H2O;N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)H=?817.625kJ/mol;408.8125kJ12. C(s)+H2O(g)=CO(g)+H2(g)△H=+131.28kJ?mol?1;N2H4(g)+O2(g)=N2(g)+2H2O△H=?534.4KJ/mol;4Al(s)+3O2(g)=2Al2O3(s)△H=?3339.6kJ?mol?1;C2H5OH(l)+3O2(g)=2CO2(g)+ 3H2O(l)△H=?1367KJ/mol13. 5.0;250mL容量瓶;胶头滴管;减少实验过程中的热量损失;环形玻璃搅拌棒;3.4;?56.8kJ?mol?1;acd;不相等;相等;偏⼩【解析】1. 解:A、电解⽔⽣成氢⽓和氧⽓的电解装置是将电能转化为化学能的装置,故A正确;B、⽩炽灯⼯作时电能转化为光能和热能,故B错误;C、物质的燃烧将化学能转化为热能和光能,主要是热能,故C正确;D、风⼒发电时,风能主要转化为电能,故D正确.故选B.A、电解⽔是电能转化为化学能;B、⽩炽灯⼯作时电能转化为光能、热能等;C、煤燃烧主要转化为热能;D、风⼒发电主要是风能转化为电能.本题考查学⽣常见的能量转化形式⽅⾯的知识,可以根据教材知识来回答,较简单.2. 解:4P(s,⽩磷)=P4(s,红磷)△H=?29.2kJ/mol,该反应是放热反应,则红磷能量⽐⽩磷低,红磷⽐⽩磷稳定,放热反应中断裂旧键所吸收的能量低于形成新键所放出的能量,A.分析可知红磷能量⽐⽩磷低,故A错误;B.则红磷能量⽐⽩磷低,磷⽐⽩磷稳定,故B错误;C.该变化是同素异形体之间的转化属于化学变化,故C错误;D.同素异形体之间的转化属于化学变化,化学反应的本质是旧键断裂新键形成的过程,故D正确;故选D.4P(s,⽩磷)=P4(s,红磷)△H=?29.2kJ/mol,该反应是放热反应,则红磷能量⽐⽩磷低,红磷⽐⽩磷稳定,放热反应中断裂旧键所吸收的能量低于形成新键所放出的能量;本题考查反应热的分析以及同素异形体的判断,题⽬难度不⼤,注意物质能量越⾼越活泼,掌握基础是解题关键.3. 解:A、部分放热反应也需要反应条件,如碳的燃烧等需要点燃,故A错误;B、根据化学反应过程中的能量转化形式分析,除了热能外,也可以是光能、电能等,故B正确;C、有的吸热反应常温下也能发⽣,如碳酸氢铵的分解,故C正确;D、参加反应的物质越多,放出热量越多,所以化学反应热效应数值与参加反应的物质多少有关,故D 正确;故选A.A、部分放热反应也需要反应条件;B、根据化学反应过程中的能量变化形式分析;C、有的吸热反应常温下也能发⽣;D、参加反应的物质越多,放出热量越多,本题主要考查了放热与吸热反应的原因、常见的吸热和放热反应,是对基本知识的考查,较简单.4. 解:A、图象分析可知反应物能量⾼于⽣成物,反应是放热反应,故A正确;B、反应可能需要吸收能量引发反应进⾏,故B正确C、反应是放热反应,反应物能量⾼于⽣成物,故C正确;D、物质能量越⾼越活泼,⽣成物⽐反应物更稳定,故D错误;故选D.A、分析图象可知反应物能量⾼于⽣成物;B、反应进⾏需要变化为活化分⼦可能需要吸收能量;C、依据化学反应能量守恒分析判断;D、物质能量越⾼越活泼;本题考查了物质能量变化的分析判断,图象分析是解题关键,题⽬较简单.5. 解:常温下,0.01mol?L?1MOH溶液的pH为10,说明MOH是弱碱:MOH(aq)+H+(aq)=M+(aq)+ H2O(l)△H1=?12.1kJ?mol? 1①,H+(aq)+OH?(aq)=H 2O(l)△H2=?57.3kJ?mol?1②,根据盖斯定律,由①?②得:MOH(aq)?M+(aq)+OH?(aq)△H=(?12.1+57.3)kJ?mol?1=+45.2kJ?mol?1,故选:D.由题意知MOH是弱碱:MOH(aq)+H+(aq)=M+(aq)+H 2O(l)△H1=?12.1kJ?mol?1①,H+(aq)+ OH?(aq)=H2O(l)△H2=?57.3kJ? mol?1②,根据盖斯定律构造MOH(aq)?M+(aq)+OH?(aq)并计算焓变.本题考查了弱电解质的判断和反应热的计算,综合性较强,注意弱电解质的判断和利⽤盖斯定律进⾏构造⽬标热化学⽅程式并计算焓变是解题的关键.6. 解:A.500mL1mol/LHCl(aq)和500mL1mol/LNaOH(aq)⽣成的⽔的物质的量是0.1mol,放出的热量是28.65KJ,故A错误;B.500mL1mol/LH2SO4(aq)和500mL1mol/LBa(OH)2(aq)反应⽣成的⽔的物质的量是1mol,但是有硫酸钡沉淀⽣成,放出的热量⽐57.3kJ⼩,故B错误;C.1000mL1.0mol/L的CH3COOH(aq)和1000mL1.0mol/L的NaOH(aq)反应⽣成的⽔的物质的量是1mol,但是醋酸是弱酸,弱酸电离吸热,放出的热量⼩于57.3kJ,故C错误;D.1000mL1.0mol/L的HCl(aq)和1000mL1.0mol/L的NaOH(aq)反应⽣成的⽔的物质的量是1mol,放出的热量是为57.3kJ,故D 正确;故选D.在稀溶液中,酸跟碱发⽣中和反应⽣成1 mol⽔时的反应热叫做中和热.必须是酸和碱的稀溶液,因为浓酸溶液和浓碱溶液在相互稀释时会放热.强酸和强碱的稀溶液反应才能保证H+(aq)+OH?(aq)=H2O(l)中和热均为57.3kJ?mol?1,⽽弱酸或弱碱在中和反应中由于电离吸收热量,反应不能⽣成沉淀,⽣成沉淀会放出热量.本题考查了中和热的数值和概念理解,反应过程中热量变化是解题关键,题⽬难度中等.7. 解:已知①N2(g)+2O2(g)=N2O4(g),△H=+8.7kJ/mol,②N2H4(g)+O2(g)=N2(g)+2H2O(g),△H=?534.0kJ/mol,利⽤盖斯定律将②×1?①可得2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g),△H=(?534.0kJ/mol)×2?(+8.7kJ/mol)=?1076.7kJ/mol,或N2H4(g)+12N2O4(g)=32N2(g)+2H2O(g);△H=?538.35kJ/mol,故答案为:2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g),△H=?1076.7kJ/mol,或N2H4(g)+12N2O4(g)=32N2(g)+2H2O(g);△H=?538.35kJ/mol.故选D.已知①N2(g)+2O2(g)=N2O4(g),△H=+8.7kJ/mol;②N2H4(g)+O2(g)=N2(g)+2H2O(g),△H=?534.0kJ/mol;利⽤盖斯定律将②×1?①可得2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g),并以此计算反应热.本题考查反应热的计算,题⽬难度不⼤,注意盖斯定律的应⽤,注意反应热的正负.8. 解:A、c 中⽣成的是液态⽔,热量多,绝对值⽐a⽓态⽔的⼤,但绝对值越⼤相应数值越⼩所以cB、d中⽣成的是液态⽔,热量多,绝对值⽐b⽓态⽔的⼤,但绝对值越⼤相应数值越⼩所以dC、燃烧反应为放热反应,△H<0,由系数确定d=2c<0;b=2a<0,故C正确;D、燃烧反应为放热反应,△H<0,由系数确定d=2c<0;b=2a<0,故D错误;故选:C.根据燃烧反应为放热反应,△H<0,由系数确定d=2c<0;b=2a<0;d中⽣成的是液态⽔,热量多,绝对值⽐b⽓态⽔的⼤,但绝对值越⼤相应数值越⼩所以d本题主要考查了反应热⼤⼩的⽐较,难度不⼤,需要注意的是a、b、c、d含有+/?的⽐较的时候要带⼊⽐较.9. 解:A.依据溴原⼦半径⼤于氯原⼦⼩于碘原⼦,半径越⼤键能越⼩分析,所以结合图表中数据可知432kJ?mol?1>E(H? Br)>298kJ?mol?1,故A正确;B.键能越⼤形成的化学键越稳定,表中键能最⼤的是H?F,最稳定的共价键是H?F键,故B正确;C.氢⽓变化为氢原⼦吸热等于氢⽓中断裂化学键需要的能量,H2(g)→2H(g)△H=+436kJ?mol?1,故C正确;D.依据键能计算反应焓变=反应物键能总和?⽣成物键能总和计算判断,△H=436KJ/mol+157KJ/mol?2×568KJ/mol=?543KJ/mol,H2(g)+F2(g)=2HF(g)△H=-543kJ?mol?1,故D错误;故选D.A.依据溴原⼦半径⼤于氯原⼦⼩于碘原⼦,半径越⼤键能越⼩分析推断;B.键能越⼤形成的化学键越稳定;C.氢⽓变化为氢原⼦吸热等于氢⽓中断裂化学键需要的能量;D.依据键能计算反应焓变=反应物键能总和?⽣成物键能总和计算判断.本题考查了化学反应能量变化和键能的关系分析判断,焓变计算⽅法是解题关键,题⽬难度中等.10. 解:A.中和热测定实验成败的关键是保温⼯作,⼤⼩烧杯之间填满碎纸条的作⽤是减少实验过程中的热量损失,故A错误;B.中和热是稀的强酸溶液和强碱溶液反应⽣成1mol⽔时放出的热量,与酸碱的⽤量⽆关,所以两反应测定的中和热相等,故B 错误;C.⽤稀硫酸与氢氧化钠溶液反应测定反应热,符合中和热的概念,故C正确;D.温度计不能⽤于搅拌溶液,所以实验中环形玻璃搅拌棒不能由温度计代替,故D错误;故选C.A.中和热测定实验成败的关键是保温⼯作,烧杯间填满碎纸条的作⽤是保温;B.中和热是稀的强酸溶液和强碱溶液反应⽣成1mol⽔时放出的热量,与酸碱的⽤量⽆关;C.中和热是稀的强酸溶液和强碱溶液反应⽣成1mol⽔时放出的热量;D.温度计不能⽤于搅拌溶液.本题考查有关中和热的测定,掌握中和热的测定原理、过程是解题的关键,难度不⼤.11. 解:(1)根据题意可以知道NH3和NaClO反应⽣成肼、NaCl和⽔,根据得失电⼦守恒和原⼦守恒来配平⽅程式即2NH3+NaClO=N2H4+NaCl+H2O,故答案为:2NH3+NaClO=N2H4+NaCl+H2O;(2)①根据12.8g液态肼即0.4mol肼与⾜量过氧化氢反应⽣成氮⽓和⽔蒸⽓,放出256.65kJ的热量,可写出热化学⽅程式:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=?641.625kJ/mol①⼜知:H2O(l)=H2O(g)△H=+44kJ/mol②将①?②×4即得液态肼与过氧化氢反应⽣成液态⽔的热化学⽅程式:N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=(?641.625kJ/mol)?(+44kJ/mol)×4=?817.625kJ/mol,故答案为:N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=?817.625kJ/mol;②根据热化学⽅程式:N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)H=?817.625kJ/mol可知,1molN2H4(l)即32g肼完全燃烧放热817.625kJ,则16g 液态肼与⾜量过氧化氢反应⽣成液态⽔时放出的热量是408.8125kJ,故答案为:408.8125kJ.(1)NH3和NaClO反应⽣成肼、NaCl和⽔,根据得失电⼦守恒和原⼦守恒来配平⽅程式.(2)①依据盖斯定律计算的⽅法结合热化学⽅程式书写⽅法写出,标注物质聚集状态和反应焓变.②依据热化学⽅程式和盖斯定律计算得到热化学⽅程式,得到反应的焓变.本题考查了反应的书写、盖斯定律的应⽤和反应热的计算,难度不⼤,注意物质的状态的不同对反应热的影响.12. 解:(1)由1g碳与适量⽔蒸⽓反应⽣成CO和H2,需吸收10.94kJ热量,则1mol碳与⽔蒸⽓反应,吸收10.94KJ×12=131.28kJ,则此反应的热化学⽅程式为C(s)+H2O(g)=CO(g)+H2(g)△H=+131.28kJ?mol?1,故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.28kJ?mol?1;=0.0625mol,可知1molN2H4(l)在O2(g)中燃烧,⽣成N2(g)和H2O(g),放(2)根据2.0g的物质的量为:232出534.4kJ热量,热化学⽅程式为:N2H4(g)+O2(g)=N2(g)+2H2O△H=?534.4KJ/mol,故答案为:N2H4(g)+O2(g)=N2(g)+2H2O△H=?534.4KJ/mol;(3)2molAl(s)与适量O2(g)反应⽣成Al2O3(s),放出1669.8kJ热量,则4Al(s)+3O2(g)=2Al2O3(s)△H=?1669.8kJ?mol?1×2=? 3339.6kJ?mol?1,故答案为:4Al(s)+3O2(g)=2Al2O3(s)△H=?3339.6kJ?mol?1;=0.15mol,(4)2.3g某液态有机物和⼀定量的氧⽓混合点燃,恰好完全燃烧,⽣成2.7g⽔物质的量= 2.7g18g/mol=0.1mol,n(C)=0.1mol,n(H)=0.3mol,n(O)=2.24LCO2(标准状况)物质的量= 2.24L22.4L/mol2.3g?0.1mol×12g/mol?0.3mol×1g/mol=0.05mol,n(C):n(H):n(O)=0.1mol:0.3mol:0.05mol=2:6;1,16g/mol化学式为C2H6O,物质的量为0.05mol,并放出68.35kJ热量,1mol有机物燃烧放热1367KJ,热化学⽅程式为:C2H6O(l)+3O2(g)=2CO2(g)+3H2O(l)△H=?1367kJ/mol;故答案为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=?1367KJ/mol.(1)由1g碳与适量⽔蒸⽓反应⽣成CO和H2,需吸收10.94kJ热量,则1mol碳与⽔蒸⽓反应,吸收10.94KJ×12=131.28kJ,并注意物质的状态来解答;=0.0625mol,可知1molN2H4(l)在O2(g)中燃烧,⽣成N2(g)和H2O(g),放(2)根据2.0g的物质的量为:232出534.4kJ热量,据此书写热化学⽅程式;(3)2molAl(s)与适量O2(g)反应⽣成Al2O3(s),放出1669.8kJ热量,则4Al(s)+3O2(g)=2Al2O3(s)△H=1669.8kJmol1×2=3339.6kJmol1,由此分析解答;=0.15mol,(4)2.3g某液态有机物和⼀定量的氧⽓混合点燃,恰好完全燃烧,⽣成2.7g⽔物质的量= 2.7g18g/mol=0.1mol,n(C)=0.1mol,n(H)=0.3mol,n(O)=2.24LCO2(标准状况)物质的量= 2.24L22.4L/mol2.3g?0.1mol×12g/mol?0.3mol×1g/mol=0.05mol,n(C):n(H):n(O)=0.1mol:0.3mol:0.05mol=2:6;1,16g/mol化学式为C2H6O,物质的量为0.05mol,并放出68.35kJ热量,1mol有机物燃烧放热1367KJ,由此书写热化学⽅程式.本题主要考查了热化学⽅程式的书写,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学⽅程式前⾯的系数成正⽐.同时还考查了反应热的计算,题⽬难度不⼤.13. 解:Ⅰ.(1)容量瓶没有245mL规格的,只能⽤250mL规格的,需要称量NaOH固体m=nM=cVM=0.5mol/L×0.25L×40g/mol=5.0g,故答案为:5.0;(2)配制0.50mol/LNaOH溶液需要⽤到的玻璃仪器有烧杯、250mL容量瓶、胶头滴管和玻璃棒,故答案为:250mL容量瓶;胶头滴管;Ⅱ.(3)中和热测定实验成败的关键是保温⼯作,⼤⼩烧杯之间填满碎泡沫塑料的作⽤是减少实验过程中的热量损失;由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒;故答案为:减少实验过程中的热量损失;环形玻璃搅拌棒;= (4)①4次温度差分别为:3.4℃,6.1℃,3.3℃,3.5℃,第⼆组数据舍去,三次温度差平均值=3.4℃+3.3℃+3.5℃33.4℃,故答案为:3.4;(H2O)=②Q=△H=?△Tcm=?3.4°C×4.18J/(g?℃)×100g=1421.2J=1.42KJ/mol,△H=?QN56.8KJ/mol,故答案为:?56.8kJ?mol?1;③a.装置保温、隔热效果差,测得的热量偏⼩,中和热的数值偏⼩,故a正确;b.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏⼤,放出的热量偏⾼,中和热的数值偏⼤,故b错误;b.分多次把NaOH溶液倒⼈盛有硫酸的⼩烧杯中,热量散失较多,测得温度偏低,中和热的数值偏⼩,故c正确;b.温度计测定NaOH溶液起始温度后直接插⼊稀H2SO4测温度,硫酸的起始温度偏⾼,测得的热量偏⼩,中和热的数值偏⼩,故d正确,故答案为:acd;(5)反应放出的热量和所⽤酸以及碱的量的多少有关,并若⽤60mL0.25mol?L?1H2SO4溶液跟50mL0.55mol?L?1NaOH溶液进⾏反应,与上述实验相⽐,⽣成⽔的量增多,所放出的热量偏⾼,但是中和热的均是强酸和强碱反应⽣成1mol⽔时放出的热,中和热相等;⼜醋酸是弱酸,电离过程吸热,所以⽤50mL0.50mol?L?1醋酸代替H2SO4溶液进⾏上述实验,测得反应前后温度的变化值会减⼩,故答案为:不相等;相等;偏⼩.Ⅰ.(1)根据公式m=nM=cVM来计算氢氧化钠的质量,但是没有245mL的容量瓶;(2)需要⽤到的玻璃仪器有烧杯、容量瓶、胶头滴管和玻璃棒;Ⅱ.(3)中和热测定实验成败的关键是保温⼯作;根据量热计的构造来判断该装置的缺少仪器;(4)①先判断温度差的有效性,然后求出温度差平均值;②根据公式Q=△H=△Tcm来计算反应的焓变;③a.装置保温、隔热效果差,测得的热量偏⼩;b.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏⼤,放出的热量偏⾼;c.分多次把NaOH溶液倒⼊盛有硫酸的⼩烧杯中,热量散失较多;d.温度计测定NaOH溶液起始温度后直接插⼊稀H2SO4测温度,硫酸的起始温度偏⾼;(5)反应放出的热量和所⽤酸以及碱的量的多少有关,并根据中和热的概念和实质来回答.本题考查热中和热概念、测定原理及反应热的计算,题⽬难度⼤,注意理解中和热的概念以及测定反应热的误差等问题.。

化学反应原理期末测试题一、选择题(共16小题,每题3分,共48分,每题有一个选项符合题意)1.下列物质间的反应,其能量变化符合下图的是()A.铁与硫粉在加热条件下的反应B.灼热的碳与二氧化碳反应C.Ba(OH)2·8H2O晶体和NH4Cl晶体混合D.碳酸钙的分解2.已知:HCN(aq)与NaOH(aq)反应的ΔH=-12.1 kJ·mol-1;HCl(aq)与NaOH(aq)反应的ΔH=-55.6 kJ·mol-1。
则HCN在水溶液中电离的ΔH等于( )A.-67.7 kJ·mol-1 B.-43.5 kJ·mol-1C.+43.5 kJ·mol-1 D.+67.7 kJ·mol-13.在同温同压下,下列各组热化学方程式中△H1>△H2的是()A. 2H2(g)+O2(g)=2H2O(l);△H1;2H2(g)+O2(g)=2H2O(g);△H2B.S(g)+O2(g)=SO2(g);△H1; S(s)+O2(g)=SO2(g);△H2C.C(s)+1/2O2(g)=CO(g);△H1; C(s)+O2(g)=CO2(g);△H2D.H2(g)+Cl2(g)=2HCl(g);△H1; 1/2H2(g)+1/2Cl2(g)=HCl(g);△H2。
4、下列关于外界条件的改变对化学反应速率影响的说法正确的是( )A、升高温度能加快吸热反应的速率,减慢放热反应速率B、增大压强不能加快前后气体体积不变的反应的反应速率C、压强的改变只有通过浓度的改变才能影响化学反应速率D、若外界条件的改变引起了正、逆反应速率的改变,就一定能引起化学平衡放热移动5、下列说法正确的是( )A、焓变是指1mol物质参加反应时的能量变化B、当反应放热时△H>0,当反应吸热时△H<0C、在加热条件下发生的反应均为吸热反应D、一个化学反应中,当反应物的能量大于生成物的能量时,反应热△H为负值6、下列说法或表示方法正确的是( )A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多B、在稀溶液中,H+(aq)+OH-(aq)=H2O(l) △H= -57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJC、由C(s,石墨)=C(s,金刚石) △H= +1.90kJ/mol可知,石墨没有金刚石稳定D、在101kPa时,2g的氢气完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) △H= -285.8kJ/mol7.将4 mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生反应:2 A(g) +B(g) 2 C(g),经2s后测得C的浓度为0.6 mol·L-1,下列几种说法中正确的是()A.用物质A表示反应的平均速率为0.3 mol·L-1·s-1B.用物质B表示反应的平均速率为0.3 mol·L-1·s-1C.2 s时物质A的转化率为70%D.2 s时物质B的浓度为0.3 mol·L-18.如图为某化学反应的速率与时间的关系示意图。
细心整理第一章《化学反响与能量》单元测试题本试卷分选择题和非选择题两局部,共 7 页,总分值 150 分,考试用时 90 分钟。
可能用到的原子量:H1 C12N14O16S32第一局部选择题〔共 90 分〕一、选择题〔此题包括 10 小题,每题 4 分,共 40 分,每题只有一个选项符合题意〕 1.以下表达正确的选项是 A .电能是二次能源B.水力是二次能源 C .自然气是二次能源D.水煤气是一次能源2.以下说法正确的选项是A. 物质发生化学变化都伴随着能量变化 B .任何反响中的能量变化都表现为热量变化C .伴有能量变化的物质变化都是化学变化 D .即使没有物质的变化,也可能有能量的变化3. 将来能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。
以下属于将来能源标准的是①自然气②煤③核能④石油⑤太阳能⑥生物质能⑦风能⑧氢能A .①②③④B.⑤⑥⑦⑧C .③⑤⑥⑦⑧D.③④⑤⑥⑦⑧4. 以下各组热化学方程式中,△H >△H 的是①C(s)+O (g)===CO 1 (g)△H 2C(s)+O (g)===CO(g)△H22122②S(s)+O(g)===SO (g)△H S(g)+O (g)===SO (g)△H 221222③H (g)+O (g)===H O(l)△H 2H (g)+O (g)===2H O(l)△H22 2 1 2 2 2 2④CaCO (s)===CaO(s)+CO (g)△H CaO(s)+H O(l)===Ca(OH) (s)△H321222A .①B .④C .②③④D .①②③5. H 2(g)+Cl 2(g)=2HCl(g)△ H =―184.6kJ·mol -1,则反响 HCl(g)=H 2(g)+Cl 2(g)的△ H 为 A .+184.6kJ·mol -1B .―92.3kJ·mol -1 C .―369.2kJ·mol -1D .+92.3kJ·mol -16.以下反响中生成物总能量高于反响物总能量的是A .碳酸钙受热分解B .乙醇燃烧细心整理细心整理C.铝粉与氧化铁粉末反响D.氧化钙溶于水7.25℃、101kPa 下,2g 氢气燃烧生成液态水,放出 285.8kJ 热量,表示该反响的热化学方程式正确的选项是A.2H (g)+O (g)==2H O(1)△H=―285.8kJ/mol2 2 2B.2H (g)+O (g)==2H O(1)△H=+571.6kJ/mol2 2 2C.2H (g)+O (g)==2H O(g)△H=―571.6kJ/molD.H 2 (g)+O 2 (g)==H 2O(1)△H=―285.8kJ/mol2 2 28.氢气、一氧化碳、辛烷、甲烷的热化学方程式分别为:H (g)+O2(g)=H2O(l)△H=-285.8kJ/mol2CO(g)+O(g)=CO2(g)△H=-283.0kJ/mol 2C H (l)+25 O (g)=8CO (g)+9H O(l)△H=-5518kJ/mol8 18 2 2 2 2CH (g)+2O (g)=CO (g)+2H O(l)△H=-89.3kJ/mol4 2 2 2一样质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是A.H (g)B.CO(g)2C.C H (l)D.CH(g)8 18 49.热化学方程式:SO(g)+O2(g) SO2(g)△H=―98.32kJ/mol,在容器中充入32molSO2和 1molO2充分反响,最终放出的热量为A.196.64kJB.196.64kJ/molC.<196.64kJD.>196.64kJ10.:CH(g)+2O (g)==CO (g)+2H O(1)△H=―Q KJ/mol4 2 2 2 12H (g)+O (g)==2H O(g)△H=―Q KJ/mol2 2 2 22H (g)+O (g)==2H O(1)△H=―Q KJ/mol2 2 2 3常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L〔已折合成标准状况〕,经完全燃烧后恢复至常温,则放出的热量为多少KJA.0.4Q +0.05Q B.0.4Q +0.05Q1 3 1 2C.0.4Q +0.1Q D.0.4Q +0.1Q1 3 1 2二、选择题〔此题包括 10 小题,每题 5 分,共 50 分。
专题1 第一单元 化学反应中的热效应 第1次周练班级: 姓名:1、下列热化学方程式书写正确的是( )A.2SO 2+O 22SO 3 ΔH= -196.6 kJ·mol -1 B.H 2(g)+21O 2(g)====H 2O(l) ΔH= -285.8 kJ·mol -1 C.2H 2(g)+O 2(g)====2H 2O(l) ΔH= -571.6 kJD.C(s)+O 2(g)====CO 2(g) ΔH= +393.5 kJ·mol -12、已知充分燃烧a g 乙炔气体时生成1 mol 二氧化碳气体和液态水,并放出热量b kJ ,则乙炔燃烧的热化学方程式正确的是( )A.2C 2H 2(g)+5O 2(g) ====4CO 2(g)+2H 2O(l) ΔH= -4b kJ·mol -1B.C 2H 2(g)+25O 2(g) ====2CO 2(g)+H 2O(l) ΔH= -2b kJ·mol -1 C.2C 2H 2(g)+5O 2(g) ====4 CO 2(g)+2H 2O(l) ΔH= -2b kJ·mol -1D.2C 2H 2(g )+5O 2(g )====4CO 2(g )+2H 2O (l ) ΔH= b kJ·mol -13、热反应方程式中,化学式前的化学计量数表示的是( )A.分子个数B.原子个数C.物质质量D.物质的量4.在25 ℃、101 kPa 下,1 g 甲醇燃烧生成CO 2和液态水时放热22.68 kJ ,下列热化学方程式正确的是( )A.CH 3OH(l)+3/2O 2(g) ====CO 2(g)+2H 2O(l) ΔH=+725.8 kJ·mol -1B.2CH 3OH(l)+3O 2(g) ====2CO 2(g)+4H 2O(l) ΔH=-1 452 kJ·mol -1C.2CH 3OH (l )+3O 2(g )====2CO 2(g )+4H 2O (l ) ΔH=-725.8 kJ·mol -1D.2CH 3OH(l)+3O 2(g) ====2CO 2(g)+4H 2O(l) ΔH=+1 452 kJ·mol -15.下列各组热化学方程式中,化学反应的ΔH 前者大于后者的是( )①C (s )+O 2(g)====CO 2(g) ΔH 1 C(s)+ 21O 2(g) ====CO(g) ΔH 2 ②S(s)+O 2(g) ====SO 2(g) ΔH 3 S(g)+O 2(g) ====SO 2(g) ΔH 4③H 2(g)+ 21O 2(g) ====H 2O(l) ΔH 5 2H 2(g)+O 2(g) ====2H 2O(l) ΔH 6 ④CaCO 3(s)====CaO(s)+CO 2(g) ΔH 7 CaO(s)+H 2O(l) ====Ca(OH)2(s) ΔH 8A.①B.④C.②③④D.①②③6.沼气是一种能源,它的主要成分是CH 4。
化学选修四课后习题及答案公司内部档案编码:[OPPTR-OPPT28-OPPTL98-OPPNN08]化学选修4 化学反应原理课后习题和答案第一章 化学反应与能量 第一节 化学反应与能量的变化P5习题1.举例说明什么叫反应热,它的符号和单位是什么2.用物质结构的知识说明为什么有的反应吸热,有的反应放热。
3.依据事实,写出下列反应的热化学方程式。
(1)1 mol N 2 (g)与适量H 2(g )起反应,生成NH 3(g ),放出 kJ 热量。
(2)1 mol N 2 (g)与适量O 2(g )起反应,生成NO 2(g ),吸收68 kJ 热量。
(3)1 mol Cu(s)与适量O 2(g )起反应,生成CuO (s ),放出157 kJ 热量。
(4)1 mol C(s)与适量H 2O (g )起反应,生成CO (g )和H 2 (g),吸收 kJ 热量。
(5)卫星发射时可用肼(N 2H 4)作燃料,1 mol N 2H 4(l)在O 2(g )中燃烧,生成N 2(g )和H2O (l ),放出622 kJ 热量。
(6)汽油的重要成分是辛烷(C 8H18),1 mol C 8H18 (l)在O 2(g )中燃烧,生成CO 2(g )和H 2O (l ),放出5 518 kJ 热量。
4.根据下列图式,写出反应的热化学方程式。
P 6习题1.举例说明什么叫反应热,它的符号和单位是什么1、化学反应过程中所释放或吸收的热量叫做反应热。
恒压条件下,它等于反应前后物质的焓变。
、符号是ΔH 、单位是kJ/mol 或kJmol -1 。
例如1molH 2(g )燃烧,生成1molH 2O (g ),其反应热ΔH =-mol 。
2.用物质结构的知识说明为什么有的反应吸热,有的反应放热。
2、化学反应的实质就是反应物分子中化学键断裂,形成新的化学键,重新组合成生成物的分子。
旧键断裂需要吸收能量,新键形成要放出能量。
绝密★启用前人教版高中化学选修四第一章化学反应与能量练习题本试卷分第Ⅰ卷和第Ⅱ卷两部分,共100分第Ⅰ卷一、单选题(共15小题,每小题4.0分,共60分)1.在1200 ℃时,天然气脱硫工艺中会发生下列反应①H2S(g)+O2(g)===SO2(g)+H2O(g)ΔH1②2H2S(g)+SO2(g)===S2(g)+2H2O(g)ΔH2③H2S(g)+O2(g)===S(g)+H2O(g)ΔH3④2S(g)===S2(g)ΔH4则ΔH4的正确表达式为()A.ΔH4=(ΔH1+ΔH2-3ΔH3)B.ΔH4=(3ΔH3-ΔH1-ΔH2)C.ΔH4=(ΔH1+ΔH2-3ΔH3)D.ΔH4=(ΔH1-ΔH2-3ΔH3)2.25 ℃、101 kPa下,C、H2、CH4和CH3OH等几种燃料的热值(指一定条件下单位质量的物质完全燃烧所放出的热量)依次是33 kJ·g-1、143 kJ·g-1、56 kJ·g-1、23 kJ·g-1。
则下列热化学方程式正确的是()A. C(s)+O2(g)===CO(g)ΔH=-396 kJ·mol-1B. CH4(g)+2O2(g)===CO2(g)+2H2O(l)ΔH=-896 kJ·mol-1C. 2H2(g)+O2(g)===2H2O(l)ΔH=-286 kJ·mol-1D. CH3OH(l)+O2(g)===CO2(g)+2H2O(l)ΔH=736 kJ·mol-13.科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。
已知断裂1 mol N—N键吸收193 kJ热量,断裂1 mol N≡N键吸收941 kJ热量,则()A. N4的熔点比P4高B. 1 mol N4气体转化为N2时要吸收724 kJ能量C. N4是N2的同系物D. 1 mol N4气体转化为N2时要放出724 kJ能量4.下列说法不正确的是()A.燃烧不一定有火焰产生B.物质跟氧气的反应就是燃烧C.物质在有限的空间内燃烧,可能会引起爆炸D.物质燃烧的剧烈程度与氧气的浓度有关5.关于能源,以下说法不正确的是()A.煤、石油、天然气等燃料属于不可再生能源B.煤、石油、水煤气可从自然界直接获取,属于一级能源C.太阳能是一级能源、新能源、可再生能源D.潮汐能来源于月球引力做功6.已知热化学方程式2H2(g)+O2(g)====2H2O(l)ΔH1=-571.6 kJ·,则关于热化学方程式2H2O(l)====2H2(g)+ O2(g)ΔH2=?的说法正确的是()A.热化学方程式中化学计量数表示分子数B.该反应ΔH2大于零C.该反应ΔH2=﹣571.6 kJ·D.该反应与上述反应属于可逆反应7.在下列能源中,属于化石能源的是()A.核能、生物质能、水能B.电能、汽油、柴油C.太阳能、地热能、风能D.煤、石油、天然气8.已知下列反应的反应热:①CH3COOH(l)+2O2(g)====2CO2(g)+2H2O(l)ΔH1=﹣870.3 kJ·③ C(s)+O2(g)====CO2(g)ΔH2=﹣393.5 kJ·④ H2(g)+O2(g)====H2O(l)ΔH3=﹣285.8 kJ·则2C(s)+2H2(g)+O2(g)====CH3COOH(l)的反应热为()A.﹣870.3 kJ·B.﹣571.6 kJ·C. +787.0 kJ·D.﹣488.3 kJ·9.用CH4催化还原NO X可以消除氮氧化物的污染,例如:①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)ΔH1① CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH2=﹣1 160 kJ•mol﹣1。
第一章《化学反应与能量》测试题原子量:H-1 O-16 C=12 Al-27 N-14 Ca- 40 V-51 Ni- 59 Cu-64一、单项选择题(每小题3分,共24分)1.下列反应属于吸热反应的是( )A. C 6H 12O 6(葡萄糖aq)+6O 2 6CO 2+6H 2OB. CH 3COOH+KOH CH 3COOK+H 2OC. 反应物的总能量大于生成物的总能量D .破坏反应物全部化学键所需能量大于破坏生成物全部化学键所需能量2.下列说法正确的是( )A .热化学方程式中,如果没有注明温度和压强,则表示反应热是在标准状况下测得的数据B .升高温度或加入催化剂,可以改变化学反应的反应热C .据能量守恒定律,反应物的总能量一定等于生成物的总能量D .物质发生化学变化一定伴随着能量变化3.下列各组热化学方程式中,△H 1>△H 2的是①C(s)+O 2(g)===CO 2(g) △H 1 C(s)+12O 2(g)===CO(g) △H 2②S(s)+O 2(g)===SO 2(g) △H 1 S(g)+O 2(g)===SO 2(g) △H 2③H 2(g)+12O 2(g)===H 2O(l) △H 1 2H 2(g)+O 2(g)===2H 2O(l) △H 2④CaCO 3(s)===CaO(s)+CO 2(g) △H 1 CaO(s)+H 2O(l)===Ca(OH)2(s) △H 2A .①B .②③④C .④D .①②③4. 已知H 2(g)+Cl 2(g)=2HCl(g) △H =―184.6kJ·m ol -1, 则反应HCl(g)=12H 2(g)+12Cl 2(g)的△H 为A .+184.6kJ·mol -1B .―92.3kJ·mol -1C .+92.3kJ·mol -1D .―369.2kJ·mol -15. 已知:(1)Zn (s )+12O 2(g )=== ZnO(s) ΔH= -348.3 kJ·mol -1,(2)2Ag(s)+ 12O 2(g )=== Ag 2O(s) ΔH= -31.0 kJ·mol -1,酶则Zn (s )+ Ag 2O(s) === ZnO(s)+ 2Ag(s)的ΔH 等于( )A . -317.3 kJ·mol -1B . -379.3 kJ·mol -1C .-332.8 kJ·mol -1D .317.3 kJ·mol -16. SF 6是一种优良的绝缘气体,分子结构中只存在S-F 键。
化学选修4《化学反应原理》课后习题和答案第一章化学反应与能量第二章第一节化学反应与能量的变化P5习题1.举例说明什么叫反应热,它的符号和单位是什么?2.用物质结构的知识说明为什么有的反应吸热,有的反应放热。
3.依据事实,写出下列反应的热化学方程式。
(1)1 mol N2 (g)与适量H2(g)起反应,生成NH3(g),放出92.2 kJ热量。
(2)1 mol N2 (g)与适量O2(g)起反应,生成NO2(g),吸收68 kJ热量。
(3)1 mol Cu(s)与适量O2(g)起反应,生成CuO(s),放出157 kJ热量。
(4)1 mol C(s)与适量H2O(g)起反应,生成CO(g)和H2 (g),吸收131.3 kJ热量。
(5)卫星发射时可用肼(N2H4)作燃料,1 mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出622 kJ热量。
(6)汽油的重要成分是辛烷(C8H18),1 mol C8H18 (l)在O2(g)中燃烧,生成CO2(g)和H2O(l),放出5 518 kJ热量。
4.根据下列图式,写出反应的热化学方程式。
P6习题1.举例说明什么叫反应热,它的符号和单位是什么?1、化学反应过程中所释放或吸收的热量叫做反应热。
恒压条件下,它等于反应前后物质的焓变。
、符号是ΔH、单位是kJ/mol或kJ•mol-1。
例如1molH2(g)燃烧,生成1molH2O(g),其反应热ΔH=-241.8kJ/mol。
2.用物质结构的知识说明为什么有的反应吸热,有的反应放热。
2、化学反应的实质就是反应物分子中化学键断裂,形成新的化学键,重新组合成生成物的分子。
旧键断裂需要吸收能量,新键形成要放出能量。
当反应完成时,若生成物释放的能量比反应物吸收的能量大,则此反应为放热反应;若生成物释放的能量比反应物吸收的能量小,反应物需要吸收能量才能转化为生成物,则此反应为吸热反应。
P10习题1、燃烧热数据对生产、生活有什么实际意义?1、在生产和生活中,可以根据燃烧热的数据选择燃料。
化学反应与能量综合训练题一选择题(每小题只有一个正确答案)1 下列与化学反应能量变化相关的叙述正确的是A ΔH ﹥0表示放热反应,ΔH ﹤0表示吸热反应B 热化学方程式的化学计量数可以表示分子数或原子数,因此必须是整数C 根据盖斯定律,可计算某些难以直接测量的反应热D 同温同压下,22()()2()H g Cl g HCl g +=在光照和点燃条件的H ∆不同2. 右图是一个一次性加热杯的示意图。
当水袋破裂时,水与固体碎块混和,杯内食物温度逐渐上升。
制造此加热杯可选用的固体碎块是( )A .硝酸铵B .生石灰C .氯化镁D .食盐3、下列反应中生成物总能量高于反应物总能量的是A .碳酸钙受热分解B .乙醇燃烧C .铝粉与氧化铁粉末反应D .氧化钙溶于水4.同温同压下,已知下列各反应为放热反应,下列热化学方程式中反应热数值最小的是( )A 、2A ( l ) +B ( l ) = 2C (g ) △H 1 B 、2A ( g ) + B ( g ) = 2C (g ) △H 2C 、2A ( g ) + B ( g ) = 2C ( l ) △H 3D 、2A ( l ) + B ( l ) = 2C ( l ) △H 45. 25 ℃,101 k Pa 时,强酸与强碱的稀溶液发生中和反应的中和热为 57.3 kJ/mol ,辛烷的燃烧热为5518 kJ/mol 。
下列热化学方程式书写正确的是( )A.2H +(aq) +24SO -(aq)+2Ba +(aq)+2OH -(aq)=BaSO 4(s)+2H 2O(1) ∆H=-57.3 kJ/mol B.KOH(aq)+12H 2 SO 4(aq)= 12K 2SO 4(aq)+H 2O(I) ∆H=-57.3kJ/mol C.C 8H 18(I)+ 252 O 2 (g)=8CO 2 (g)+ 9H 2O(g) ∆H=-5518 kJ/mol D.2C 8H 18(g)+25O 2 (g)=16CO 2 (g)+18H 2O(1) ∆H=-5518 kJ/mol6. 下列热化学方程式书写正确的是(H ∆的绝对值均正确)( )A .C 2H 5OH (l )+3O 2(g )==2CO 2(g )+3H 2O (g ) △H=—1367.0 kJ/mol (燃烧热)B .NaOH (aq )+HCl (aq )==NaCl (aq )+H 2O (l ) △H=+ 57.3kJ/mol (中和热)C .S (s )+O 2(g )===SO 2(g ) △H=—269.8kJ/mol (反应热)D .2NO 2 == O 2 + 2NO △H=+116.2kJ/mol (反应热)7. 下列各组热化学方程式中,化学反应的△H 前者大于后者的是( )①C(s)+O 2(g)=CO 2(g);△H 1C(s)+1/2O 2(g)=CO(g);△H 2 ②S(s)+O 2(g)=SO 2(g);△H 3S(g)+O 2(g)=SO 2(g);△H 4 ③H 2(g)+1/2O 2(g)=H 2O(l);△H 52H 2(g)+O 2(g)=2H 2O(l);△H 6 ④CaCO 3(s)=CaO(s)+CO 2(g);△H 7 CaO(s)+H 2O(l)=Ca(OH)2(s);△H 8A .①B .④C .②③④D .①②③8. 已知:2H2(g)+ O2(g)=2H2O(l) ΔH= -571.6KJ· mol-1CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH= -890KJ· mol-1现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695KJ,则原混合气体中H2与CH4的物质的量之比是( )A.1∶1 B.1∶3 C.1∶4 D.2∶39. 下列有关热化学方程式及其叙述正确的是()。
A.氢气的燃烧热为285.5 kJ·mol-1,则水分解的热化学方程式为:2H2O(l)==2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1B.已知2C(石墨,s)+O2(g)===2CO(g)ΔH=-221 kJ·mol-1,则石墨的燃烧热ΔH= -110.5 kJ·mol-1C.已知N2(g)+3H2(g)2NH3(g)ΔH=-92.4 kJ·mol-1,则在一定条件下将1 mol N2和3 mol H2置于一密闭容器中充分反应后,可放出92.4 kJ的热量D.已知乙醇和乙烯的燃烧热ΔH分别为-1 366.8 kJ·mol-1和-1 411.0 kJ·mol-1,则乙烯水化制乙醇的热化学方程式为C2H4(g)+H2O(l)===C2H5OH(l) ΔH=-44.2 kJ·mol-1 10. 25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是( )A.C(s)+ 1/2 O2(g)=CO(g) △H= ―393.5 kJ/molB.2H2(g)+O2(g)=2H2O(l) △H= +571.6 kJ/molC.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= ―890.3 kJ/molD.C6H12O6(s) +6O2(g)=6CO2(g)+6H2O(l) △H=―2800 kJ/mol11.已知热化学方程式:SO2(g)+ 1/2 O2(g) SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )A.196.64kJ B.196.64kJ/mol C.<196.64kJ D.>196.64kJ12、根据下列热化学方程式分析,C(s)的燃烧热△H等于()C(s) + H2O(l) === CO(g) + H2(g) △H1=+175.3k J·mol—12CO(g) + O2(g) == 2CO2(g) △H2=—566.0 k J·mol—12H2(g) + O2(g) == 2H2O(l) △H3=—571.6 k J·mol—1A. △H1 + △H2—△H3B.2△H1 + △H2 + △H3C. △H1 + △H2/2 + △H3D. △H1 + △H2/2+ △H3/213、将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如右图所示(实验中始终保持V 1+V2=50mL)。
下列叙述正确的是()A.做该实验时环境温度为22℃B.该实验表明化学能可能转化为热能C.NaOH溶液的浓度约为1.0mol/LD.该实验表明有水生成的反应都是放热反应14.强酸与强碱在稀溶液中发生中和反应的热化学方程式为H+(aq)+OH-(aq)===H2O(l)ΔH =-57.3 kJ·mol-1,向3份同体积0.2 mol ·L-1的NaOH溶液中分别加入适量的稀醋酸、浓硫酸、稀硝酸,恰好完全反应的热效应ΔH1、ΔH2、ΔH3的关系正确的是()A.ΔH1>ΔH2>ΔH3B.ΔH1>ΔH3>ΔH2C.ΔH2>ΔH1>ΔH3D.ΔH2>ΔH3>ΔH115、单斜硫和正交硫转化为二氧化硫的能量变化图如右,下列说法正确的是( )A、S(s,单斜) = S(s,正交) △H = +0.33kJ·mol -1B、正交硫比单斜硫稳定C、相同物质的量的正交硫比单斜硫所含有的能量高D、①式表示断裂lmol O2中的共价键所吸收的能量比形成1mol SO2中的共价键所放出的能量少297.16kJ16.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ·mol-1②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9kJ·mol-1下列说法正确的是()A.CH3OH的燃烧热为192.9kJ·mol-1B.反应①中的能量变化如右图所示C.CH3OH转变成H2的过程一定要吸收能量D.根据②推知反应CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)所放出的热量小于192.9kJ·mol-1。
17、白磷与氧可发生如下反应:P4+5O2== P4O10。
已知断裂下列化学键需要吸收的能量分别为:P-P:a kJ·mol-1、P-O:b kJ·mol-1、P=O:c kJ·mol-1、O=O:d kJ·mol-1,根据图示的分子结构和有关数据估算该反应的 H,其中正确的是A. (6a+5d-4c-12b) kJ·mol-1B. (4c+12b-6a-5d) kJ·mol-1C. (4c+12b-4a-5d) kJ·mol-1D. (4a+5d-4c-12b) kJ·mol-118.下列反应既属于氧化还原反应,又属于吸热反应的是( )。
A.锌粒与稀硫酸的反应B.灼热的木炭与CO2的反应C.甲烷在空气中燃烧的反应 D.Ba(OH)2 •8H2O晶体与NH4Cl晶体的反应19.已知可逆反应2SO2+O2SO3,当生成2mol SO3时放出热量为Q,现将1mol SO2和0.5mol O2在相同条件下反应生成SO3,放出的热量为Q1,则() A.Q1=21Q B.Q1<2 1 Q C.2Q1>Q D.无法判断二填空题18.红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。
反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
根据上图回答下列问题:(1)P和Cl2反应生成PCl3的热化学方程式。
(2)PCl5分解成PCl3和Cl2的热化学方程式:_________________________________ ,(3)P和Cl2分两步反应生成1molPCl5的△H3= _________,P和Cl2一步反应生成1molPCl5的△H4______ △H3(填“大于”、“小于”或“等于”)。
19. 50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在图示的装置中进行中和反应。
通过测定反应过程中所放出的热量可计算中和热。