二烯烃和共轭体系
- 格式:ppt
- 大小:595.00 KB
- 文档页数:34



第四章 二烯烃和共轭体系思考题习题4.1 下列化合物有无顺反异构体?若有,写出其构型式并命名。
(P119)(1) 1,3-戊二烯 CH 2=CH CH=CHCH 3解:有2个顺反异构体!C=CCH 3HCH 2=CHHC=CH CH 3CH 2=CHH(Z)- 1,3-戊二烯 (E)- 1,3-戊二烯(2) 2,4,6-辛三烯 CH 3CH=CH CH=CH CH=CHCH 3 解:有6个顺反异构体!C=C C=CHC=C HH CH 3H H CH 3HC=C C=CHC=C HCH 3HH H CH 3HC=CC=C H C=CHCH 3HCH 3H HH(Z,Z,Z)- 2,4,6-辛三烯 (Z,Z,E)- 2,4,6-辛三烯 (E,Z,E)- 2,4,6-辛三烯C=CC=C C=C HHHH CH 3CH 3H HC=CC=CC=C H HCH 3HHH HCH 3C=CC=C C=C HHCH 3H HCH 3H H(E,E,E)- 2,4,6-辛三烯 (E,E,Z)- 2,4,6-辛三烯 (Z,E,Z)- 2,4,6-辛三烯习题4.2 下列各组化合物或碳正离子或自由基哪个较稳定?为什么?(P126)(1) 3-甲基-2,5-庚二烯 和 5-甲基-2,4-庚二烯√CH 3CH=CCH 2CH=CHCH 3CH 3CH 3CH=CHCH=CCH 2CH 3CH 3π-π共轭无π-π共轭有(2)(CH 3)2C=CHCH 2CH 3CH=CHCH 2CH 2=CHCH 2、和(CH 3)2C=CHCH 2CH 3CH=CHCH 2CH 2=CHCH 26个超共轭σ-H 3个超共轭σ-H 0个超共轭σ-H 稳定性:>>(3)(CH 3)2CHCHCH=CH 2(CH 3)2CCH 2CH=CH 2(CH 3)2CCH 2CH 3、和 (CH 3)2CHCHCH=CH 2(CH 3)2CCH 2CH=CH 2(CH 3)2CCH 2CH 3稳定性:>>有p -π共轭p -π共轭无p -π共轭无给电子性:CH 3CH=CH 2>(4)、和CH 2CH=CHCH=CH 2CH 2CH=CHCH 2CH 3CH 3CHCH 2CH=CH 2稳定性:>>有π-π共轭CH 2CH=CHCH=CH 2CH 2CH=CHCH 2CH 3CH 3CHCH 2CH=CH 2p -π有共轭π-π无共轭π-π无共轭p -π有共轭p -π共轭无 (5)3 , (CH 3)22 , CH 32CH 3 和 (CH 3)3甲基自由基 一级自由基 二级自由基 三级自由基(6)(CH 2CH=CH)2, CH 22 和 CH 35个sp 2杂化碳共轭 3个sp 2杂化碳共轭 成单电子不在p 轨道上,不参与共轭共轭程度更大共轭程度相对较小习题4.3 解释下列事实:(P126)(1)CH 3CH 2CH=CHCH 3CH 3CH 2CH 2CHCH 3CH 3CH 2CHCH 2CH 3HCl+(主)(次)稳定性:>CH 3CH 2CHCH 2CH 3CH 3CH 2CH 2CHCH 3(2)CH 33CH 3CH 3CH 2CCH 3CH 3CH 3CHCHCH 3CH 3+HCl(主)(次)稳定性:>CH 3CH 2CCH 3CH 3CH 3CHCHCH 3CH 3(3)+HBr , 过氧化苯甲酰o(96%)(4%)CH 3CH=CH 2CH 3CH 2CH 2Br CH 3CHCH 3>稳定性:CH 32Br CH 3CHCH 2BrCH 3CH=CH 2CH 3CHCH 2Br CH 3CHCH 2BrPhCOOH + BrPhCOO+(过氧化苯甲酰)2PhCOOPhCO OCPh O O机理:... ...习题4.4 什么是极限结构?什么是共振杂化体?一个化合物可以写出的极限结构式增多标志着什么?(P130)解:极限结构——对真实结构有贡献,但不能完全代表真实结构的经典结构式;共振杂化体——由若干个极限结构式表示的该化合物的真实结构。

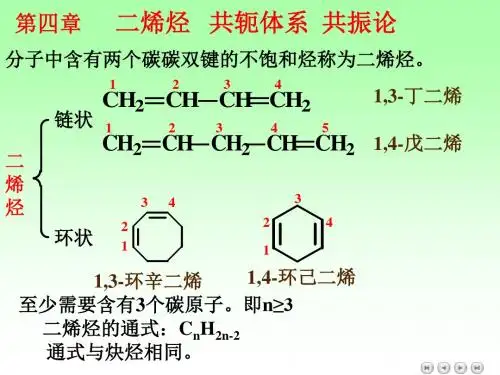
一二烯烃分子中含有不止一个双键的开链烃,按照双键数目的多少,分别叫做二烯烃,三烯烃.....至多烯烃等。
其中以二烯烃最为重要。
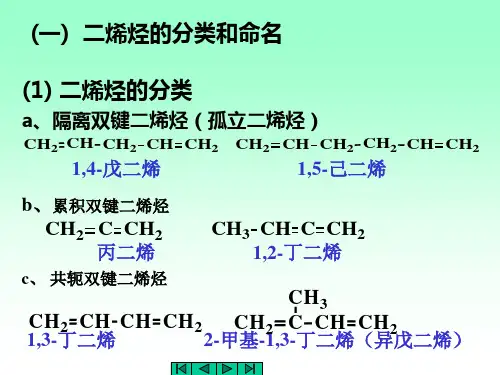
而根据二烯烃中双键位置的不同,又可以分为三类:a 累积二烯烃:两个双键连接在同一个碳原子上。
B 共轭二烯烃:两个双键之间,有一个单键相隔。
C 隔离二烯烃:两个双键之间,有两个或以上的单键相隔。
在这里主要介绍共轭二烯烃的性质。
1共轭二烯烃的结构以及共轭效应:1,3—丁二烯是最简单的共轭二烯烃,下面就以它为例来说明共轭二烯烃的结构。
在丁二烯分子中,四个碳原子和六个氢原子都处在同一个平面上。
其每一个碳原子都是sp2杂化,它们以sp2杂化轨道与相邻的碳原子相互交盖形成碳碳单键,与氢原子的1S轨道形成碳氢单键。
分子中一共形成了三个碳碳单键和六个碳氢单键,sp2杂化碳原子的三个σ键指向三角形的三个顶点,三个σ键相互之间的夹角都接近120°。
由于每一个碳原子的σ键都排列在一个平面上,所以就形成了分子中所有σ键都在一个平面的结构,此外,每一个碳原子都有一个未参与杂化的p轨道,它们都和丁二烯分子所在的平面垂直,因此这四个p轨道互相平行,在四个碳原子之间都有电子云交盖,从而电子也并不固定在两个原子之间,从而发生离域。
也就是说四个电子在四个原子轨道形成的共轭体系中流动,并不固定在某一位置。
2 共轭二烯烃的性质A 1,2—加成和1,4—加成共轭二烯烃和卤素,氢卤酸等都容易发生亲电加成,但可产生两种加成产物,如下所示:(1,2—加成产物和1,4—加成产物的键线式)1,2—加成产物是一分子试剂在同一个双键的两个碳原子上的加成,而1,4—加成产物则是一分子试剂加载共轭双键的两端碳原子上,同时原来的双键变为单键,而双键之间的单间变为双键。
1,3—丁二烯之所以有这两种加成方式,与其共轭结构有密切关系。
下面以溴化氢与丁二烯的加成来说明这一原理。
丁二烯与溴化氢的加成第一步也是H+的进攻,加成反应可能发生在C(1)或者C(2)上,然后生成相应的碳正离子(I)和(II)对于这两种碳正离子来说,双键上的碳原子,以及带有正电荷(在键线式中所表达出来的)的碳原子都是sp2杂化,而在(I)碳正离子中,三个碳原子剩余的p轨道均平行于三个碳原子锁组成的平面,因此它们之间存在共轭效应,从而正电荷并不只是单纯的聚集在同一个碳原子上,电荷因共轭效应而被分配到三个碳原子上,并且在C(2)和C(4)上的正电荷相对较多,从而分子比较稳定,生成(I)碳正离子所需要的活化能相对更低,而(II)碳正离子则没有共轭效应,因此反应总是向着(I)碳正离子的方向进行。