初中九年级化学教学双向细目表汇总
- 格式:doc
- 大小:880.50 KB
- 文档页数:19
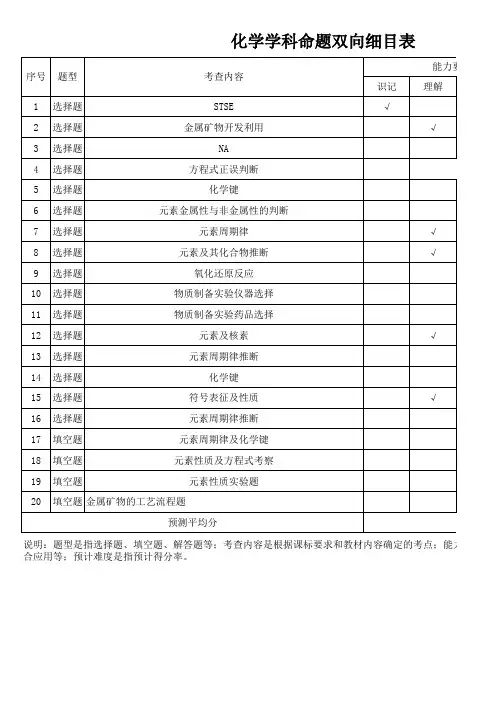
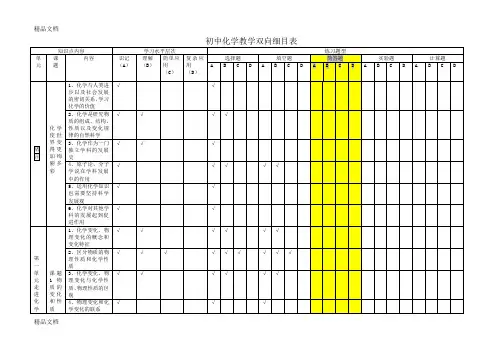
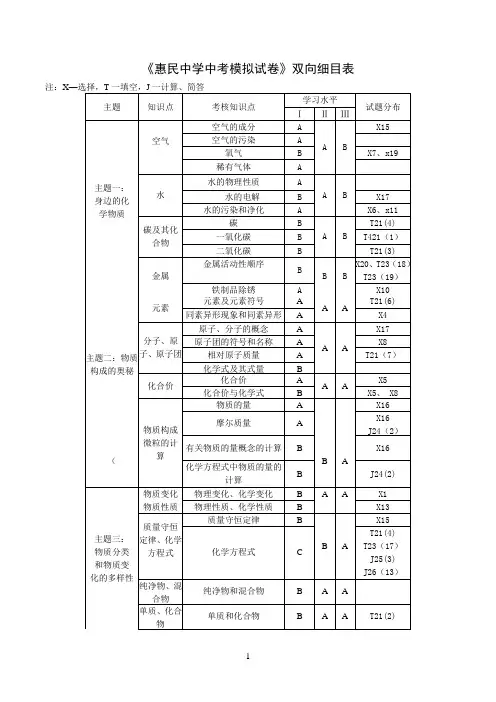
《惠民中学中考模拟试卷》双向细目表注:X—选择,T一填空,J一计算、简答主题知识点考核知识点学习水平试题分布ⅠⅡⅢ主题一:身边的化学物质空气空气的成分 AA BX15空气的污染 A氧气 B X7、x19稀有气体 A水水的物理性质 AA B水的电解 B X17水的污染和净化 A X6、x11碳及其化合物碳 BA BT21(4)一氧化碳 B T421(1)二氧化碳 B T21(3)金属金属活动性顺序BB BX20、T23(18)T23(19)铁制品除锈 A X10主题二:物质构成的奥秘元素元素及元素符号 AA AT21(6) 同素异形现象和同素异形 A X4分子、原子、原子团原子、分子的概念 AA AX17 原子团的符号和名称 A X8相对原子质量 A T21(7)化学式及其式量 B化合价化合价 AA AX5化合价与化学式 B X5、 X8物质构成微粒的计算物质的量 A X16摩尔质量 AX16J24(2)(有关物质的量概念的计算 BB AX16 化学方程式中物质的量的计算B J24(2)主题三:物质分类和物质变化的多样性物质变化物质性质物理变化、化学变化 B A A X1物理性质、化学性质 B X13 质量守恒定律、化学方程式质量守恒定律 BB AX15化学方程式 CT21(4)T23(17)J25(3)J26(13)纯净物、混合物纯净物和混合物 B A A单质、化合物单质和化合物 B A A T21(2)氧化物、酸、碱、盐氧化物 BA AT25(5)盐酸 B J24硫酸 B X10 氢氧化钠 B X18氢氧化钙 B T23(16)常见的盐 B X20、J26 酸碱盐的溶解性 A J26(11)(12)有机化合物有机化合物的概念 AA AX3 几种常见的有机化合物 A化学反应的类型化合、分解、置换、复分解(含中和)BA AX9 氧化还原反应 A T26(1)主题四:溶液物质的溶解水的分散性 AB AX2物质溶解的过程 A T22(14)(15)浊液 A溶液、溶质、溶剂 B X2饱和溶液、不饱和溶液 B T22(9)溶解度固体物质溶解度的概念 AB AT22(12) 影响物质溶解度的因素 B T22(10)(11)关于溶解度的计算 C T22(12)(13) 结晶、结晶水合物晶体和结晶 A A A X22结晶水和结晶水合物 A X14溶液中溶质的质量分数溶液中溶质的质量分数 BA AX12 有关溶液中溶质质量分数的计算C溶液的酸碱性溶液的pH AA AX6酸碱指示剂 A主题五:化学和生活家用燃料常见的家用燃料 AB BX17燃料的充分燃烧 B化肥化肥的分类 AA B氮肥 A焰火焰色反应 AA BJ26(10)焰色反应的应用 B J26(10)主题六:化学实验活动气体的制备氧气的实验室制法 BB BT25(3)(4)二氧化碳的实验室制法 B J25(9)简易启普发生器 B J25(6)(7)(8)物质的性质金属活动性 BB AT22(18)稀硫酸的化学性质 B X10物质的分离过滤 BB AX11 结晶 B物质的检验盐酸、硫酸的鉴别. BB A碳酸盐的检验 B J26(12)溶液酸碱性的检验 B X6。
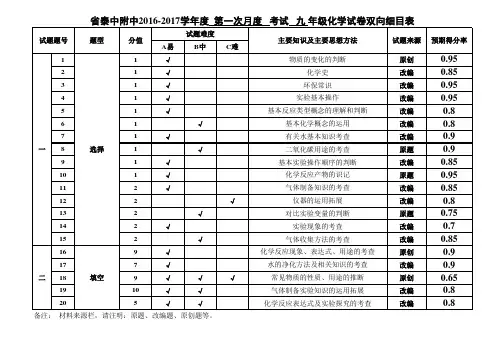
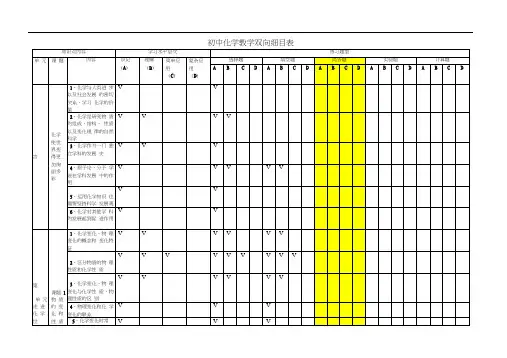
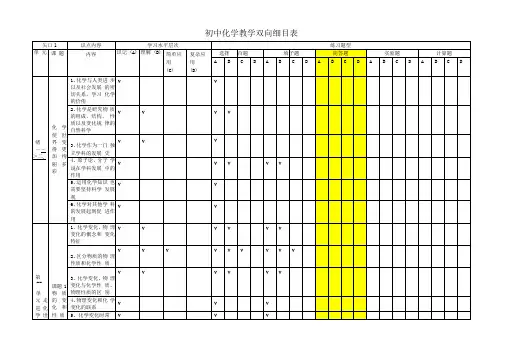
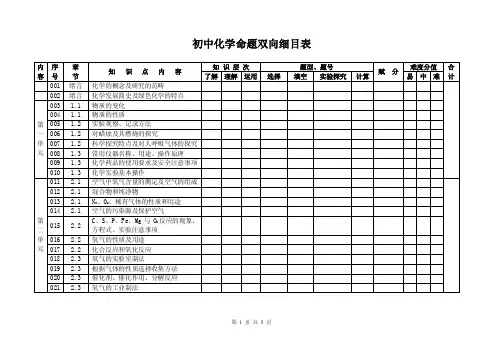



化学双向细目表《化学双向细目表之化学式》同学们,今天咱们来好好唠唠化学式这个事儿。
化学式就像是化学世界里每个物质的“身份证”,它能告诉咱们这个物质是由啥组成的。
先说说化学式里的元素符号吧。
这元素符号就像每个原子的名字,比如H代表氢原子,O代表氧原子。
那原子们是怎么凑在一起组成分子或者化合物的呢?这就涉及到化学键啦。
化学键就好比是原子之间的小钩子。
离子键呢,就像是带正电和负电的原子像超强磁铁般吸在一起。
比如说氯化钠(NaCl),钠原子(Na)容易失去一个电子变成带正电的钠离子(Na⁺),氯原子(Cl)容易得到一个电子变成带负电的氯离子(Cl⁻),这一正一负就像磁铁的两极,吸得死死的,这就是离子键。
共价键呢,就是原子共用小钩子连接。
就像两个人共同拿着一个东西,互相牵制着。
比如说氢气(H₂),两个氢原子各自拿出一个小钩子(电子)来共用,这样就形成了共价键,组成了氢气分子。
那在化学的世界里啊,还有一个很有趣的概念叫化学平衡。
这化学平衡呢,咱们可以把它比作拔河比赛。
反应物和生成物就像两队人。
在拔河开始的时候,两边的力量不一样,可能反应物这边力量大,反应就朝着生成物的方向进行得快。
但是随着反应进行,生成物这边的力量慢慢增加,反应物这边力量慢慢减小。
直到最后达到一种状态,就是正逆反应速率相等,就像两队人谁也拉不动谁了,这时候浓度也不再变化了,这就是化学平衡。
咱们再说说分子的极性。
这分子的极性就类似小磁针。
比如说水(H₂O),它是极性分子。
氧一端就像磁针南极带负电,氢一端就像北极带正电。
你看水分子的形状是弯弯的,就像小磁针有两端不同的极性。
而二氧化碳(CO₂)呢,它是直线对称的,就像一个两边一样重的哑铃,是个非极性分子。
还有配位化合物,这就像一场聚会。
中心离子就是聚会的主角,配体呢就是提供孤对电子共享的小伙伴。
比如说在[Cu(NH₃)₄]²⁺这个配位化合物里,铜离子(C u²⁺)就是主角,氨分子(NH₃)就是小伙伴,氨分子把自己的孤对电子拿出来和铜离子共享,就形成了这样一个配位化合物。
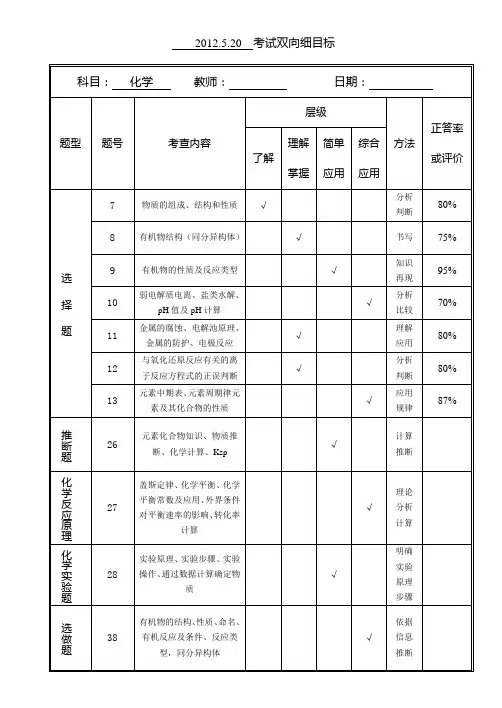
九年级化学知识点细目表化学是一门研究物质及其变化的科学。
无论是在学校还是在日常生活中,我们都会接触到各种各样的化学现象和化学物质。
九年级是化学学习的关键年级,下面将给大家列举九年级化学的知识点细目表,帮助大家系统地学习和掌握化学的基本知识。
第一章:物质的分类与性质1.1 物质的分类- 纯净物和混合物的定义及区别- 纯物质的分类:元素和化合物- 混合物的分类:均质混合物和非均质混合物1.2 物质的性质- 物质的物理性质:颜色、密度、熔点、沸点等- 物质的化学性质:与其他物质发生反应的能力第二章:常见物质的性质与应用2.1 金属与非金属- 金属的性质:导电性、导热性、延展性、塑性等- 金属的应用:铜、铁、铝等2.2 矿石与冶金- 矿石的定义及分类- 冶金的基本原理及步骤- 矿石中的常见金属:铁、铜、铝等2.3 化学肥料与农业- 化学肥料的分类及应用- 化学肥料对植物生长的影响第三章:化学反应3.1 化学方程式- 化学反应的基本概念与表达方式- 平衡反应方程式的平衡条件3.2 反应速率- 反应速率的定义及影响因素- 反应速率与化学平衡的关系3.3 氧化还原反应- 氧化还原反应的基本概念与常见类型- 氧化还原反应在日常生活中的应用第四章:酸碱与盐4.1 酸碱的定义与性质- 酸碱的定义及酸碱指示剂的作用- 酸碱溶液的中和反应4.2 酸盐与碱盐- 酸盐与碱盐的定义及特点- 酸盐与碱盐在实际生活中的应用第五章:物质的组成与结构5.1 元素周期表- 元素周期表的组成和特点- 周期表中元素的排列规律5.2 原子结构- 原子的基本组成:质子、中子和电子- 原子结构对元素性质的影响5.3 分子与离子- 分子和离子的定义及区别- 分子与离子在物质性质和反应中的作用第六章:分子结构与化学键6.1 共价键- 共价键的定义与形成- 共价键的特点与性质6.2 离子键- 离子键的定义与形成- 离子键在化合物中的作用6.3 金属键- 金属键的定义与特点- 金属键在金属中的作用以上是关于九年级化学知识点的细目表,通过系统地学习,我们能够更加深入地了解物质的分类、性质和变化规律。