药品召回流程图
- 格式:doc
- 大小:23.50 KB
- 文档页数:2

召回的处置流程
(一)药品(医用耗材)管理部门对可能存在安全隐患的药品(医用耗材)进行调查评估,确认药品(医用耗材)存在安全隐患的,应当决定召回,并立即通知有关药品(医用耗材)经营企业、使用部门停止销售和使用,必要时还应当发布院内警示,提醒临床科室和患者关注被召回产品存在的健康危害。
(二)召回时限要求
一级召回在1日内,二级召回在3日内,三级召回在7日内。
(三)药品(医用耗材)召回后,管理部门应起草调查评估报告,内容应当包括以下内容:
1.召回药品(医用耗材)的具体情况,包括名称、批次等基本信息等:
2.实施召回的原因;
3.调查评估结果。
(四)经核查和评价,有证据证明召回不彻底、或者需要采取其他更为有效的措施的,应重新召回或者在更广范围内召回。
(五)应将召回结果或评估情况及时与药品(医用耗材)供应商沟通,取得药品(医用耗材)供应商的支持和协作,必要时向医院主管部门以及药监和卫生行政管理部门报告。
药品召回处置流程:。

药品模拟召回方案制定:年月日审核:年月日年月日批准:年月日药业股份有限公司1、目的:1.1 加强我公司对产品召回管理工作。
1.2 提高产品出现危害性或潜在危害时的主动撤回的执行力,将危害程度和范围消除或降低到最小程度。
2、依据:2.1《药品生产质量管理规范》、《中华人民共和国药品管理法》、《药品召回管理条例》2.2《产品召回管理制度》《药品突发事件应急预案》3、适用范围本方案适用于我公司药品安全突发事件的召回处理工作。
4、组织机构及职责4.1设立产品召回工作小组。
组长:程雪翔副组长:苏小飞、彭发扬成员:质量部负责人李平、生产部负责人吴扬勇、仓储部负责人张义霞、销售部主管朱冰雪、生产车间主任董萍、财务部负责人漆家丽、行政人事负责人刘秀4.3部门职责4.3.1组长(或质量受权人)负责下达“药品召回指令”,组织审核召回计划、负责召回全过程的领导决策和异常情况处理,组织协调召回过程相关工作。
4.3.2质量部负责制定模拟召回方案并组织实施,评价模拟召回效果;确认召回级别,负责组织对药品安全隐患调查及评估,制定召回计划并组织实施,负责对生产过程规范操作、工艺技术等进行调查;负责对召回的产品进行检验等。
4.3.3生产部负责参与制定产品召回计划、协助质量部门对生产过程规范操作、工艺技术等进行调查等;4.3.4销售部负责参与制定产品召回计划、完成召回产品清单、负责召回过程中与客户进行沟通、通知客户停止销售或使用;收集各销售渠道的反馈信息;负责与客户协商替代性供应方案或补偿方案等;协调产品召回和召回产品的运输等事宜。
4.3.5仓储部负责参与制定产品召回计划、配合完成召回产品清单、负责接收和隔离存放召回产品等;4.3.6财务部参与制定产品召回计划、负责召回产品补偿行动的财务处理等。
4.3.7行政人事部负责公用车辆、外来人员的接待、食宿安排以及其他社会关系的协调。
5、产品召回原因:假定已经发货的养血口服液产品(批号130401,规格: 10ml ,入库数量98000支)存在安全隐患(澄清度不合格),可能会给消费者健康造成危害,决定召回。

药品召回管理程序1.目的建立药品召回系统和召回程序,保证药品质量,保证公众用药安全有效。
2.范围适用于本公司生产销售的药品召回管理,本公司其他产品召回参照本规程执行。
3.术语或定义3.1.药品召回:是指药品生产企业按照规定的程序收回已上市销售的存在安全隐患的药品。
3.2.根据召回活动发起主体不同,药品召回分为主动召回和责令召回两类:主动召回:药品生产企业通过信息的收集分析,调查评估,根据事件的严重程度,在没有官方强制的前提下主动对存在安全隐患的药品做出召回;责令召回:药品监督管理部门通过调查评估,认为存在潜在安全隐患,企业应当召回药品而未主动召回的,责令企业召回药品。
4.职责企业负责人、质量管理负责人、销售负责人、生产负责人、财务负责人对本标准的实施负责。
质量管理负责人负责监督检查。
5.程序5.1 药品召回的级别5.1.1一级召回5.1.1.1使用该药品可能引起严重健康危害;5.1.2二级召回5.1.2.1使用该药品可能引起暂时的或者可逆的健康危害;5.1.3三级召回5.1.3.1使用该药品一般不会引起健康危害,但由于其他原因需要召回的。
5.2药品召回的时限5.2.1一级召回时限应在24小时以内全面展开药品召回工作;5.2.2二级召回时限应在48小时以内全面展开药品召回工作;5.2.3三级召回时限应在72小时以内全面展开药品召回工作。
5.3召回负责人5.3.1企业负责人或质量负责人为召回负责人。
5.4.药品召回的参加人员5.4.1一级召回:企业负责人、销售部负责人、销售员、质量管理负责人、QA 室人员、生产部负责人、生产管理人员、财务部负责人、财务核算员、供应负责人、保管员;5.4.2二级召回:企业负责人、销售部负责人、销售员、质量管理负责人、QA 室人员、生产部负责人、财务部负责人、财务核算员、供应负责人、保管员;5.4.3三级召回:企业负责人、销售部负责人、销售员、质量管理负责人、QA 室人员、供应负责人、保管员。
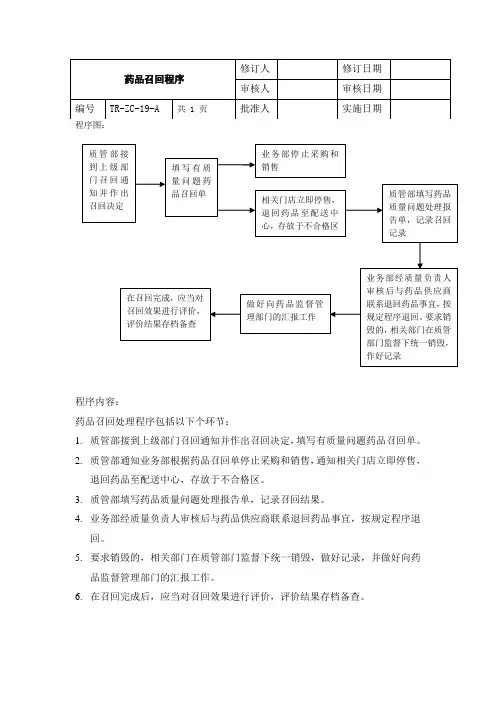
程序图:
程序内容:
药品召回处理程序包括以下个环节:
1.质管部接到上级部门召回通知并作出召回决定,填写有质量问题药品召回单。
2.质管部通知业务部根据药品召回单停止采购和销售,通知相关门店立即停售,
退回药品至配送中心,存放于不合格区。
3.质管部填写药品质量问题处理报告单,记录召回结果。
4.业务部经质量负责人审核后与药品供应商联系退回药品事宜,按规定程序退
回。
5.要求销毁的,相关部门在质管部门监督下统一销毁,做好记录,并做好向药
品监督管理部门的汇报工作。
6.在召回完成后,应当对召回效果进行评价,评价结果存档备查。


药品召回制度及处置流程为了加强药品安全使用的管理,按照国家食品药品监督管理局《药品召回管理办法》的有关规定,制定本制度。
一、药品召回药品召回,是指按照规定的程序收回已上市销售的存在安全隐患的药品。
二、有下列情况发生的必须召回药品1.药品调配、发放错误。
2.已证实或高度怀疑药品被污染。
3.制剂、分装不合格或分装差错。
4.药品使用过程中发现或患者投诉并证实为不合格药品。
5.药品监督管理部门公告的质量不合格药品、假药、劣药、召回药品。
6.已过期失效的药品。
7.生产商、供应商主动召回的药品。
三、医院药品召回处理流程(一)启动药品召回流程:1、接到上级部门的药品召回通知或国家通报的问题药品,药学科马上电话通知各科室停止使用该药品,并将该药品从各病区和药房退回药库,等待处理。
2、临床科室发现所用药品出现严重不良反应后,应及时与药学科联系并在院内网首页填写《药品不良反应/事件报告表》,临床药学科对药品不良反应进行分析、评价;药学科封存并暂停使用该药品,并报告主管领导。
3、如系药品质量问题,使用部门应及时与药学科联系,药学科封存并暂停使用该药品,由药库通知配送公司,联系退药事宜,并报告主管领导。
(二)药品召回按其紧急程度分为两级1.一级召回:24小时内召回药库(药房)。
查找处方、病历,找到用药患者,通知其停止服用并取回药品。
本方法仅限于继续使用这种药品将对患者可能产生1严重不良影响的药品召回。
2.二级召回:一周内召回药库(药房)。
当发现药品缺陷,但这种缺陷药品使用后不会对患者健康产生不良影响,可采用的二级召回方式。
(三)召回药品并填报药品召回记录,专人妥善保管于指定场所。
药库管理员可根据不同情况上报科室、质量管理部门、主管领导;及时与医疗卫生行政部门、食品药品监督管理部门、质量检验部门、生产商或供应商联系,按程序处理药品。
(四)药库、质量管理部门对召回药品处理应当有详细的记录,并向省、市药品监督管理部门报告。
必须销毁的药品,应当在药品监督管理部门监督下销毁。

药品召回制度与处置流程
一、为了加强药品安全使用的管理,按照国家食品药品监督管理局《药品召回管理办法》及其它有关规定,制定本制度。
二、本制度所称药品召回,是指药品生产企业按照规定的程序收回已上市销售的存在安全隐患的药品以及医院发现存在安全隐患的药品。
包括:
(一)各级主管部门通知召回或停止销售的药品;
(二)药品监督管理部门公告的质量不合格药品;
(三)药品安全监督抽验发现质量不合格药品;
(四)自查质量可疑或临床应用短期内出现多起严重不良反应的质量可疑药品;
(五)自查或药品安全监督抽验发现质量可疑的本院制剂。
三、接到主管部门药品召回通知、不合格药品通报或发现质量可疑药品或制剂,药库立即用院内短信和电话通知各科室停止使用该药品,并将该药品从各病区和药房退回药库。
四、被召回或不合格药品按计划及时退回药品经营企业依法处理。
五、对质量可疑药品或制剂与药品经营企业协商退换或报送药品监督管理部门进行质量检验。
若检验报告质量合格时继续使用。
检验报告质量不合格药品退回药品经营企业;质量不合格制剂院内销毁。
召回药品处理流程图。
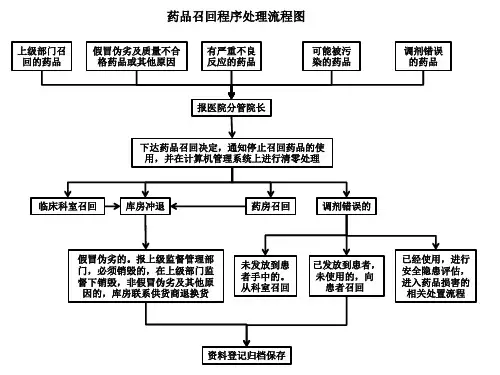

1.持有人经调查评估后,确定药品存在质量问题或者其他安全隐患
的,应当立即决定并实施召回,同时通过企业官方网站或者药品相关行业媒体向社会发布召回信息。
召回信息应当包括以下内容:药品名称、规格、批次、持有人、药品生产企业、召回原因、召回等级等。
2.实施一级、二级召回的,持有人还应当申请在所在地省、自治区、
直辖市人民政府药品监督管理部门网站依法发布召回信息。
省、自治区、直辖市人民政府药品监督管理部门网站发布的药品召回信息应当与国家药品监督管理局网站链接
3.持有人作出药品召回决定的,一级召回在1日内,二级召回在3
日内,三级召回在7日内,应当发出召回通知,通知到药品生产企业、药品经营企业、药品使用单位等,同时向所在地省、自治区、直辖市人民政府药品监督管理部门备案调查评估报告、召回计划和召回通知。

药品召回工作程序目的:规范药品召回的工作程序。
适用范围:药品的召回。
责任:质量部、生产部、储运部、销售部对本标准的实施负责。
内容:1、药品召回的级别1.1、一级召回1.1.1、使用该药品可能引起严重健康损害或者死亡;1.1.2、药品存在质量缺陷可能或已经对本公司的信誉或经济利益造成损失。
1.2、二级召回1.2.1、使用该药品可能引起暂时的或者可逆的健康损害;1.2.2、药品存在质量缺陷可能或已经对本公司的信誉或经济利益造成损失。
1.3、三级召回1.3.1、使用该药品一般不会引起健康损害;1.3.2、药品存在质量缺陷可能或已经对本公司的信誉或经济利益造成损失。
2、召回负责人2.1、总经理或质量部门负责人为三级召回负责人。
2.2、总经理为一级召回、二级召回的负责人。
3、药品召回的时限3.1、一级召回时限应在24小时以内全面展开药品召回工作。
3.2、二级召回时限应在48小时以内全面展开药品召回工作。
3.3、三级召回时限应在72小时以内全面展开药品召回工作。
4、召回药品的存放:召回的药品放置在公司仓库退货区或异地封存。
5、药品召回的参加人员5.1、一级召回:总经理、副总经理、销售部负责人、销售部管理员、销售员、质量部负责人、质量管理员、物资管理部负责人、仓库保管员、生产部负责人、生产管理员、财务部负责人、财务核算员。
5.2、二级召回:总经理、销售部负责人、市场销售管理员、销售员、质量部负责人、质量管理员、物资管理部负责人、仓库保管员。
5.3、三级召回:总经理或副总经理、销售部负责人、市场销售管理员、销售员、质量部负责人、质量管理员、物资管理部负责人、仓库保管员。
6、在下列情况下实施药品召回6.1、药品留样观察中发现质量不合格情况;6.2、用户(接种者、医生、经销商)来信、来人投诉药品质量情况,经调查属实;6.3、药品质量监督管理部门抽检通报有质量问题的药品;6.4、用户反映有未知的药品不良反应;6.5、国家已通报淘汰的药品;6.6、其它认为需要召回的药品;6.7、药品包装标签说明书内容或者设计印制存在缺陷,影响用药安全的;6.8、执行国家有关的药品召回规定。

药品召回管理制度1.药品召回指当发生、发现或高度怀疑药品质量问题、事件,或由于发生、发现、高度怀疑工作质量的问题、事件可能导致影响患者安全与诊疗质量时,药学部应当立即报告主管院领导及医务科等相关部门,按照既定的原则、程序和方法,收回药品。
2.有下列情况发生的,必须召回药品:(1)调剂发药错误。
(2)有证据证实,或高度怀疑药品被污染。
(3)制剂、分装不合格,或制剂、分装差错。
(4)在验收、保管、养护、发放、使用过程中发现的不合格药品。
(5)药品使用者投诉并得到证实的不合格药品。
(6)药品监督管理部门公告的质量不合格药品、假药、劣药、召回药品。
(7)临床发现有严重不良反应的药品按有关规定应召回的。
(8)已过失效期的药品。
(9)生产商、供应商主动召回的药品。
3.根据药品安全隐患的严重程度,药品召回分为三级:(1)一级召回:使用该药品可能引起严重健康危害的;(2)二级召回:使用该药品可能引起暂时的或者可逆的健康危害的;(3)三级召回:使用该药品一般不会引起健康危害,但由于其他原因需要召回的。
4.根据召回分级与药品销售和使用情况,科学设计药品召回计划并组织实施。
药库接到召回通知后,立即通知药学部各部门,立即封存待召回药品,停止发放。
一级召回在24小时内、二级召回在48小时内召回医院内所有应召回的药品,查找处方、病历,找到用药患者,通知其停止服用并取回药品;三级召回在72小时内召回医院内所有应召回的药品,有患者要求退回药品且符合规定时,收回药品。
5.当需召回的情形发生时,由药学部质量领导小组决定召回药品的名称、规格、生产商、召回范围、召回级别、药品替换、主要执行人员等。
6.药品质量管理员负责药品召回工作的组织、协调、检查和监督。
布置实施召回方案,监督各部门的执行,决定或请示决定紧急事项的处理,保持与医疗部门、药品行政监督管理部门、药品质量检验部门、生产商、供应商的联系,调查导致召回的原因。
7.药学部药房负责接收患者退回的药品,统一、专人妥善保管,填写《药学部药品召回登记表》,报质量管理员。