肉桂酸的制备实验.PPT
- 格式:doc
- 大小:114.50 KB
- 文档页数:3



实验五:肉桂酸的制备一、实验目的:1.学习肉桂酸的制备方法。
2.了解肉桂酸的性质和用途。
3.掌握化学实验的基本操作技能。
二、实验原理:肉桂酸(Cinnamic acid),分子式为C9H8O2,是一种具有较好药用和香料用价值的有机化合物,广泛应用于药品、香料、化妆品、合成材料及涂料等领域。
肉桂酸在自然界中分布广泛,常见于桂皮、辣椒、月桂、香菇、甜菜、薄荷等植物中。
肉桂酸的制备方法主要有以下两种:1.由肉桂醛和氧化剂氧气或过氧化氢反应得到肉桂酸。
2.由苯甲酸和丙烯酸酯反应得到肉桂酸。
本实验采用第二种方法。
三、实验材料:苯甲酸,丙烯酸酯,氢氧化钠,浓硫酸,无水乙醇,氯化钠。
四、实验步骤:1.称取苯甲酸10g和丙烯酸酯15mL,倒入250mL容量瓶中,加入少量氢氧化钠,并加入70mL无水乙醇。
2.在加热器上加热水浴,将容量瓶放入其中,调节水浴温度,使温度控制在70-80℃之间,并加入适量的玻璃珠。
3.加入10mL浓硫酸,搅拌均匀,并继续在水浴中加热反应1小时。
4.将反应混合物倒入分液漏斗中,加入25mL水,摇匀,放置静置分层,取下有机相,再加入25mL饱和氯化钠溶液,摇匀,静置分层,取下有机相。
5.用无水钠硫酸干燥有机相,收集纯净的肉桂酸。
五、实验注意事项:1.防止饮入和皮肤接触,避免对人体、环境产生危害。
2.实验中应注意安全,严格遵守实验室安全操作规程。
3.操作过程中应小心轻放,避免玻璃器皿破裂。
4.实验结束后要认真清洗实验器 material 如,保持实验室清洁卫生。
六、实验结果和分析:将干燥后的产物红色粉末放入试管中,加入少量苯,搅拌并观察其溶解度,如能快速溶解则为纯净的肉桂酸。
肉桂酸是一种白色或苍白色的柔软固体,其熔点为132-135℃,可溶于苯、乙醇、苦味酮等有机溶剂,微溶于水。
在常温下稳定,但受光照射易产生色素。
肉桂酸作为香料,在调味食品、饮料、糕点、糖果等方面有着广泛的应用;在化妆品、药品、涂料等领域也有重要作用。

肉桂酸的制备一、实验目的和要求1、熟悉柏琴反应的原理,了解肉桂酸的制备原理和方法。
2、掌握回流,水蒸汽蒸馏的操作。
二、反应原理芳香醛和酸酐在碱性催化剂存在下,可发生类似羟醛缩合的反应。
生成α、β不饱和芳香酸,称为Perkin 反应。
催化剂通常是用相应酸酐的羧酸钾或钠,有时也可用K 2CO 3或叔胺代替,典型的例子是肉桂酸的制备。
碱的作用是促使酸酐的烯醇化,生成醋酸酐碳负离子,接着与芳醛发生亲核加成,最后,经β消去,产生肉桂酸盐。
三、药品试剂,操作步骤(略)四、操作重点及注意事项1、所用仪器必须是干燥的。
因乙酐遇水能水解成乙酸,无水CH 3COOK ,遇水失去催化作用,影响反应进行。
2、放久了的醋酐易潮解吸水成乙酸,故在实验前必须将乙酐重新蒸馏,否则会影响产率。
3、久置后的苯甲醛易自动氧化成苯甲酸,这不但影响产率而且苯甲酸混在产物中不易除净,影响产物的纯度,故苯甲醛使用前必须蒸馏。
+CHO (CH 3CO)2O 170-180 C _3COOK _CH=CH _COOH CH 3COOH +4、无水醋酸钾,必须是新配制的,它的吸水性很强,操作要快。
它的干燥程度对反应能否进行和产量的提高都有明显的影响。
5、加热回流,控制反应呈微沸状态,如果反应液激烈沸腾易使乙酸酐蒸气冷凝管送出影响产率。
6、在反应温度下长时间加热,肉桂酸脱成苯乙烯,进而生成苯乙烯低聚物。
7、反应物必须趁热倒出,否则易凝成块状。
8、中和时必须使溶液呈碱性,控制pH=8较合适,不能用NaOH中和,否则会发生坎尼查罗反应。
生成的苯甲酸难于分离出去,影响产物的质量。
五、思考题1、苯甲醛和丙酸酐在无水的丙酸钾存在下相互作用得到什么产物?写出反应式?答:2、反应中,如果使用与酸酐不同的羧酸盐,会得到两种不同的芳香丙烯酸,为什么?答:酸性条件下,羧酸盐自身也能形成碳负离子,因而反应体系中存在两种不同的碳负离子。

肉桂酸的制备实验 HEN system office room 【HEN16H-HENS2AHENS8Q8-HENH1688】肉桂酸的制备实验一、实验原理利用柏琴(Perkin)反应制备肉桂酸。
一般认为脂肪酸钾盐或钠盐为催化剂,提供CH3COO-负离子,从而使脂肪酸酐生成负碳离子,然后负碳离子和醛或羧酸衍生物(酐和酯)分子中的羰基发生亲核加成,形成中间体。
在珀金反应中,是碳酸钾夺取乙酐分子中的α-H,形成乙酸酐负碳离子。
实验所用的仪器必须是干燥的。
主反应:副反应:在本实验中,由于乙酸酐易水解,无水碳酸钾易吸潮,反应器必须干燥。
提高反应温度可以加快反应速度,但反应温度太高,易引起脱羧和聚合等副反应,所以反应温度控制在150~170℃左右。
未反应的苯甲醛通过水蒸气蒸馏法分离。
机理:【此机理中的碱为无水乙酸钾】二、反应试剂、产物、副产物的物理常数三、药品四、实验流程图五、实验装置图(1)合成装置(2)水蒸气蒸馏(3)抽滤装置(4)干燥装置六、实验内容在250ml三口烧瓶中放入3ml( ,新蒸馏过的苯甲醛、8ml,新蒸馏过的乙酸酐,以及研细的无水碳酸钾。
三口烧瓶的侧口插入一根200℃温度计,温度计要求插入液面以下,采用空气冷凝管缓缓回流加热45min。
由于反应中二氧化碳逸出,可观察到反应初期有大量泡沫出现。
反应完毕,在搅拌下向反应液中分批加入20ml水,再慢慢加入碳酸钠中和反应液至pH等于8。
然后进行水蒸汽蒸馏,蒸出未反应完的苯甲醛。
待三口烧瓶中的剩余液体冷却后,加入活性炭煮沸10-15min,进行趁热过滤,将滤液冷却至室温,在搅拌下用浓盐酸酸化至刚果红试纸变蓝(或溶液pH=3)。
冷却,待晶体析出后进行抽滤,用少量冷水洗涤沉淀。
抽干,让粗产品在空气中晾干。
产量:约(产率约65%)。
粗产品可用热水或3:1的水-乙醇重结晶。
肉桂酸有顺反异构体,通常以反式存在。
纯肉桂酸为微有桂皮香气的无色针状晶体。
熔点mp=133℃。


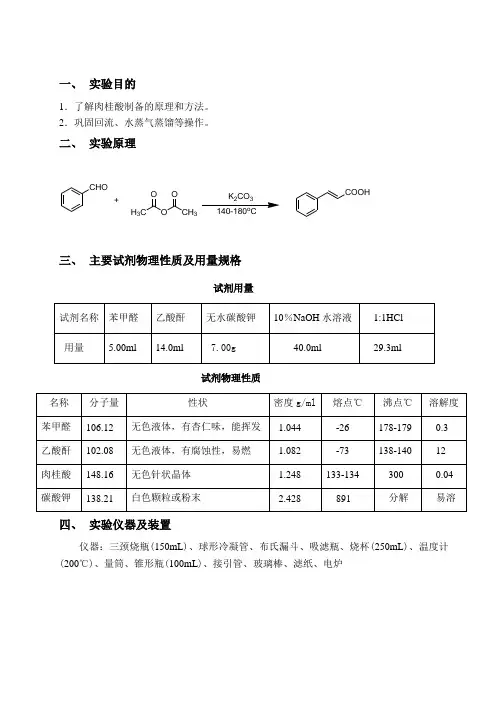
一、实验目的1.了解肉桂酸制备的原理和方法。
2.巩固回流、水蒸气蒸馏等操作。
二、实验原理CHO+H3C O CH3O O COOH三、主要试剂物理性质及用量规格试剂用量试剂物理性质四、实验仪器及装置仪器:三颈烧瓶(150mL)、球形冷凝管、布氏漏斗、吸滤瓶、烧杯(250mL)、温度计(200℃)、量筒、锥形瓶(100mL)、接引管、玻璃棒、滤纸、电炉水蒸气蒸馏装置反应装置五、实验步骤及现象六、 实验结果表面皿质量m=39.14g 产品和表面皿总质量M=44.78g 产品质量=M-m=44.78-39.14=5.64gCHO+H 3CO CH 3O O COOH理论产量=0.05×148=7.4g实际产率=实际产量/理论产量×100%=5.64/7.4×100%=76.22%七、 结果与讨论实验注意事项1、所用仪器必须是干燥的。
因乙酐遇水能水解成乙酸,影响反应进行。
2、加热回流,控制反应呈微沸状态,如果反应液激烈沸腾易使乙酸酐蒸出影响产率。
3、在蒸馏过程中,要经常检查安全管中的水位是否正常,如发现其突然升高,意味着有堵塞现象,应立即打开止水夹,移去热源,使水蒸汽发生器与大气相通,避免发生事故(如倒吸),待故障排除后再行蒸馏。
如发现T 形管支管处水积聚过多,超过支管部分,也应打开止水夹,将水放掉,否则将影响水蒸汽通过。
4、当馏出液澄清透明,不含有油珠状的有机物时,即可停止蒸馏,这时也应首先打开夹子,然后移去热源。
5、防止在反应温度下长时间加热,肉桂酸脱成苯乙烯,进而生成苯乙烯低聚物。
6、反应物必须趁热倒出,否则易凝成块状。
热过滤时必须是真正热过滤,布氏漏斗要事先在沸水中取出,动作要快。
7、进行脱色操作时一定取下烧瓶,稍冷之后再加热活性炭。
8、肉桂酸要结晶彻底,进行冷过滤;不能用太多水洗涤产品。
9、回流和蒸馏时通冷凝水都要小一点。
误差分析1、过滤时部分晶体残留在烧杯中和滤纸上造成损失。


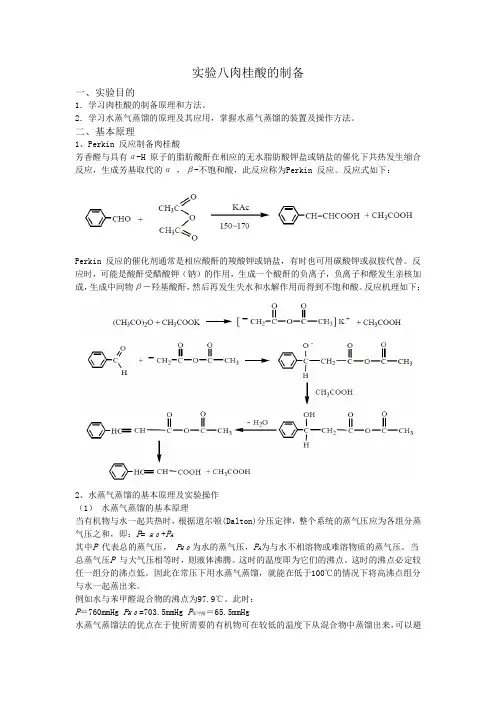
实验八肉桂酸的制备一、实验目的1.学习肉桂酸的制备原理和方法。
2.学习水蒸气蒸馏的原理及其应用,掌握水蒸气蒸馏的装置及操作方法。
二、基本原理1、Perkin 反应制备肉桂酸芳香醛与具有α-H 原子的脂肪酸酐在相应的无水脂肪酸钾盐或钠盐的催化下共热发生缩合反应,生成芳基取代的α,β-不饱和酸,此反应称为Perkin 反应。
反应式如下:Perkin 反应的催化剂通常是相应酸酐的羧酸钾或钠盐,有时也可用碳酸钾或叔胺代替。
反应时,可能是酸酐受醋酸钾(钠)的作用,生成一个酸酐的负离子,负离子和醛发生亲核加成,生成中间物β-羟基酸酐,然后再发生失水和水解作用而得到不饱和酸。
反应机理如下:2、水蒸气蒸馏的基本原理及实验操作(1)水蒸气蒸馏的基本原理当有机物与水一起共热时,根据道尔顿(Dalton)分压定律,整个系统的蒸气压应为各组分蒸气压之和,即:P= H O +P A其中P 代表总的蒸气压,P H O 为水的蒸气压,P A为与水不相溶物或难溶物质的蒸气压。
当总蒸气压P 与大气压相等时,则液体沸腾。
这时的温度即为它们的沸点。
这时的沸点必定较任一组分的沸点低。
因此在常压下用水蒸气蒸馏,就能在低于100℃的情况下将高沸点组分与水一起蒸出来。
例如水与苯甲醛混合物的沸点为97.9℃。
此时:P=760mmHg P H O =703.5mmHg P苯甲醛=65.5mmHg水蒸气蒸馏法的优点在于使所需要的有机物可在较低的温度下从混合物中蒸馏出来,可以避免在常压下蒸馏时所造成的损失,提高分离提纯的效率。
同时在操作和装置方面也较减压蒸馏简便一些,所以水蒸气蒸馏可以应用于分离和提纯有机物。
水蒸气蒸馏常在下列情况下使用:(a)混合物中含有大量的固体,通常的蒸馏、过滤、萃取等分离方法都不适用。
(b)混合物中含有焦油状物质,采用通常的蒸馏、萃取等方法非常困难。
(c)在常压下蒸馏高沸点有机物质会发生分解。
被提纯物质必须具备以下几个条件:(a)不溶或难溶于水。
肉桂酸的制备实验一、实验原理利用柏琴Perkin反应制备肉桂酸;一般认为脂肪酸钾盐或钠盐为催化剂,提供CH3COO-负离子,从而使脂肪酸酐生成负碳离子,然后负碳离子和醛或羧酸衍生物酐和酯分子中的羰基发生亲核加成,形成中间体;在珀金反应中,是碳酸钾夺取乙酐分子中的α-H,形成乙酸酐负碳离子;实验所用的仪器必须是干燥的;主反应:副反应:在本实验中,由于乙酸酐易水解,无水碳酸钾易吸潮,反应器必须干燥;提高反应温度可以加快反应速度,但反应温度太高,易引起脱羧和聚合等副反应,所以反应温度控制在150~170℃左右;未反应的苯甲醛通过水蒸气蒸馏法分离;机理:此机理中的碱为无水乙酸钾二、反应试剂、产物、副产物的物理常数三、药品四、实验流程图五、实验装置图1合成装置2水蒸气蒸馏 3抽滤装置4干燥装置六、实验内容在250ml三口烧瓶中放入3ml ,新蒸馏过的苯甲醛、8ml,新蒸馏过的乙酸酐,以及研细的无水碳酸钾;三口烧瓶的侧口插入一根200℃温度计,温度计要求插入液面以下,采用空气冷凝管缓缓回流加热45min;由于反应中二氧化碳逸出,可观察到反应初期有大量泡沫出现;反应完毕,在搅拌下向反应液中分批加入20ml水,再慢慢加入碳酸钠中和反应液至pH等于8;然后进行水蒸汽蒸馏,蒸出未反应完的苯甲醛;待三口烧瓶中的剩余液体冷却后,加入活性炭煮沸10-15min,进行趁热过滤,将滤液冷却至室温,在搅拌下用浓盐酸酸化至刚果红试纸变蓝或溶液pH=3;冷却,待晶体析出后进行抽滤,用少量冷水洗涤沉淀;抽干,让粗产品在空气中晾干;产量:约产率约65%;粗产品可用热水或3:1的水-乙醇重结晶;肉桂酸有顺反异构体,通常以反式存在;纯肉桂酸为微有桂皮香气的无色针状晶体;熔点mp=133℃;一制备阶段:1.安装反应装置:按1合成装置图,三口烧瓶的中间口连接空气冷凝管注:冷凝管上口不能用塞子塞住,要与大气相通,常压反应,侧口插入一根200℃温度计,温度计要求插入液面以下注:水银球不能接触瓶壁,另一侧口加一个空心塞;2.投料:在250ml三口烧瓶中依次放入3ml 新蒸馏过的苯甲醛、8ml 新蒸馏过的醋酐以及研细的无水碳酸钾;应在放空心塞的侧口依次加入药品3.加热:缓缓加热,回流45min;要控制加热速度,使三口瓶内温度计读数不能超过170℃;由于反应中二氧化碳逸出,可观察到反应初期有大量泡沫出现;二纯化阶段:1.分解未反应的原料乙酸酐:反应完毕,在搅拌下向反应液中分批加入20ml水2.使肉桂酸转化为肉桂酸钠盐:慢慢加入碳酸钠中和反应液至pH等于8;3.除去未反应的原料苯甲醛:然后进行水蒸汽蒸馏,蒸出未反应完的苯甲醛;4.脱色与吸附树脂状物:待三口烧瓶中的剩余液体冷却后,加入活性炭煮沸10-15min,进行趁热过滤;1加活性炭时三口瓶内的剩余液体只需要稍微冷却即可;2此步水蒸气蒸馏装置先不要拆卸,只需在三口瓶的侧口加入活性炭后,继续蒸馏10min即可,这样做操作简单,同时又可以彻底除去未反应的苯甲醛;3若拆卸了水蒸气蒸馏装置,那么当加完活性炭煮沸时,需要安装回流装置,在三口瓶的中间口连接回流冷凝管,两侧口需要用空心塞堵上,操作上较麻烦;千万不能敞口煮沸,会挥发出有毒的物质,不安全;5.酸化析出肉桂酸:将滤液冷却至室温,在搅拌下用浓盐酸酸化至刚果红试纸变蓝或溶液pH = 3,析出大量晶体;如何计算酸化时所需要浓盐酸的最低用量ml6.分离粗产品:将酸化后的溶液充分冷却至室温,待晶体析出完全后进行抽滤;7.洗涤粗产品:用少量冷水洗涤沉淀,抽干;“少量冷水”是指水量大小只是仅能够达到将布氏漏斗上的固体产品润湿即可,不可形成悬浮液8.干燥产品:让粗产品在热水浴上干燥,如图4所示;9.称重产品:约产率约%;粗产品可用热水或3:1的水-乙醇重结晶;肉桂酸有顺反异构体,通常以反式存在;纯肉桂酸为微有桂皮香气的无色针状晶体;熔点mp=133℃;七、思考题1、本实验利用碳酸钾代替perkin反应中的醋酸钾,使反应时间缩短,那么具有何种结构的醛能进行perkin反应答:醛基与苯环直接相连的芳香醛能发生Perkin反应;2、用水蒸气蒸馏能除去什么能不能不用水蒸气蒸馏如何判断蒸馏终点答:①除去未反应的苯甲醛;②不行,必须用水蒸气蒸馏,因为混合物中含有大量的焦油状物质,通常的蒸馏、过滤、萃取等方法都不适用;③当流出液澄清透明不再含有有机物质的油滴时,即可断定水蒸汽蒸馏结束也可用盛有少量清水的锥形瓶或烧杯来检查是否有油珠存在;3、在perkin反应中,醛和具有R2CHCOOCOCHR2结构的酸酐相互作用,能得到不饱和酸吗为什么答:不能;因为具有R2CHCO2O结构的酸酐分子只有一个α-H原子;4、苯甲醛和丙酸酐在无水丙酸钾存在下,相互作用得到什么产物答:可得到α-甲基肉桂酸即:α-甲基-β-苯基丙烯酸;5、制备肉桂酸时,往往出现焦油,它是怎样产生的又是如何除去的答:产生焦油的原因是:在高温时生成的肉桂酸脱羧生成苯乙烯,苯乙烯在此温度下聚合所致,焦油中可溶解其它物质;产生的焦油可用活性炭与反应混合物碱溶液一起加热煮沸,焦油被吸附在活性炭上,经过滤除去;6、在肉桂酸制备实验中,为什么要缓慢加入固体碳酸钠来调解pH值答:对于酸碱中和反应,若加入碳酸钠的速度过快,易产生大量二氧化碳的气泡,可能会冲出反应瓶,而且不利于准确调节pH值,将会可能过多加入固体碳酸钠,造成溶液碱性过强,而引起浪费;7、久置的苯甲醛中有何杂质如何除去为什么要除去苯甲醛中的杂质答:久置的苯甲醛中含有较多的苯甲酸杂质;采用蒸馏的方法除去采用空气冷凝管,收取176~180℃的馏分供使用;若不先除去,则混在肉桂酸产品中,由于结构相似,不易除去;8、制备肉桂酸时为何采用水蒸汽蒸馏答:因为在反应混合物中含有未反应的苯甲醛油状物,它在常压下蒸馏时易氧化分解,故采用水蒸汽蒸馏,以除去未反应的苯甲醛;9、在肉桂酸制备实验中,能否在水蒸汽蒸馏前用氢氧化钠代替碳酸钠来中和水溶液答:不能;因为苯甲醛在强碱存在下可发生Cannizzaro反应;10、用水蒸气蒸馏的物质应具备什么条件答:1随水蒸气蒸出的物质应不溶或难溶于水;2在沸腾下与水长时间共存而不起化学变化;3在一定大气压下,要有一定的蒸汽压;11、什么情况下需要采用水蒸汽蒸馏答:下列情况需要采用水蒸气蒸馏:1混合物中含有大量的固体,通常的蒸馏、过滤、萃取等方法都不适用;2混合物中含有焦油状物质,采用通常的蒸馏、萃取等方法都不适用;3在常压下蒸馏会发生分解的高沸点有机物质;12、怎样正确进行水蒸汽蒸馏操作答:1在进行水蒸气蒸馏之前,应认真检查水蒸气蒸馏装置是否严密;2开始蒸馏时,应将T形管的止水夹打开,当水蒸气发生器里的水沸腾,有大量水蒸气溢出时再旋紧夹子,使水蒸气进入三颈烧瓶中,并调整加热速度,以馏出速度2-3滴/秒为宜;3操作中要随时注意安全管中的水柱是否有异常现象发生,若有,应立即打开夹子,停止加热,找出原因,排除故障后方可继续加热;13、肉桂酸制备时,所用的原料苯甲醛与乙酸酐都应该采用蒸馏的方法进行纯化处理,请问蒸馏这两种原料时的蒸馏装置有什么不同答:蒸馏苯甲醛时,采用的是普通蒸馏装置,使用空气冷凝管;在接收管上的支管处不需要连接无水氯化钙干燥管;蒸馏乙酸酐时,采用如下的蒸馏装置,沸点℃,可以使用空气冷凝管,因不太高,也可以使用直型冷凝管;而且要使接收产品用的三角烧瓶与接收管之间密封,接收管上的支管处要连接无水氯化钙干燥管,避免空气中的水蒸气进入系统;见下图:14、肉桂酸实验在制备阶段有哪些仪器需要干燥为什么答:凡是能与试剂相接触的仪器都需要洁净、干燥的;如:三口瓶、空气冷凝管、温度计、玻璃塞又叫空心塞、量筒;因为这些仪器若不干燥,其残存的水会造成乙酸酐水解,从而减少乙酸酐的实际用量,可能会影响化学反应进行的程度;问:量取苯甲醛的量筒若没有彻底干燥,会不会对该反应产生影响15、肉桂酸的制备方法有哪些答:1铂金Perkin合成法:2苯乙烯—四氯化碳法:3苯甲醛—丙酮法:4苯甲醛—醋酸法:这是一个气相反应合成的方法,将苯甲醛和60%醋酸于350℃气化通过装有催化剂的反应器,催化剂是将碱性催化剂固载于铝硅酸盐、SiO2-Al2O3或者硅胶等上制的; 5苄叉二氯—无水醋酸钠法:6克脑文格尔Knoevenagel缩合反应制备法:九、资料肉桂酸有顺、反两种异构体;注:顺肉桂酸常见有三种形式,III最稳定,称为“别肉桂酸”,I和II称为“异肉桂酸”,还有一种最不稳定形式,熔点32℃,它能很快转化为I;I可经紫外、日光照射转化为IV以及二聚物;IV有最稳定的和天然存在的两种形式,其饱和甲醇溶液用紫外光照射可转化为顺式;。
一、实验目的1、学习肉桂酸的制备原理和方法。
2、学习水蒸气蒸馏的原理及其应用,掌握水蒸气蒸馏的装置及操作方法。
二、实验原理反应式为:反应机理:(CH 3CO)2O + CH 3COOK[COOCH 2CO CH 3]K ++ CH 3COOHO OCH 2O CH 3C O H+C O -HCH 2OOCH 3O CH 3COOHC OH HCH 2OO CH 3O - 2HCCHOOCH 3O 水解HCCHCOOH + CH 3COOH三、 主要试剂及物理性质表一、主要试剂及其物理性质四、试剂用量规格五、仪器装置实验仪器:150 mL 三口烧瓶,球形冷凝管,直形冷凝管,支管接引管,锥形瓶,量筒,烧杯,布氏漏斗,吸滤瓶,表面皿,温度计实验装置图图一、制备肉桂酸的反应装置图图二、水蒸气蒸馏装置图六、实验步骤及现象七、实验结果产品性状:白色粉末略带黄色。
M(理论)=0.05×148.16=7.408gM(实际)=7.01g产率=7.01÷7.408×100%=94.63%八、实验讨论数据讨论:产率较高,干燥不完全;产品非纯白色,纯度不高。
注意事项:1、仪器在使用前要干燥,否则影响反应的进行;2、加热回流,控制反应呈微沸状态,如果反应液激烈沸腾易使乙酸酐蒸出影响产率;3、控制回流蒸气上升高度不超过2个球。
肉桂酸的制备
一、实验目的 实验目的 1、掌握由 Perkin 反应制备 α, β-不饱和酸的原理和方法。
2、进一步巩固回流、水蒸汽蒸馏、重结晶等基本操作。
二、实验原理 实验原理 肉桂酸是生产冠心病药物“心可安”的重要中间体。
其酯类衍生物是配制香精和食品香料的重要原料。
它在农用塑料和感光树脂等精 细化工产品的生产中也有着广泛的应用。
系统命名:3-苯基丙烯酸 属 α, β-不饱和酸 Perkin 反应:芳香醛和酸酐在碱性催化剂作用下,发生类似羟醛缩合的作用,生成 α, β-不饱和芳香酸的反应。
主反应:
碱催化剂一般为酸酐相应羧酸的钾盐或钠盐,本实验采用醋酸钾作为碱催化剂。
反应机理:
三、操作步骤
四、数据记录和处理 略 五、实验注意事项
.所用仪器必须是干燥的。
因乙酐遇水能水解成乙酸,无水 CH3COOK,遇水失去催化作用,影响反应进行。
无水碳酸钾也应烘干至恒重,
否则将会使乙酸酐水解而导致实验产率降低。
2.放久了的醋酐易潮解吸水成乙酸,故在实验前必须将乙酐重新蒸馏,否则会影响产率。
.久置后的苯甲醛易自动氧化成苯甲酸,这不但影响产率而且苯甲酸混在产物中不易除净,影响产物的纯度,故苯甲醛使用前必须蒸馏。
4.无水醋酸钾的吸水性很强,操作要快。
它的干燥程度对反应能否进行和产量的提高都有明显的影响。
制反应呈微沸状态,如果反应液激烈沸腾易使乙酸酐蒸气冷凝管送出影响产率。
6.在反应温度下长时间加热,肉桂酸脱成苯乙烯,进而生成苯乙烯低聚物。
7.反应物必须趁热倒出,否则易凝成块状。
的质量。
实验中视具体情况,反应时间可以延长,并用 TLC 技术进行反应过程跟踪。
明确水蒸气蒸馏应用于分离和纯化时其分离对象的适用范围,保证水蒸气蒸馏顺利完成。
浓硫酸的滴加要缓慢,要分批滴加。
多。
六、思考题 1.苯甲醛和丙酸酐在无水的 丙酸钾存在下相互作用得到什么产物?写出反应式?
.缩合反应宜缓慢升温,以防苯甲醛氧化。
反应开始后,由于逸出二氧化碳,有泡沫出现,随着反应的进行,会自动消失。
加热回流,控
.中和时必须使溶液呈碱性,控制 pH=8较合适,不能用 NaOH 中和,否则会发生坎尼查罗反应。
生成的苯甲酸难于分离出去,影响产物
铬酸氧化醇是一个放热反应,实验中必须严格控制反应温度以防反应过于剧烈。
反应中控制好温度,温度过低反应困难,过高则副反应增
答: 2.反应中,如果使用与酸酐不同的羧酸盐,会得到两种不同的芳香丙烯酸,为什么? 答:酸性条件下,羧酸盐自身也能形成碳负离子,因而反应体系中存在两种不同的碳负离子。
主要试剂及产品的物理常数: 文献值) (文献值 主要试剂及产品的物理常数: 文献值) ( 名 称 分 子 量 10 6.1 2 性 状 无 色 液 体 无 乙 酸 酐 色 10 2.0 8 刺 激 液 体 肉 桂 酸 无 14 8.1 6 色 结 晶 1.2 48 133 -13 4 300 1.3 900 1.0 82 138 -73 -14 0 ∞ ∞ ∞ 1.5 450 1.0 44 178 -26 -17 9 折 光 率 比 重 熔 点 ℃ 沸 点 ℃ 水 溶解度:克/100ml 溶剂 醇 醚
苯 甲 醛
。