选修4第一章化学反应与能量单元测试题
- 格式:doc
- 大小:112.50 KB
- 文档页数:5

选修4作业(三)第一章化学反应与能量单元测试一、选择题(本题共10小题,每小题只有一个正确选项)1.下列叙述正确的是A.反应的活化能越小,单位时间内有效碰撞越多。
B.反应的活化能越大,单位时间内有效碰撞越多。
C.反应的活化能越小,单位时间内有效碰撞越少。
D.反应的活化能太小,单位时间内几乎无有效碰撞。
2.已知反应X+Y==M+N为放热反应,对该反应的下列说法中正确的是A.X的能量一定高于MB.Y的能量一定高于NC.X和Y的总能量一定高于M和N的总能量D.因该反应为放热反应,故不必加热就可发生3.下列说法错误的是A.热化学方程式各物质前的化学计量数不表示分子个数只代表物质的量B.热化学方程式未注明温度和压强,△H表示标准状况下的数据C.同一化学反应,化学计量数不同,△H值不同,化学计量数相同而状态不同,△H 值也不相同D.化学反应过程所吸收或放出的热量与参加反应的物质的物质的量成正比4.强酸和强碱的稀溶液的中和热可表示为:H+(aq)+OH-(aq)=H2O(1) △H =—57.3kJ/mol 已知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(1) △H =—Q1kJ/mol 1/2 H2SO4(浓) + NaOH(aq) == 1/2Na2SO4(aq) +H2O(1) △H =—Q2kJ/molHNO3(aq)+KOH(aq)=KNO3(aq)+H2O(1) △H =—Q3kJ/mol 上述反应均为溶液中的反应,则Q1、Q2、Q3的大小关系为A.Q1=Q2=Q3B.Q2>Q1>Q3C.Q2>Q3>Q1D.Q2=Q3>Q15.在相同的温度和压强下,将32g硫分别于纯氧中和空气中完全燃烧,令前者的反应热为△H1,后者的反应热为△H2,则关于△H1和△H2的相对大小,正确的判断是A.△H1=△H2B.△H1>△H2C.△H1<△H2D.无法判断6.工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3,已知该反应为一放热反应。

高中化学学习材料唐玲出品第一章《化学反应与能量》单元测试一、选择题1.下列关于热化学反应的描述中正确的是A .HCl 和NaOH 反应的中和热ΔH =-57.3kJ/mol ,则H 2SO 4和Ca(OH)2反应的中和热 ΔH =2×(-57.3)kJ/molB .CO(g)的燃烧热是283.0kJ/mol ,则2CO 2(g) =2CO(g)+O 2(g)反应的 ΔH =+566.0kJ/molC .需要加热才能发生的反应一定是吸热反应D .1mol 甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热2.已知葡萄糖的燃烧热是2804 kJ/ mol ,当它氧化生成1 g 水时放出的热量是( )A .26.0 kJB .51.9 kJC .155.8 kJD .467.3 kJ3.(07上海)氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车倍受青睐。
我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。
氢能具有的优点包括( ) ①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行A .①②B .①③C .③④D .②④4.下列说法中不正确的是( )A .反应是放热还是吸热要由反应物和生成物所具有的总能量来决定B .放热的反应在常温下一定很容易发生C .需要加热才能发生的反应可能是吸热反应也可能是放热反应D .在101KPa 时,1mol 碳完全燃烧生成二氧化碳气体时放出的热量为碳的燃烧热5.已知: ①)g (O 21)g (H 22+=H 2O (g ) △H 1=a kJ ·1mol -, ②)g (O )g (H 222+=2H 2O (g )△H 2=b kJ ·1mol -,③)g (O 21)g (H 22+=H 2O (l ) △H 3=c kJ ·1mol -, ④)g (O )g (H 222+=2H 2O (l ) △H 4=d kJ ·1mol -。

选修(一)4第一章化学反应与能量单元测试题一、选择题(每小题只有一个选项符合题意) 1.下列说法正确的是A .物质发生化学变化都伴随着能量变化B .任何反应中的能量变化都表现为热量变化C .伴有能量变化的物质变化都是化学变化D .即使没有物质的变化,也可能有能量的变化 2.炽热的炉膛内有反应:C(s)+O 2(g)==CO 2(g);△H = -392KJ/mol ,往炉膛内通入水蒸气时,有如下反应:C(s)+H 2O(g)==H 2(g)+CO(g);△H = +131KJ/mol ,CO(g)+1/2O 2(g)==CO 2(g);△H = -282KJ/mol ,H 2(g)+1/2O 2(g)==H 2O(g);△H =-241KJ/mol ,由以上反应推断往炽热的的炉膛内通入水蒸气时A .不能节省燃料,但能使炉火瞬间更旺B .虽不能使炉火瞬间更旺,但可以节省燃料C .既能使炉火瞬间更旺又可以节省燃料D .既不能使炉火瞬间更旺,又不能节省燃料 3.根据下列热化学方程式,判断氢化物的稳定性顺序正确的是21N 2(g)+ 23H 2 (g)=NH 3(g);ΔH =-46.19kJ·mol —1 21H 2(g)+ 21Cl 2(g)=HCl (g);ΔH =-92.36kJ·mol —1 21I 2(g)+ 21H 2 (g)=HI (g);ΔH =+25.96kJ·mol —1 A. HCl>NH 3>HI B.HI>HCl>NH 3 C.HCl> HI > NH 3D.NH 3> HI > HCl4.氢气、一氧化碳、辛烷、甲烷的热化学方程式分别为:H 2(g)+1/2O 2(g)=H 2O(l) △H =-285.8kJ/mol CO(g)+1/2O 2(g)=CO 2(g)△H =-283.0kJ/mol C 8H 18(l)+25/2O 2(g)=8CO 2(g)+9H 2O(l) △H =-5518kJ/molCH 4(g)+2O 2(g)=CO 2(g)+2H 2O(l) △H =-89.3kJ/mol相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是A . H 2(g)B . CO(g)C .C 8H 18(l)D . CH 4(g) 5.根据以下3个热化学方程式:2H 2S(g)+3O 2(g)=2SO 2(g)+2H 2O(l)△H=―Q 1kJ/mol2H 2S(g)+O 2(g)=2S (s)+2H 2O(l) △H =―Q 2 kJ/mol 2H 2S(g)+O 2(g)=2S (s)+2H 2O(g) △H =―Q 3 kJ/mol 判断Q1、Q2、Q3三者关系正确的是Q1>Q2>Q3 B . Q1>Q3>Q2 C . Q3>Q2>Q1 D . Q2>Q1>Q3 6.已知热化学方程式:H 2O(g)=H 2(g) + 1/2O 2(g) △H = +241.8kJ /mol H 2(g)+ 1/2O 2(g) = H 2O(1) △H = -285.8kJ /mol 当1g液态水变为水蒸气时,其热量变化是 A .吸热88kJ B .吸热2.44KJ C .放热44kJ D .吸热44KJ7.同温同压下,已知下列各反应为放热反应,下列各热化学方程式中热量数值最小的是A 、2A ( l ) +B ( l ) = 2C (g ) △H 1 B 、2A ( g ) + B ( g ) = 2C (g ) △H 2 C 、2A ( g ) + B ( g ) = 2C ( l ) △H 3D 、2A ( l ) + B ( l ) = 2C ( l ) △H 4 8.已知热化学方程式:SO 2(g)+12O 2(g)SO 3(g) △H = ―98.32kJ /mol ,在容器中充入2molSO 2和1molO 2充分反应,最终放出的热量为A . 196.64kJB . 196.64kJ /molC .<196.64kJD .>196.64kJ9. 已知25℃、101kPa 条件下:4Al (s) + 3O 2 (g) == 2Al 2O 3 (s) △H = -2834.9 kJ·mol -1 4Al (s) +2O 3 (g) ==2Al 2O 3 (s) △H = -3119.91kJ·mol -1由此得出的结论正确的是A .等质量的O 2比O 3能量低,由O 2变O 3为吸热反应B .等质量的O 2比O 3能量低,由O 2变O 3为放热反应C .O 3比O 2稳定,由O 2变O 3为吸热反应D .O 2比O 3稳定,由O 2变O 3为放热反应10.强酸与强碱的稀溶液发生中和反应的热效应:H +(aq)+OH -(aq)=H 2O(1)⊿H=-57.3kJ /mol 。

《化学反应与能量》单元检测题一、单选题1.已知反应:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1③2SO2(g)+O2(g)⇌2SO3(g) ΔH=-Q kJ·mol-1(Q>0)下列结论正确的是( )A.碳的燃烧热等于110.5 kJ·mol-1B.稀硫酸与稀氢氧化钡溶液反应生成1 mol水时放出57.3 kJ的热量C.相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量D.将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热Q kJ,则此过程中有2 mol SO2(g)被氧化2.下列说法正确的是( )A.利用键长及键能的数据可判断:稳定性44CH<SiHB.金属的电子气理论,可以解释金属易导电易腐蚀的原因C.化学反应过程中一定有化学键的变化,这是反应过程中能量变化的本质原因D.活化能越大就代表化学反应需要吸收或放出的能量就越大3.一种“即食即热型快餐”适合外出旅行时使用。
其内层是用铝箔包裹的、并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是()A.浓硫酸与水B.生石灰与水C.熟石灰与水D.氯化钠与水4.下列与化学反应能量变化相关的叙述正确的是A.生成物总能量一定低于反应物总能量B.ΔH的大小与热化学方程式的计量系数无关C.应用盖斯定律可计算某些难以直接测量的反应焓变D.同温同压下,H2(g)+Cl2(g)===2HC1(g)在光照和点燃条件下的ΔH不同5.下列说法正确的是A.H2(g)的燃烧热△H=-285.8 kJ/mol,则2H2O(g)=2H2(g)+O2(g) △H=+571.6 kJ/molB.反应物的总能量低于生成物的总能量时,该反应为放热反应C.由石墨比金刚石稳定可知:c(金刚石,s)=c(石墨,s) △H<0D.已知:298K时,N2(g)+3H2(g) 2NH3(g) △H=-92.0 kJ/mol。


选修4第一章《化学反应与能量》单元测试题一、选择题(每小题只有1个选项符合题意)1.未来新能源的特点是资源丰富、使用时对环境无污染或污染很小,且可以再生。
下列符合未来新能源标准的是:①天然气②煤③石油④太阳能⑤生物质能⑥风能⑦氢能()A.①②③④B.③⑤⑥⑦C.④⑤⑥⑦D.③④⑤⑥⑦2.下列叙述正确的是( )A.水能是二次能源B..电能是二次能源C.天然气是可再生能源D.水煤气是可再生能源3.下列过程一定释放出能量的是()A.化合反应B.分解反应C .原子组成分子 D.分子拆成原子4.下列选项中说明乙醇作为燃料的优点的是()①燃烧时发生氧化反应②充分燃烧的产物不污染环境③乙醇是一种再生能源④燃烧时放出大量热量A. ①②③B. ①②④C. ①③④D.②③④5.下列反应既属于氧化还原反应,又属于吸热反应的是()A. 灼热的碳与CO2的反应B. Ba(OH)2·8H2O与NH4Cl的反应C. 铝片与稀盐酸反应D. 甲烷在氧气中的燃烧反应6.下列说法正确的是A.化学反应都伴随着能量的变化B.个别化学反应与能量变化无关C.化学反应都要放出能量D.放热反应的发生无需任何条件7.下列说法正确的是( )A.需要加热才能发生的反应一定是吸热反应B.吸热反应不加热的条件一定不能发生C.放热的反应在常温下一定很容易发生D.反应是放热的还是吸热的须看反应物和生成物所具有的总能量的相对大小8.下列各图中,表示正反应是吸热反应的图是.( )9.右图是一个一次性加热杯的示意图。
当水袋破裂时,水与固体碎块混和,杯内食物温度逐渐上升。
制造此加热杯可选用的固体碎块是( )A.硝酸铵B.氯化镁C.生石灰D.食盐10.已知H2(g)+Cl2(g)=2HCl(g) △H= ―184.6kJ·mol-1,则反应HCl(g)=1/2H2(g)+1/2Cl2(g)的△H为( )A.+184.6kJ·mol-1B.―92.3kJ·mol-1C.+92.3kJ D.+92.3kJ·mol-111.已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )A.H2O(g)=H2(g)+1/2 O2(g) △H=+242kJ•mol-1B.2H2(g)+O2(g)=2H2O(l)△H=-484kJ•mol-1C.H2(g)+1/2O2(g) =2H2O(g) △H=+242k J•mol-1D.2H2(g)+O2(g)=2H2O(g)△H=+484kJ•mol-1 12.根据以下3个热化学方程式:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H=-Q1 kJ/mol,2H2S(g)+O2(g)=2S (s)+2H2O(l) △H=-Q2 kJ/mol,2H2S(g)+O2(g)=2S (s)+2H2O(g)△H=-Q3 kJ/mol,判断Q1、Q2、Q3三者关系正确的是( )A.Q1>Q2>Q3 B.Q1>Q3>Q2C.Q3>Q2>Q1 D.Q2>Q1>Q313. 已知:(1)Zn(s)+1/2O2(g)===ZnO(s),ΔH= -348.3 kJ·mol-1,(2)2Ag(s)+ 1/2O2(g)=== Ag2O(s),ΔH= -31.0 kJ·mol-1,则Zn(s)+ Ag2O(s)===ZnO(s)+ 2Ag(s)的ΔH等于()A.-379.3 kJ·mol-1B.-317.3 kJ·mol-1C.-332.8 kJ·mol-1D.317.3 kJ·mol-1 14.1mol碳完全燃烧后可放出393.5KJ的热量,下列热化学方程式正确的是()A.C(s)+O2(g)=CO2(g);△H=+393.5 kJ/molB.C(s)+1/2O2(g)=CO(g);△H =-393.5 kJ/molC.C + O2 = CO2 ; △H =-393.5 kJ/molD. C(s)+O2(g)=CO2(g)△H =-393.5 kJ/mol 15.在一定条件下,CO和CH4燃烧的热化学方程式分别为:2CO(g) + O2(g) = 2CO2(g) △H =-566 kJ/mol;CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) △H =-890 kJ/mol由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为( ) A.2912kJ B.2953kJ C.3236kJ D.3867kJ16.下列属于直接利用太阳辐射能的方式的是①光-热转换②光-电转换③光-化学能转换④光-生物质能转换A.①②③ B.①③④ C.①②④ D.①②③④17.已知(l)H2(g)+1/2O2(g)=H2O(g);△H1=a kJ/mol(2)2H2(g)+O2(g)=2H2O(g);△H2=b kJ/mol(3)H2(g)+1/2O2(g)=H2O(l);△H3=c kJ/mol(4)2H2(g)+O2(g)=2H2O(l);△H4=d kJ/mol下列关系式中正确的是()A.a<c <0 B.b>d>0 C.2a=b<0 D.2c=d>0 18.已知有热化学方程式:SO2(g)+ 1/2 O2(g) SO3(g);△H =-98.32kJ/mol现有4molSO2参加反应,当放出314.3kJ热量时,SO2的转化率最接近于( )A.40%B.50%C.80%D.90%19.强酸和强碱的稀溶液的中和热可表示为:H+(aq)+OH-(aq)=H2O(1) △H = -57.3kJ/mol已知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O △H = - Q1kJ/mol 1/2 H2SO4(浓) + NaOH(aq) == 1/2Na2SO4(aq) +H2O(1) △H = - Q2kJ/molHNO3(aq)+KOH(aq)=KNO3(aq)+H2O(1) △H = - Q3kJ/mol 上述反应均为溶液中的反应,则Q1、Q2、Q3的绝对值大小的关系为( )A.Q1=Q2=Q3B.Q2>Q1>Q3C.Q2>Q3>Q1D.Q2=Q3>Q120.已知下列两个热化学方程式:2H2(g)+O2(g)=2H2O(l);ΔH=-571.6kJ/mol C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);ΔH=-2220kJ/mol实验测得氢气和丙烷的混合气体共5mol,完全燃烧时放出热量3847kJ,则混合气体中氢气和丙烷的体积比为()A.1:3 B.1:4 C.3:1 D.1:1二、选择题(每小题有2个选项符合题意)21. S(单斜)和S(正交)是硫的两种同素异形体。
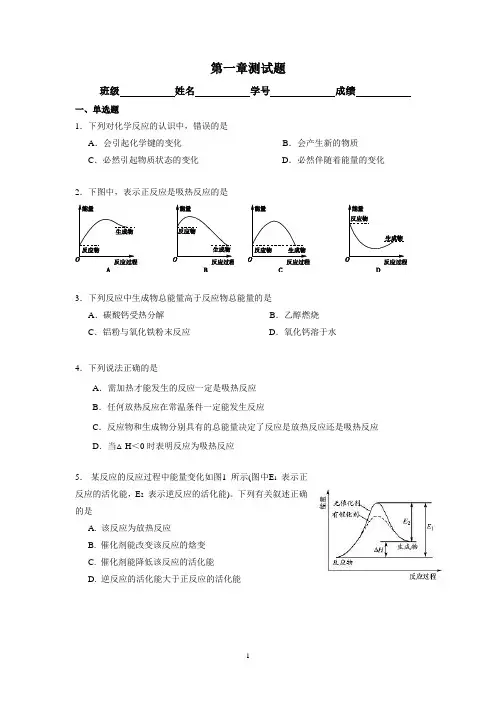
第一章测试题班级姓名学号成绩一、单选题1.下列对化学反应的认识中,错误的是A.会引起化学键的变化B.会产生新的物质C.必然引起物质状态的变化D.必然伴随着能量的变化2.下图中,表示正反应是吸热反应的是3.下列反应中生成物总能量高于反应物总能量的是A.碳酸钙受热分解B.乙醇燃烧C.铝粉与氧化铁粉末反应D.氧化钙溶于水4.下列说法正确的是A.需加热才能发生的反应一定是吸热反应B.任何放热反应在常温条件一定能发生反应C.反应物和生成物分别具有的总能量决定了反应是放热反应还是吸热反应D.当△H<0时表明反应为吸热反应5.某反应的反应过程中能量变化如图1 所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。
下列有关叙述正确的是A. 该反应为放热反应B. 催化剂能改变该反应的焓变C. 催化剂能降低该反应的活化能D. 逆反应的活化能大于正反应的活化能6.1g 碳与适量水蒸气反应生成CO 和H 2,需吸收10.94kJ 热量,此反应的热化学方程式为A.C + H 2O == CO + H 2 ΔH = +131.3 kJ·mol -1B. C(s)+ H 2O(g) == CO(g) + H 2(g) ΔH = +10.94 kJ·mol -1C. C(s)+ H 2O(l) == CO(g) + H 2(g) ΔH = +131.3 kJ·mol -1D. C(s)+ H 2O(g) == CO(g) + H 2(g) ΔH = +131.3 kJ·mol -17.已知:H 2(g)+F 2(g)===2HF(g) ΔH = -270 kJ· mol -1,下列说法正确的是A .2 L 氟化氢气体分解成1 L 氢气和1 L 氟气吸收270 kJ 热量B .1 mol 氢气与1 mol 氟气反应生成2 mol 液态氟化氢放出的热量小于270 kJC .在相同条件下,1 mol 氢气与1 mol 氟气的能量总和大于2 mol 氟化氢气体的能量D .1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270 kJ 热量8.下列各组中的两个反应,前一个反应放出的热量比后一个反应放出的热量多的是(反应物参与反应的物质的量均按化学方程式中的化学计量数计算)①2H 2(g)+O 2(g)===2H 2O(g) 2H 2(g)+O 2(g)===2H 2O(l)②C(s)+O 2(g)===CO 2(g) C(s)+12O 2(g)===CO(g) A .只有① B .只有② C .①②D .①②都不符合题意9.已知热化学方程式:SO2(g)+ 12O 2(g) SO 3(g) △H = -98.32 kJ /mol ,在容器中充入1molSO 2和0.5molO 2充分反应,最终放出的热量为A .98.32 kJB .196.64kJ /molC .<98.32 kJD .>98.32 kJ10.已知H 2(g)+Cl 2(g)=2HCl(g) △H = -184.6 kJ·mol -1, 则反应:HCl(g)=12H 2(g)+12Cl 2(g)的△H 为:A .+184.6 kJ·mol -1B .-92.3 kJ·mol -1C .-369.2 kJ·mol -1D . +92.3 kJ·mol -111. 已知:2Zn (s )+O 2(g )=2ZnO (s ) △H =-701.0kJ·mol -12Hg (l )+O 2(g )=2HgO (s ) △H =-181.6kJ·mol -1则反应Zn (s )+ HgO (s )=ZnO (s )+ Hg (l )的△H 为A . +519.4kJ·mol -1B .+259.7 kJ·mol -1C . -259.7 kJ·mol -1D . -519.4kJ·mol -112.已知:2CO(g)+O 2(g) 2CO 2(g) △H =-566kJ·mol -1N 2(g)+O 2(g) 2NO(g) △H =+180kJ·mol -1则2CO(g)+2NO(g) N 2(g)+2CO 2(g) 的△H 是A .-386 kJ·mol -1B .+386 kJ·mol -1C .-746 kJ·mol -1D .+746 kJ·mol -113.根据以下3个热化学方程式:2H 2S(g) + 3O 2(g) = 2SO 2(g) + 2H 2O(l) △H =-Q 1 kJ/mol2H 2S(g) + O 2(g) = 2S (s) + 2H 2O(l) △H =-Q 2 kJ/mol2H 2S(g) + O 2(g) =2S (s) + 2H 2O(g) △H =-Q 3 kJ/mol判断Q 1、Q 2、Q 3三者关系正确的是A . Q 1>Q 2>Q 3B . Q 1>Q 3>Q 2C . Q 3>Q 2>Q 1D . Q 2>Q 1>Q 3 14.已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(l Q 、2Q 均为正值):22H (g)+Cl (g)2HCl(g)+Q H (g)+Br (g)2HBr(g)+Q →→ △H =-Q 1 kJ/mol 22g )2H C l (g )+QH (g )+B r (g )2H B r (g )+Q →→ △H =-Q 2 kJ/mol 有关上述反应的叙述正确的是A .12Q >QB .生成物总能量均高于反应物总能量C .生成1molHCl 气体时放出l Q 热量D .1mol HBr(g)具有的能量小于1mol HBr(1)具有的能量15.根据碘与氢气反应的热化学方程式(i) I 2(g) + H 2(g)2HI(g) △H = -9.48 kJ/mol (ii) I 2(S) + H 2(g)2HI(g) △H = +26.48 kJ/mol下列判断正确的是A .254g I 2(g)中通入2gH 2(g),反应放热9.48 kJB .1 mol 固态碘与1 mol 气态碘所含的能量相差17.00 kJC .反应(i)的产物比反应(ii)的产物稳定D .反应(ii)的反应物总能量比反应(i)的反应物总能量低16.在298K 、100kPa 时,已知:2222()(g)2()H O g O H g =+ ⊿1H 22(g)(g)2l(g)Cl H HC += ⊿2H 2222(g)2(g)4l(g)(g)Cl H O HC O +=+ ⊿3H 则⊿3H 与⊿1H 和⊿2H 间的关系正确的是A .⊿3H =⊿1H +2⊿2HB ⊿3H =⊿1H +⊿2HC. ⊿3H =⊿1H -2⊿2HD. ⊿3H =⊿1H - ⊿2H17.已知:2CO(g)+O 2(g)=2CO 2(g) ΔH =-566 kJ/molNa 2O 2(s)+CO 2(g)=Na 2CO 3(s)+ 21O (g)2ΔH =-226 kJ/mol 根据以上热化学方程式判断,下列说法正确的是A .CO 的燃烧热为283 kJB .右图可表示由CO 生成CO 2的反应过程和能量关系C .2Na 2O 2(s)+2CO 2(s)=2Na 2CO 3(s)+O 2(g) ΔH >-452 kJ/molD .CO(g)与Na 2O 2(s)反应放出509 kJ 热量时,电子转移数为6.02×1023二、填空题18.由氢气和氧气反应生成1 mol 水蒸气放热241.8kJ ,写出该反应的热化学方程式:_ 。

第一章《化学反应与能量》测试题一、单选题(每小题只有一个正确答案)1.下列反应不需要加热就能进行的吸热反应是()A.碳酸钙分解 B.甲烷在氧气中燃烧C.灼热的炭与二氧化碳反应 D.Ba(OH)2•8H2O与NH4Cl反应2.已知氢气和碳燃烧的热化学方程式为:①2H2(g)+O2(g)=2H2O(l) △H1=-akJ·mol-1②H2(g)+1/2O2(g)=H2O(g) △H2=-bkJ·mol-1③C(s)+1/2O2(g)=CO(g) △H3=-ckJ·mol-1④C(s)+O2(g)=CO2(g) △H4=-dkJ·mol-1下列说法错误的是A.氢气的燃烧热为△H=-akJ·mol-1B.c<dC.一氧化碳的燃烧热为△H=-(d-c)kJ·mol-1D.0.5a>b3.将煤块粉碎、经脱硫处理、在适当过量的空气中燃烧, 这样处理的目的是:①使煤充分燃烧, 提高煤的利用率②减少SO2的产生,避免造成“酸雨”③减少有毒的CO产生, 避免污染空气④减少CO2的产生,避免“温室效应”A.①②③B.②③④C.①③④D.①②③④4.下列说法正确的是()A.所有反应的反应热都可以由实验直接测定B.任何化学反应都需要用活化能来引发C.200ºC、101KPa时,1g氢气与碘蒸气作用生成HI气体,放出7.45kJ热量,则此过程的热化学方程式可表示为:molkJHHIIHggg/9.142)()(2)(2-=∆=+D.物质发生化学变化都伴随着能量变化5.偏二甲肼[(CH3)2N-NH2](N为-2价)与N2O4是常用的火箭推进剂,发生的化学反应如下:(CH3)2N-NH2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(g)△H<0,下列说法不正确的是()A.该反应在任何情况下都能自发进行B.1mol(CH3)2N-NH2含有11mol共价键C.反应中,氧化产物为CO2,还原产物为N2 D.反应中,生成1molCO2时,转移8mole-6.已知:①2H2(g)+O2(g)===2H2O(l) ΔH=-570.0 kJ·mol-1;②CO(g)+1 2O2(g)===CO2(g) ΔH=-280 kJ·mol-1。

人教版选修4《第1章化学反应与能量》单元测试卷一、选择题(单选,共12分)1.(2分)下列说法中,正确的是()A.物质发生化学反应时不一定伴随着能量变化B.伴随能量变化的物质变化都是化学变化C.在一个确定的化学反应中,反应物的总能量与生成物的总能量一定不同D.在一个确定的化学反应中,反应物的总能量总是高于生成物的总能量2.(2分)热化学方程式中的化学计量数表示()A.分子个数 B.原子个数 C.物质的质量D.物质的量3.(2分)已知热化学方程式:2H2O(l)=2H2(g)+O2(g);△H1=+571.6kJ/mol,2H2(g)+O2(g)=2H2O(g);△H2=﹣483.6kJ/mol.当1g 液态水变成气态水时,对其热量变化的下列描述:①放出;②吸收;③2.44kJ;④4.88kJ;⑤88kJ,其中正确的是()A.②和⑤B.①和③C.②和④D.②和③4.(2分)已知:CH3CH2CH2CH3(g)+6.5O2(g)═4CO2(g)+5H2O(l)△H=﹣2878kJ•mol﹣1,(CH3)2CHCH3(g)+6.5O2(g)═4CO2(g)+5H2O(l)△H=﹣2869kJ•mol﹣1下列说法正确的是()A.正丁烷分子储存的能量大于异丁烷分子B.正丁烷的稳定性大于异丁烷C.异丁烷转化为正丁烷的过程是一个放热过程D.异丁烷分子中的碳氢键比正丁烷的多5.(2分)由氢气和氧气反应生成1mol水蒸气放出241.8kJ的热量,1g水蒸气转化为液态水放出2.45kJ的热量,则下列热化学方程式书写正确的是()A.H2(g)+O2(g)=H2O(l);△H=﹣285.9 kJ/molB.H2(g)+O2(g)=H2O(l);△H=﹣241.8 kJ/molC.H2(g)+O2(g)=H2O(l);△H=+285.9 kJ/molD.H2(g)+O2(g)=H2O(l);△H=+241.8 kJ/mol6.(2分)乙醇汽油是一种由粮食及各种植物纤维加工成的燃料乙醇和普通汽油按一定比例混配形成的新型替代能源.下列关于乙醇汽油的说法不正确的是()A.推广使用乙醇汽油有助于减轻大气污染,改善大气环境B.使用乙醇汽油有助于促进粮食(特别是陈粮)转化,提高农民收入,促进经济发展C.使用乙醇汽油可大大降低油料价格D.乙醇是二级能源,也是一种可再生能源二、选择题(多选,1~2个选项符合题意,共36分)7.(3分)已知Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0;则下列关于该反应的叙述不正确的是()A.该反应中旧键断裂需吸收能量,新键形成需放出能量,所以物质总能量不变B.上述热化学方程式中的△H的值与反应物的用量无关C.该反应的化学能可以转化为电能D.反应物的总能量高于生成物的总能量8.(3分)下列说法或表示方法中正确的是()A.等质量的硫蒸气和硫磺固体分别完全燃烧,后者放出的热量多B.氢气的燃烧热为285.8kJ•mol﹣1,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=+571.6 kJ•mol﹣1C.Ba(OH)2•8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l)△H<0D.已知中和热为57.3kJ•mol﹣1,若将含0.5mol H2SO4的溶液与含1mol NaOH的溶液混合,放出的热量可能大于57.3kJ9.(3分)同温同压下,下列各热化学方程式(△H均小于0)中反应热的绝对值最大的是()A.2A(l)+B(l)=2C(g)B.2A(g)+B(g)=2C(g)C.2A(g)+B(g)=2C(l)D.2A(l)+B (l)=2C(l)10.(3分)含有11.2g KOH的稀溶液与1L 0.1mol/L的H2SO4溶液反应,放出11.46kJ的热量,该反应的中和热用化学方程式表示为()A.KOH(aq)+H2SO4(aq )═K2SO4(aq)+H2O(l)△H=﹣11.46 kJ/molB.2KOH(aq)+H2SO4(aq)═K2SO4(aq)+2H2O(l)△H=﹣114.6 kJ/molC.2KOH(aq)+H2SO4(aq)═K2SO4(aq)+2H2O(l)△H=114.6 kJ/molD.KOH(aq)+H2SO4(aq )═K2SO4(aq)+H2O(l)△H=﹣57.3 kJ/mol11.(3分)已知25℃、101kPa条件下:4Al(s)+3O2(g)═2Al2O3(s)放出2834.9kJ热量,4Al(s)+2O3(g)═2Al2O3(s)放出3119.91kJ热量.由此得出的结论正确的是()A.等质量的O2比O3能量低,由O2变O3为吸热反应B.等质量的O2比O3能量低,由O2变O3为放热反应C.O3比O2稳定,由O2变O3为吸热反应D.O2比O3稳定,由O2变O3为放热反应12.(3分)已知标准状况下5.6LCO完全燃烧放出的热量能使200g 15.5℃的水温度升高到100℃,水的比热容是4.186×10﹣3kJ/(g•℃),下列表示CO燃烧热的热化学方程式是()A.CO(g)+O2(g)=CO2(g);△H=﹣282.95 kJ/molB.2CO(g)+O2(g)=2CO2(g);△H=﹣565.9 kJ/molC.CO(g)+O2(g)=CO2(g);△H=﹣70.7 kJ/molD.CO(g)+O2(g)=CO2(g);△H=﹣565.9 kJ/mol13.(3分)在相同条件下,下列三个化学反应反应热分别以△H1、△H2、△H3表示,(1)2H2(g)+O2(g)=2H2O(g);△H1(2)2H2(g)+O2(g)=2H2O(1);△H2(3)H2(g)+O2(g)═H2O(g);△H3,则△H1、△H2和△H3的关系是()A.△H1=△H2=△H3B.△H1>△H2,△H1=2△H3C.△H1<△H2,△H2=2△H3D.无法比较14.(3分)1mol CH4气体完全燃烧生成CO2(g)和H2O(g)放出的热量是802kJ,但当不完全燃烧生成CO (g)和H2O(g)放出的热量是519kJ,如果将1mol CH4与一定量的O2燃烧生成CO(g)、CO2(g)和H2O (g),并释放出660.5kJ的热量,则一定量的O2的质量为()A.32 g B.48 g C.56 g D.64 g15.(3分)已知在101kPa时,C(石墨)、H2和CO的燃烧热分别为393.5kJ/mol、285.8kJ/mol和282.8kJ/mol.现有H2和CO组成的混合气体112L(标况),经充分燃烧后,放出总热量为1420kJ,并生成液态水.下列热化学方程式或描述中正确的是()A.2CO(g)+O2(g)═2CO2(g);△H=+282.8 kJ/molB.2H2(g)+O2(g)═2H2O(g);△H=﹣571.6 kJ/molC.C(石墨,s)+O2(g)═CO(g);△H=﹣110.7 kJ/molD.燃烧前混合气体中H2的体积百分数为50%16.(3分)已知H﹣H键能为436KJ/mol,H﹣N键能为391KJ/mol,根据化学方程式:N2+3H2=2NH3△H=﹣92KJ/mol,则N≡N键的键能是()A.431 KJ/mol B.946 KJ/mol C.649 KJ/mol D.869 KJ/mol17.(3分)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是①CH3OH(g)+H2O(g)═CO2(g)+3H2(g);△H=+49.0kJ•mol﹣1②CH3OH(g)+O2(g)═CO2(g)+2H2(g);△H=﹣192.9kJ•mol﹣1下列说法正确的是()A.CH3OH的燃烧热为192.9kJ•mol﹣1B.反应①中的能量变化如图所示C.CH3OH转变成H2的过程一定要吸收能量D.根据②推知反应:CH3OH(l)+O2(g)=CO2(g)+2H2(g)的△H>﹣192.9kJ•mol﹣118.(3分)已知:①2C(s)+O2(g)═2CO(g)△H=﹣221.0kJ/mol②C(s)+O2(g)═CO2(g)△H=﹣393.51kJ/mol计算反应C(s)+CO2(g)═2CO(g)的反应热△H为()A.+172.51 kJ/mol B.﹣283.01 kJ/mol C.+283.01 kJ/mol D.+504.00 kJ/mol三、(本题包括4小题,共32分)19.(6分)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量.(1)写出该反应的热化学方程式.(2)已知H2O(l)═H2O(g)△H=+44kJ•mol﹣1,则16g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是kJ.(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是.20.(6分)已知热化学方程式:Mg(OH)2(S)=MgO(S)+H2O(g);△H1=+81.5kJ/molAl(OH)3(S)=Al2O3(S)+H2O(g);△H1=+87.7kJ/mol(1)Mg(OH)2和Al(OH)3起阻燃作用的主要原因是.(2)等质量Mg(OH)2和Al(OH)3起阻燃作用效果较好的是.21.(6分)如图所示,写出下列热化学方程式,并回答问题.(1).(2).(3)Q1与Q2的关系:Q1Q2(填“>”、“<”或“=”).22.(14分)化学反应过程发生物质变化同时常常伴能量变化,它以热能形式表现出来,叫反应热,它有很多种,燃烧热,中和热等.(1)许多化学反应的反应热可以直接测量,测量仪器叫做.(2)下列△H表示物质燃烧热的是(填序号);表示中和热的是(填“△H1、△H2、或△H3”等).A.2H2(g)+O2(g)═2H2O(l);△H1B.C(s)+O2(g)═CO(g);△H2C.CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H3D.C(s)+O2(g)═CO2(g);△H4E.C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l);△H5F.NaOH(ag)+HCl(ag)═NaCl(ag)+H2O(l);△H6G.2NaOH(ag)+H2SO4(ag)═Na2SO4(ag)+2H2O(l);△H7(3)已知15g乙烷完全燃烧生成CO2和液态水,放热a kJ,下列热化学方程式正确是.A.C2H6(g)+O2(g)═2CO2(g)+3H2O(l);△H1=+2a kJ/molB.C2H6(g)+O2(g)═2CO2(g)+3H2O(g);△H2=﹣2a kJ/molC.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l);△H3=﹣4a kJ/molD.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g);△H4=﹣2a kJ/mol(4)充分燃烧一定丁烷放出热量161.9kJ,生成的CO2恰好与5mol/L 100mL KOH溶液完全反应生成正盐,则燃烧1mol丁烷放出能量为.(5)进一步研究表明,化学反应能量变化与键能有关.键能简单理解断开1mol化学键吸收能量.下表是键能X=.四、(本题包括2道,共20分)23.(12分)CO、CH4均为常见的可燃性气体.(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是(2)已知在101kPa时,CO的燃烧热为283kJ/mol.相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是.(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2中完全燃烧后,恢复到原温度和压强.①若混合气体与O2恰好完全反应,产生bmL CO2,则混合气体中CH4的体积分数为(保留2位小数).②若燃烧后气体体积缩小了mL,则a与b关系的数学表达式是.24.(8分)①CaCO3(s)=CaO(s)+CO2(g);△H1=+175.7kJ/mol,②C(s)+O2(g)=CO2(g);△H2=﹣393.5kJ/mol.求1t 碳酸钙生成生石灰理论上需含杂质10%焦炭多少千克?人教版选修4《第1章化学反应与能量》单元测试卷参考答案一、选择题(单选,共12分)1.C;2.D;3.D;4.A;5.A;6.C;二、选择题(多选,1~2个选项符合题意,共36分)7.A;8.D;9.C;10.D;11.A;12.A;13.B;14.C;15.C;16.B;17.D;18.A;三、(本题包括4小题,共32分)19.N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.625 kJ•mol-1;408.8;生成物为氮气和水,不污染空气;20.Mg(OH)2和Al(OH)3受热分解时吸收大量的热,使环境温度下降;同时生成的耐高温、稳定性好的MgO、Al2O3覆盖在可燃物表面,阻燃效果更佳;Mg(OH)2;21.A(g)+B(g)=C(g)△H=-Q1KJ/mol;C(g)=A(g)+B(g)△H=+Q2KJ/mol;=;22.量热计;△H4、△H5;△H6;C;2590.4kJ;433.75;四、(本题包括2道,共20分)23.1:4;CH4(g)+2O2(g)=CO2(g)+2H2O(1);△H=-891.45kJ/mol;0.33;b≥a;24.。

《化学反应与能量》单元检测题一、单选题1.实验室用4mol SO2与2molO2在一定条件下进行下列反应:2SO2(g)+O2(g)2SO3(g);△H=-197kJ·mol-1,当放出 315.2kJ热量时,SO2转化率为A.40% B.50% C.80% D.90% 2.下列图中的实验,能达到实验目的的是( )A.证明稳定性:Na2CO3>NaHCO3B.证明非金属性:Cl>Br>IC.验证镁和盐酸反应的热效应D.除去 Cl2中的杂质气体 HCl3.下列各组物质的燃烧热相等的是A.碳和二氧化碳B.1mol碳和3mol碳C.3mol乙炔(C2H2)和1mol苯D.淀粉和纤维素4.《淮南万毕术》中有“曾青得铁,则化为铜,外化而内不化”,下列说法中正确的是A.“外化”时化学能转化为热能B.“化为铜”表明铁转化为铜C.“内不化”是因为内部的铁活泼性较差D.反应中溶液由蓝色转化为黄色5.根据下图提供的信息,下列所得结论正确的是A .该反应是吸热反应B .该反应的生成物比反应物稳定C .该反应一定可以设计成为原电池D .该反应向外界放出的热量为E 2-E 36.下列热化学方程式及有关应用的叙述中,正确的是( )A .若2H 2(g)+O 2(g)=2H 2O(g) ΔH=-483.6kJ/mol ,则H 2的燃烧热为241.8 kJ/molB .已知强酸与强碱在稀溶液里反应的中和热为57.3 kJ/mol ,则H 2SO 4(aq)+ Ba(OH)2(aq)=BaSO 4(s)+2H 2O(l) ΔH =-114.6 kJ/molC .500℃、30MPa 下,将0.5mol N 2和1.5mol H 2置于密闭的容器中充分反应生成NH 3(g),放热19.3kJ ,其热化学方程式为:N 2(g)+3H 2(g) 2NH 3(g) ΔH =-38.6 kJ/molD .已知25℃、101kPa 条件下:4Al(s)+3O 2(g)=2Al 2O 3(s) ΔH =-2834.9 kJ/mol ,4Al(s)+2O 3(g)=2Al 2O 3(s) ΔH =-3119.1 kJ/mol ,则O 2比O 3稳定7.已知胆矾溶于水时,溶液温度降低。

第一章《化学反应与能量》单元测试题一、单选题(每小题只有一个正确答案)1.下列有关光合作用的说法不正确的是()A.将无机物转化为有机物 B.反应物的总能量高于生成物的总能量C.将太阳能转变为化学能 D.是自然界碳元素循环的重要途径2。
H2与O2发生反应的过程用模型图示如下(“﹣"表示化学键):下列说法不正确的是 ( )A.过程Ⅰ是吸热过程B.过程Ⅲ一定是放热过程C.该反应过程所有旧化学键都断裂,且形成了新化学键D.该反应的能量转化形式只能以热能的形式进行3。
下列说法不正确的是( )A. 1 g氢气在氧气中完全燃烧生成气态水,放出的热量为120。
9 kJ,氢气的燃烧热大于 241。
8 kJ•mol﹣1B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放出的热量为19.3 kJ,其热化学方程式为N2(g)+3H2(g)====2NH3(g)ΔH=﹣38.6 kJ·mol−1C.常温下,若反应C(s)+CO2(g)====2CO(g)不能自发进行,则该反应的ΔH>0D.已知中和热为﹣57.3 kJ·mol−1,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量要大于57.3 kJ4。
对于:2C4H10(g)+13O2(g)===8CO2(g)+10H2O(l) ΔH=-5 800 kJ·mol-1的叙述错误的是()A.该反应的反应热为ΔH=-5 800 kJ·m ol-1,是放热反应B.该反应的ΔH与各物质的状态有关,与化学计量数也有关C.该式的含义:25 ℃、101 kPa下,2 mol C4H10气体完全燃烧生成CO2和液态水时放出热量 5800 kJD.该反应为丁烷燃烧的热化学方程式,由此可知丁烷的燃烧热为-5 800 kJ·mol-15。
第一章《化学反应与能量》测试题原子量:H-1 O-16 C=12 Al-27 N-14 Ca- 40 V-51 Ni- 59 Cu-64一、单项选择题(每小题3分,共24分)1.下列反应属于吸热反应的是( )A. C 6H 12O 6(葡萄糖aq)+6O 2 6CO 2+6H 2OB. CH 3COOH+KOH CH 3COOK+H 2OC. 反应物的总能量大于生成物的总能量D .破坏反应物全部化学键所需能量大于破坏生成物全部化学键所需能量2.下列说法正确的是( )A .热化学方程式中,如果没有注明温度和压强,则表示反应热是在标准状况下测得的数据B .升高温度或加入催化剂,可以改变化学反应的反应热C .据能量守恒定律,反应物的总能量一定等于生成物的总能量D .物质发生化学变化一定伴随着能量变化3.下列各组热化学方程式中,△H 1>△H 2的是①C(s)+O 2(g)===CO 2(g) △H 1 C(s)+12O 2(g)===CO(g) △H 2②S(s)+O 2(g)===SO 2(g) △H 1 S(g)+O 2(g)===SO 2(g) △H 2③H 2(g)+12O 2(g)===H 2O(l) △H 1 2H 2(g)+O 2(g)===2H 2O(l) △H 2④CaCO 3(s)===CaO(s)+CO 2(g) △H 1 CaO(s)+H 2O(l)===Ca(OH)2(s) △H 2A .①B .②③④C .④D .①②③4. 已知H 2(g)+Cl 2(g)=2HCl(g) △H =―184.6kJ·m ol -1, 则反应HCl(g)=12H 2(g)+12Cl 2(g)的△H 为A .+184.6kJ·mol -1B .―92.3kJ·mol -1C .+92.3kJ·mol -1D .―369.2kJ·mol -15. 已知:(1)Zn (s )+12O 2(g )=== ZnO(s) ΔH= -348.3 kJ·mol -1,(2)2Ag(s)+ 12O 2(g )=== Ag 2O(s) ΔH= -31.0 kJ·mol -1,酶则Zn (s )+ Ag 2O(s) === ZnO(s)+ 2Ag(s)的ΔH 等于( )A . -317.3 kJ·mol -1B . -379.3 kJ·mol -1C .-332.8 kJ·mol -1D .317.3 kJ·mol -16. SF 6是一种优良的绝缘气体,分子结构中只存在S-F 键。
《化学反应与能量》单元检测题一、单选题1.下列反应属于吸热反应的是A.甲烷在空气中燃烧B.酸碱中和反应C.氯化铵受热分解D.镁条与盐酸反应2.分析下面化学键键能数据,判断下列分子中受热时最不稳定的是( )化学键H-H H-F H-Br H-I键能(kJ/mol) 436 565 368 297A.氢气B.氟化氢C.溴化氢D.碘化氢3.一种利用热化学循环制氢的原理如图所示。
下列关于该循环的说法正确的是()A.能量转化形式为化学能→太阳能B.取之不尽的太阳能是可再生能源C.Mn元素表现出三种化合价D.总反应的热化学方程式为:2H2O(l)=O2(g)+2H2(g)△H>04.有关能量与能源的说法正确的是A.原电池是将电能转变为化学能的装置B.逆反应的活化能总是大于正反应的活化能C.新能源中的太阳能、风能、生物质能等,都是可再生能源D.同温同压下,22H(g)+Cl(g)=2HCl(g)在光照和点燃条件下的ΔH不同5.下列有关化学反应与能量的说法正确的是A.化学反应中能量变化的大小与反应物的质量多少无关B.燃煤发电中的能量转化过程是:化学能→热能→机械能→电能C.风力、流水、原煤、电力、天然气都属于一次能源D.石墨和金刚石由同种元素组成,故它们之间的相互转化不涉及能量变化6.强酸与强碱的稀溶液发生中和反应的热效应为: H+(aq)+OH-(aq)===H2O(l)ΔH =-57.3kJ·mol-1。
分别向1 L 0.5mol/L的NaOH溶液中加入①浓硫酸;②稀硫酸;③稀盐酸,恰好完全反应的热效应分别为ΔH1、ΔH2、ΔH3,下列关系正确的是( )A.ΔH1>ΔH2>ΔH3B.ΔH1<ΔH2<ΔH3C.ΔH1=ΔH2<ΔH3D.ΔH1<ΔH2=ΔH37.下列化学反应属于吸热反应的是A.木炭燃烧 B.铝热反应C.碳与二氧化碳在高温下反应 D.氢氧化钠和硝酸反应8.下列说法中正确的是A.因为3O2=2O3是吸热反应,所以臭氧比氧气的化学性质更活泼B.需要加热的化学反应一定是吸热反应,不需要加热就能进行的反应一定是放热反应C.吸热反应就是反应物的总能量比生成物的总能量高D.物质发生化学反应时都伴随着能量变化,伴随能量变化的物质变化也一定是化学变化9.下列各项与氧化还原反应无关的是A.明矾净化水B.燃烧C.臭氧消毒游泳池D.食物的腐败10.下列物质的变化过程中:①H2在Cl2中燃烧②碳酸钙分解③铝热反应④酸碱中和反应⑤缓慢氧化⑥H2O分解⑦NaOH固体溶于水⑧铁和稀H2SO4反应⑨Ba(OH)2·8H2O和NH4Cl反应⑩工业合成氨,说法正确的是:A.属于放热反应的有:①③④⑤⑦⑧⑩B.反应⑨在搅拌的过程中有刺激性气味的气体产生可以证明该反应是吸热反应C.擦拭过机器的废旧棉纱在不通风的角落里自燃的现象可以证明缓慢氧化是放热反应D.目前科学研究的前沿是寻找合适的催化剂,降低反应⑥的焓变,从而使水的分解更容易11.下列说法或表示方法正确的是A.等质量的硫蒸气和硫粉分别完全燃烧,后者放出的热量多B.化学反应A2(g)+2B2(g)===2AB2(g)能量变化如图所示,该反应为放热反应C.在25℃、101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)2H2O(l)△H= -285.8kJ·mol-1D.在稀溶液中,H+(aq)+OH-(aq)H2O(l)△H=-57.3kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,整个过程放出的热量大于57.3kJ12.已知:2Zn(s)+O2(g)=2ZnO(s) △H1=-701.0kJ·mol-1①,2Hg(l)+O2(g)=2HgO(s)△H2=-181.6kJ·mol-1②,则Zn(s)+HgO(s)=ZnO(s)+Hg(l)的△H为A.+519.4kJ·mol-1B.-181.6kJ·mol-1C.-259.7kJ·m ol-1D.-519.4kJ·mol-113.下列化学用语对事实的表述不正确...的是A.由Na和Cl 形成离子键的过程:B.Na2S做沉淀剂可处理含Hg2+的工业污水:Hg2++S2-=HgS↓C.CH3COOH溶液与NaOH溶液反应放出热量H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1D.闪锌矿(ZnS)经CuSO4溶液作用转化为铜蓝(CuS):ZnS+Cu2+=CuS+Zn2+二、实验题14.某化学兴趣小组要完成中和热的测定。
高二化学选修4第一章化学反应与能量单元测试题、选择题(本题包括 16小题,每小题3分,共48分,每小题只有一个选项符合题意) 1.下列叙述正确的是B. 水力是二次能源D.水煤气是一次能源)A. 化学反应除了生成新物质外,还伴随着能量的变化B. 放热反应都不需要加热就能发生C. 吸热反应在一定条件(如常温、加热等)也能发生D. 化学反应是放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量3 •未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。
下列 属于未来新能源标准的是 4•下列各组热化学方程式中,△ H i > △ H 2的是A .①B .④C .②③④D .①②③5、下列说法或表示方法正确的是A .等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多B. 由C (石墨)= C (金刚石);△ H = + I.90 kJ/mol 可知,金刚石比石墨稳定C.在101kPa 时,2g 氢气完全燃烧生成液态水,放出285.8kJ 热量,氢气燃烧的热化学方程式表示为:2H 2(g )+O 2(g )= 2H 2OQ ); △ H = - 285.8kJ/molD. 在稀溶液中, H +(aq )+ OH -(aq ) = H 20(1); △ H = - 57.3kJ/mol,若将含 0.5molH 2SO 4的浓硫酸与含ImolNaOH 的溶液混合,放出的热大于57.3kJ6. 下列反应中生成物总能量高于反应物总能量的是 A .碳酸钙受热分解 B .乙醇燃烧 C .铝粉与氧化铁粉末反应D .氧化钙溶于水7. 据人民网2001年9月4日报道,有一集团拟将在太空建立巨大的集光装置,把太阳光变 TiO 2成激光用于分解海水制氢,其反应可表示为: 2H 20激光=2H 202 。
有下列几种说法:① 水分解反应是放热反应;② 氢气是一级能源;③ 使用氢气作燃料有助于控制温室 效应;④若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条 件。
高中化学学习资料金戈铁骑整理制作人教版选修 4 第一章《化学反响与能量》单元测试题1.以下措施不能够达到节能减排目的的是()A .利用太阳能制氢燃料B.用家用汽车代替公交车C.利用潮汐能发电 D .用节能灯代替白炽灯2. 未来氢气将作为新能源的优点的是()①燃烧时发生氧化反响②充分燃烧的产物不污染环境③氢气是一种再生能源④燃烧时放出大量热量A. ①②③B. ①②④C. ①③④D. ②③④3.以下变化过程,属于放热反响的是()①液态水变成水蒸气② 酸碱中和反响③ 浓H2SO4稀释④ 固体NaOH溶于水⑤ H2在Cl 2中燃烧⑥ 弱酸电离A 、②③④⑤B 、②③④C、②⑤D、①③⑤4.以下对化学反响的认识错误的选项是)(A .必然有化学键的变化B .必然会产生新的物质C.必然有物质状态的变化 D .必然陪同着能量的变化5.25℃、 101 kPa 下, 2g 氢气燃烧生成液态水,放出285.8kJ 热量,表示该反响的热化学方程式正确的选项是()A . 2H2(g)+O 2(g) == 2H 2O(1)△H =―/ molB.2H2(g)+ O 2(g) == 2H 2O(1)△H = +571.6 kJ /molC. 2H2(g)+O 2(g) == 2H 2O(g)△H =― 571.6 kJ/molD . H2(g)+1/2O 2(g) == H 2O(1)△ H=―/ mol6.热化学方程式 C(s)+ H2O(g)CO(g) +H 2(g);△ H=表示()A .碳和水反响吸取 131.3kJ 能量B . 1mol 碳和 1mol 水反响生成一氧化碳和氢气,并吸取131.3kJ 热量C. 1mol 固态碳和 1mol 水蒸气反响生成一氧化碳气体和氢气,并吸热D . 1 个固态碳原子和 1 分子水蒸气反响吸热7.已知 25℃、 101kPa 条件下:4Al (s) + 3O 2 (g) == 2Al 2O3 (s)-1△ H = -2834.9 kJ · mol4Al (s) +2O 3 (g) == 2Al 2O3 (s)△ H = -3119.91 kJ ·mol -1由此得出的结论正确的选项是()A .等质量的O2比 O3能量低,由O2变 O3为吸热反响B .等质量的O2比 O3能量低,由O2变 O3为放热反响C. O3比 O2牢固,由O2变 O3为吸热反响D . O2比 O3牢固,由O2变 O3为放热反响8.在同温同压下 ,以下各组热化学方程式中,△H2>△ H 1的是A . 2H2(g)+O 2(g) =2H 2O(g),△ H1; 2H 2(g)+O 2(g) =2H 2O(l) ,△ H2B. S(g)+O2(g)= SO2(g) ,△H 1; S(s)+O2(g) =SO2(g),△H 2 1△ H1; C(s)+O 2(g)= CO2(g),△ H2 C. C(s)+ O2(g)= CO(g) ,211D. H2(g)+Cl 2(g)= 2HCl(g) ,△H1;2H2(g)+2Cl 2(g) =HCl(g) ,△ H29.甲烷是一种高效干净的新能源,0.25mol 甲烷完好燃烧生成液态水时放出222.5kJ 热量,则以下热化学方程式中正确的选项是()A. 2CH 4(g) + 4O 2 (g) == 2CO2(g) + 4H 2O(l)H= +890 kJ mol·-1B. CH 4(g) + 2O 2(g) == CO2(g) +2H 2O(l)H = +890 kJ mol·-1C. CH 4(g) + 2O 2(g) == CO2(g) +2H 2O(l)H = -890 kJ mol·-1D. 2CH 4(g) + 4O 2 (g) == 2CO2(g) + 4H 2O(l)H = - 890 kJ mol·-110.以下关于中和热的说法不正确的选项是()A .已知以下热化学方程式:2H2(g)+O 2(g) === 2H 2O(g)△ H=-484kJ?mol-1,则氢气的燃烧热为242kJ?mol -1B .中和反响的实质是H + 与 OH -结合生成水,若有其他物质生成,这部分反响热不在中和热内C .物质的燃烧热可利用仪器由实验测得D .中和热不包括物质溶解、电离、水合等过程中的热效应11. 已知 H 2(g)、C 2H 4(g)和 C 2H 5OH(1) 的燃烧热分别是285.8kJ mol · -1、1 411.0kJ mol · -1 和kJ ·mol -1 ,则由 C 2H 4(g)和 H 2O(l) 反响生成 C 2H 5OH(l) 的 △ H 为()A. - 44.2 kJ mol · -1B. +44.2 kJ -1mol ·C. - 330 kJ mol · -1D. +330 kJ mol ·-112.已知( 1)H 2( g ) +1/2O 2( g ) ===H 2 O ( g ) △ H 1=a kJ mol · -1 ( 2)2H 2(g ) +O 2 (g ) ===2H 2O (g ) △H 2=b kJ mol · -1 ( 3)H 2( g ) +1/2O 2( g ) ===H 2 O ( l ) △H 3=c kJ mol · -1 ( 4)2H 2(g ) +O 2 (g ) ===2H 2O (l ) △ H 4=d kJ mol · -1 以下关系式中正确的选项是( )A . a<c<0B. b> d>0C.2a=b<0D.2c=d>013. 已知热化学方程式:① C 2H 2 (g) + 5 O 2 (g) == 2CO 2(g) + H 2O(l)H 1= -1301.0 kJ?mol -12② C(s)+ O 2(g) == CO 2(g) △ H 2= -393.5 kJ?mol -1③ H 2(g)+1O 2(g) == H 2O(1)△ H 3 = -285.8 kJ · mol -12则反响④ 2C(s)+ H 2(g) == C 2 H 2(g) 的△ H 为( )A. +228.2 kJ · mol -1B. -228.2 kJ · mol -1C. +1301.0 kJ · mol -1D. +621.7 kJ · mol -114.常温常压下,断裂1mol (理想)气体分子化学键所吸取的能量或形成1mol (理想)气体分子化学键所放出的能量称为键能(单位为-1)下表是一些键能数据 ( KJ ·mol- 1)化学键键能 化学键 键能 化学键 键能 化学键 键能C—H414C— F489H — F565F— F158H-H436H-N391( 1)依照键能数据计算以下反响的反响热△H:CH 4(g) +4F2(g)﹦ CF4( g) +4HF( g)△ H( 2)依照键能和反响热化学方程式1/2N 2(g)+3/2H 2(g) =NH 3 (g )△ H = — 46 kJ mol·-1计算N≡N的键能。
选修4第一章化学反应与能量单元测试题一、选择题(每小题只有一个选项符合题意) 1.下列措施不能达到节能减排目的的是A .利用太阳能制氢燃料B .用家用汽车代替公交车C .利用潮汐能发电D .用节能灯代替白炽灯2.2007年3月,温家宝指出“优化结构、提高效益和降低消耗、保护环境”,这是我国国民经济和社会发展的基础性要求。
你认为下列行为不符合这个要求的是A. 大力发展农村沼气,将废弃的秸轩转化为清洁高效的能源B. 加快太阳能、风能、生物质能、海洋能等清洁能源的开发利用C. 研制开发以水代替有机溶剂的化工涂料D. 将煤转化成气体燃料可以有效地减少“温室效应”的气体产生 3.下列说法正确的是A .物质发生化学变化都伴随着能量变化B .任何反应中的能量变化都表现为热量变化C .伴有能量变化的物质变化都是化学变化D .即使没有物质的变化,也可能有能量的变化4.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。
下列属于未来新能源标准的是①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能A .①②③④B .⑤⑥⑦⑧C .③⑤⑥⑦⑧D .③④⑤⑥⑦⑧5.炽热的炉膛内有反应:C(s)+O 2(g)==CO 2(g);△H = -392KJ/mol ,往炉膛内通入水蒸气时,有如下反应:C(s)+H 2O(g)==H 2(g)+CO(g);△H = +131KJ/mol ,CO(g)+1/2O 2(g)==CO 2(g);△H = -282KJ/mol ,H 2(g)+1/2O 2(g)==H 2O(g);△H =-241KJ/mol ,由以上反应推断往炽热的的炉膛内通入水蒸气时 A .不能节省燃料,但能使炉火瞬间更旺 B .虽不能使炉火瞬间更旺,但可以节省燃料 C .既能使炉火瞬间更旺又可以节省燃料D .既不能使炉火瞬间更旺,又不能节省燃料6.分析右面的能量变化示意图,确定下列选项中正确的是A. 2 A (g )+ B(g) 2 C (g );△H <0B. 2 A (g )+ B(g)2 C (g ); △H >0C. 2A + B 2 C ;△H <0D. 2C 2 A +B ;△H <07.根据下列热化学方程式,判断氢化物的稳定性顺序正确的是21N 2(g)+ 23H 2 (g) =NH 3(g) ;ΔH =-46.19kJ ·mol —1 21H 2(g)+ 21Cl 2(g)=HCl (g) ;ΔH =-92.36kJ ·mol —1 21I 2(g)+ 21H 2 (g) =HI (g) ;ΔH =+25.96kJ ·mol —1 A. HCl>NH 3>HIB.HI > HCl > NH 3C.HCl> HI > NH 3D.NH 3> HI > HCl8.氢气、一氧化碳、辛烷、甲烷的热化学方程式分别为:H 2(g)+1/2O 2(g)=H 2O(l) △H =-285.8kJ/mol CO(g)+1/2O 2(g)=CO 2(g) △H =-283.0kJ/mol C 8H 18(l)+25/2O 2(g)=8CO 2(g)+9H 2O(l) △H =-5518kJ/mol CH 4(g)+2O 2(g)=CO 2(g)+2H 2O(l) △H =-89.3kJ/mol 相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是 A . H 2(g) B . CO(g) C . C 8H 18(l) D . CH 4(g) 9.根据以下3个热化学方程式:2H 2S(g)+3O 2(g)=2SO 2(g)+2H 2O(l) △H =―Q 1 kJ/mol 2H 2S(g)+O 2(g)=2S (s)+2H 2O(l) △H =―Q 2 kJ/mol 2H 2S(g)+O 2(g)=2S (s)+2H 2O(g) △H =―Q 3 kJ/mol判断Q 1、Q 2、Q 3三者关系正确的是A . Q 1>Q 2>Q 3B . Q 1>Q 3>Q 2C . Q 3>Q 2>Q 1D . Q 2>Q 1>Q 3 10.已知热化学方程式:H 2O(g)=H 2(g) + 1/2O 2(g) △H = +241.8kJ /mol H 2(g)+ 1/2O 2(g) = H 2O(1) △H = -285.8kJ /mol当1g 液态水变为水蒸气时,其热量变化是A .吸热88kJB . 吸热2.44KJC .放热44kJD . 吸热44KJ11.同温同压下,已知下列各反应为放热反应,下列各热化学方程式中热量数值最小的是A 、2A ( l ) +B ( l ) = 2C (g ) △H 1 B 、2A ( g ) + B ( g ) = 2C (g ) △H 2 C 、2A ( g ) + B ( g ) = 2C ( l ) △H 3D 、2A ( l ) + B ( l ) = 2C ( l ) △H 4 12.已知热化学方程式:SO 2(g)+ 12O 2(g)SO 3(g) △H = ―98.32kJ /mol ,在容器中充入2molSO 2和1molO 2充分反应,最终放出的热量为低高 物质所具有的总能量2 A (g) + B(g)2 C (g)A.196.64kJ B.196.64kJ/mol C.<196.64kJ D.>196.64kJ13.如下图所示,△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,下列说法或表示式正确的是A. C(s、石墨)== C(s、金刚石)△H= +1.9 kJ•mol-1B. 石墨和金刚石的转化是物理变化C. 金刚石的稳定性强于石墨D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ14.已知25℃、101kPa条件下:4Al (s) + 3O2 (g) == 2Al2O3 (s) △H = -2834.9 kJ·mol-14Al (s) +2O3 (g) ==2Al2O3 (s) △H = -3119.91 kJ·mol-1由此得出的结论正确的是A.等质量的O2比O3能量低,由O2变O3为吸热反应B.等质量的O2比O3能量低,由O2变O3为放热反应C.O3比O2稳定,由O2变O3为吸热反应D.O2比O3稳定,由O2变O3为放热反应15.强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(1) ⊿H=-57.3kJ/mol。
向1L0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸②浓硫酸③稀硝酸,恰好完全反应时的热效应⊿H1、⊿H2、⊿H3的关系正确的是A.⊿H1>⊿H2>⊿H3B.⊿H1<⊿H3<⊿H2C.⊿H1<⊿H2<⊿H3D.⊿H1>⊿H3>⊿H216.已知:CH4(g)+2O2(g)→CO2(g)+2H2O(g) ΔH=- Q1 ;2H2(g)+O2(g) ==2H2O(g) ΔH=- Q2;H2O(g)==H2O(l) ΔH=- Q3常温下,取体积比为4:1的甲烷和H2的混合气体112L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为A. 4Q1+0.5Q2B. 4Q1+Q2+10Q3C. 4Q1+2Q2D. 4Q1+0.5Q2+9Q317.已知:CH3CH2CH2CH3(g)+6.5O2(g)==4CO2(g)+5H2O(l) ΔH=-2 878 kJ·mol-1(CH3)2CHCH3(g)+6.5O2(g) ==4CO2(g)+5H2O(l) ΔH=-2 869kJ·mol-1下列说法正确的是A. 正丁烷分子储存的能量大于异丁烷分子B. 正丁烷的稳定性大于异丁烷C. 异丁烷转化为正丁烷的过程是一个放热过程D. 异丁烷分子中的碳氢键比正丁烷的多18.已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO4•5H2O(s) === CuSO4(s)+5H2O(l) △H=+Q2 kJ·mol 1则Q1、Q2的关系为A. Q1<Q2B. Q1>Q2C. Q1=Q2D. 无法确定二、填空题19.在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。
已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出该反应的热化学方程式__________________________________________。
(2)已知H2O(l)====H2O(g);△H=+44kJ·mol-1,则16 g液态肼燃烧生成氮气和液态水时,放出的热量是________kJ。
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是________________________。
(4)已知N2(g)+2O2(g)====2 NO2(g);△H=+67.7 kJ·mol-1,N2H4(g)+O2(g)=== N2(g)+2H2O (g);△H=-534 kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式________________________________________。
(5)已知:N2 (g) +2O2 (g) =2NO2 (g)△H = + 67.7kJ/molN2H4 (g) +O2 (g) =N2(g) +2H2O (g) △H = -543kJ/mol1/2H2 (g) +1/2F2 (g) =HF (g) △H = -269kJ/molH2 (g) +1/2O2 (g) =H2O (g) △H = -242kJ/mol有人认为若用氟代替二氧化氮作氧化剂,则反应释放能量更大,肼和氟反应的热化学方程式:。
20.用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。
通过测定反应过程中所放出的热量可计算中和热。
回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃用品是。
(2)烧杯间填满碎纸条的作用是。
(3)大烧杯上如不盖硬纸板,求得的中和热数值(填“偏大、偏小、无影响”)(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等、不相等”),所求中和热(填“相等、不相等”)(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会;(填“偏大”、“偏小”、“无影响”)。