化学键和晶体类型
- 格式:pdf
- 大小:330.35 KB
- 文档页数:12

晶体第五课化学键及晶格类型
晶体第五课:化学键及晶格类型
化学键及晶格类型
晶体中的原子之间的相互作用主要有以下几种情况:
.化学键:包括离子键、共价键和金属键。
.非化学性作用:范德华力(分子键)
一般来说,一种晶体通常以一种化学键为主,其物理性质也是由这种占主导地位的化学键决定,因此,我们根据晶体内占主导地位的化学键类型来划分晶体的晶格类型,对应于离子键、共价键、金属键、分子键,就有离子晶格、原子晶格、金属晶格、分子晶格。
但是,晶体中的原子往往不是由单纯一种键型相互作用而构成,大多数情况下,在形成的晶体中各种键型都有存在,只是程度不同而已。
极化、电子离域、轨道重叠等因素相互作用,产生不同程度的键型变异。
这就是由著名化学家唐有祺教授1963年提出的键型变异原理。
键型递变是化学中常见的现象,可以用键型四面体直观表示。
由于分子间的作用力很弱,分子键所形成的分子晶格类型的晶体大多透明、不导电、硬度很小、有较低的熔、沸点,、易挥发,许多物质在常温下呈气态或液态。
有些分子晶体,如H2O、NH3、CH3CH2OH等除了范德华力外还有氢键的作用,它们的熔沸点较高。


化学键和晶体知识点整理化学键是指由原子之间相互作用形成的连接。
常见的化学键包括共价键、离子键和金属键等。
晶体是指由具有规则排列的原子、离子或分子构成的固体。
共价键是由原子间的电子共享形成的化学键。
共价键的形成需要原子间的电子云重叠,使得两个原子间的电子得以共享。
共价键可以根据电子云的重叠程度分为σ键和π键。
共价键的强度与共享电子的数量有关,共享电子的数量越多,共价键的强度越大。
离子键是由带正电荷的阳离子和带负电荷的阴离子之间的吸引力形成的化学键。
离子键的形成是由于电荷相互作用所引起的。
离子键的强度较大,常见于具有明显电荷差异的元素或化合物,如NaCl。
金属键是金属元素或合金中的金属离子之间的相互作用形成的化学键。
金属键的形成是由于金属离子的正电荷与自由电子的负电荷之间的相互作用所引起的。
金属键通常具有高的导电性和热导性。
晶体是由原子、离子或分子等按照规则的排列方式组成的固体。
晶体具有明确的外观形状,均匀的内部结构以及特定的物理性质。
晶体的结构可以通过X射线衍射等方法进行研究。
晶体的结构可以分为离子晶体、共价晶体和金属晶体等。
离子晶体的结构由带正电荷和带负电荷的离子相互排列构成。
共价晶体的结构由共价键相互连接的原子或分子构成。
金属晶体的结构由金属离子排列构成,金属离子之间通过金属键相互连接。
晶体的性质受到晶格结构和晶体内部相互作用的影响。
晶格结构决定了晶体的外观形状以及晶体的物理性质,如硬度、熔点等。
晶体内部相互作用决定了晶体的化学性质,如溶解度、反应活性等。
晶格结构可以通过晶体学研究方法进行研究和描述。
晶体学研究包括晶体的晶胞、点阵和晶体对称性等方面。
晶胞是晶体的最小单位,包括一组原子、离子或分子。
点阵是一组规则排列的点,用来描述晶体的周期性结构。
晶体的对称性是指晶体具有不同方向和位置上的相似性。
晶体的应用广泛,包括材料科学、电子学、光学以及生物学等领域。
晶体材料具有优异的光学、电学和力学性质,被广泛应用于激光器、光纤通信、电子器件等领域。

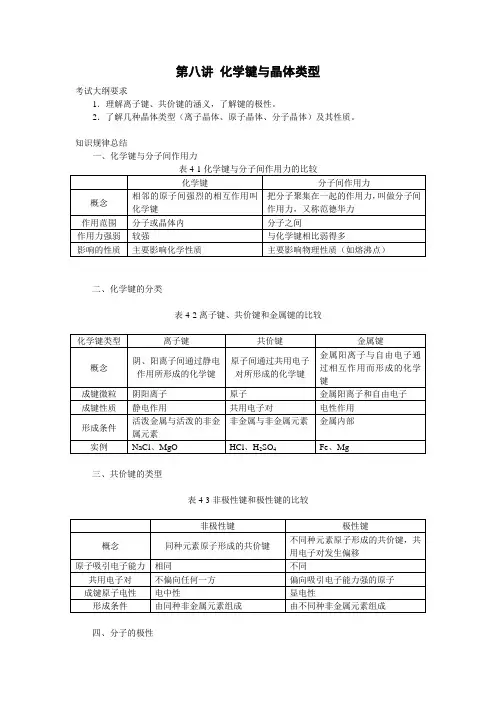
第八讲化学键与晶体类型考试大纲要求1.理解离子键、共价键的涵义,了解键的极性。
2.了解几种晶体类型(离子晶体、原子晶体、分子晶体)及其性质。
知识规律总结一、化学键与分子间作用力二、化学键的分类表4-2离子键、共价键和金属键的比较三、共价键的类型表4-3非极性键和极性键的比较四、分子的极性1.非极性分子和极性分子表4-4 非极性分子和极性分子的比较2.常见分子的类型与形状表4-5常见分子的类型与形状比较3.分子极性的判断(1)只含有非极性键的单质分子是非极性分子。
(2)含有极性键的双原子化合物分子都是极性分子。
(3)含有极性键的多原子分子,空间结构对称的是非极性分子;空间结构不对称的为极性分子。
注意:判断AB n型分子可参考使用以下经验规律:①若中心原子A的化合价的绝对值等于该元素所在的主族序数,则为非极性分子,若不等则为极性分子;②若中心原子有孤对电子(未参与成键的电子对)则为极性分子,若无孤对电子则为非极性分子。
五、晶体类型1.分类表4-6各种晶体类型的比较2极性溶剂,熔化时能够导电,溶沸点高多数溶剂,导电性差,熔沸点很高液能够导电,溶沸点低电和热的良导体,熔沸点高或低实例食盐晶体金刚石氨、氯化氢镁、铝2.物质溶沸点的比较(1)不同类晶体:一般情况下,原子晶体>离子晶体>分子晶体(2)同种类型晶体:构成晶体质点间的作用大,则熔沸点高,反之则小。
①离子晶体:离子所带的电荷数越高,离子半径越小,则其熔沸点就越高。
②分子晶体:对于同类分子晶体,式量越大,则熔沸点越高。
③原子晶体:键长越小、键能越大,则熔沸点越高。
(3)常温常压下状态①熔点:固态物质>液态物质②沸点:液态物质>气态物质3.“相似相溶”规律极性分子组成的溶质易溶于由极性分子组成的溶剂;非极性分子组成的溶质易溶于由非极性分子组成的溶剂。
思维技巧点拨一、化学键及分子极性的判断【例1】下列叙述正确的是A.P4和NO2都是共价化合物l4和NH3都是以极性键结合的极性分子C.在CaO和SiO2晶体中,都不存在单个小分子D.甲烷的结构式:是对称的平面结构,所以是非极性分子【解析】P4和NO2分子中都含有共价键,但P4是单质,故选项A错误。

第六讲 化学键与晶体结构(必考点)一、 化学键1、定义:相邻的两个或多个原子之间强烈的相互作用,通常叫做化学键。
例如:水的结构式为H-O-H ,H -O 之间存在着强烈的相互作用,而H 、H 之间相互作用非常弱,没有形成化学键。
2、化学键类型 : ⎪⎩⎪⎨⎧金属键共价键(含配位键)离子键3、三种化学键的比较:离 子 键 共 价 键 金 属 键形成过程 阴阳离子间的静电作用 原子间通过共用电子对所形成的相互作用金属阳离子与自由电子间的相互作用构成元素 典型金属(含NH 4+)和典型非金属、含氧酸根非 金 属 金 属实 例 离子化合物,如典型金属氧化物、强碱、大多数盐 多原子非金属单质、气态氢化物、非金属氧化物、酸等金 属※ 配位键:配位键属于共价键,它是由一方提供孤对电子,另一方提供空轨道所形成的共价键,例如:NH 4+的形成在NH 4+中,虽然有一个N -H 键形成过程与其它3个N -H 键形成过程不同(一对电子由N 原子单独提供,H +提供空轨道),但是一旦形成之后,4个共价键就完全相同。
4、共价键的三个键参数概 念 意 义键长 分子中两个成键原子核间距离(米) 键长越短,化学键越强,形成的分子越稳定键能 对于气态双原子分子AB ,拆开1molA-B 键所需的能量 键能越大,化学键越强,越牢固,形成的分子越稳定键角 键与键之间的夹角 键角决定分子空间构型①、键长、键能决定共价键的强弱和分子的稳定性:原子半径越小,键长越短,键能越大,分子越稳定。
比较共价键的强弱实际上就是比较成键原子半径大小,这就依靠对元素周期律的掌握。
例如HF 、HCl 、HBr 、HI 分子中:X 原子半径:F<Cl<Br<IH-X 键键长:H-F<H-Cl<H-Br<H-IH-X 键键能:HF>HCl>HBr>HIH-X 分子稳定性:HF>HCl>HBr>HI②、键角决定分子空间构型,分子空间构型又决定分子的极性以及它们参加反应后产物的空间构型与极性,应特别记忆以下分子的键角和空间构型:分子空间构型 键 角 实 例5、共价键的极性不同原子间形成的共价键一定是极性共价键,同种原子间形成的共价键一定是非极性共价键。

化学键知识知识点一化学键的定义一、化学键:使离子相结合或使原子相结合的作用力叫做化学键。
相邻的(两个或多个)离子或原子间的强烈的相互作用。
【对定义的强调】(1)首先必须相邻。
不相邻一般就不强烈 (2)只相邻但不强烈,也不叫化学键 (3)“相互作用”不能说成“相互吸引”(实际既包括吸引又包括排斥) 一定要注意“相邻..”和“强烈..”。
如水分子里氢原子和氧原子之间存在化学键,而两个氢原子之间及水分子与水分子之间是不存在化学键的。
二、形成原因:原子有达到稳定结构的趋势,是原子体系能量降低。
三、类型:离子键化学键 共价键 极性键 非极性键知识点二离子键和共价键一、离子键和共价键比较二、非极性键和极性键知识点三离子化合物和共价化合物通常以晶体形态存在(1)当一个化合物中只存在离子键时,该化合物是离子化合物(2)当一个化合中同时存在离子键和共价键时,以离子键为主,该化合物也称为离子化合物(3)只有..当化合物中只存在共价键时,该化合物才称为共价化合物。
(4)在离子化合物中一般既含有金属元素又含有非金属元素;共价化合物一般只含有非金属元素(NH4+例外)注意:(1)离子化合物中不一定含金属元素,如NH4NO3,是离子化合物,但全部由非金属元素组成。
(2)含金属元素的化合物不一定是离子化合物,如A1C13、BeCl2等是共价化合物。
、知识点四电子式和结构式的书写方法一、电子式:1.各种粒子的电子式的书写:(1)原子的电子式:常把其最外层电子数用小黑点“·”或小叉“×”来表示。
例如:(2)简单离子的电子式:①简单阳离子:简单阳离子是由金属原子失电子形成的,原子的最外层已无电子,故用阳离子符号表示,如Na+、Li+、Ca2+、Al3+等。
②简单阴离子:书写简单阴离子的电子式时不但要画出最外层电子数,而且还应用括号“[]”括起来,并在右上角标出“n—”电荷字样。
例如:氧离子、氟离子。
③原子团的电子式:书写原子团的电子式时,不仅要画出各原子最外层电子数,而且还应用括号“[]”括起来,并在右上角标出“n—”或“n+”电荷字样。

化学键分子结构与晶体结构化学键是指化学元素之间的相互作用力,包括共价键、离子键和金属键。
化学键的不同类型决定了分子或晶体的性质和结构。
共价键是两个原子之间的电子共享。
当两个原子都需要电子来达到稳定的电子壳结构时,它们可以共享一对电子形成一个共价键。
共价键的形成使得原子在空间上非常接近,形成分子。
分子中的化学键可以是单一、双重或三重共价键,取决于共享的电子对数目。
离子键是由于正离子和负离子之间的静电力而形成的。
在离子化合物中,金属元素向非金属元素转移电子,从而形成正离子和负离子。
正离子和负离子之间的相互吸引力引发了离子键的形成。
离子晶体的结构通常由正负离子的周期排列所组成。
金属键是金属元素之间电子共享的结果。
金属元素通常有多个价电子,这些价电子可以自由地在金属中移动。
金属键的形成使得金属元素形成具有特定结晶结构的金属。
金属的物质性质通常是导电、导热和可塑性。
分子结构是由共价键连接的原子所组成的。
分子结构的确定需要知道各个原子之间的连接方式和空间排列。
分子结构的性质直接影响着分子的性质,如化学反应的活性、分子的极性和分子间作用力。
晶体结构是由许多原子、离子或分子按照一定的排列顺序在晶格中组成的。
晶体结构具有高度有序性,可以通过晶体学方法来研究和描述。
晶体结构的种类多种多样,包括离子晶体、共价晶体和分子晶体等。
晶体的结构决定了其物理、化学和光学性质,如晶体的硬度、折射率和热膨胀系数等。
总之,化学键是不同原子之间的相互作用力,可以分为共价键、离子键和金属键。
分子结构是由共价键连接的原子所组成的。
晶体结构是离子、原子或分子按照一定顺序在晶格中排列的结构。
化学键、分子结构和晶体结构共同决定了分子和晶体的性质和行为。

晶体结合类型
晶体结合类型
晶体是由原子、分子或离子按照一定的空间排列方式组成的固体物质。
晶体结合类型是指晶体中原子、分子或离子之间的相互作用方式。
根
据这种相互作用方式,可以将晶体结合类型分为离子型、共价型、金
属型和分子型四类。
一、离子型
离子型晶体是由阳离子和阴离子通过电荷吸引力相互作用而形成的。
阳离子和阴离子之间的相互作用力量很强,因此这种晶体一般具有高
熔点和难溶于水等特点。
常见的离子型晶体有氯化钠、硫酸钠等。
二、共价型
共价型晶体是由原子通过共用电子对形成化学键而形成的。
这种化学
键与电荷吸引力不同,其强度较弱,因此这种晶体一般具有较低的熔
点和易溶于水等特点。
常见的共价型晶体有硅化物、碳化物等。
三、金属型
金属型晶体是由金属原子通过金属键相互作用而形成的。
金属键是一种特殊的共价键,其强度较大,因此这种晶体一般具有高熔点和良好的导电性等特点。
常见的金属型晶体有铜、铁等。
四、分子型
分子型晶体是由分子通过范德华力相互作用而形成的。
范德华力是一种弱的相互作用力,因此这种晶体一般具有较低的熔点和易溶于水等特点。
常见的分子型晶体有冰、葡萄糖等。
结语
总之,不同类型的晶体结合方式决定了它们在物理和化学性质上的差异。
对于材料科学和化学领域来说,深入了解不同类型晶体结合方式对于探索新材料和改进已有材料具有重要意义。
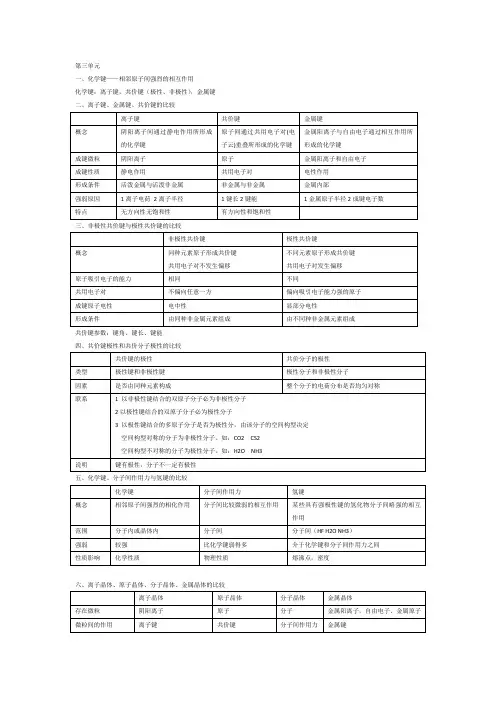
第三单元
一、化学键——相邻原子间强烈的相互作用
化学键:离子键,共价键(极性、非极性),金属键二、离子键、金属键、共价键的比较
三、非极性共价键与极性共价键的比较
共价键参数:键角、键长、键能
四、共价键极性和共价分子极性的比较
五、化学键、分子间作用力与氢键的比较
六、离子晶体、原子晶体、分子晶体、金属晶体的比较
七、晶体熔沸点比较
1 不同类晶体:一般情况下,原子晶体〉离子晶体〉分子晶体
2 同类晶体
离子晶体:离子所带电荷数越高,离子半径越小,熔沸点越高分子晶体:式量越大熔沸点越高
原子晶体:键长越小,键能越大,熔沸点越高
3 常温常压状态
熔点:固体〉液体沸点:液体〉气体。

典型晶体结构类型晶体结构是指晶体中原子、离子或分子的排列方式。
根据晶体中化学键和原子排列的性质,可以将晶体结构分为许多不同的类型。
下面将介绍一些典型的晶体结构类型。
1.离子晶体结构:离子晶体是由离子通过静电力相互作用形成的晶体。
其中,阳离子和阴离子通过离子键连接。
离子晶体的典型例子包括氯化钠(NaCl)和氧化铝(Al2O3)。
在这些晶体中,正离子在晶体中形成一个晶格,负离子在晶体中形成另一个晶格。
离子晶体结构稳定,具有高熔点和良好的电导性。
2.共价晶体结构:共价晶体是由共价键连接的原子或分子形成的晶体。
在共价晶体中,原子通过共用电子形成稳定的化学键。
典型的共价晶体结构包括金刚石、石英和硅晶体。
这些晶体具有高硬度、高熔点和良好的热导性。
3.金属晶体结构:金属晶体是由金属元素形成的晶体。
金属晶体的特点是原子间有大量自由电子可以运动,因此具有良好的导电性和导热性。
金属晶体结构可以分为紧密堆积结构和体心立方结构。
紧密堆积结构中,原子排列紧密,如铜和铝。
体心立方结构中,原子在晶格的每个球站的中心和每个面心站位的中心分别占据一个位置,如铁和钨。
4.分子晶体结构:分子晶体是由分子通过范德华力连接形成的晶体。
在分子晶体中,分子通过互相排列并通过弱范德华力相互作用形成3D晶体结构。
分子晶体具有较低的熔点和较弱的化学键。
典型的分子晶体包括蓝绿宝石和冰。
5.共价网络晶体结构:共价网络晶体是由每个原子通过共价键连接形成的大的晶体结构。
共价网络晶体具有非常高的熔点和硬度。
典型的共价网络晶体包括石墨和二硫化碳。
除了这些典型的晶体结构类型,还有许多其他类型的晶体结构,例如层状晶体、孔隙晶体和液晶体等。
每种晶体结构具有独特的性质和应用。
了解不同类型的晶体结构有助于我们理解晶体的性质,并在材料科学和工程中应用晶体材料。
高中化学知识点总结:化学键和晶体结构1.化学键:相邻原子间强烈的相互作用叫作化学键。
包括离子键和共价键(金属键)。
2.离子建(1)定义:使阴阳离子结合成化合物的静电作用叫离子键。
(2)成键元素:活泼金属(或NH4+)与活泼的非金属(或酸根,OH-)(3)静电作用:指静电吸引和静电排斥的平衡。
3.共价键(1)定义:原子间通过共用电子对所形成的相互作用叫作共价键。
(2)成键元素:一般来说同种非金属元素的原子或不同种非金属元素的原子间形成共用电子对达到稳定结构。
(3)共价键分类:①非极性键:由同种元素的原子间的原子间形成的共价键(共用电子对不偏移)。
如在某些非金属单质(H2、Cl2、O2、P4…)共价化合物(H2O2、多碳化合物)、离子化合物(Na2O2、CaC2)中存在。
②极性键:由不同元素的原子间形成的共价键(共用电子对偏向吸引电子能力强的一方)。
如在共价化合物(HCl、H2O、CO2、NH3、H2SO4、SiO2)某些离子化合物(NaOH、Na2SO4、NH4Cl)中存在。
4.非极性分子和极性分子(1)非极性分子中整个分子电荷分布是均匀的、对称的。
极性分子中整个分子的电荷分布不均匀,不对称。
(2)判断依据:键的极性和分子的空间构型两方面因素决定。
双原子分子极性键→极性分子,如:HCl、NO、CO。
非极性键→非极性分子,如:H2、Cl2、N2、O2。
多原子分子,都是非极性键→非极性分子,如P4、S8。
有极性键几何结构对称→非极性分子,如:CO2、CS2、CH4、Cl4。
几何结构不对称→极性分子,如H2O2、NH3、H2O。
5.分之间作用力和氢键(1)分子间作用力把分子聚集在一起的作用力叫作分子间作用力。
又称范德华力。
①分子间作用力比化学键弱得多,它对物质的熔点、沸点等有影响。
②一般的对于组成和结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔点、沸点也越高。
(2)氢键某些物质的分子间H核与非金属强的原子的静电吸引作用。
化学键与晶体类型基础知识归纳一、晶体类型1、离子晶体:阴、阳离子以一定的数目比、并按照一定的方式依靠离子键结合而成的晶体。
如“NaCl、CsCl 构成晶体的微粒:阴、阳离子;微粒间相互作用:离子键;物理性质:熔点较高、沸点高,较硬而脆,固体不导电,熔化或溶于水导电。
2、原子晶体:晶体内相临原子间以共价键相结合形成的空间网状结构。
如:金刚石、晶体硅、碳化硅、二氧化硅构成晶体的微粒:原子;微粒间相互作用:共价键;物理性质:熔沸点高,高硬度,导电性差。
3、分子晶体:通过分子间作用力互相结合形成的晶体。
如:所有的非金属氢化物,大多数的非金属氧化物,绝大多数的共价化合物,少数盐(如AlCl3)。
构成晶体的微粒:分子;微粒间相互作用:范德华力;物理性质:熔沸点低,硬度小,导电性差。
4、金属晶体(包括合金):由失去价电子的金属阳离子和自由电子间强烈的作用形成的。
构成晶体的微粒:金属阳离子和自由电子;微粒间相互作用:金属键;物理性质:熔沸点一般较高部分低,硬度一般较高部分低,导电性良好。
二、化学键1、离子键:使阴、阳离子结合成化合物的静电作用。
离子键存在于离子化合物中,活泼的金属与活泼的非金属形成离子键。
2、金属键:在金属晶体中,金属阳离子与自由电子间的强烈相互作用。
金属键存在于金属和合金中。
3、共价键:分子中或原子晶体、原子团中,相邻的两个或多个原子通过共用电子对所形成的相互作用。
(1)非极性共价键:由同种元素的原子间通过共用电子对形成的共价键,又称为非极性键。
存在于非金属单质中。
某些共价化合物分子中也有非极性键,如:H2O2中的O-O键,C2H6中的C-C键等。
少数离子化合物中也有非极性键,如:Na2O2中的O-O键,CaC2中的碳碳三键等。
(2)极性共价键:不同种元素的原子形成分子时共用电子对偏向吸引电子能力强的原子而形成的共价键,又称为极性键。
所有的共价化合物分子中都存在极性键,离子化合物的原子团中也存在极性键。
化学键与晶体类型教学目标1.理解离子键、共价键的涵义,理解极性键和非极性键。
2.了解极性分子和非极性分子,了解分子间作用力,能用有关原理解释一些实际问题。
3.了解几种晶体类型(离子晶体、原子晶体、分子晶体和金属晶体)及其性质,了解各类晶体内部微粒间的相互作用,能够根据晶体的性质判断晶体类型等。
4.能对原子、分子、化学键等微观结构进行三维空间想像,重视理论联系实际、用物质结构理论解释一些具体问题。
教学内容化学键一、化学键1、概念:相邻的原子之间的强烈的相互作用叫做化学键关键词:相邻、强烈、相互作用(与结合力的区别)2、形成化学键后:(1)原子形成稳定结构(2)原子间存在强烈的相互作用(3)体系能量降低3、化学反应的本质:4、化学键的分类:化学键:二、离子键1. 概念使阴、阳离子结合成化合物的静电作用叫做离子键。
(1)成键粒子:(2)成键条件:活泼的金属元素(IA,IIA)与活泼的非金属元素(VIA,VIIA)①活泼金属元素:Na、K、Ca、Mg……活泼非金属元素:O、S、F、Cl……②活泼的金属元素和酸根阴离子(SO42-,NO3-)及OH-③铵根阳离子和酸根阴离子(或活泼非金属元素)④很活泼的金属与氢气反应生成的氢化物如Na、K、Ca与H。
(3)成键的本质阴阳离子间的静电作用(静电引力和斥力)2、成键的主要原因活泼的原子通过得失电子,形成阴、阳离子,它们之间通过静电引力和斥力达到平衡,从而形成稳定的结构,使体系的能量降低。
IA、IIA和VIA、VIIA 大多数盐离子键的存在所有强碱活泼金属氧化物3. 离子化合物(1)概念:由阴、阳离子相互作用而构成的化合物(含离子键)。
(2)常见的离子化合物强碱、大多数盐、活泼金属氧化物特例:全由非金属元素组成的离子化合物:如NH4NO3(3)含离子键的化合物一定是离子化合物。
4、离子键强弱的判断(了解)离子半径越小,阴阳离子间的作用力越强,离子键越强例:KCl NaCl MgCl2NaCl离子间强弱与性质的关系离子键越强,化合物的熔沸点越高例:KCl NaCl MgO CaO【练练】1、下列说法正确的是:A. 离子键就是使阴、阳离子结合成化合物的静电引力B. 所有金属与所有非金属原子之间都能形成离子键C. 在化合物CaCl2中,两个氯离子之间也存在离子键D. 钠原子与氯原子结合成氯化钠后体系能量降低2、下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合成稳定化合物的是:A. 10与12B.8与17C. 11与17D.6与143. 离子化合物溶于水或熔化时离子键是否发生变化?转化成自由移动的离子,离子键即被破坏。