4化学键和分子结构
- 格式:ppt
- 大小:768.02 KB
- 文档页数:96


![化学原理[4]化学键与分子结构-2](https://uimg.taocdn.com/2b692b22c77da26924c5b049.webp)

化学键与分子结构的关系化学键是在化学反应中形成的一种化学结合。
它对于构建分子结构和决定物质的性质至关重要。
在化学中,共价键、离子键和金属键是最常见的三种化学键。
本文将讨论这些化学键与分子结构之间的关系。
1. 共价键与分子结构共价键是由两个非金属原子之间的电子共享形成的。
电子共享能力的不同可以导致不同类型的共价键,如单、双或三重共价键。
共价键的形成决定了分子的几何结构和空间构型。
例如,水分子(H2O)由两个氢原子和一个氧原子组成。
每个氢原子与氧原子之间通过共用电子配对形成共价键。
由于氧原子比氢原子更电负,它的电子云更集中,在分子中形成了两个类似于“V”形的共价键角度约为104.5度。
这种几何结构使水分子呈现出极性,并导致了一系列特殊的性质,如高沸点、高表面张力和溶解度。
2. 离子键与分子结构离子键是由一个阴离子和一个阳离子之间的电荷吸引力形成的。
在离子键中,电子从金属原子转移到非金属原子,形成正负电荷,从而吸引彼此。
离子键的强度比共价键高得多,因此离子化合物通常具有高熔点和硬度。
例如,氯化钠(NaCl)是一个由钠离子和氯离子组成的晶体。
钠离子失去一个电子成为正离子,氯离子获得一个电子成为负离子,通过电的吸引力形成了离子键。
这种离子结构使得氯化钠在固态下是一个晶体,但在溶液中则以离散的离子存在。
3. 金属键与分子结构金属键是由金属原子间的电子云共享形成的。
金属键在金属中形成一个连续的电子海,并对金属的性质产生重要影响。
金属键具有高导电性(电子在金属中的自由移动),高热导率和可塑性。
例如,铁(Fe)是一个典型的金属元素。
铁原子通过金属键形成一个紧密排列的网络,在其中电子可以自由移动。
这种金属结构使铁具有特殊的性质,如高强度、高熔点和良好的导电性。
总而言之,化学键的类型直接决定了分子结构的几何形状和物质的性质。
共价键决定了分子的形状和极性,离子键导致形成离子晶体,而金属键形成具有特殊物理性质的金属结构。


化学键与分子结构化学键是指原子间的相互作用力,它决定了分子的结构和性质。
在化学中,常见的化学键包括共价键、离子键和金属键。
本文将分别介绍这些化学键以及它们对分子结构的影响。
一、共价键共价键是两个或多个原子通过电子的共用而形成的化学键。
共价键的强度取决于原子之间电子的共享程度和电子云的重叠程度。
共价键的形成使得原子能够达到稳定的电子结构,从而形成分子。
共价键可以进一步分为单键、双键和三键。
1. 单键单键是一对原子间共享一个电子对形成的共价键。
它们通常是通过轨道的重叠来实现电子的共享。
单键的键能较低,结构松散,所以分子在空间上具有较高的自由度。
2. 双键双键是两对原子间共享两个电子对形成的共价键。
它们相较于单键更强,键能更高,分子更加稳定。
双键结构比单键结构更为刚性,分子一般比较扁平。
3. 三键三键是三对原子间共享三个电子对形成的共价键。
它们是最强的共价键,键能最高,分子最为稳定。
由于三键的存在,许多分子呈线性结构。
二、离子键离子键是由带正电的金属离子和带负电的非金属离子之间的静电相互作用形成的化学键。
离子键的强度通常比共价键更大,因此离子化合物具有高熔点和高沸点。
离子键的结构比共价键更加有序和紧密,离子排列规则。
三、金属键金属键是由金属原子通过电子的共享形成的化学键。
在金属中,原子间的外层电子形成共同的电子云,这种共享形成一种特殊的金属键。
金属键的存在使得金属具有良好的导电性和热导性。
化学键的类型决定了分子的结构和性质。
共价键使得分子具有较高的自由度和灵活性,而离子键使得分子有序排列,具有较高的熔点和沸点。
金属键使金属具有特殊的性质,如导电和热导。
总结起来,化学键的类型与分子结构有密切关系,不同类型的化学键决定了分子的稳定性、形状以及物理化学性质。
深入理解化学键与分子结构对于研究化学反应机理和合成新材料具有重要意义。

![化学原理[4]化学键与分子结构4](https://uimg.taocdn.com/725608ea551810a6f524865d.webp)
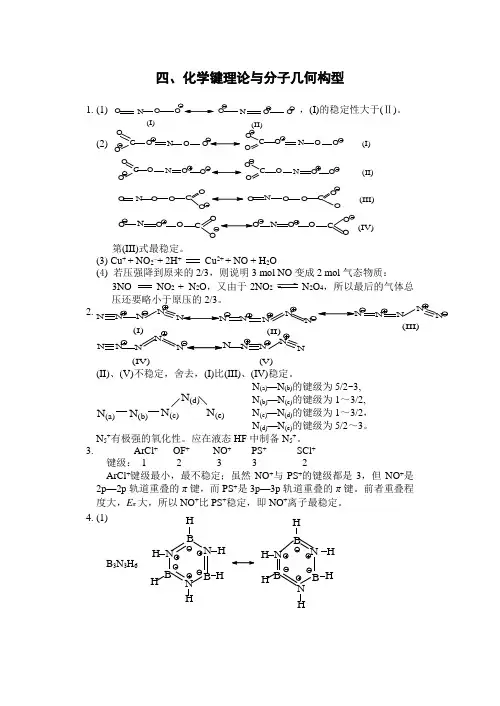
四、化学键理论与分子几何构型1. (1),(I)的稳定性大于(Ⅱ)。
(2)C OOO N O C OO O N O O (I)O C OO N OOCOO ONOO(II)O N O O CO OO NOOC O O (III)ONOOC ON OOCO O(IV)第(III)式最稳定。
(3) Cu + + NO 2–+ 2H + Cu 2+ + NO + H 2O(4) 若压强降到原来的2/3,则说明3 mol NO 变成2 mol 气态物质:3NO NO 2 + N 2O ,又由于2NO 2N 2O 4,所以最后的气体总压还要略小于原压的2/3。
2. N NN N NNNN N(IV)(V)(II)、(V)不稳定,舍去,(I)比(III)、(IV)稳定。
N (a)N (b)N (c)N (d)N (e) N (a)—N (b)的键级为5/2~3,N (b)—N (c)的键级为1~3/2,N (c)—N (d)的键级为1~3/2,N (d)—N (e)的键级为5/2~3。
N 5+有极强的氧化性。
应在液态HF 中制备N 5+。
3. ArCl + OF + NO + PS + SCl + 键级: 1 2 3 3 2ArCl +键级最小,最不稳定;虽然NO +与PS +的键级都是3,但NO +是2p —2p 轨道重叠的π键,而PS +是3p —3p 轨道重叠的π键。
前者重叠程度大,E π大,所以NO +比PS +稳定,即NO +离子最稳定。
4. (1)B 3N 3H 6N H H H H H N B N B B H H H H H H NB B H N BNO N O O O N O O (I)(II)N N N N N N N N N N (I)(II)N N N N N(III)(2) HH H HH H Cl HH H ClCl B 3N 3H 6 3HCl N N N B B B(3) 无机苯的三甲基取代物有:B N B N B N HHHCH 3H 3CCH 3B NB N B N CH 3CH 3H 3CH HHB B N B N CH 3HHHCH 3CH 3(I)(Ⅱ)(III)B N B N B N CH 3HCH 3HCH 3H B N B N B N CH 3H H CH 3HH 3CB NB N B N CH 3H 3CH 3HH(IV) (V) (Ⅵ)实际上只有四种类型,因为II 、IV ;IV 、VI 属于同类型中的几何异构体。


分子结构与化学键分子是由两个或多个原子通过化学键连接在一起形成的,是构成物质的基本单位。
分子结构及其中的化学键种类和性质对物质的性质和反应起着重要作用。
本文将介绍分子结构的基本概念、化学键的种类以及它们的特点和重要性。
一、分子结构的基本概念分子结构是指分子中原子的相对排列方式和连接方式。
分子结构的确定有助于我们理解分子的性质和化学反应的机制。
分子结构的研究可以使用各种实验技术和理论模型,如X射线衍射、核磁共振、质谱等。
二、化学键的种类化学键是连接原子的力,可以根据电子的相互作用类型来分类。
以下是几种常见的化学键:1. 共价键:共价键是通过原子间的电子共享而形成的化学键。
电子在原子核附近的空间中移动,并在原子之间形成稳定结构。
共价键可以是单键、双键或三键,取决于原子之间共享的电子对数目。
2. 金属键:金属键主要存在于金属元素之间。
金属中的原子通过自由移动的电子形成金属键。
金属键具有高导电性和高热导性,是金属的特有性质之一。
3. 离子键:离子键是由正负电荷之间的强电吸引力形成的化学键。
通常情况下,金属和非金属元素之间形成离子键,非金属元素得到电子形成负离子,金属元素失去电子形成正离子,形成电中性的化合物。
4. 氢键:氢键是一种特殊的化学键,主要存在于氢原子与较电负性的原子(如氧、氮、氟)之间。
氢键的强度较弱,但却在生物分子和许多化合物的结构和性质中起到重要作用。
三、化学键的特点和重要性1. 化学键稳定性:化学键的稳定性直接影响物质的性质和化学反应的进行。
共价键通常稳定性较高,而离子键和氢键较脆弱。
金属键的特点是高导电性和高热导性。
2. 化学键的长度和键能:化学键的长度和键能是描述键强度和键的特性的重要参数。
键长和键能与原子种类、电子共享程度、电负性等因素相关。
3. 化学键的影响:化学键的种类和性质直接影响物质的热学性质、电学性质、光学性质等。
例如,共价键的特性决定了分子的稳定性和化学反应的方式;离子键的强度和离子半径决定了固体的结晶结构和性质。
化学键与分子的结构化学键是指原子之间形成的各种相互作用力,它在化学反应中起到了重要的作用。
化学键的类型多种多样,包括离子键、共价键和金属键等。
通过不同类型的化学键,原子能够结合形成分子,从而构建出各种物质的结构。
一、离子键离子键是由正负电荷之间的相互作用力所形成的化学键。
它通常发生在金属和非金属之间或者非金属之间。
离子键的形成过程涉及到原子的电离和电子的转移。
在一个化学反应中,一个原子失去一个或多个电子,成为正离子;另一个原子获得这些电子,成为负离子。
正离子和负离子之间的静电吸引力就形成了离子键。
离子键通常具有较高的熔点和沸点,因为它们之间的相互作用力较强。
二、共价键共价键是由共享电子对形成的化学键。
它通常发生在非金属原子之间。
共价键的形成过程涉及到原子之间电子的互相吸引力。
原子通过共享电子对来实现稳定的电子配置。
共价键的强度通常取决于原子间的电负性差异。
电负性较大的原子对电子的吸引力较强,形成的共价键也较强。
共价键可以分为单键、双键和三键等,取决于原子间共享的电子对数目。
三、金属键金属键是在金属原子之间形成的化学键。
金属键的特点是原子之间的电子云相互重叠,形成一个大的电子云。
金属原子之间的吸引力主要来自于这个共享的电子云中的自由电子。
这种形成方式使得金属键具有很好的导电性和热导性。
金属键通常是非局域化的,也就是不局限于特定的两个原子之间,而是在整个金属中形成。
不同类型的化学键在分子的结构中起到了不同的作用。
离子键常见于离子晶体的结构中,如氯化钠。
共价键通常构成了有机物和分子化合物的基本结构,如甲烷分子。
金属键则是金属晶体的基础,如铜。
通过这些化学键的组合和排列,我们可以构建出多样化的分子结构,从而实现了丰富多样的化学反应和性质。
总结起来,化学键是分子结构的重要组成部分。
离子键、共价键和金属键等不同类型的化学键在分子中起到了不同的作用。
通过理解和研究化学键与分子结构之间的关系,我们可以深入探索物质的性质和化学反应的机理,从而推动化学科学的发展。
化学键与分子结构的空间构型与实例解析化学键是构成分子的基本元素之一,它决定了分子的结构和性质。
化学键的类型和结构对于分子的空间构型具有重要影响。
本文将围绕化学键的概念展开讨论,并通过实例解析不同类型化学键与分子结构之间的关系。
一、共价键的空间构型与实例解析共价键是指通过原子间共享电子而形成的化学键。
共价键的长度、角度和构型对于分子的空间形态具有重要影响。
下面以水分子(H₂O)为例进行分析。
水分子由两个氢原子和一个氧原子组成,氧原子与两个氢原子之间形成的两条共价键呈V字形。
这种空间构型使得水分子在三维空间呈现出角度为104.5°的“V”字形状。
共价键的构型对水分子的性质产生了重要影响,使得水具有极性,能够形成氢键和其他分子相互作用。
二、离子键的空间构型与实例解析离子键是通过正负离子间的相互吸引力而形成的化学键。
离子键的空间构型与各离子之间的排列方式密切相关。
以氯化钠(NaCl)为例进行讨论。
氯化钠是由氯离子和钠离子通过离子键结合而形成的晶体。
在晶体中,钠离子和氯离子按照等间距排列,并形成六方最密堆积结构。
离子键的空间构型使得氯化钠晶体具有高熔点、良好的溶解性和电导性等特点。
三、金属键的空间构型与实例解析金属键是指金属原子通过电子云的共享而形成的化学键。
金属键的特点是具有自由移动的电子云,对分子的空间构型具有一定影响。
以金属铝(Al)为例进行分析。
金属铝由一个原子间的金属键构成。
在金属键中,金属原子的外层电子形成共享电子云,使得金属具有良好的导电性和延展性。
金属键的空间构型对金属的热膨胀性也有影响。
综上所述,化学键的类型和结构对于分子的空间构型产生重要影响。
不同类型的化学键以及它们的空间构型所带来的特性和性质,使得分子和物质表现出多样化的现象。
因此,对于化学键与分子结构的空间构型与实例的分析和理解,有助于我们更好地理解和研究分子的结构和性质。
(以上内容为参考,请根据实际情况和需要进行修改。
第四章化学键与分子构造增补习题【选择题】1.以下卤化物中,离子键成分大小次序正确的选项是()。
A.CsF>RbCl>KBr>NaI B.CsF>RbBr>KCl>NaFC.RbBr>CsI>NaF>KCl D.KCl>NaF>CsI>RbBr2.以下物质中沸点高低次序正确的选项是()。
A.H2Te>H2Se>H2S>H2O B.H2Se>H2S>H2O>H2Te;C.H2O>H2S>H2Se>H2Te D.H2O>H2Te>H2Se>H2S3.既能权衡元素金属性强弱,又能权衡其非金属性强弱的物理量是()。
A.电负性B.电离能C.电子亲和能D.偶极矩4.Pb2+、Bi3+离子均属何种电子构型()。
A.18B.18+2C.8D.9~175.以下离子型化合物熔点最低的是()。
A.NaF B.BaO C.SrO D.MgO 6.以下各化学键中极性最大的是()。
A.B-Cl B.Ba-Cl C.Be-Cl D.Br-Cl7.以下分子中属于非极性分子的是()。
A.CHCl3B.PCI3C.CO2D.HCl8.以下分子中,空间构型不是直线的是()。
A.CO B.H2O C.CO D.HgCI229.以下说法中错误的选项是()。
A.杂化轨道有益于形成σ键B.杂化轨道均参加成键C.采纳杂化轨道成键,更能知足轨道最大重迭原理D.采纳杂化轨道成键,能提升原子成键能力10.BF4-离子中,B原子采纳的杂化轨道是()。
A.spB.sp2C.sp3D.不等性sp3 11.以下分子中,构型是平面三角形的分子是(A.CO2 B.PCl3)。
C.BCl3D.NH312.以下分子中键角最大的是()。
A.PCl3 B.NH3C.SiCl4D.CO2 13.以下对于杂化轨道理论的说法中正确的选项是()。
化学键与分子结构化学键是指原子之间通过电荷的吸引力而形成的结合力。
它决定了分子的性质和化学反应的进行方式。
在化学中,分子结构又是指分子中原子之间的相对位置和关联方式。
化学键和分子结构是化学研究中的重要概念,对于理解物质的性质和相互作用具有关键性的作用。
一、离子键离子键是一种通过离子之间的电荷相互吸引形成的化学键。
通常涉及到金属和非金属原子的相互作用。
金属原子往往失去电子而形成正离子,非金属原子则接受这些电子而形成负离子。
正负离子之间的相互吸引力就构成了离子键。
离子键的典型例子是氯化钠(NaCl),其中钠离子(Na+)和氯离子(Cl-)通过离子键相互连接。
二、共价键共价键是一种通过两个或多个原子共享电子而形成的化学键。
共价键通常涉及到非金属原子之间的相互作用。
在共价键中,原子通过共享电子以使得每个原子达到稳定的电子结构。
共价键的强度取决于所共享电子对的数量和共享电子对的距离。
当两个原子间的电子对数量越多、距离越近时,共价键越稳定。
典型的共价键化合物包括水分子(H2O)和甲烷分子(CH4)。
三、极性键与非极性键化学键可以根据电子的相对吸引程度分为极性键和非极性键。
极性键是指在化学键中,电子的共享不平均,其中一个原子对电子的吸引力更强,而另一个原子对电子的吸引力较弱。
结果,形成了带有正电荷的极性原子和带有负电荷的极性原子。
非极性键则是指在化学键中,电子的共享非常均匀,两个原子对电子的吸引力相等。
极性键的典型例子是水分子中的氧-氢键,而非极性键的典型例子是氧气分子(O2)中的氧氧键。
四、分子结构分子结构是指分子中原子之间的相对位置和关联方式。
它涉及到原子间的键长、键角和立体构型。
分子结构不仅关系到分子的化学性质,也对分子的物理性质产生影响。
分子结构的确定通常通过实验方法,如X射线晶体学、核磁共振(NMR)等技术。
分子结构的研究对于理解化学反应机理、药物设计和材料科学具有重要意义。
总结:化学键和分子结构是化学研究中不可或缺的重要概念。
分子与分子键:分子结构和化学键的类型分子是由两个或多个原子通过化学键连接而成的,它们以一定的方式排列在一起,形成了不同种类的分子结构。
分子结构的形成与分子间的化学键类型有着密切的关系。
本文将从分子结构和化学键的类型两个方面来介绍分子与分子键的关系。
一、分子结构分子结构描述了分子中各个原子的排列方式和相互之间的关系。
根据分子中原子之间的连接方式,可以将分子结构分为线性结构、分支结构和环状结构。
1. 线性结构线性结构的分子由一条直线上的原子构成,原子间通过共价或离子键相连接。
例如,氢气(H2)的分子结构就是线性的,两个氢原子通过共价键连接在一起。
2. 分支结构分支结构的分子由一个或多个支链与主链相连而成。
支链与主链的连接点被称为侧基。
例如,异丙醇(C3H8O)的分子就是分支结构,它由三个碳原子和一个氧原子构成,其中一个碳原子上连接着一个甲基。
3. 环状结构环状结构的分子由一个或多个原子形成一个环状结构。
例如,蔗糖(C12H22O11)的分子就是环状结构,它由12个碳原子、22个氢原子和11个氧原子构成一个环。
二、化学键的类型化学键是用来连接原子的强力化学键。
根据原子间的电荷差异、共享电子对数目和电子云重叠程度,可以将化学键分为共价键、离子键和金属键。
1. 共价键共价键是由两个原子之间共享电子对而形成的。
它主要存在于非金属元素之间,在分子中连接了原子之间的化学键。
共价键可以进一步分为单键、双键和三键,取决于原子间共享的电子对数目。
例如,氨气(NH3)中氮原子与三个氢原子之间通过共价单键连接。
2. 离子键离子键是由正负电荷相互吸引而形成的键。
它主要存在于金属元素和非金属元素之间,形成了离子晶体的结构。
离子键是通过转移电子形成的,阳离子和阴离子之间通过吸引力相互连接。
例如,氯化钠(NaCl)的晶体结构由钠阳离子和氯阴离子通过离子键连接。
3. 金属键金属键是存在于金属元素之间的键。
它的形成是由于金属元素中的自由电子形成了电子海,多个金属原子通过共享这些自由电子而连接在一起。