溶解过程中的能量变化知识讲解
- 格式:ppt
- 大小:8.71 MB
- 文档页数:26
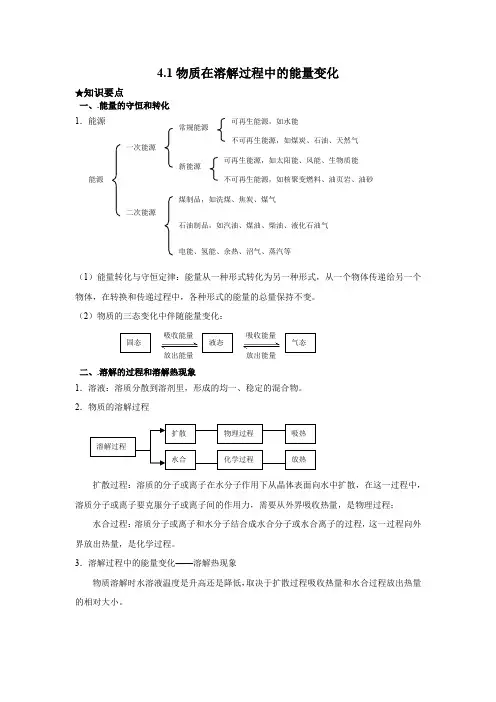
4.1物质在溶解过程中的能量变化★知识要点一、.能量的守恒和转化 1.能源(1)能量转化与守恒定律:能量从一种形式转化为另一种形式,从一个物体传递给另一个物体,在转换和传递过程中,各种形式的能量的总量保持不变。
(2)物质的三态变化中伴随能量变化:二、.溶解的过程和溶解热现象1.溶液:溶质分散到溶剂里,形成的均一、稳定的混合物。
2.物质的溶解过程扩散过程:溶质的分子或离子在水分子作用下从晶体表面向水中扩散,在这一过程中,溶质分子或离子要克服分子或离子间的作用力,需要从外界吸收热量,是物理过程; 水合过程:溶质分子或离子和水分子结合成水合分子或水合离子的过程,这一过程向外界放出热量,是化学过程。
3.溶解过程中的能量变化——溶解热现象物质溶解时水溶液温度是升高还是降低,取决于扩散过程吸收热量和水合过程放出热量的相对大小。
扩散 溶解过程 水合 物理过程 化学过程 吸热放热 能源 一次能源 二次能源 新能源 常规能源 可再生能源,如水能 不可再生能源,如煤炭、石油、天然气 可再生能源,如太阳能、风能、生物质能 不可再生能源,如核聚变燃料、油页岩、油砂 煤制品,如洗煤、焦炭、煤气石油制品,如汽油、煤油、柴油、液化石油气 电能、氢能、余热、沼气、蒸汽等 吸收能量 固态 液态 气态吸收能量 放出能量 放出能量三、溶解和结晶1.溶解:溶质分散到溶剂中的过程。
2.结晶:晶态溶质从溶液中析出的过程。
3.溶解和结晶的宏观现象和微观过程溶解和结晶作为宏观现象是不能同时观察到的。
但是,就微观粒子的运动状态而言,溶解和结晶这两个过程则是同时进行的相反(互逆)的过程,即在溶液里溶质进行溶解的同时,也进行着结晶,在一定条件下建立起一个动态平衡体系——溶解平衡。
4.溶解平衡在一定条件下的饱和溶液中,当物质溶解速率和物质晶体析出速率相等,这个溶液体系就达到了溶解平衡状态。
若改变外界的条件(包括改变溶剂量或温度),则可不同程度地改变微观粒子的溶解速率和结晶速率,原来的溶解平衡被破坏,并在新条件下建立新的平衡。


溶解过程中能量的变化是什么?
概述
溶解是物质从固态或气态转变为液态的过程。
在溶解过程中,
存在能量的转化和变化。
本文将探讨溶解过程中能量的变化以及相
关的能量转化原理。
能量转化原理
在溶解中,主要存在以下几种能量转化:
1. 吸热过程:当溶质与溶剂之间的相互作用力破坏时,需要提
供能量,这导致了能量的吸收。
因此,溶解过程中可以发生吸热反应。
2. 放热过程:当溶质与溶剂之间的相互作用力形成时,释放出
能量,这导致了能量的放出。
因此,溶解过程中可以发生放热反应。
能量变化
溶解过程中的能量变化可以包括以下几个方面:
1. 温度变化:当溶质与溶剂发生吸热反应时,会导致溶液的温
度升高;而当溶质与溶剂发生放热反应时,会导致溶液的温度降低。
2. 热量变化:吸热反应和放热反应分别导致溶解过程中的热量
增加和减少。
吸热反应吸收了外界的热量,使溶解过程变冷;而放
热反应释放出热量,使溶解过程变热。
3. 势能变化:溶质与溶剂之间的相互作用力形成或破坏时,会
引起势能的变化。
溶解过程中会伴随着溶质与溶剂之间的相互作用
能的变化。
结论
根据上述的能量转化原理和能量变化,我们可以总结出在溶解
过程中能量的变化是多方面的,包括吸热过程、放热过程以及温度、热量和势能的变化。
深入理解溶解过程中的能量变化有助于我们更
好地理解溶解现象及其相关的物理化学原理。

沪科版高一化学必修一剖析物质变化中的能量变化知识点高一新学期大家要学习很多化学知识点,相对于其它学科来说化学知识点比较琐碎,因此在课下多进行复习巩固,下面为大家带来沪科版高一化学必修一剖析物质变化中的能量变化知识点,希望对大家学好高一化学知识有帮助。
一、物质在溶解中的能量变化1、两大守恒定律:在不与环境发生物质和能量交换的体系中,不论发生何种变化,体系中的质量和能量都不会改变,分别称为质量守恒定律和能量守恒定律。
2、溶解中的能量变化:溶解时,同时发生两个过程。
一是溶质的微粒离开固体(液态)表面扩散到溶剂中去,这一过程吸收热量,是物理过程;另一个过程是溶质的微粒和溶剂分子生成溶剂化合物和或水合离子,这一过程放出热量,是化学过程。
这两个过程中总是伴随着能量的变化,表现形式是放热或者吸热现象。
3、溶解平衡:结晶和溶解是同时进行的相反的两个过程,当单位时间内扩散到溶液里的溶质微粒数目,与回到固体溶质表面的溶质微粒数目相等,也就是溶质溶解的速率等于结晶的速率时,我们称之为达到了溶解平衡。
这时的溶液是饱和溶液。
二、放热反应和吸热反应化学上把有热量放出的化学反应称为放热反应,把吸收热量的化学反应称为吸热反应。
与反应条件没有必然联系,而决定于反应物和生成物具有的总能量的相对大小。
类型比较放热反应吸热反应。
定义有热量放出的化学反应吸收热量的化学反应。
形成原因反应物具有的总能量大于生成物具有的总能量反应物具有的总能量小于生成物具有的总能量。
与化学键强弱的关系生成物分子成键时释放出的总能量大于反应物分子断裂时吸收的总能量生成物分子成键时释放出的总能量小于反应物分子断裂时吸收的总能量。
表示方法:H﹤0或+QH﹥0或-Q三、燃烧热和中和热1、燃烧热:25℃、在101kPa时,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,单位为kJ/mol。
燃烧热是以1mol物质完全燃烧所放出来的热量来定义的,且燃烧产物必须是稳定的氧化物。




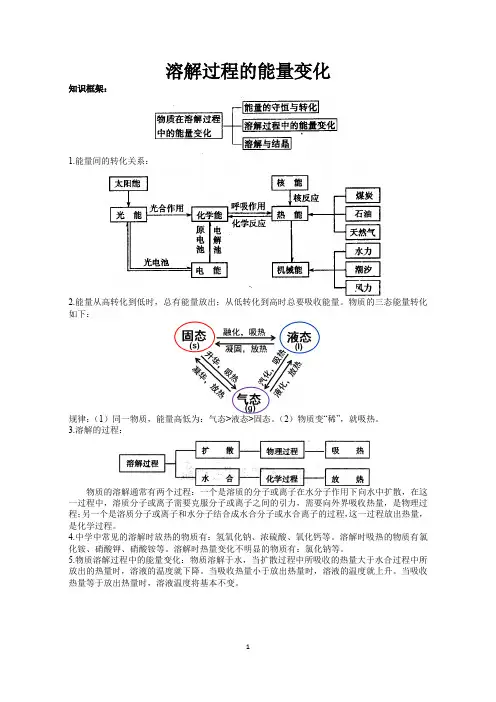
溶解过程的能量变化知识框架:1.能量间的转化关系:2.能量从高转化到低时,总有能量放出;从低转化到高时总要吸收能量。
物质的三态能量转化如下:规律:(1)同一物质,能量高低为:气态>液态>固态。
(2)物质变“稀”,就吸热。
3.溶解的过程:物质的溶解通常有两个过程:一个是溶质的分子或离子在水分子作用下向水中扩散,在这一过程中,溶质分子或离子需要克服分子或离子之间的引力,需要向外界吸收热量,是物理过程;另一个是溶质分子或离子和水分子结合成水合分子或水合离子的过程,这一过程放出热量,是化学过程。
4.中学中常见的溶解时放热的物质有:氢氧化钠、浓硫酸、氧化钙等。
溶解时吸热的物质有氯化铵、硝酸钾、硝酸铵等。
溶解时热量变化不明显的物质有:氯化钠等。
5.物质溶解过程中的能量变化:物质溶解于水,当扩散过程中所吸收的热量大于水合过程中所放出的热量时,溶液的温度就下降。
当吸收热量小于放出热量时,溶液的温度就上升。
当吸收热量等于放出热量时,溶液温度将基本不变。
6.溶解:当把固体溶质加入水后,溶质表面的分子或离子由于本身的振动以及受到水分子的撞击和吸引会逐渐脱离固体表面进入水中,扩散到各个部分成为溶液,这个过程称为溶解。
7.结晶:已溶解的溶质分子或离子,在溶液中不停地运动着,当它们跟未溶解的固体表面碰撞时,又可重新被吸引到固体表面上来,这个过程称为结晶。
8.溶解和结晶的关系:溶解和结晶这两个过程则是同时进行的相反(互逆)的过程,即在溶液里溶质进行溶解的同时,也进行着结晶,在一定条件下建立起一个动态平衡体系。
若改变外界的条件(包括改变溶剂量或温度),则可不同程度地改变微观粒子的溶解速率和结晶速率。
9.溶液。
10.结晶水:溶质从其水溶液里析出而形成晶体时,晶体里常常有一定数目的水分子,这样的水分子叫做结晶水。
晶体中的这种水分子,是作为晶体结构中的一种成分而存在于晶体中的。
有些盐溶于水中会形成稳定的水合离子,当这些盐从水溶液里结晶出来时,就带有一定数目的水分子。

