最新版药典中的对照品汇总
- 格式:docx
- 大小:41.10 KB
- 文档页数:6

附件:辛酸钠XinsuannaSodium CaprylateC8H15NaO2166.20 本品按无水物计算,含C8H 15NaO2应不得少于99.0%。
【性状】本品为白色或类白色结晶性粉末。
本品在水或冰醋酸中易溶,在乙醇中略溶,在丙酮中几乎不溶。
【鉴别】(1)取本品约20mg,加水0.5ml 溶解后,加甲氧基苯乙酸试液(取甲氧基苯乙酸2.7g,加10%氢氧化四甲铵的甲醇溶液6ml 溶解后,加乙醇20ml,摇匀,贮存于聚乙烯容器中)1.5ml,于冰浴中冷却30 分钟,生成大量白色结晶性沉淀;置20℃的水浴中,搅拌5 分钟,沉淀不消失;加氨试液1ml, 沉淀完全溶解;再加16%碳酸铵溶液1ml ,没有沉淀生成。
(2)在有关物质项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
【检査】碱度取本品2.5g,加水25ml 溶解后,依法测定(通则0631),pH 值应为8.0~10. 5。
溶液的澄清度与颜色取本品2.5g,加水25ml 溶解后,依法检查(通则0901 与通则0902),溶液应澄清无色。
如显色,与橙黄色1 号标准比色液(通则0901 第一法)比较,不得更深。
水分取本品,照水分测定法(通则0832 第一法)测定,含水分不得过3.0% 。
重金属取本品2.0g,加冰醋酸-水-乙醇(5:10:85)25ml 溶解后,作为供试品溶液。
依法检查(通则0821 第一法),含重金属不得过百万分之五。
有关物质取本品约0.12g,加水5ml 溶解后,加稀硫酸1ml,摇匀,加乙酸乙酯10ml,振摇提取后,静置使分层,取乙酸乙酯层,加无水硫酸钠干燥后,取上清液作为供试品溶液;精密量取1ml,置100ml 量瓶中,用乙酸乙酯稀释至刻度,摇匀,精密量取5ml,置50ml 量瓶中,用乙酸乙酯稀释至刻度,摇匀,作为对照溶液。
另取辛酸对照品约10mg,加乙酸乙酯10ml 使溶解,作为对照品溶液。

一、《中华人民共和国药典》简称《中国药典》,依据《中华人民共和国药品管理法》组织制沱和颁布实施。
《中国药典》一经颁布实施,英所载同品种或相关内容的上版药典标准或原国家药品标准即停止使用。
《中国药典》由一部、二部、三部.四部及其增补本组成。
一部收载中药,二部收载化学药品,三部收载生物制品及相关通用技术要求,四部收载通用技术要求和药用辅料。
除特別注明版次外,《中国药典》均指现行版。
本部为《中国药典》四部。
二、《中国药典》主要由凡例、通用技术要求和品种正文构成。
凡例是为正确使用《中国药典》.对品种正文、通用技术要求以及药品质量检验和检泄中有关共性问题的统一规定和基本要求。
通用技术要求包括《中国药典》收载的通则、指导原则以及生物制品通则和相关总论等。
《中国药典》各品种项下收载的内容为品种正文。
三、药品标准由品种正文及其引用的凡例、通用技术要求共同构成。
本版药典收载的凡例、通则/生物制品通则.总论的要求对未载入本版药典的其他药品标准具同等效力。
四、凡例和通用技术要求中釆用“除另有规立外”这一用语,表示存在与凡例或通用技术要求有关规泄不一致的情况时,则在品种正文中另作规窪,并据此执行。
五、品种正文所设各项规左是针对符合《药品生产质量管理规范》(Good Manufacturing Practices, GMP)的产品而言。
任何违反GMP或有未经批准添加物质所生产的药品,即使符合《中国药典》或按照《中国药典》未检出其添加物质或相关杂质,亦不能认为其符合规泄。
六、《中国药典》的英文需称为Pharmacopoeia of the People's Republic of China;英文简称为Chinese Pharmacopoeia:英文缩写为ChPo通用技术要求七、通则主要包括制剂通则、其他通则、通用检测方法。
制剂通则系为按照药物剂型分类, 针对剂型特点所规左的基本技术要求。
通用检测方法系为各品种进行相同项目检验时所应采用的统一规定的设备.程序、方法及限度等。
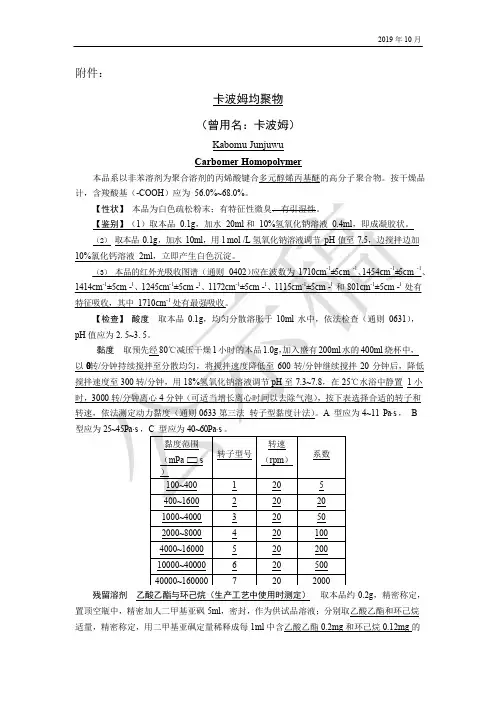
附件:卡波姆均聚物(曾用名:卡波姆)Kabomu JunjuwuCarbomer Homopolymer本品系以非苯溶剂为聚合溶剂的丙烯酸键合多元醇烯丙基醚的高分子聚合物。
按干燥品计,含羧酸基(-COOH)应为56.0%~68.0%。
乙酸乙酯与环己烷(生产工艺中使用时测定)置顶空瓶中,精密加人二甲基亚砜5ml,密封,作为供试品溶液;分别取乙酸乙酯和环己烷适量,精密称定,用二甲基亚砜定量稀释成每1ml 中含乙酸乙酯0.2mg 和环己烷0.12mg 的混合溶液,精密量取5ml ,置顶空瓶中,密封,作为对照品溶液。
照残留溶剂测定法(通则0861 第二法)测定,用100%二甲基聚硅氧烷为固定液(或极性相近的固定液)的毛细管柱,程序升温,起始温度为40℃,维持3 分钟,以每分钟5℃的速率升温至120℃,维持20 分钟,再以每分钟20 ℃的速率升温至220℃,维持3 分钟,再以每分钟20℃的速率升温至240℃,维持8 分钟;进样口温度260℃,检测器温度260℃;顶空瓶平衡温度为85°C ,平衡时间为90 分钟。
取对照品溶液与供试品溶液分别顶空进样。
按外标法以峰面积计算,含乙酸乙酯不得过0.5% ,环己烷不得过0.3%。
苯取苯适量,精密称定,用二甲基亚砜定量稀释制成每1ml 中含苯1.0mg 的溶液。
精密量取该溶液适量,加水定量稀释制成每1ml 中含苯0.5μg 的溶液,作为苯储备液。
取本品约炽灼残渣取本品1.0g,依法检查(通则0841),遗留残渣不得过2.0%。
重金属取炽灼残渣项下遗留的残渣,依法检查(通则0821 第二法),含重金属不得过百万分之二十。
【含量测定】取本品约0.4g,精密称定,加水400ml,充分溶胀后加氯化钾2g,照电位滴定法(通则0701),用氢氧化钠滴定液(0.25mol/L)滴定。
每1ml 氢氧化钠滴定液(0.25mol/L)相当于11.25mg 的-COOH。
【类别】药用辅料,软膏基质和释放阻滞剂。


附件:间甲酚JianjiafenMetacresolOHCH3本品为由合成法制得的3-甲基苯酚。
含C7H8O 应为98.0%~102.0%。
【性状】本品为无色或微黄色液体;有刺激性臭味。
本品在乙醇或二氯甲烷中易溶,在水中略溶。
C7H8O 108.14 [108-39-4]【鉴别】(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)本品的红外光吸收图谱应与对照品的图谱一致(通则0402)。
【检查】酸度取本品1.5ml,置100ml 量瓶中,用水溶解并稀释至刻度,摇匀,作为供试品溶液;精密量取25ml,加甲基红指示液0.15ml,用氢氧化钠滴定液(0.01mol/L)滴定至溶液显黄色,消耗氢氧化钠滴定液(0.01mol/L)不得过0.50ml。
溶液的澄清度与颜色取酸度检查项下的供试品溶液,依法检查(通则0901),溶液应无色;如显浑浊,与3 号浊度标准液(通则0902 第一法)比较,不得更浓。
有关物质取本品适量,精密称定,用甲醇定量稀释制成每1ml 中约含10mg 的溶液,作为供试品溶液;精密量取适量,用甲醇定量稀释制成每1ml 中约含间甲酚5μg与50μg的溶液,摇匀,作为灵敏度测试溶液与自身对照溶液;另取甲苯适量,精密称定,用甲醇定量稀释制成每1ml 中约含甲苯8.9μg的对照品溶液。
照含量测定项下的色谱条件,取灵敏度测试溶液1µl ,注入气相色谱仪,记录色谱图,间甲酚峰信噪比应不小于10;精密量取对照品溶液、自身对照溶液与供试品溶液各1µl,注入气相色谱仪,记录色谱图,按外标法以峰面积计算,甲苯不得过0.089%;按自身对照法以间甲酚面积计算,邻甲酚与对甲酚均不得过0.5%,单个杂质不得过0.10%,总杂质不得过1.0%。
不挥发物取本品2.0g,置已恒重的蒸发皿中,于水浴上蒸干后,在105℃干燥1 小时,遗留残渣不得过2mg(0.1%)。


二甲基亚砜ErjiajiyafengDimethyl SulfoxideC2H6OS 78.13 [67-68-5]本品可由二甲硫醚在氧化氮存在下通过空气氧化制得;也可以从制造纸浆的副产物中制得。
本品按无水物计算,应不得少于99.5%。
【性状】本品为无色液体。
本品与水、乙醇或乙醚能任意混溶,在烷烃中不溶。
折光率本品的折光率(通则0622)为1.478~1.480。
相对密度本品的相对密度(通则0601)为1.095-1.105。
【鉴别】(1)取本品5ml,置试管中,加氯化镍50mg,振摇使溶解,溶液呈黄绿色,置50℃水浴中加热,溶液呈绿色或蓝绿色,放冷,溶液呈黄绿色。
(2)本品的红外光吸收图谱应与对照品的图谱一致(通则0402)。
【检查】酸度取本品50.0g,加水100ml溶解后,加酚酞指示液0.1ml,用氢氧化钠滴定液(0.01mol/L)滴定至溶液显粉红色,消耗氢氧化钠滴定液(0.01mol/L)的体积不得过5.0ml。
吸光度取本品适量,通入干燥氮气15分钟,以水为空白,照紫外-可见分光光度法(通则0401),立即测定,在275nm波长处的吸光度不得大于0.30;在285nm与295nm波长处的吸光度不得大于0.20;在285nm与295nm波长处的吸光度与275nm波长处的吸光度的比值,分别不得过0.65与0.45;在270~350nm的波长范围内,不得有最大吸收峰。
氢氧化钾变深物精密量取本品25ml,置50ml量瓶中,加水0.5ml与氢氧化钾1.0g,密塞,在水浴上加热20分钟,放冷,将溶液置1cm吸收池中,以水为空白溶液,照紫外-可见分光光度法(通则0401),在350nm的波长处测定吸光度,不得大于0.023。
水分取本品,照水分测定法(通则0832第一法1)测定,含水分不得过0.2%。
有关物质取本品5.0g,精密称定,置10ml量瓶中,精密加内标溶液(取二苯甲烷适量,加丙酮稀释制成每1ml中含1.25mg的溶液)1ml,用丙酮稀释至刻度,摇匀,作为供试品溶液;另取本品50.0mg,精密称定,置100ml量瓶中,精密加内标溶液10ml,用丙酮稀释至刻度,摇匀,作为对照溶液;取二甲基亚砜对照品50.0mg[1],精密称定,置100ml量瓶中,精密加内标溶液10ml,用丙酮稀释至刻度,摇匀,作为对照品溶液;照气相色谱法(通则0521)试验,以聚乙二醇20M(或极性相似)为固定液的毛细管柱为色谱柱,柱温为150℃,进样口温度为230℃,检测器温度为250℃,分流比为20∶1。
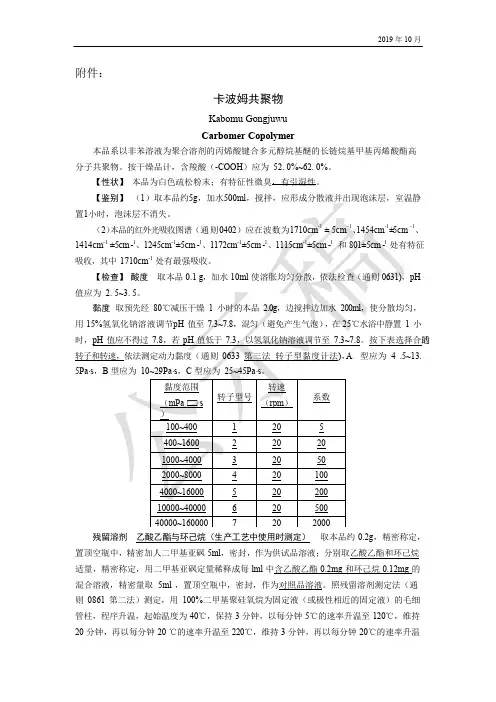
附件:卡波姆共聚物Kabomu GongjuwuCarbomer Copolymer本品系以非苯溶液为聚合溶剂的丙烯酸键合多元醇烷基醚的长链烷基甲基丙烯酸酯高分子共聚物。
按干燥品计,含羧酸(-COOH)应为52. 0%~62. 0%。
【性状】本品为白色疏松粉末;有特征性微臭,有引湿性。
乙酸乙酯与环己烷(生产工艺中使用时测定)置顶空瓶中,精密加人二甲基亚砜5ml,密封,作为供试品溶液;分别取乙酸乙酯和环己烷适量,精密称定,用二甲基亚砜定量稀释成每lml 中含乙酸乙酯0.2mg 和环己烷0.12mg 的混合溶液,精密量取5ml ,置顶空瓶中,密封,作为对照品溶液。
照残留溶剂测定法(通则0861 第二法)测定,用100%二甲基聚硅氧烷为固定液(或极性相近的固定液)的毛细管柱,程序升温,起始温度为40℃,保持3 分钟,以每分钟5℃的速率升温至120℃,维持20 分钟,再以每分钟20 ℃的速率升温至220℃,维持3 分钟,再以每分钟20℃的速率升温至240℃,维持8 分钟;进样口温度260℃,测器温度260℃;顶空瓶平衡温度为85°C ,平衡时间为90 分钟。
取对照品溶液与供试品溶液分别顶空进样。
按外标法以峰面积计算,含乙酸乙酯不得过0.5% ,环己烷不得过0.3%。
苯取苯适量,精密称定,用二甲基亚砜定量稀释制成每1ml 中含苯1.0mg 的溶液。
精密量取该溶液适量,加水定量稀释制成每1ml 中含苯0.5μg 的溶液,作为苯储备液。
取本品约250mg,精密称定,置顶空瓶中,精密加入氯化钠水溶液(20mg/ml)10.0 ml,机械混合均匀(约30 分钟),密封,作为供试品溶液,此溶液应在配制后3 小时内进样;取本品约250mg,精密称定,置顶空瓶中,精密加入氯化钠水溶液(20mg/ml)9.0ml,机械混合均匀(约30 分钟),精密加入苯储备液1ml,机械混合均匀(约1 分钟),密封,作为对照品溶液。

附件:羟丙基倍他环糊精Qiangbingji Beita HuanhujingHydroxypropyl Betadex本品为倍他环糊精与1,2- 环氧丙烷的醚化物, 按无水物计算,含羟丙氧基(-OCH2CHOHCH3)应为19.6%~26.3%。
【性状】本品为白色或类白色的无定形或结晶性粉末;无臭;引湿性强。
本品极易溶于水或丙二醇,易溶于甲醇或乙醇,几乎不溶于丙酮或三氯甲烷。
【鉴别】(1)本品的红外光吸收图谱应与对照品图谱一致(通则0402)。
(2)取本品5%的水溶液0.5ml,置10ml 试管中,加10%α-萘酚的乙醇溶液2 滴,摇匀,沿试管壁缓缓加入硫酸1ml,在两液界面处即现紫色环。
【检查】酸碱度取本品1.0g,加水40ml 溶解后,依法检查(通则0631),pH 值应为5.0~7.5。
溶液的澄清度与颜色取本品2.5g,加水25ml 使溶解,依法测定(通则0901 与0902),溶液应澄清无色。
氯化物取本品0.1g,依法检查(通则0801),与标准氯化钠溶液5.0ml 制成的对照液比较,不得更浓(0.05%)。
放电导率精密称取本品5.0g,以干燥品计,置50ml 容量瓶中,加蒸馏水(预先煮沸并置至室温)溶解并稀释至刻度。
在20℃下测定溶液的电导率(通则0681),应不得过200μS/cm。
同时进行空白对照校正。
至有关物质精密称取本品2.5g,置25ml 容量瓶,精密加60℃的水15ml,振摇溶解,放室温,加水稀释至刻度,摇匀,作为供试品溶液;另取倍他环糊精对照品25mg 和1,2-丙二醇对照品50mg,精密称定,置100ml 容量瓶,加水稀释至刻度,摇匀,作为对照品溶液。
照高效液相色谱法(通则0512)测定,用苯基键合硅胶为填充剂;水为流动相;用示差折光检测器;柱温40℃;检测器温度40℃。
取对照品溶液和供试品溶液各20µl,分别注入液相色谱仪,倍他环糊精和丙二醇的分离度应不得小于4,记录色谱图至倍他环糊精保留时间的6 倍。

附件:山梨醇溶液Shanlichun RongyeSorbitol Solution本品为山梨醇、少量的单糖、多糖及其他麦芽糖醇、甘露醇等的混合物,系部分水解淀粉经氢化制得。
本品含D-山梨糖醇(C6H14O6)不少于45.0%(g/g)(非结晶山梨醇溶液);含D-山梨糖醇(C6H14O6)不少于64.0%(g/g)(结晶山梨醇溶液)。
【性状】本品为澄清、无色、糖浆状液体。
旋光度取本品约7.0g,置50ml 量瓶中,加硼砂6.4g 与水适量。
静置1h,偶尔摇动,用水稀释至刻度。
(如溶液不澄清,应滤过),依法测定(通则0621),比旋度应为+1.5°至+ 3.5°(非结晶山梨醇溶液);旋光度应为0°至+ 1.5°(结晶山梨醇溶液)。
电导率取本品50.0ml,作为供试品溶液;另取新沸放冷的纯化水100ml 作为空白溶液。
将供试品溶液与空白溶液置25℃±1 ℃的水浴中保温1 小时后,缓缓搅拌,用电导率仪测定,以铂黑电极作为测定电极,先用空白溶液冲洗电极3 次后,测定空白溶液的电导率,其电导率值应不得过5.0µS/cm。
取出电极,再用供试品溶液冲洗电极3 次后,测定供试品溶液的电导率,经空白校正后,不得过10µS/cm。
【鉴别】(1)取本品约1.4g,加水75ml 使溶解,作为供试品溶液;取上述溶液3ml 至15cm 试管,加新制的10%邻苯二酚试液3ml,摇匀,加硫酸6ml,摇匀,加热30s,即显深粉色或酒红色。
(2)在含量测定项下记录的色谱中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
【检查】酸度取本品1.4g,加水至10ml,依法检查(通则0631),pH 值应为5.0~7.5。
溶液的澄清度与颜色取本品7.0g,置50ml 量瓶中,用水稀释至刻度,混匀,依法检查(通则0901 与通则0902),溶液应澄清无色。
还原糖取本品适量(含无水物3.3g),置锥形瓶中,加3ml 水使溶解,加碱性枸橼酸铜试液20ml,加玻璃珠或沸石数粒,加热使在4~6 分钟内沸腾,保持沸腾3 分钟。

l第一部分:生化药的基本概况l第二部分:2010年版中国药典生化药归总第一部分:生化药的基本概况1、生化药的定义2、生化药的发展1、生化药的定义•生化药物是我国医药产品的一个大类。
•生化药主要从动、植物及微生物发酵提取的、化学合成、生物-化学半合成或用现代生物重组技术制得的一类药品•尤其对于严重危害人类健康和生命的疾病,如心脑血管病、癌症、糖尿病和病毒疾患等有其独特的治疗效果。
深受人民的欢迎和重视。
2、生化药的发展历程医药行业的发展状况0%5%10%15%20%25%30%35%40%行业2009年增长率第二部分:2010年版中国药典生化药归总为贯彻党的十七大精神,落实科学发展观,建国以来的第九版药典——《中国药典》2010年版,已完成增修订任务,目前已经正式出版发行。
宗旨:l提高药典质量,l应用高新技术,l解决安全隐患,l赶超国际水平。
本届药典生化药修订工作的特点l时间短l任务重l难度大l要求高一、氨基酸及其衍生物类1、基本介绍该类品种是组成蛋白质的基本单位。
组成人体蛋白质的氨基酸只有20种左右,均为L-a-氨基酸(除甘氨酸外)。
因为是人类健康的基本营养成分,故在救死扶伤中扮演十分重要角色。
临床上除单方使用aa外,其还是复方aa注射液的主要组成成分。
临床上常用的氨基酸注射液有3aa、6aa、9aa、11aa、15aa、17aa、18aa(I-II)等。
从1985年销售100万瓶,到2008年销售量已经达到2亿万瓶,市场潜力很大,前景美好。
2、2010年版中国药典收载的氨基酸及其衍生物类品种牛磺酸及其制剂(片、散、颗粒、胶囊、滴眼液);盐酸精氨酸及其制剂(片、注射液);色氨酸;谷氨酸(钠)及其制剂(片、注射液、钾注射液);组氨酸及盐酸组氨酸;脯氨酸;精氨酸;酪氨酸;丝氨酸;异亮氨酸;亮氨酸;赖氨酸(盐酸、醋酸、苄达);缬氨酸;门冬酰胺(片)、甘氨酸(冲洗液)、胱氨酸(片、盐酸)、丙氨酸、甲硫氨酸(片)、苏氨酸、苯丙氨酸、谷丙甘氨酸胶囊、乙酰半胱氨酸(滴眼液、颗粒)、乙酰谷氨酸(注射液)、羧甲司坦(口服溶液、片、颗粒)等53个品种。
附件:明胶空心胶囊Mingjiao Kongxin JiaonangVacant Gelatin Capsules本品系由胶囊用明胶加辅料制成的空心硬胶囊。
【性状】本品呈圆筒状,系由可套合和锁合的帽和体两节组成的质硬且有弹性的空囊。
囊体应光洁、色泽均匀、切口平整、无变形、无异臭。
本品分为透明(两节均不含遮光剂)、半透明(仅一节含遮光剂)、不透明(两节均含遮光剂)三种。
蒸至溶液几乎无色,用水稀释至40ml,照硫酸盐检查法(通则0802)检查,如显浑浊,与标准硫酸钾溶液3.75ml 制成的对照液比较,不得更浓(0.01%)。
对羟基苯甲酸酯类(此项适用于以对羟基苯甲酸酯类作为抑菌剂的工艺)取本品约0.5g,精密称定,置已加热水30ml 的分液漏斗中,振摇使溶解,放冷,精密加乙醚50ml,小心振摇,静置分层,精密量取乙醚层25ml,置蒸发皿中,蒸干乙醚,用流动相转移至5ml 量瓶中并稀释至刻度,摇匀,作为供试品溶液;另精密称取羟苯甲酯、羟苯乙酯、羟苯丙酯、羟苯丁酯对照品各25mg,置同一250ml 量瓶中,加流动相溶解并稀释至刻度,摇匀,精密量取5ml 置25ml 量瓶中,用流动相稀释至刻度,摇匀,作为对照品溶液。
照高效液相色谱法(通则0512)试验,用十八烷基硅烷键合硅胶为填充剂,以甲醇-0.02mol/L 醋酸铵(58∶ 42)为流动相,检测波长为254nm,理论板数按羟苯乙酯峰计算应不低于1600。
精密量取供试品溶液与对照品溶液各10μl,分别注入液相色谱仪,记录色谱图;供试品溶液如出现与对照品溶液相应的峰,按外标法以峰面积计算,含羟苯甲酯、羟苯乙酯、羟苯丙酯与羟苯丁酯的总量不得过0.05%。
氯乙醇(此项适用于环氧乙烷灭菌的工艺)取本品适量,剪碎,称取2.5g,置具塞锥形瓶中,加正己烷25ml,浸渍过夜,将正己烷液移至分液漏斗中,精密加水2ml,振摇提取,取水溶液作为供试品溶液。
另取氯乙醇适量,精密称定,加正己烷溶解并定量稀释成每1ml中约含柱温110100ml试验,用柱温45(0.000117.5%。
中华人民共和国药典凡例《中华人民共和国药典》(以下简称《中国药典》)是国家监督管理药品质量的法定技术标准。
“凡例”是解释和使用《中国药典》(一部)正确进行质量检定的基本指导原则,并把与正文、附录及质量检定有关的共性问题加以规定,避免在全书中重复说明。
“凡例”中的有关规定具有法定的约束力。
凡例和附录中采用“除另有规定外”这一修饰语,表示存在与凡例或附录有关规定未能概括的情况时,在正文各论中另作规定。
名称及编排一、正文品种中文名称按笔画数顺序排列,同笔画数的字按起笔笔形-丨丿丶乛顺序排列;单列的炮制品及单味提取物、油脂等排在各该药材的后面;制剂中同一品种因规格不同需单列者,在其名称后加括号注明规格;附录按分类编码。
二、第一品种项下根据品种和剂型不同,按顺序可分别列有:(1)中文名称(必要时用括号加注副名),汉语拼音名与拉丁名;(2)来源;(3)处方;(4)制法;(5)性状;(6)鉴别;(7)检查;(8)浸出物;(9)含量测定;(10)性味与归经;(11)功能与主治;(12)用法与用量;(13)注意;(14)规格;(15)贮藏;(16)制剂等。
标准规定三、药材的质量标准,一般按干品规定,特殊需用鲜品者,同时规定鲜品的标准,并规定鲜品用法与用量。
四、药材原植(动)物的科名、植(动)物名、学名、药用部位(矿物药注明类、族、矿石名或岩石名、主要成分)及采收季节和产地加工等,均属各该药材的来源范畴。
药用部位一般系指已除去非药用部分的商品药材。
采收(采挖等)和产地加工即对药用部位而言。
五、药材产地加工及炮制规定的干燥方法如下:(1)烘干、晒干、阴干均可的,用“干燥”;(2)不宜用较高温度烘干的,则用“晒干”或“低温干燥”(一般不超过60℃);(3)烘干、哂干均不适宜的,用“阴干”或“晾干”;(4)少数药材需要短时间干燥,则用“曝哂”或“及时干燥”。
制剂中的干燥系指烘干,不宜高温烘干的用“低温干燥”。
六、同一名称有多种来源的药材,其性状有明显区别的均分别描述。
附件:聚乙二醇2000Juyi’erchun 2000Polyethylene Glycol 2000本品为环氧乙烷和水缩聚而成的混合物,分子式以H(OCH2CH2)n OH 表示,其中n 代表氧乙烯基的平均数。
【性状】本品为白色蜡状固体或颗粒状粉末;略有特臭。
本品在水、乙醇中易溶。
凝点本品的凝点(通则0613)为45~50℃。
黏度取本品25.0g,置100ml 量瓶中,加水溶解并稀释至刻度,摇匀,用毛细管内径为0.6mm 的平氏黏度计,依法测定(通则0633 第一法),在40℃时的运动黏度为3.5~4.5 mm2/s。
【鉴别】(1)取本品0.05g,加稀盐酸5ml 和氯化钡试液1ml,振摇,滤过;在滤液中加入10%磷钼酸溶液1ml,产生黄绿色沉淀。
(2)取本品0.1g,置试管中,加入硫氰酸钾和硝酸钴各0.1g,混合后,加入二氯甲烷5ml,溶液呈蓝色。
【检查】平均分子量取本品约6.0g,精密称定,置干燥的250ml 具塞锥形瓶中,精密加邻苯二甲酸酐的吡啶溶液(取邻苯二甲酸酐14g,溶于无水吡啶100ml 中,放置过夜,备用)25ml,摇匀,加少量无水吡啶于锥形瓶口边缘封口,置沸水浴中,加热30 分钟,取出冷却,精密加入氢氧化钠滴定液(0.5mol/L)50ml,以酚酞的吡啶溶液(1→100)为指示剂,用氢氧化钠滴定液(0.5mol/L)滴定至显红色,并将滴定的结果用空白实验校正。
供试量(g)与4000 的乘积,除以消耗氢氧化钠滴定液(0.5mol/L)的容积(ml),即得供试品的平均分子量,应为1800~2200。
酸度取本品1.0g,加水20ml 溶解后,依法测定(通则0631),pH 值应为4.0~7.0。
溶液的澄清度与颜色取本品5.0g,加水50ml 溶解后,依法检查(通则0901 与通则0902),溶液应澄清无色;如显浑浊,与2 号浊度标准液(通则0902 第一法)比较,不得更浓;如显色,与黄色2 号标准比色液(通则0901 第一法)比较,不得更浓。
附件:聚维酮K30Juweitong K30Povidone K30号浊度标准液比较,不得更浓;如显色,与黄色1号或棕红色2号标准比色液比较(通则0901第一法),不得更深。
K值取本品1.00g(按无水物计算),精密称定,置100ml量瓶中,加水适量使溶解,并稀释至刻度,在25℃±0.2 ℃恒温水浴中放置1小时后,依法检查(通则0633第二法),测得相对黏度ηr,按下式计算K值,应为27.0~32.0。
式中W 为供试品的重量(按无水物计算),g。
醛取本品1.0g,置100ml 量瓶中,加磷酸盐缓冲液(取磷酸二氢钾1.74g,加水80ml溶解后,用1mol/L 氢氧化钾溶液调节pH 值至9.0,再加水稀释至100ml,即得)溶解并稀释至刻度,摇匀,密塞,在60℃恒温水浴中放置1 小时后,放冷,作为供试品溶液。
另取乙醛合氨三聚体0.140g,置200ml 量瓶中,用水溶解并稀释至刻度,摇匀,精密量取1ml,置100ml 量瓶中,加磷酸盐缓冲液稀释至刻度,摇匀,作为对照品溶液。
精密量取供试品溶液0.5ml,置比色皿中,依次加磷酸盐缓冲液2.5ml,烟酰胺腺嘌呤二核苷酸溶液(取β-烟酰胺腺嘌呤二核苷酸适量,置玻璃瓶中,加磷酸盐缓冲液溶解并稀释制成每1ml 含4mg的溶液,4℃存放,4 周内稳定)0.2ml,加盖,混匀,在22℃±2℃水浴中放置2~3 分钟,以水为参比,照紫外-可见分光光度法(通则0401),在340nm 的波长处测定吸光度;再在同一供试品溶液中N-乙烯基吡咯烷酮与相邻色谱峰分离度应符合要求。
精密量取供试品溶液与对照品溶液各20µl,分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算,不得过0.001%。
试2-吡咯烷酮取本品适量,精密称定,加水溶解并稀释成每1ml 含5mg 的溶液,作为供品溶液。
取2-吡咯烷酮对照品适量,精密称定,加水溶解并稀释为每1ml 含0.1mg 的溶液,作为对照品溶液。